| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
sGC/Soluble Guanylate Cyclase; Soluble guanylate cyclase (sGC) (EC50 = 14 nM for stimulation of sGC in the presence of the heme cofactor; EC50 = 1.4 μM for stimulation of heme-free sGC) [1]
|
|---|---|
| 体外研究 (In Vitro) |
Vericiguat(0.01 μM 至 100 μM)刺激重组 sGC 浓度依赖性,1.7 倍至 57.6 倍。当与 NO 供体二乙胺/一氧化氮复合物 (DEA/NO) 结合使用时,vericiguat 和 DEA/NO 在较宽的浓度范围内对酶活性具有协同作用。在 Vericiguat (100 μM) 和 DEA/NO (100 nM) 的最高浓度下,sGC 的比活性是基线的 341.6 倍。 Vericiguat 刺激 sGC 报告细胞系浓度依赖性,EC50 为 1005±145 nM。 Vericiguat 浓度依赖性地抑制去氧肾上腺素诱导的兔隐动脉环、兔主动脉环和犬股静脉环的收缩,IC50 值分别为 798、692 和 3072 nM。 Vericiguat 浓度依赖性地抑制 U46619 诱导的猪冠状动脉环收缩,IC50 为 956 nM[1]。
Vericiguat(BAY 1021189)以剂量依赖方式刺激sGC。在血红素辅因子存在的情况下,其刺激活性较强,EC50为14 nM;即使在无血红素(无血红素sGC)的情况下,仍保留刺激活性,EC50为1.4 μM。它可增加人脐静脉内皮细胞(HUVECs)和大鼠主动脉平滑肌细胞中的cGMP生成,在浓度分别为10 μM和1 μM时观察到最大效应。该化合物在浓度高达10 μM时不抑制磷酸二酯酶(PDEs)1-5,表明对sGC具有选择性[1] |
| 体内研究 (In Vivo) |
Vericiguat(化合物 24)(口服;3 mg/kg,10 mg/kg;每日一次;21 天)在 L-NAME 治疗的肾素转基因大鼠高血压诱导的终末器官损伤模型中维持心肾功能。此外,与对照组相比,Vericiguat 治疗组的总体死亡率显着降低[1]。动物模型:L-NAME处理的肾素转基因大鼠[1] 剂量:3 mg/kg、10 mg/kg 给药方法:口服;给药方式:口服。 3毫克/公斤、10毫克/公斤;每天一次; 21 天结果:导致血压升高显着减弱,但 3/10 mg/kg 治疗组的血压总体升高并未停止。导致右心室和左心室的心脏肥大显着且呈剂量依赖性减少。对于肾脏损伤,Vericiguat 导致肾损伤分子 Kim-1 和骨桥蛋白表达显着减少,这些分子被用作肾损伤和功能障碍的生物标志物。导致存活率显着且呈剂量依赖性增加。每日一次3mg/kg和10mg/kg治疗组的大鼠存活率分别为70%和90%。相比之下,安慰剂组21天后的存活率仅为25%。
在麻醉犬中,静脉注射Vericiguat(BAY 1021189)(0.3、1和3 mg/kg)可剂量依赖性降低平均动脉压(MAP),分别降低8、15和24 mmHg,且不影响心率。在清醒的自发性高血压大鼠(SHRs)中,口服给药(3、10和30 mg/kg)可降低收缩压(SBP),分别降低14、22和31 mmHg,效果至少持续8小时。在心肌梗死诱导的心力衰竭大鼠模型中,长期口服治疗(10 mg/kg/天,持续4周)与溶媒对照组相比,可改善左心室射血分数(LVEF)并减少左心室舒张末期容积(LVEDV)[1] |
| 酶活实验 |
高纯度sGC[1]
酶活性通过α-[32P]-GTP形成[32P]-cGMP来测量,根据Hoenicka等人和Schermuly等人进行了修改。修改包括分别使用200μM、3 mM和1 mM浓度的GTP、Mn2+/Mg2+和cGMP。仔细选择酶浓度,使底物周转率低于10%,从而避免底物或辅因子耗竭。在0.2μg/mL的蛋白质浓度下对纯化酶进行表征。所有测量均进行两次,重复五次。对于酶的表征,sGC的比活性表示为x倍刺激与比基础活性。该试验中DMSO的最高浓度为1%(v/v),本身对cGMP的产生没有任何影响。[1] CYP抑制试验[1] 根据所述的测定条件,通过CYP异构体介导的标准探针代谢产物的形成在体外评估24的抑制效力(详情请参阅支持信息)。为了研究时间依赖性,对CYP3A4进行了预孵育实验。 将重组人sGC(含血红素)与不同浓度的Vericiguat(BAY 1021189)在GTP存在下孵育。使用竞争性免疫测定法测量cGMP生成,以确定对含血红素sGC的EC50。对于无血红素sGC,先对酶进行预处理以去除血红素,然后与该化合物和GTP孵育,同样通过定量cGMP水平确定对无血红素sGC的EC50。此外,通过将PDEs 1-5与该化合物孵育并使用底物转化法测量其活性来进行PDE抑制试验,证实浓度高达10 μM时无显著抑制作用[1] |
| 细胞实验 |
重组sGC过表达细胞系[1]
如前所述,使用重组sGC过表达细胞系测定测试化合物的细胞活性。(34)简而言之,将细胞以25μL的体积铺在白色384孔Greiner Bio-One微孔板上,并在培养基中培养1或2天。移除培养基,用含腔肠素的无钙酪胺加载细胞3小时。将10μL体积的受试化合物在无钙Tyrode中的连续稀释液施加到细胞上6分钟。此后,将35μL含钙的Tyrode(终浓度:3 mM)加入细胞中,并在不透光的盒子中使用CCD相机测量发射的光40秒。最小有效浓度(MEC)被确定为观察到基础发光值增加≥3倍的浓度 大鼠和人肝细胞的体外清除率测定[1] 使用改良的Janus机器人系统(PerkinElmer)在37°C、pH 7.4、总体积为1.5 mL的条件下与肝细胞进行孵育。孵育混合物含有1×106个细胞/mL(根据用台盼蓝染色后通过显微镜测定的细胞存活率进行校正)、1μM底物和Williams培养基E。最终MeCN浓度≤1%。在2、10、20、30、50、70和90分钟后,从培养混合物中取出125μL的等分试样,并将其分配到含有MeCN(250μL)的96孔板中以停止反应。在1000g离心后,通过LC-MS/MS(AB Sciex Triple Quad 5500)分析上清液。 使用肝细胞根据半衰期数据计算体外清除值,反映底物耗竭,使用以下方程式进行:CL′内在[mL/(min·kg)]=(0.693/体外t1/2[min])(肝脏重量[g肝脏/kg体重])(细胞号[1.1×108]/肝脏重量[g])/(细胞号[1×106]/孵育体积[mL])。使用非限制性充分搅拌模型估算CLlood:充分搅拌的CLlood[L/(h·kg)]=(QH[L/。计算时,使用了以下值:人体比肝重量为21g/kg体重,肝血流量为1.32L/(h·kg),肝脏中的细胞数量估计为1.1×108个细胞/g肝脏;大鼠肝脏比重为32g/kg体重,肝血流量为4.2L/(h·kg),肝脏细胞数估计为1.1×108个细胞/g肝脏 Caco-2渗透性测定[1] Artursson和Karlsson测试了测试化合物在Caco-2细胞单层中的体外渗透性,Caco-2是一种成熟的体外系统,用于预测胃肠道的渗透性。将Caco-2细胞接种在24孔插入板上,并允许其生长14-16天。对于渗透性研究,将测试化合物溶解在DMSO中,用运输缓冲液[Hanks缓冲盐溶液,进一步补充葡萄糖(最终浓度19.9 mM)和HEPES(最终浓度9.8 mM)]稀释至最终测试浓度2μM。为了测定顶端到基底外侧的通透性(Papp A-B),将试验化合物溶液加入细胞单层的顶端侧,并将转运缓冲液加入单层的基底外侧。为了测定基底外侧到顶端的通透性(Papp B-A),将试验化合物溶液加入细胞单层的基底外侧,并将转运缓冲液加入单层的顶端。在实验开始时从供体室中取样以确认质量平衡。在37°C下孵育2小时后,从两个隔室中取样。通过LC-MS分析样品,并计算表观渗透系数。外排率计算为Papp B-A/Papp A-B。对每个细胞单层进行路西法黄渗透性测定,以确保细胞单层的完整性,并对每批进行阿替洛尔(低渗透性标志物)和柳氮磺胺吡啶(活性排泄标志物)的渗透性测定作为质量控制。 将HUVECs和大鼠主动脉平滑肌细胞接种在培养板中并生长至汇合。用浓度范围为0.01至10 μM的Vericiguat(BAY 1021189)处理细胞30分钟。使用cGMP免疫测定试剂盒测量细胞内cGMP水平。结果显示cGMP呈浓度依赖性增加,在10 μM(HUVECs)和1 μM(平滑肌细胞)时出现最大反应[1] |
| 动物实验 |
L-NAME-treated renin transgenic rats
3 mg/kg, 10 mg/kg Oral administration; 3 mg/kg, 10 mg/kg; once daily; 21 days Rat Heart Langendorff Preparation[1] Male Wistar rats (200–250 g) were anesthetized using Narcoren (100 mg/kg ip). The heart was rapidly excised and connected to a Langendorff perfusion system. The heart was perfused at a constant flow rate of 10 mL/min with Krebs–Henseleit buffer solution equilibrated with 95% O2 and 5% CO2. The perfusion solution contained (in mmol/L): NaCl 118, KCl 3, NaHCO3 22, KH2PO4 1.2, MgSO4 1.2, CaCl2 1.8, glucose 10, and sodium pyruvate 2. A pressure transducer registered the perfusion pressure in the system. The left ventricular pressure was measured using a second pressure transducer connected to a water-filled balloon which was inserted into the left ventricle via the left atrium. The end diastolic pressure was initially set to 8–10 mmHg by adjusting the volume of the balloon. The hearts were spontaneously beating. The signals from the pressure transducer were amplified, registered, and used for the calculation of the heart frequency and + dP/dtmax by a personal computer. 24 was dissolved in a mixture of 10% DMSO and 90% saline and infused for 20 min with increasing concentration steps into the aortic cannula at a rate of 1% of the total flow rate. All values are presented as relative changes of baseline values before compound application. Chronic Treatment Study with L-NAME-Treated Renin Transgenic Rats[1] Fifty male renin transgenic rats carrying an additional mouse renin gene [RenTG(mRRen2)27] at the age of 8 weeks were used. L-NAME was chronically administered via the drinking water (50 mg/L) in all study groups. Animals were randomly allocated to three study groups: placebo (control) (n = 20), 24 low dose, and 24 high dose (3 and 10 mg/kg per day, respectively, administered po by gavage qd, n = 15 per group). Blood pressure was measured via the tail-cuff method once before the start of the study (day 0) to exclude preexisting differences between the groups and on day 7, 14, and 21. Body weight and survival were assessed on day 1, 8, and 15 and at the study end. At the end of the study (day 22), all animals were anesthetized, blood was collected, and animals were sacrificed; blood was taken in order to assess plasma parameters, and the heart was dissected into the left and right ventricles and was weighed to assess potential heart hypertrophy. Creatinine, urea, and renin activity in plasma were determined after extraction, as previously described. Pharmacokinetic Parameters after Intravenous and Oral Application in Rats and Dogs[1] For in vivo pharmacokinetic experiments, male Wistar rats and female beagle dogs were used. Intravenous application was carried out with a species-specific plasma/DMSO formulation in rats and with a H2O/PEG 400/EtOH formulation in dogs. Oral application in both species was by gavage with a H2O/PEG 400/EtOH formulation. For simplification of blood drawing in rats, a silicone catheter was implanted into the right vena jugularis externa. The surgery was performed at least 1 d before substance application under isoflurane anesthesia and additional administration of an analgetic (atropine/rimadyl 3:1, 0.1 mL sc). Blood drawing (usually more than 10 time points) was done in a time window that included at least two time points after 24 h (postsubstance application). Blood was passed into heparinized tubes. Afterward, blood plasma was obtained by centrifugation at 1000g. Where necessary, the plasma was stored at −20 °C until further analysis. An internal standard was added to the sample, calibration, and qualifier solutions. The internal standard could also have been a compound from a different chemical class than the analyte of interest. Afterward, protein precipitation was performed by using an excess of MeCN. A buffer solution was added with a composition based on the mobile phases used in subsequent liquid chromatography. After centrifugation at 1000g, the supernatant was analyzed by LC-MS using different C18 reversed-phase columns and various mobile phase compositions. Quantification of the substance was conducted by using peak height or area calculated from extracted ion chromatograms of specific selected ion-monitoring experiments or high-resolution LC-MS experiments. From the plasma concentration–time course, the pharmacokinetic parameters CL (clearance), t1/2 (terminal half-life), VSS (volume of distribution at steady state), and F (bioavailability after oral administration) were calculated by using a validated internal pharmacokinetic calculation software. Because substance quantification was done in plasma, the blood/plasma distribution needed to be analyzed to calculate a blood clearance value. Therefore, a defined amount of the substance was added to blood in heparinized tubes and incubated for 20 min by gently swinging. The plasma was obtained by centrifugation at 1000g. The cblood/cplasma value was calculated after measurement of the substance concentration in plasma and blood by using peak height or area calculated from extracted ion chromatograms of specific selected ion-monitoring experiments or high-resolution LC-MS experiments. - For anesthetized dogs: Vericiguat (BAY 1021189) was dissolved in a vehicle (containing ethanol, polyethylene glycol 400, and water) and administered intravenously at doses of 0.3, 1, and 3 mg/kg. MAP and heart rate were monitored continuously for 2 hours post-administration. - For conscious SHRs: The compound was administered orally via gavage at doses of 3, 10, and 30 mg/kg, dissolved in the same vehicle. SBP was measured using tail-cuff plethysmography at 1, 2, 4, 6, and 8 hours post-dose. - For heart failure rats (post-myocardial infarction): The compound was administered orally once daily at 10 mg/kg/day for 4 weeks, starting 1 week after infarction. Cardiac function (LVEF, LVEDV) was assessed using echocardiography at the end of the treatment period [1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
每日一次口服10mg维利西呱后,心力衰竭患者的平均稳态Cmax和AUC分别为350 mcg/L和6,680 mcg•h/L,Tmax为1小时。与食物同服时,口服维利西呱的绝对生物利用度约为93%——与食物同服可降低药代动力学变异性,使Tmax延长至约4小时,并使Cmax和AUC分别增加41%和44%。 口服放射性标记的维利西呱后,约53%的放射性物质从尿液中回收,45%从粪便中回收。一项人体质量平衡研究发现,尿液中回收的药物约含40.8%的N-葡萄糖醛酸苷代谢物、7.7%的其他代谢物和9%的原药,而粪便中回收的药物几乎全部为原药维利西呱。 在健康受试者中,维利西呱的稳态分布容积约为44升。 维利西呱是一种低清除率药物,在健康志愿者中观察到的血浆清除率为1.6升/小时,在收缩性心力衰竭患者中观察到的血浆清除率为1.3升/小时。 代谢/代谢物 维利西呱主要通过II相结合反应代谢,CYP介导的氧化代谢在其整体生物转化中占比很小(<5%)。主要非活性代谢物维利西呱N-葡糖醛酸苷(M1)由UGT1A9生成,少量由UGT1A1生成。其他已鉴定的代谢物包括一种去苄基化化合物和一种M15代谢物,后者被认为是氧化代谢的产物,但这些代谢物的特征尚不明确。 生物半衰期 在心力衰竭患者中,维利西呱的半衰期为30小时。 - 在大鼠中,维利西呱(BAY 1021189)的口服生物利用度为73%。静脉注射(1 mg/kg)后,清除率为13 mL/min/kg,稳态分布容积(Vss)为1.2 L/kg,末端半衰期为3.6小时。在犬类中,口服生物利用度为 65%,清除率为 9 mL/min/kg,稳态分布容积 (Vss) 为 0.9 L/kg,末端半衰期为 4.2 小时。该化合物代谢不广泛,血浆中主要成分为未代谢的母体药物 [1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在预注册试验中,接受维利西呱治疗的患者中有 2% 报告出现血清转氨酶升高伴轻度胆红素升高,但安慰剂组也报告了类似的发生率,且这些异常无需调整剂量或停药即可自行消退。这些异常被认为是心力衰竭加重和充血性肝损伤的结果。目前尚无已发表的关于维利西呱治疗导致临床症状明显或出现黄疸的肝损伤的报告,但维利西呱的总体临床经验有限。 可能性评分:E(不太可能是临床明显肝损伤的原因)。 蛋白结合 维利西呱在血浆中与蛋白质广泛结合(约 98%),主要与血清白蛋白结合。在为期两周的大鼠毒性研究中,口服剂量高达 300 mg/kg/天的维利西呱(BAY 1021189)未引起显著不良反应。未观察到体重、食物消耗量或临床化学参数(肝肾功能)的变化。在大鼠和人血浆中,血浆蛋白结合率均较高(93-95%)[1] |
| 参考文献 | |
| 其他信息 |
药效学
维利西呱通过直接刺激细胞内环磷酸鸟苷 (cGMP) 的生成,引起血管平滑肌松弛和血管扩张。维利西呱的半衰期相对较长(约 30 小时),因此可以每日一次给药。动物生殖研究表明,维利西呱用于妊娠雌性动物时可能具有胚胎-胎儿毒性——在器官形成期对妊娠兔给予维利西呱时,观察到主要血管和心脏发育缺陷以及自发性流产/胚胎吸收。开始使用维利西呱治疗前应排除妊娠的可能性,并在整个治疗期间以及停药后一个月内采取有效的避孕措施。 维利西呱 (BAY 1021189) 是一种首创的可溶性鸟苷酸环化酶刺激剂,旨在用于治疗慢性心力衰竭。它通过直接刺激可溶性鸟苷酸环化酶(sGC)发挥作用,提高环磷酸鸟苷(cGMP)水平,从而导致血管舒张和改善心脏功能。该化合物对sGC的选择性优于其他靶点,且具有良好的药代动力学特性,支持口服给药[1]。维利西呱是一种吡唑并吡啶类化合物,其化学名称为5-氟-1H-吡唑并[3,4-b]吡啶,其中1位氨基氢被2-氟苄基取代,3位氢被4,6-二氨基-5-[(甲氧羰基)氨基]嘧啶-2-基取代。它是一种可溶性鸟苷酸环化酶刺激剂,用于治疗慢性心力衰竭。它具有可溶性鸟苷酸环化酶激活剂、血管舒张剂和抗高血压剂的作用。它是一种氨基嘧啶、吡唑并吡啶、氨基甲酸酯和有机氟化合物。 维利西呱是一种可溶性鸟苷酸环化酶 (sGC) 的直接刺激剂,用于治疗收缩性心力衰竭,以降低死亡率和住院率。sGC 酶是 NO-sGC-cGMP 信号通路的关键组成部分,该通路有助于调节心血管系统。sGC 酶是存在于血管平滑肌细胞(以及其他细胞类型)中的细胞内酶,可在 NO (NO) 激活下催化环磷酸鸟苷 (cGMP) 的合成。cGMP 作为第二信使,激活一系列下游信号级联反应,从而引发多种效应。这些不同的细胞效应表明,cGMP 生成不足(主要是由于 NO 生物利用度不足)与多种心血管疾病的发病机制有关。作为可溶性鸟苷酸环化酶 (sGC) 的直接刺激剂,维利西呱可减轻对功能性 NO-sGC-cGMP 轴的需求,从而有助于预防心力衰竭中因 sGC 活性降低而导致的心肌和血管功能障碍。维利西呱于 2021 年 1 月获得 FDA 批准,由默克公司研发,商品名为 Verquvo,用于治疗某些收缩性心力衰竭患者。虽然维利西呱并非首个获得 FDA 批准的 sGC 刺激剂(利奥西呱于 2013 年获批用于治疗肺动脉高压),但其独特之处在于,其结构修饰显著降低了其对氧化代谢的敏感性,从而延长了半衰期,并允许每日一次给药。 维利西呱是一种可溶性鸟苷酸环化酶刺激剂。维利西呱的作用机制是作为鸟苷酸环化酶刺激剂。 维利西呱是一种口服有效的可溶性鸟苷酸环化酶 (sGC) 刺激剂,sGC 是诱导血管舒张的一氧化氮作用的关键酶,用于治疗慢性心力衰竭患者,以降低死亡和住院风险。维利西呱治疗期间血清转氨酶升高的发生率较低,但尚未发现与临床上明显的急性肝损伤病例相关。 维利西呱是一种口服生物利用度高的可溶性鸟苷酸环化酶 (sGC) 刺激剂,具有血管舒张活性。口服后,维利西呱直接刺激 sGC 的催化活性,并增加细胞内第二信使环磷酸鸟苷 (cGMP) 的生成,cGMP 由三磷酸鸟苷 (GTP) 衍生而来。这导致平滑肌松弛和血管扩张。可溶性鸟苷酸环化酶 (sGC) 是一种含血红素的胞质信号酶,它催化 GTP 在一氧化氮 (NO) 与血红素结合后生成环磷酸鸟苷 (cGMP)。维利西呱 (Vericiguat) 可独立于 NO 刺激 sGC,并与 NO 产生协同作用。 维利西呱是一种小分子药物,其临床试验阶段最高为 IV 期(涵盖所有适应症),于 2021 年首次获批,用于治疗心血管疾病和心力衰竭,并有 2 个在研适应症。该药物已被美国食品药品监督管理局 (FDA) 列入黑框警告。 一种鸟苷酸环化酶刺激剂;已获 FDA 批准用于治疗慢性心力衰竭。 首个可溶性鸟苷酸环化酶 (sGC) 刺激剂利奥西呱 (riociguat) 近期作为肺动脉高压的新型治疗选择而上市。尽管利奥西呱具有优异的药理学特性,但由于其半衰期短,需要每日三次给药,因此其在其他心血管疾病中的应用受到限制。为了进一步优化此类化合物,我们发现了有趣的构效关系,并显著降低了氧化代谢。这些研究最终发现了每日一次给药的sGC刺激剂维利西呱(化合物24,BAY 1021189),目前该药物正处于治疗慢性心力衰竭的III期临床试验阶段。[1] |
| 分子式 |
C19H16F2N8O2
|
|---|---|
| 分子量 |
426.3795
|
| 精确质量 |
426.136
|
| 元素分析 |
C, 53.52; H, 3.78; F, 8.91; N, 26.28; O, 7.50
|
| CAS号 |
1350653-20-1
|
| PubChem CID |
54674461
|
| 外观&性状 |
Light yellow to brown solid powder
|
| LogP |
3.082
|
| tPSA |
151.08
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
31
|
| 分子复杂度/Complexity |
622
|
| 定义原子立体中心数目 |
0
|
| SMILES |
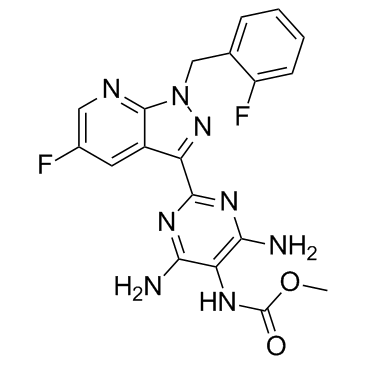
FC1C([H])=NC2=C(C=1[H])C(C1=NC(=C(C(N([H])[H])=N1)N([H])C(=O)OC([H])([H])[H])N([H])[H])=NN2C([H])([H])C1=C([H])C([H])=C([H])C([H])=C1F
|
| InChi Key |
QZFHIXARHDBPBY-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C19H16F2N8O2/c1-31-19(30)25-14-15(22)26-17(27-16(14)23)13-11-6-10(20)7-24-18(11)29(28-13)8-9-4-2-3-5-12(9)21/h2-7H,8H2,1H3,(H,25,30)(H4,22,23,26,27)
|
| 化学名 |
methyl N-[4,6-diamino-2-[5-fluoro-1-[(2-fluorophenyl)methyl]pyrazolo[3,4-b]pyridin-3-yl]pyrimidin-5-yl]carbamate
|
| 别名 |
Vericiguat; BAY1021189; BAY-10-21189; BAY10-21189; BAY 1021189; BAY-1021189; Verquvo; Methyl (4,6-diamino-2-(5-fluoro-1-(2-fluorobenzyl)-1H-pyrazolo[3,4-b]pyridin-3-yl)pyrimidin-5-yl)carbamate; MK-1242; BAY-1021189; Vericiguat [INN]; UNII-LV66ADM269; BAY 10-21189
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 60~85 mg/mL (140.7~199.4 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.86 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80+,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.3453 mL | 11.7266 mL | 23.4533 mL | |
| 5 mM | 0.4691 mL | 2.3453 mL | 4.6907 mL | |
| 10 mM | 0.2345 mL | 1.1727 mL | 2.3453 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。