| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
β adrenergic receptor
- The primary target of Vilanterol is the human β₂-adrenoceptor (β₂-AR). In vitro binding assays show a Ki value of 0.017 nM for human β₂-AR, and in functional assays (cAMP production in CHO cells expressing human β₂-AR), it has an EC₅₀ of 0.12 nM [1] - Based on structure-activity relationship (SAR) studies, Vilanterol exhibits potent β₂-AR agonist activity with an EC₅₀ range of 0.08–0.15 nM in CHO cells expressing human β₂-AR, and >1000-fold selectivity over β₁-AR and β₃-AR (EC₅₀ for β₁-AR > 100 nM, β₃-AR > 100 nM) [5] - In human bronchial smooth muscle cells, Vilanterol induces bronchorelaxation by activating β₂-AR, with an EC₅₀ of 0.1 nM for inhibiting acetylcholine-induced bronchoconstriction [3] |
|---|---|
| 体外研究 (In Vitro) |
维兰特罗对 β2-AR 相对于其他 β-AR 受体亚型(β2 和 β3)的选择性是通过测试维兰特罗在表达人 β1-、β2- 和 β3 的 CHO 细胞中引起浓度依赖性 cAMP 增加的能力来确定的-AR。 Vilanterol 被证明对 β2-AR 具有高度选择性,其选择性比 β2- 和 β3-AR 亚型至少高 1000 倍。该分析结果表明,在 Gpp(NH)p 存在的情况下,[3H]Vilanterol 的低亲和力 pKD 为 9.44±0.07 (n=4),高亲和力 pKD 为 10.82±0.12 (n=4),低亲和力 pKD 为 10.82±0.12 (n=4)。在没有 Gpp(NH)p 的情况下,亲和力 pKD 9.47±0.17 (n=4)。此外,在不存在 Gpp(NH)p (37°C) 的情况下,观察到 [3H]Vilanterol 的低亲和力 pKD 为 9.52±0.24 (n=4)[1]。三芬那酯维兰特罗是一种新型吸入长效 β2 激动剂,在体外具有固有的 24 小时活性,正在开发中与吸入皮质类固醇糠酸氟替卡松联合治疗慢性阻塞性肺病和哮喘[2]。维兰特罗是一种新型长效 β2 激动剂 (LABA),具有固有的 24 小时活性,用于每日一次临床治疗慢性阻塞性肺疾病 (COPD) 和哮喘,与吸入型新型皮质类固醇糠酸氟替卡松联合使用,同样具有 24 小时活性[3]。
- 维兰特罗(Vilanterol)强效激活β₂-AR以刺激cAMP生成。在稳定表达人β₂-AR的CHO细胞中,用维兰特罗(0.01–10 nM)处理30分钟,可剂量依赖性诱导cAMP蓄积,EC₅₀为0.12 nM;最大反应达到完全激动剂异丙肾上腺素的95% [1] - 维兰特罗(Vilanterol)具有长效β₂-AR激活特性。在β₂-AR结合解离实验中,维兰特罗从人β₂-AR上的解离半衰期(t₁/₂)为7.5小时,而参考长效β₂激动剂(LABA)沙美特罗的解离半衰期仅为1.2小时 [1] - 维兰特罗(Vilanterol)与人umeclidinium(毒蕈碱拮抗剂)协同舒张人支气管。在离体人支气管环中,维兰特罗(0.01–0.1 nM)与umeclidinium(0.1–1 nM)联合处理,对乙酰胆碱诱导的收缩的舒张效果(最大舒张率85–90%)显著高于单独用药(维兰特罗单独用药60–65%,umeclidinium单独用药55–60%)[2] - 维兰特罗(Vilanterol)可经代谢失活以降低全身活性。在人肝微粒体中,维兰特罗被CYP3A4快速代谢为无活性代谢产物(M1、M2),代谢清除率为150 μL/min/mg蛋白,未检测到活性代谢产物 [4,5] |
| 体内研究 (In Vivo) |
化合物13f(维拉托醇)在体外具有高效力、选择性、起效快和作用持续时间长,并且被发现在体内持续时间长、在大鼠中口服生物利用度低,并且被快速代谢。13f(维拉托醇)的结晶盐被鉴定为具有适合吸入给药的性质[5]。
- 在健康受试者中,吸入维兰特罗(Vilanterol)(10–50 μg)可剂量依赖性舒张支气管:给药后1小时,第1秒用力呼气容积(FEV₁)较基线增加15–25%,效果持续24小时(24小时时FEV₁仍较基线高10–15%)[3] - 在哮喘或慢性阻塞性肺疾病(COPD)患者中,吸入维兰特罗(Vilanterol)(25 μg,每日1次)可改善肺功能:治疗2周时FEV₁增加200–300 mL,24小时支气管舒张效果维持12周,无快速减敏(疗效丧失)迹象 [3] - 在卵清蛋白诱导的过敏性气道收缩豚鼠模型中,吸入维兰特罗(Vilanterol)(0.01–1 μg/kg)可剂量依赖性降低气道阻力40–70%,效果持续>24小时;治疗剂量下未观察到心率显著升高(β₁-AR介导的副作用)[1] |
| 酶活实验 |
对于 [ 3 H]Vilanterol,进行了涉及饱和、缔合和解离的结合动力学研究,以计算平衡解离常数 (KD)、受体总数 ( Bmax)、结合率 (kon) 和解离率 (koff)。将膜与浓度逐渐增加的 [ 3 H]Vilanterol (0.01-1.3 nM) 一起孵育 5 小时以实现饱和结合(体积为 1.4 mL,以防止配体耗尽)。过滤前将膜与不同浓度的 [ 3 H]Vilanterol (0.1-1.9 nM) 一起孵育长达 1 小时,以促进缔合结合。将膜与固定浓度的 [ 3 H]Vilanterol (1.1 nM) 预孵育 1 小时,以促进解离结合。然后通过在结合缓冲液(10 μM 冷维兰特罗)中稀释来触发解离,并在过滤前继续孵育不同的时间长达 8 小时。与 [ 3 H]Vilanterol 一样,[ 3 H]CGP12177 也可实现饱和结合(浓度升至约 0.01-2.8 nM)。竞争性结合置换研究,其中将膜与固定浓度的 [ 3 H]Vilanterol (0.2 nM) 和浓度不断增加的未标记激动剂/拮抗剂一起孵育 5 小时,然后过滤,以确定β2-AR激动剂和拮抗剂的亲和力。为了保证结合曲线是单相的,在完成所有竞争结合置换研究期间存在 100 µM Gpp(NH)p [1]。
- β₂-AR结合实验: 1. 从表达人β₂-AR的CHO细胞中制备细胞膜,用结合缓冲液(Tris-HCl、MgCl₂、EDTA)重悬至10 μg蛋白/孔。 2. 向细胞膜中加入系列稀释的维兰特罗(Vilanterol)(0.001–10 nM)和0.1 nM [³H]-二氢阿普洛尔([³H]-DHA,β-AR放射性配体),25°C孵育1小时。 3. 通过预浸泡在结合缓冲液中的玻璃纤维滤膜过滤,分离结合态与游离态[³H]-DHA,用冰浴缓冲液洗涤3次。 4. 液体闪烁计数器检测放射性,用Cheng-Prusoff方程计算Ki值,非特异性结合由1 μM普萘洛尔定义 [1] - CYP3A4代谢实验: 1. 在反应缓冲液(Tris-HCl、MgCl₂、NADPH)中,将维兰特罗(Vilanterol)(1 μM)与人肝微粒体(0.5 mg蛋白/mL)在37°C下孵育。 2. 在0、5、10、20、30分钟时收集样本,用含内标的乙腈终止反应。 3. 10,000 × g离心10分钟,上清液注入LC-MS/MS定量剩余的维兰特罗。 4. 以维兰特罗浓度对数对时间作图,通过斜率计算消除速率,进而得到代谢清除率 [4] |
| 细胞实验 |
DiscoveRx cAMP(全细胞)肾上腺素能β1、β2和β3激动剂测定[5]
HitHunter DiscoveRx cAMP测定使用分裂酶互补读数来捕获整个细胞或从细胞膜产生的cAMP含量。测定中使用的分裂酶是β-半乳糖苷酶,通过发光读数进行测量。简言之,表达人β1、β2或β3的CHO细胞在室温下解冻,在PBS中稀释并离心。然后将细胞以(200万个细胞/mL)重悬于含有10µM IBMX的不含酚红的DMEM中。将20000个细胞加入含有受试化合物的384孔板中并孵育30-45分钟。根据HitHunter DiscoveRx试剂盒说明书测量cAMP含量。基本上,裂解细胞,并加入抗cAMP的抗体以及两个β-gal片段,一个与cAMP连接(酶供体),一个至19酶受体,形成活性酶。底物被活性酶水解,用于EFC检测(发光)β-gal活性。在Viewlux上读取之前,将最终测定混合物在室温下孵育以平衡3小时。将所有化合物以10mM的浓度溶解在DMSO中,并且对于所有测定,DMSO浓度在整个板上是恒定的。将所有数据标准化为每个板上16个高和16个低对照孔的平均值。然后对归一化数据进行四参数逻辑拟合,以确定pEC50和最大渐近线值。所引用的值为算术平均值±SEM。通过将试验化合物获得的最大渐近线比率除以异丙肾上腺素获得的最大渐近线比率来确定本征活性(IA)。内在活性的引用值是几何平均值以及95%置信下限和置信上限。通过从效力产生的β2 pEC50中减去β1或β3的pEC50来确定选择性比。 - CHO-β₂细胞cAMP实验: 1. 将表达人β₂-AR的CHO细胞接种于96孔板(5×10⁴细胞/孔),在DMEM + 10% FBS中培养过夜。 2. 更换为含0.1% BSA的无血清DMEM,加入系列稀释的维兰特罗(Vilanterol)(0.01–10 nM),37°C孵育30分钟。 3. 加入裂解缓冲液,使用HTRF cAMP试剂盒(激发波长320 nm,发射波长665 nm/620 nm)检测cAMP水平。 4. 用四参数逻辑模型拟合剂量-反应曲线,计算EC₅₀ [1] - 人支气管平滑肌细胞舒张实验: 1. 从供体肺中分离人支气管平滑肌细胞,在DMEM + 10% FBS中培养至融合。 2. 接种于24孔板,生长至80%融合后,无血清培养24小时。 3. 用维兰特罗(Vilanterol)(0.001–10 nM)预处理1小时,加入乙酰胆碱(1 μM)诱导收缩。 4. 图像分析软件测量细胞长度,舒张百分比计算公式:(收缩长度 - 处理后长度)/(收缩长度 - 基线长度)× 100% [3] |
| 动物实验 |
大鼠药代动力学研究。[5]
雄性Han Wistar大鼠(体重约250 g)在给药前禁食18小时。13f(维兰特罗)醋酸盐配制成DMSO-PEG 200-蒸馏水(10:30:60,v/v/v)溶液用于口服给药,配制成DMSO-生理盐水(10:90,v/v)溶液用于静脉给药。大鼠分别通过灌胃管口服或经尾静脉静脉注射给药,标称剂量分别为2 mg 13f碱基/kg和0.25 mg 13f碱基/kg。分别于给药后0.03小时(仅限静脉注射)、0.08小时、0.25小时、0.5小时、0.75小时、1小时、2小时、3小时(仅限口服)、4小时、6小时和8小时,通过心脏穿刺采集血样(每个时间点n=2只动物)。血液经离心分离制备血浆,并用液相色谱-质谱联用仪(LCMS/MS)分析血浆中13F的含量。采用非房室模型方法,根据血浆浓度-时间曲线计算药代动力学参数。 - 豚鼠过敏性气道收缩模型: 1. 于第0天和第7天,用卵清蛋白(100 μg,腹腔注射)致敏6-8周龄豚鼠。 2. 于第14天,用雾化卵清蛋白(1% w/v)激发以诱导气道收缩,并使用全身容积描记法测量基线气道阻力。 3. 通过气雾吸入给予维兰特罗(0.01-1 μg/kg)(溶于生理盐水,雾化时间5分钟);对照组接受生理盐水。 4. 分别于给药后1、6、12和24小时测量气道阻力;通过心电图记录心率以评估β₁-肾上腺素能受体(β₁-AR)的副作用[1] - 大鼠药代动力学模型: 1. 通过气管内滴注给予雄性Sprague-Dawley大鼠维兰特罗(0.1–1 μg/kg)(溶于0.9%生理盐水+0.1%吐温80)。 2. 分别于给药后0.083、0.25、0.5、1、2、4、8、12和24小时经尾静脉采集血样(0.2 mL),离心分离血浆。 3. 用乙酸乙酯从血浆中提取维兰特罗,并通过液相色谱-串联质谱法(LC-MS/MS)进行分析。 4. 使用以下方法计算药代动力学参数(Cmax、Tmax、AUC₀-∞、t₁/₂):非房室模型分析[4] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
维兰特罗血浆浓度可能无法预测治疗效果。健康受试者吸入维兰特罗后,血药浓度峰值 (Cmax) 出现在 5 至 15 分钟。吸入给药后,维兰特罗主要经肺部吸收,口服吸收的贡献可忽略不计。重复吸入维兰特罗后,14 天内达到稳态,药物累积量可达 1.7 倍。吸入给药时,维兰特罗的绝对生物利用度为 27.3%,这主要归因于吸入部分经肺部吸收。由于首过代谢广泛,吞咽部分的维兰特罗口服生物利用度较低 (<2%)。慢性阻塞性肺疾病 (COPD) 患者的全身暴露量 (AUC) 比健康受试者高 24%。哮喘患者的全身暴露量(AUC)比健康受试者低21%。 口服放射性标记的维兰特罗后,质量平衡显示70%的放射性标记物存在于尿液中,30%存在于粪便中。 对健康受试者进行静脉给药后,稳态平均分布容积为165升。 静脉给药后,维兰特罗的药代动力学显示其血浆清除率高达108升/小时。 代谢/代谢物 维兰特罗主要通过细胞色素P450 3A4 (CYP3A4)代谢为一系列代谢物,这些代谢物的β1和β2受体激动剂活性显著降低。主要的代谢途径是通过 O-脱烷基化,高达 78% 的回收剂量以 O-脱烷基化代谢物的形式消除,而 N-脱烷基化和 C-脱烷基化途径则较少,仅占回收剂量的 5%。 生物半衰期 多次吸入给药测定的维兰特罗有效半衰期为 11 小时。多次吸入 25 微克维兰特罗测定的血浆消除半衰期,在慢性阻塞性肺病 (COPD) 患者中为 21.3 小时,在哮喘患者中为 16.0 小时。单次吸入给药的血浆消除半衰期平均为 2.5 小时。 - 吸收:在人体内,吸入的维兰特罗主要在肺部吸收;由于在肺部和肝脏中广泛的首过代谢,其全身生物利用度低于 10%。血浆达峰时间(Tmax)为吸入后 10–20 分钟 [3,4] - 分布:维兰特罗在人体内的分布容积 (Vd) 为 120–150 L,表明其组织分布广泛。血浆蛋白结合率为 93%,无浓度依赖性结合(0.1–10 ng/mL)[4] - 代谢:维兰特罗主要通过 CYP3A4 在人体内代谢。主要代谢物(M1:羟基化衍生物,M2:O-去烷基化衍生物)无活性,不具有 β₂-肾上腺素能受体激动剂活性 [4,5] - 排泄:维兰特罗及其代谢物主要通过粪便(占剂量的 70–75%)和尿液(占剂量的 15–20%)排泄。人体血浆消除半衰期(t₁/₂)为2.5-3小时[4] |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期影响
◉ 哺乳期用药概述 虽然目前尚无关于哺乳期使用维兰特罗的公开数据,但相关药物特布他林的数据表明,预计极少量药物会分泌到母乳中。维兰特罗仅存在于复方制剂中,例如 Breo Ellipta 和 Anoro Ellipta。多篇综述的作者一致认为,由于吸入性支气管扩张剂的生物利用度低且用药后母体血清浓度低,因此哺乳期使用此类药物是可以接受的。出于类似原因,Breo Ellipta 和 Anoro Ellipta 等复方制剂可能也可接受。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白质结合 体外人血浆蛋白结合率平均为 94%。 - 在健康受试者中,吸入 Vilanterol(每日一次,每次 10–50 μg,持续 14 天)耐受性良好。不良事件较轻:震颤(5% 的受试者)、头痛(3%)和心悸(1%);肝功能(ALT、AST)或肾功能(BUN、肌酐)无显著变化[3] - 体外试验中,维兰特罗在Ames试验或染色体畸变试验中未显示遗传毒性。在大鼠中,重复吸入剂量(高达10 μg/kg/天,持续28天)未引起肺、心、肝或肾脏的组织病理学改变[4] - 维兰特罗的药物相互作用可能性极低。与CYP3A4抑制剂(例如酮康唑)合用可使血浆维兰特罗AUC增加2倍,但由于全身暴露量低,无需调整剂量[4] |
| 参考文献 |
[5]. Synthesis and structure-activity relationships of long-acting beta2 adrenergic receptor agonists incorporating metabolic inactivation: an antedrug approach. J Med Chem . 2010 Jun 10;53(11):4522-30. doi: 10.1021/jm100326d.
|
| 其他信息 |
维兰特罗是一种二氯苯衍生物,以三苯甲酸盐的形式用于治疗慢性阻塞性肺疾病(COPD)。它是一种β-肾上腺素能激动剂和支气管扩张剂。它是一种醚类化合物,属于仲氨基化合物、苯甲醇类化合物、酚类化合物和二氯苯类化合物。它是维兰特罗(1+)的共轭碱。
维兰特罗是一种选择性长效β2-肾上腺素能激动剂(LABA),具有24小时的固有活性,可用于每日一次治疗COPD和哮喘。这是由于需要长效β2-肾上腺素能激动剂来克服患者依从性差(由于给药频率或给药方案复杂)的问题。维兰特罗的设计基于沙美特罗的分子骨架,特别是作为沙美特罗的类似物,通过修饰沙美特罗分子生成具有(R)-构型的同手性化合物。维兰特罗对β2肾上腺素能受体的选择性分别比对β1和β3肾上腺素能受体高1000倍和400倍,且起效速度比沙美特罗更快。此外,维兰特罗的作用持续时间也显著长于沙美特罗,其支气管扩张作用可持续22小时。维兰特罗的药理作用归因于其对细胞内腺苷酸环化酶的刺激,该酶催化三磷酸腺苷(ATP)转化为环磷酸腺苷(cAMP)。环磷酸腺苷(cAMP)水平升高与支气管平滑肌松弛和抑制肺部肥大细胞释放超敏反应介质有关。维兰特罗已获准用于多种复方制剂,例如与糠酸氟替卡松联合使用(商品名:BREO ELLIPTA)、与溴化乌美溴铵联合使用(商品名:ANORO ELLIPTA)以及与糠酸氟替卡松和溴化乌美溴铵联合使用(商品名:TRELEGY ELLIPTA)。 BREO ELLIPTA 是首个获得 FDA 批准的含维兰特罗产品,于 2013 年 5 月获批,随后是 ANORO ELLIPTA(2013 年 12 月)和 TRELEGY ELLIPTA(2020 年 9 月)。虽然这三种产品均获批用于慢性阻塞性肺疾病 (COPD) 的维持治疗,但只有 TRELEGY ELLIPTA 和 BREO ELLIPTA 分别获批用于 18 岁及以上和 5 岁及以上患者的哮喘维持治疗。 维兰特罗是一种 β2 肾上腺素能激动剂。维兰特罗的作用机制是作为 β2 肾上腺素能激动剂。 维兰特罗是一种长效 β2 肾上腺素能激动剂,具有支气管扩张作用。给药后,维兰特罗可刺激肺部β2肾上腺素能受体,从而激活腺苷酸环化酶,催化三磷酸腺苷 (ATP) 转化为环磷酸腺苷 (cAMP)。cAMP 浓度升高可舒张支气管平滑肌,缓解支气管痉挛,并减少炎症细胞介质的释放,尤其是肥大细胞的炎症介质释放。 药物适应症 维兰特罗获准用于多种复方制剂,例如与糠酸氟替卡松联合使用(商品名:Breo Ellipta),与溴化乌美溴铵联合使用(商品名:Anoro Ellipta),以及与糠酸氟替卡松和溴化乌美溴铵联合使用(商品名:Trelegy Ellipta)。 Breo Ellipta 于 2013 年获得 FDA 批准,适用于 COPD 患者(包括慢性支气管炎和肺气肿)气流阻塞的长期每日一次维持治疗,以及 18 岁及以上可逆性阻塞性气道疾病患者的每日一次哮喘维持治疗。Anoro Ellipta 适用于 COPD 患者的维持治疗,Trelegy Ellipta 适用于 COPD 患者的维持治疗以及 18 岁及以上患者的哮喘维持治疗。 FDA 标签 作用机制 维兰特罗是一种选择性长效 β2-肾上腺素能激动剂。其药理作用归因于刺激细胞内腺苷酸环化酶,该酶催化三磷酸腺苷 (ATP) 转化为环磷酸腺苷 (cAMP)。环磷酸腺苷 (cAMP) 水平升高与支气管平滑肌松弛和肺部肥大细胞释放超敏反应介质的抑制有关。 - 维兰特罗 是一种新型长效β₂-肾上腺素能受体激动剂 (LABA),设计用于每日一次吸入给药,适用于哮喘和慢性阻塞性肺疾病 (COPD) 的维持治疗 [1,3] - 维兰特罗 的长效特性归因于其与β₂-肾上腺素能受体 (β₂-AR) 的缓慢解离(解离半衰期 t₁/₂ = 7.5 小时),从而将支气管扩张作用延长至 24 小时 [1] - 维兰特罗 采用代谢失活设计(前药策略):经 CYP3A4 快速代谢产生无活性代谢物,从而减少全身性 β₁-AR 介导的副作用(例如心动过速)。 [5] 维兰特罗常与长效毒蕈碱受体拮抗剂乌美溴铵(LAMA)联合用于治疗慢性阻塞性肺疾病(COPD),因为它们的协同支气管舒张作用比单药治疗更能改善肺功能[2] |
| 分子式 |
C₂₄H₃₃CL₂NO₅
|
|---|---|
| 分子量 |
486.43
|
| 精确质量 |
485.173
|
| 元素分析 |
C, 59.26; H, 6.84; Cl, 14.58; N, 2.88; O, 16.45
|
| CAS号 |
503068-34-6
|
| 相关CAS号 |
Vilanterol trifenatate; 503070-58-4; 503068-34-6; 503070-59-5 (cinnamate)
|
| PubChem CID |
10184665
|
| 外观&性状 |
Light yellow to yellow ointment
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
646.7±55.0 °C at 760 mmHg
|
| 闪点 |
344.9±31.5 °C
|
| 蒸汽压 |
0.0±2.0 mmHg at 25°C
|
| 折射率 |
1.579
|
| LogP |
2.97
|
| tPSA |
91.18
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
16
|
| 重原子数目 |
32
|
| 分子复杂度/Complexity |
466
|
| 定义原子立体中心数目 |
1
|
| SMILES |
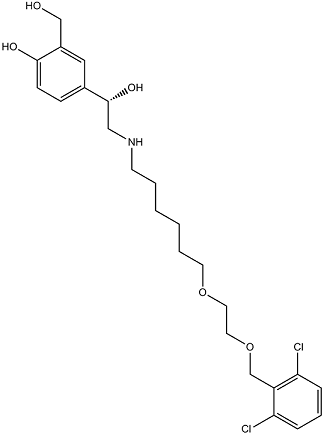
OC1=CC=C([C@@H](O)CNCCCCCCOCCOCC2=C(Cl)C=CC=C2Cl)C=C1CO
|
| InChi Key |
DAFYYTQWSAWIGS-DEOSSOPVSA-N
|
| InChi Code |
InChI=1S/C24H33Cl2NO5/c25-21-6-5-7-22(26)20(21)17-32-13-12-31-11-4-2-1-3-10-27-15-24(30)18-8-9-23(29)19(14-18)16-28/h5-9,14,24,27-30H,1-4,10-13,15-17H2/t24-/m0/s1
|
| 化学名 |
4-[(1R)-2-[6-[2-[(2,6-dichlorophenyl)methoxy]ethoxy]hexylamino]-1-hydroxyethyl]-2-(hydroxymethyl)phenol
|
| 别名 |
GW642444; GW-642444; GW 642444-X; GW642444; GW-642444; GW 642444; XGW 642444X
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
May dissolve in DMSO (in most cases), if not, try other solvents such as H2O, Ethanol, or DMF with a minute amount of products to avoid loss of samples
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.14 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (5.14 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.14 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0558 mL | 10.2790 mL | 20.5579 mL | |
| 5 mM | 0.4112 mL | 2.0558 mL | 4.1116 mL | |
| 10 mM | 0.2056 mL | 1.0279 mL | 2.0558 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT06066606 | Recruiting | Drug: Placebo Drug: Vilanterol and Fluticasone Furoate (low dose) Drug: Vilanterol and Fluticasone Furoate (high dose) |
Exercise Performance | Morten Hostrup, PhD | October 5, 2023 | Not Applicable |
| NCT04522596 | Recruiting | Drug: Umeclidinium/vilanterol Other: Placebo |
Copd Heart Failure |
Luis Puente Maestu | May 21, 2021 | Phase 4 |
| NCT04536675 | Completed | Drug: Placebo Drug: Vilanterol and Umeclidinium Bromide |
Non Small Cell Lung Cancer Chronic Obstructive Pulmonary Disease |
Samsung Medical Center | April 1, 2021 | Phase 3 |
| NCT04265105 | Completed | Drug: fluticasone-vilanterol Drug: Standard Preparation |
Asthma | Royal College of Surgeons in Ireland - Medical University of Bahrain |
December 22, 2021 | Phase 2 Phase 3 |
| NCT03315000 | Completed | Drug: Fluticasone Furoate Drug: Placebos |
Asthma | University of Saskatchewan | October 13, 2017 | Phase 4 |