| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 体外研究 (In Vitro) |
AIM-100(2-10 μM;48 小时)通过阻断 AKT 酪氨酸磷酸化和 Ack1 激活,导致细胞周期停滞在 G1 期。除了 Ack1/AKT Tyr 磷酸化之外,AIM-100 还可抑制源 Ack1 激活。 AIM-100 除了抑制 Ack1 激活之外,还抑制 AR Tyr267 磷酸化及其不稳定性,导致共济失调毛细血管扩张 (ATM)。雄激素受体 (AR) 与 PSA、NKX3.1 和 TMPRSS2 启动子的结合以及 AR 聚合活性均可被 AIM-100 抑制 [3]。它还可以阻止 pTyr267-AR 磷酸化。
|
|---|---|
| 体内研究 (In Vivo) |
AIM-100 (4 mg/kg) 降低杏仁核去势裸鼠中共济失调毛细血管扩张破裂 (ATM) 的表达,从而抑制去势抵抗性放射性去势肥胖癌 (CRPC) 异种移植肿瘤的形成 [2]。
|
| 动物实验 |
本研究采用雄性裸鼠(去势)进行异种移植研究。将LNCaP-caAck细胞(2×10⁶个细胞)悬浮于100 μL PBS中,并与100 μL Matrigel混合。将细胞悬液皮下注射至小鼠侧腹部。[2] 药物治疗方面,将AIM-100溶解于二甲基亚砜(DMSO)中,并以4 mg/kg体重/次的剂量进行腹腔注射(ip)。治疗方案从肿瘤细胞注射后第7天开始。小鼠分别于第7、11、15、19、23和27天接受共6次注射。每周使用游标卡尺测量两次肿瘤体积。[2] 在某些实验中,肿瘤细胞在注射到小鼠体内之前接受1.5 Gy的辐射照射。后续的药物治疗方案相同。 [2]实验结束时,处死小鼠,切除肿瘤,固定,石蜡包埋,切片进行免疫组织化学分析。[2]
|
| 参考文献 |
|
| 精确质量 |
371.163
|
|---|---|
| 元素分析 |
C, 74.37; H, 5.70; N, 11.31; O, 8.61
|
| CAS号 |
873305-35-2
|
| PubChem CID |
11501591
|
| 外观&性状 |
White to yellow solid powder
|
| LogP |
5.22
|
| tPSA |
60.18
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
492
|
| 定义原子立体中心数目 |
1
|
| SMILES |
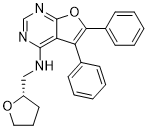
C1C[C@H](OC1)CNC2=C3C(=C(OC3=NC=N2)C4=CC=CC=C4)C5=CC=CC=C5
|
| InChi Key |
XNFHHOXCDUAYSR-SFHVURJKSA-N
|
| InChi Code |
InChI=1S/C23H21N3O2/c1-3-8-16(9-4-1)19-20-22(24-14-18-12-7-13-27-18)25-15-26-23(20)28-21(19)17-10-5-2-6-11-17/h1-6,8-11,15,18H,7,12-14H2,(H,24,25,26)/t18-/m0/s1
|
| 化学名 |
N-[[(2S)-oxolan-2-yl]methyl]-5,6-diphenylfuro[2,3-d]pyrimidin-4-amine
|
| 别名 |
AIM-100 AIM100 AIM 100
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~134.61 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.73 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.73 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.73 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT02022813 | COMPLETED | Dietary Supplement: Supplemental parenteral nutrition (SPN) | Critical Illness | Centre Hospitalier Universitaire Vaudois | 2014-04 | Not Applicable |
|
|