| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|

| 靶点 |
CTX-M-15(IC50=5 nM);TEM-1(IC50=8 nM )
β-lactamase enzymes (Serine class A and C) TEM-1 β-lactamase (IC50: 8 nM)[1] CTX-M-15 β-lactamase (IC50: 5 nM)[1] KPC-2 β-lactamase, Enterobacter cloacae P99 β-lactamase, Pseudomonas aeruginosa AmpC β-lactamase (Avibactam is described as a less potent inhibitor of KPC-2, P99, and AmpC compared to TEM-1 and CTX-M-15)[1] |
|---|---|
| 体外研究 (In Vitro) |
Avibactam (NXL104) 是一种几乎没有抗菌活性的分子,可抑制 A 类和 C 类 β-内酰胺酶。 Avibactam 可灭活除金属型和不动杆菌 OXA 碳青霉烯酶之外的最重要的 β-内酰胺酶 [2]。
- β-内酰胺酶抑制:Avibactam通过共价结合不可逆地占据A/C类β-内酰胺酶的活性位点,形成可逆的酰基酶中间体。对KPC-2的IC50为38 nM,对TEM-1为8 nM。这种抑制可恢复β-内酰胺类抗生素对耐药菌的活性[1,5] - 协同抗菌活性:与头孢他啶联用,Avibactam将产碳青霉烯酶肺炎克雷伯菌的MIC90从>256 mg/L(头孢他啶单用)降至8 mg/L(联用)。对表达CTX-M-15的大肠杆菌,MIC90从128 mg/L降至4 mg/L [4,5] - 突变体筛选:肠杆菌科细菌在头孢洛林+Avibactam压力下连续传代,筛选出孔蛋白突变体(如OmpC/F缺失)和β-内酰胺酶变异体(如TEM-1突变),对含Avibactam的联合用药MIC升高2–8倍[2] Avibactam是A类和C类丝氨酸β-内酰胺酶的共价、缓慢可逆抑制剂。它抑制模型酶TEM-1的表现二级失活速率常数大于1.6 x 10^5 M^-1 s^-1。从TEM-1解离的去酰化速率常数为0.045 min^-1,对应的驻留时间半衰期(t1/2)为16分钟。其抑制作用是可逆的,去酰化过程中再生完整的Avibactam分子,而非发生水解或不可逆重排。通过酰基-酶交换实验,该可逆酰化机制也在CTX-M-15、KPC-2、阴沟肠杆菌P99和铜绿假单胞菌AmpC酶中得到证实。[1] |
| 体内研究 (In Vivo) |
阿维巴坦钠表现出活性缓慢恢复,解离率为 0.045±0.022 min-1,转换为停留时间半衰期 (tt1/2) 为 16±8 分钟。测得的 Avibactam 解离速率表明,通过水解或可逆性发生缓慢脱酰作用,这与之前报道的 Avibactam 抑制 TEM-1 的极长 t1/2 值(>1 或 >7 d)形成对比[1]。 Avibactam 是一种新型有前景的 β-内酰胺酶抑制剂,可克服 β-内酰胺酶引起的耐药性。小鼠大腿或鼻内注射约 106 CFU 的铜绿假单胞菌,引起肺炎,并给予 8 种不同(单次)皮下剂量的头孢他啶和阿维巴坦,组合浓度范围为 1 至 128 mg/kg 体重增加 2 倍。头孢他啶末期血浆中的平均估计半衰期为 0.28 小时(SD,0.02 小时),阿维巴坦的平均估计半衰期为 0.24 小时(SD,0.04 小时)。分布体积分别为 0.80 升/千克(SD,0.14 升/千克)和 1.18 升/千克(SD,0.34 升/千克)[3]。
- 杀菌效力:在KPC-2阳性肺炎克雷伯菌感染的中性粒细胞减少小鼠模型中,单用头孢他啶(1024 mg/kg)疗效微弱(大腿菌落数4×10⁸–8×10⁸ CFU),而联用Avibactam(4:1比例)实现杀菌(菌落数2×10⁴–3×10⁴ CFU)。在大鼠腹腔脓肿模型中,联用治疗较单用头孢他啶减少细菌负荷6 log CFU/脓肿[4] - 药代动力学特征:小鼠体内Avibactam终末半衰期为0.24 ± 0.04小时,分布容积1.18 ± 0.34 L/kg,快速渗透至感染组织上皮衬液(ELF)。皮下注射64 mg/kg后,ELF浓度超过KPC-2 IC50(38 nM)的时间≥6小时[3,5] Avibactam与头孢洛林或头孢他啶联用,在临床前动物感染模型以及针对由革兰氏阴性菌引起的严重感染的II期临床试验中显示出疗效。[1] |
| 酶活实验 |
在 200 μL 反应体积中,将 1 μM TEM-1 在有或没有 5 μM Avibactam 的情况下在 37°C 下孵育 5 分钟,然后进行两个超滤柱 (UFC) 步骤以去除过量的抑制剂(带 Biomax 膜的 Ultrafree-0.5,5 -kDa 截止值)。在 4°C 下以 10,600×g 离心 8 分钟。每个超滤步骤后,用 180 μL 测定缓冲液稀释 20 μL 截留物,以恢复原始酶浓度。两次UFC处理后,通过液相色谱/MS/MS对游离阿维巴坦的量进行定量,发现其<原始浓度的5%。通过测量酰基酶样品中的 TEM-1 活性(稀释 4,000 倍)与未经 UFC 处理的酶进行比较来评估 UFC 期间的蛋白质损失,发现损失<5%[1]。
酰化动力学测定: 使用常规光谱和停流光谱法研究Avibactam对TEM-1 β-内酰胺酶的抑制起始过程。通过将TEM-1酶加入到含有硝基头孢菌素底物及Avibactam(或不存在)的溶液中启动反应。通过在460或490 nm处连续测量吸光度来监测酶活性。在不同Avibactam浓度下,测定形成被抑制酶的观测准一级速率常数(k_obs)。将数据拟合到两步可逆抑制模型,以推导酶失活的表现二级速率常数。[1] 去酰化速率测定: 使用跳跃稀释法测量Avibactam抑制后TEM-1酶活性恢复的速率常数。将酶(1 µM)与抑制剂(5 µM Avibactam)在37°C下孵育5分钟以形成酰基-酶复合物(EI)。然后将该复合物在测定缓冲液中稀释4000倍。通过加入硝基头孢菌素并在微孔板读数器中于490 nm处连续监测吸光度来跟踪酶活性的恢复。将数据拟合方程以获得去酰化速率常数(k_off)。[1] 酰基-酶复合物的制备与分析: 为进行质谱和平衡研究,将TEM-1(1 µM)与Avibactam(5 µM)在37°C下孵育5分钟以制备共价酰基-酶复合物。使用具有分子量截留膜的离心超滤装置去除过量的游离抑制剂。在变性条件下仍保留酰基-酶加合物证实了其共价性质。通过将高浓度Avibactam与TEM-1孵育24小时,并通过¹H NMR光谱和质谱分析混合物,确认了不存在水解,仅检测到完整的Avibactam。[1] 平衡与酰基-酶交换研究: 为证明可逆抑制,将制备的酰基-TEM-1复合物(EI)进行系列稀释并使其平衡。使用蛋白质质谱、酶活性测定和小分子质谱法测量平衡时酰基-酶、游离酶和游离抑制剂的比例。此外,进行了酰基-酶转移实验。例如,将酰化的TEM-1与未结合的CTX-M-15酶混合。通过质谱监测Avibactam部分从TEM-1到CTX-M-15的时间依赖性转移,表明完整的Avibactam被释放并重新酰化另一个酶分子。[1] |
| 细胞实验 |
将过夜肉汤培养的细胞 (~109 cfu) 铺在补充有 (i) 1-16 倍 MIC 的头孢洛林加阿维巴坦 (1 或 4 mg/L) 或 (ii) 1 或 4 的头孢洛林的 Mueller-Hinton 琼脂上。 mg/L 加阿维巴坦,浓度为 1-8 倍,可将头孢洛林 MIC 降低至 1 或 4 mg/L。过夜孵育后对菌落进行计数并保留代表[2]。
采用微量稀释肉汤法测定最小抑菌浓度(MIC)。对16株KPC-2菌株和1株OXA-232产碳青霉烯酶肺炎克雷伯菌进行了不同浓度头孢他啶-阿维巴坦的时间杀伤曲线测定。采用棋盘法测定头孢他啶-阿维巴坦联合氨曲南对28株NDM和2株NDM联用产碳青霉烯酶的肺炎克雷伯菌的体外增效杀菌效果。根据计算等级,选择具有协同杀菌作用的药物作为抑菌浓度指标。对其中12株菌株进行头孢他啶-阿维巴坦联合氨曲南的体外杀菌试验。[3] 目的:头孢他林+阿维巴坦(NXL104)是一种具有a类和C类肠杆菌科β-内酰胺酶活性的新型联合抑制剂。我们调查了其突变抗性的风险。 方法:利用广谱β-内酰胺酶(ESBLs)、AmpC β-内酰胺酶和KPC β-内酰胺酶从肠杆菌科中寻找单步和多步突变体并对其进行鉴定。 结果:头孢他林+阿维巴坦MIC倍数低的琼脂上发生过生长,但单步突变的频率<10(-9)。大多数突变体是不稳定的,只有三个在继代培养中仍然具有抗性。首先,从CTX-M-15阳性的大肠杆菌中,头孢他林+阿维巴坦的MIC升高,但生物体对头孢他林的抗性降低,对其他氧亚胺-头孢菌素的抗性丧失,当突变体bla(CTX-M-15)克隆到大肠杆菌DH5α时,这种情况仍然存在。测序鉴定出CTX-M-15变异中Lys237Gln的替换。另外两个稳定的单步突变体来自ampc低表达的阴沟肠杆菌菌株;这些对其他β-内酰胺的抗性没有改变或略有降低。两者都从AmpC的Ω环中删除了213-226氨基酸。从AmpC诱导和抑制的大肠杆菌中,通过多步选择获得了稳定的突变体,这些突变体不同程度地降低了AmpC和OmpF的表达,以及/或AmpC中Asn366His/Ile的替换。 结论:稳定的耐药突变体难以选择。AmpC-抑制的大肠杆菌有孔蛋白丢失或AmpC改变,包括Ω环缺失。CTX-M-15中的Lys237Gln替代产生了抗性,但在很大程度上消除了ESBL活性。[2] |
| 动物实验 |
动物模型:6周龄BALB/c小鼠(雌性),肺炎克雷伯菌Y8株感染模型[4]
剂量:0.375 mg/g,与头孢他啶联合使用 给药途径:感染后4小时开始,每8小时皮下注射一次,持续10天 结果:感染组小鼠4天内死亡70%,PBS组小鼠13天内全部死亡。感染后每8小时给予抗生素,持续10天,治疗组小鼠全部存活;然而,停止抗生素治疗后,对照组小鼠4天内全部死亡。与感染组相比,治疗组小鼠肝脏和脾脏的菌落形成单位(CFU)计数降低。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
阿维巴坦和头孢他啶主要经肾脏排泄。 阿维巴坦和头孢他啶的稳态分布容积分别为22.2升和17升。 阿维巴坦和头孢他啶的清除率分别为约12升/小时和约7升/小时。 代谢/代谢物 在人肝脏制剂中未观察到阿维巴坦的代谢。未代谢的阿维巴坦是人血浆和尿液中主要的药物相关成分。 80-90% 的头孢他啶以原形排出体外。 生物半衰期 头孢他啶-阿维巴坦的半衰期约为 2.7-3.0 小时。 阿维巴坦从 TEM-1 β-内酰胺酶上的脱酰基速率为 0.045 min⁻¹,对应于酶-抑制剂复合物的停留时间半衰期 (t₁/₂) 为 16 分钟。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
5.7%-8.2% 的阿维巴坦与血浆蛋白结合,而头孢他啶的蛋白质结合率低于 10%。 |
| 参考文献 |
|
| 其他信息 |
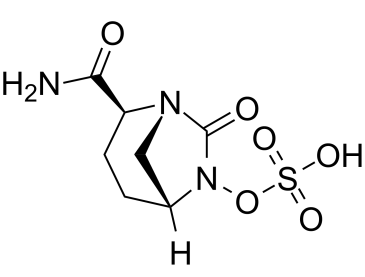
阿维巴坦(Avibactam)属于氮杂双环烷类化合物,其化学名称为(2S,5R)-7-氧代-1,6-二氮杂双环[3.2.1]辛烷-2-甲酰胺,其中6位氨基氢被磺氧基取代。它以钠盐形式与头孢他啶五水合物联合使用,用于治疗包括肾盂肾炎在内的复杂性尿路感染。阿维巴坦具有抗菌、抗微生物和抑制β-内酰胺酶(EC 3.5.2.6)的作用。它是一种单羧酸酰胺,属于脲类化合物、氮杂双环烷类化合物和羟胺O-磺酸类化合物。它是阿维巴坦(1-)的共轭酸。
阿维巴坦是一种非β-内酰胺类β-内酰胺酶抑制剂,可与头孢他啶(Avycaz)联合使用。该组合于2015年2月25日获得FDA批准,用于与甲硝唑联合治疗复杂性腹腔内感染,以及治疗复杂性泌尿道感染,包括由耐药病原体(包括多重耐药革兰氏阴性菌)引起的肾盂肾炎。由于临床安全性和有效性数据有限,Avycaz应保留用于18岁以上且无其他治疗选择有限的患者。 阿维巴坦是一种β-内酰胺酶抑制剂。阿维巴坦的作用机制是作为β-内酰胺酶抑制剂。 药物适应症 AVYCAZ(头孢他啶-阿维巴坦)与甲硝唑联合使用,适用于治疗由以下敏感微生物引起的复杂性腹腔内感染:大肠杆菌、肺炎克雷伯菌、奇异变形杆菌、斯氏普罗维登斯菌、阴沟肠杆菌、产酸克雷伯菌和铜绿假单胞菌,适用于18岁及以上患者。 AVYCAZ 还适用于治疗由以下敏感微生物引起的复杂性尿路感染,包括肾盂肾炎:大肠杆菌、肺炎克雷伯菌、科氏柠檬酸杆菌、产气肠杆菌、阴沟肠杆菌、弗氏柠檬酸杆菌、变形杆菌属和铜绿假单胞菌,适用于 18 岁及以上患者。 FDA 标签 作用机制 阿维巴坦是一种非β-内酰胺类β-内酰胺酶抑制剂,它通过独特的共价可逆机制灭活某些β-内酰胺酶(Ambler A 类β-内酰胺酶,包括肺炎克雷伯菌碳青霉烯酶、Ambler C 类和某些 Ambler D 类β-内酰胺酶),并保护头孢他啶免受某些β-内酰胺酶的降解。阿维巴坦能迅速到达细菌周质空间,并达到足以恢复头孢他啶对耐头孢他啶、产生β-内酰胺酶菌株的活性的浓度。阿维巴坦不会降低头孢他啶对头孢他啶敏感菌的活性。 阿维巴坦是一种β-内酰胺酶抑制剂,目前正与β-内酰胺类药物联合用于治疗革兰氏阴性菌感染,并处于临床开发阶段。阿维巴坦属于一种不含β-内酰胺核心结构但能共价酰化其β-内酰胺酶靶标的结构类抑制剂。我们利用TEM-1酶,通过测定酰化反应的结合速率和脱酰化反应的解离速率来表征阿维巴坦的抑制作用。脱酰化反应的解离速率为0.045 min⁻¹,这使得我们能够研究TEM-1的脱酰化途径。我们利用核磁共振(NMR)和质谱(MS)证明,脱酰化是通过完整阿维巴坦的再生而非水解实现的。除TEM-1外,我们还发现另外四种具有临床意义的β-内酰胺酶在酰化后也能释放完整的阿维巴坦。我们发现阿维巴坦是一种共价的、缓慢可逆的抑制剂,这在β-内酰胺酶抑制剂中是一种独特的抑制机制。[1] 背景:近年来,耐碳青霉烯类肠杆菌科细菌(CRE)感染的发生率迅速上升。由于CRE菌株通常对大多数抗菌药物耐药,因此该感染患者的死亡率往往很高。这给临床感染管理带来了严峻的挑战。本研究旨在探讨头孢他啶-阿维巴坦单独使用或与氨曲南联合用药对产KPC或NDM碳青霉烯酶肺炎克雷伯菌的体外和体内杀菌活性,并探索针对其耐药菌株感染的新型临床治疗方案。[3] 方法:采用微量肉汤稀释法测定最小抑菌浓度(MIC)。对16株KPC-2型和1株OXA-232型碳青霉烯酶肺炎克雷伯菌进行不同浓度头孢他啶-阿维巴坦的时间-杀菌曲线试验。本研究采用棋盘格法,对28株NDM菌株和2株NDM合并KPC碳青霉烯酶肺炎克雷伯菌菌株,测定了头孢他啶-阿维巴坦联合氨曲南的体外协同杀菌作用。根据计算等级,筛选出具有协同杀菌作用的药物作为抑菌浓度指数(ICI)。对其中12株菌株进行了头孢他啶-阿维巴坦联合氨曲南的体外杀菌试验。在小鼠模型中,研究了头孢他啶-阿维巴坦对KPC碳青霉烯酶肺炎克雷伯菌Y8菌株感染的疗效。[3] 结果:时间-杀菌曲线试验表明,2MIC、4MIC和8MIC浓度的头孢他啶-阿维巴坦对耐药菌株均表现出显著的杀菌活性。然而,在28株NDM菌株和2株NDM合并KPC碳青霉烯酶肺炎克雷伯菌中,仅有7株对头孢他啶-阿维巴坦治疗敏感,MIC50和MIC90分别为64 mg/L和256 mg/L。头孢他啶-阿维巴坦联合氨曲南的抗菌药物敏感性试验显示,90%(27/30)的菌株中两种药物具有协同作用,3.3%(1/30)的菌株中具有相加作用,6.6%(2/30)的菌株中无明显作用。未发现拮抗作用。后续的杀菌试验也证实了上述结果。头孢他啶-阿维巴坦对小鼠肺炎克雷伯菌Y8株感染的治疗效果显示,感染组小鼠4天内死亡率达70%,13天内全部死亡。细菌载量检测结果显示,感染组和治疗组小鼠血液中的细菌数量无显著差异。然而,与感染组相比,治疗组小鼠脾脏和肝脏中的菌落形成单位(CFU)计数较低,表明头孢他啶-阿维巴坦对细菌具有显著的杀菌作用,并具有一定的治疗效果。[3] 结论:本研究表明,头孢他啶-阿维巴坦对产KPC-2和OXA-232碳青霉烯酶的肺炎克雷伯菌具有显著的杀菌作用。与氨曲南联用时,对产NDM碳青霉烯酶的肺炎克雷伯菌表现出更强的协同杀菌作用。[3] 阿维巴坦属于二氮杂双环辛烷(DBO)类非β-内酰胺类β-内酰胺酶抑制剂。其作用机制涉及β-内酰胺酶活性位点丝氨酸的共价可逆酰化,形成氨甲酰-酰基-酶中间体。与经典的β-内酰胺类抑制剂不同,阿维巴坦的脱酰化是通过分子内环化反应再生完整的抑制剂,而非水解。这种独特的可逆机制使得单个抑制剂分子能够潜在地灭活多个酶分子。 阿维巴坦目前正处于临床开发阶段(截至本文发表时为II期和III期),与头孢曲林和头孢他啶联合用于治疗严重的革兰氏阴性菌感染。[1] |
| 分子式 |
C7H11N3O6S
|
|---|---|
| 分子量 |
265.24374
|
| 精确质量 |
265.036
|
| 元素分析 |
C, 31.70; H, 4.18; N, 15.84; O, 36.19; S, 12.09
|
| CAS号 |
1192500-31-4
|
| 相关CAS号 |
Avibactam sodium;1192491-61-4;Avibactam sodium hydrate;2938989-90-1;Avibactam sodium dihydrate
|
| PubChem CID |
9835049
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.9±0.1 g/cm3
|
| 折射率 |
1.679
|
| LogP |
-3.2
|
| tPSA |
139.61
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
17
|
| 分子复杂度/Complexity |
457
|
| 定义原子立体中心数目 |
2
|
| SMILES |
O=S(ON1[C@]2([H])CC[C@@H](C(N)=O)[N@@](C2)C1=O)(O)=O
|
| InChi Key |
NDCUAPJVLWFHHB-UHNVWZDZSA-N
|
| InChi Code |
InChI=1S/C7H11N3O6S/c8-6(11)5-2-1-4-3-9(5)7(12)10(4)16-17(13,14)15/h4-5H,1-3H2,(H2,8,11)(H,13,14,15)/t4-,5+/m1/s1
|
| 化学名 |
(2S,5R)-2-carbamoyl-7-oxo-1,6-diazabicyclo[3.2.1]octan-6-yl hydrogen sulfate
|
| 别名 |
Avibactam Free Acid; NXL-104; NXL104; Avibactam; 1192500-31-4; Avibactam free acid; AVE-1330A free acid; Avibactam (free acid); Nxl-104 free acid; [(2S,5R)-2-carbamoyl-7-oxo-1,6-diazabicyclo[3.2.1]octan-6-yl] hydrogen sulfate; NXL 104
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~125 mg/mL (~471.27 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (7.84 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (7.84 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (7.84 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.7702 mL | 18.8509 mL | 37.7017 mL | |
| 5 mM | 0.7540 mL | 3.7702 mL | 7.5403 mL | |
| 10 mM | 0.3770 mL | 1.8851 mL | 3.7702 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT01689207
Conditions:Complicated Infection|Bacterial InfectionsLink: https://clinicaltrials.gov/ct2/show/NCT01291602
Conditions:Healthy Male and Female Japanese VolunteersLink: https://clinicaltrials.gov/ct2/show/NCT01290900
Conditions:Healthy Male Volunteers
Title:A Study to Assess the Levels of Two Antibiotics in the Blood When Given Together and Separately
Status:Completed
updateDate:2017-09-01
Ctid:NCT01430910
Link: https://clinicaltrials.gov/ct2/show/NCT01430910
Conditions:HealthyLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2014-003244-13
Condition:Complicated urinary tract infectionsLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2011-003895-35
Condition:Complicated Intra-Abdominal Infection (cIAI)Link: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2011-003893-97
Condition:Complicated Intra-Abdominal Infection (cIAI)Link: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2010-022487-12
Condition:Complicated Urinary Tract InfectionLink: https://www.clinicaltrialsregister.eu/ctr-search/search?query=2008-005604-54
Condition:Complicated intra-abdominal infections (cIAI) in hospitalised adults
|
|
|
|