| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
描述:阿维巴坦(NXL-104;NXL104;Avycaz)是一种共价/可逆的非β-内酰胺类β-内酰胺酶抑制剂,于2015年2月25日获得美国食品药品监督管理局(FDA)批准,可与头孢他啶联合用于治疗细菌感染,包括由多重耐药革兰氏阴性菌引起的感染。它对β-内酰胺酶TEM-1和CTX-M-15的IC50值分别为8 nM和5 nM。
| 靶点 |
CTX-M-15(IC50=5 nM);TEM-1(IC50=8 nM )
- Class A and C β-lactamases (e.g., TEM-1, CTX-M-15, KPC-2). IC50 values: 8 nM (TEM-1), 5 nM (CTX-M-15), 38 nM (KPC-2) - Class D β-lactamases (partial inhibition, e.g., OXA-232) [4] Avibactam is a covalent, reversible, non-β-lactam β-lactamase inhibitor that targets serine β-lactamases. It acylates the active-site serine residue of class A and C β-lactamases. [1] |
|---|---|
| 体外研究 (In Vitro) |
阿维巴坦的抗菌活性较低,它能抑制A类和C类β-内酰胺酶,但不能抑制金属型β-内酰胺酶或不动杆菌OXA碳青霉烯酶[2]。
头孢他啶-阿维巴坦(0-256 mg/L)的MIC50和MIC90均为8 mg/L,可抑制16株blaKPC-2阳性和1株blaOXA-232阳性肺炎克雷伯菌的生长[4]。 - β-内酰胺酶抑制:阿维巴坦通过共价相互作用与A/C类β-内酰胺酶的活性位点不可逆地结合,形成可逆的酰基-酶中间体。对于KPC-2,IC50 = 38 nM;对于TEM-1,IC50 = 8 nM。这种抑制作用可恢复β-内酰胺类抗生素对耐药菌的活性[1,5] - 协同抗菌活性:阿维巴坦与头孢他啶联用时,可将产碳青霉烯酶肺炎克雷伯菌的MIC90从>256 mg/L(单独使用头孢他啶)降低至8 mg/L(联用)。对于表达CTX-M-15的大肠杆菌,MIC90从128 mg/L降低至4 mg/L[4,5] - 突变体筛选:用头孢洛林+阿维巴坦连续传代肠杆菌科细菌,筛选出对阿维巴坦敏感性降低的孔蛋白突变体(例如,OmpC/F缺失)和β-内酰胺酶变体(例如,TEM-1突变)。这些突变体对含阿维巴坦的组合表现出2至8倍更高的MIC值[2] 阿维巴坦抑制TEM-1 β-内酰胺酶,其表观二级失活速率常数>1.6 × 10⁵ M⁻¹·s⁻¹(由kobs与抑制剂浓度的斜率确定)[1] -阿维巴坦从TEM-1脱酰基解离的速率常数(koff)为0.045 ± 0.022 min⁻¹,对应的半衰期(t₁/₂)为16 ± 8 min[1] -在跳跃稀释试验中,与克拉维酸和他唑巴坦相比,阿维巴坦对TEM-1活性的恢复较慢。 [1] 核磁共振 (NMR) 和质谱 (MS) 分析表明,阿维巴坦与 TEM-1 在 37°C 下孵育 24 小时后仍保持完整,未检测到水解(损失 <5%,半衰期 >14 天)。[1] 变性后 TEM-1 的质谱分析证实了阿维巴坦对其的共价酰化作用。[1] 平衡滴定实验表明,阿维巴坦与 TEM-1 形成的酰基-酶复合物 (EI) 解离,释放出完整的阿维巴坦,其平衡解离常数 Kd 为 2.1 ± 1.0 nM(通过蛋白质质谱、小分子质谱和酶活性测定)。[1] 等温滴定量热法 (ITC) 测得阿维巴坦与 TEM-1 结合的 Kd 为 3.3 ± 0.4 nM。 [1]酰基酶转移实验表明,阿维巴坦可以从酰化TEM-1转移至apo-CTX-M-15、KPC-2、阴沟肠杆菌P99和铜绿假单胞菌AmpC β-内酰胺酶,表明其在多种临床相关酶中发生可逆酰化。[1] |
| 体内研究 (In Vivo) |
头孢他啶-阿维巴坦(0.375 mg/g;皮下注射;每 8 小时一次,持续 10 天)对细菌有显著影响,并且在感染肺炎克雷伯菌 Y8 株的小鼠模型中显示出一定的治疗效果[3]。在肺部感染的中性粒细胞减少小鼠中,阿维巴坦(64 mg/kg;皮下注射;一次)在终末期血浆中的平均估计半衰期为 0.24 小时[3]。
- 杀菌功效:在感染表达 KPC-2 的肺炎克雷伯菌的中性粒细胞减少小鼠中,单独皮下注射头孢他啶(1024 mg/kg)的效果甚微(最终计数:4×10⁸–8×10⁸ CFU/大腿),而与阿维巴坦(4:1 比例)联合给药则达到杀菌活性(最终计数:2×10⁴–3×10⁴ CFU/大腿)。在大鼠腹部脓肿模型中,与单独使用头孢他啶相比,联合治疗使细菌负荷降低了 6 log CFU/脓肿 [4] - 药代动力学特征:在小鼠中,阿维巴坦的末端半衰期为 0.24 ± 0.04 小时,分布容积为 1.18 ± 0.34 L/kg,并能快速渗透到感染组织的上皮衬液 (ELF) 中。皮下注射(64 mg/kg)后,ELF 浓度超过 KPC-2 IC50 (38 nM) ≥6 小时 [3,5] 在由铜绿假单胞菌(头孢他啶 MIC 64 mg/L;头孢他啶-阿维巴坦 MIC 4 mg/L,其中阿维巴坦浓度为 4 mg/L)引起的大腿或肺部感染的中性粒细胞减少小鼠中,将阿维巴坦与不同剂量(每种化合物 1–128 mg/kg)的头孢他啶联合皮下注射。[3] - 药代动力学分析显示,阿维巴坦的血浆药代动力学呈线性且与剂量成正比,与感染类型(大腿或肺部)和剂量组合无关。[3] - 阿维巴坦的平均终末血浆半衰期为 0.24 ± 0.04 小时。 [3] - 阿维巴坦的分布容积为 1.18 ± 0.34 L/kg。[3] - 总阿维巴坦的上皮衬液 (ELF) 与血浆 AUC 比值为 0.20 ± 0.02,游离阿维巴坦的该比值为 0.22 ± 0.02。[3] - 未观察到头孢他啶与阿维巴坦之间的药代动力学相互作用。[3] - 阿维巴坦的剂量 (mg/kg) 与血浆 AUC (mg·h/L) 之间的总体关系为:log AUC = -0.5896 + 1.070 × log(阿维巴坦剂量)。[3] |
| 酶活实验 |
在 200 μL 的反应体系中,将 1 μM TEM-1 与 5 μM Avibactam 或不添加 Avibactam 于 37°C 孵育 5 分钟,然后进行两次超滤柱(UFC)处理以去除过量的抑制剂(Ultrafree-0.5,Biomax 膜,5 kDa 截留分子量)。在 4°C 下以 10,600×g 离心 8 分钟。每次超滤后,取 20 μL 截留液用 180 μL 测定缓冲液稀释,以恢复酶的原始浓度。经过两次超滤处理后,通过液相色谱-串联质谱法(LC/MS/MS)定量分析游离 Avibactam 的含量,发现其低于原始浓度的 5%。通过测量酰基酶样品中 TEM-1 的活性(稀释 4000 倍)来评估 UFC 过程中蛋白质的损失,并与未经 UFC 处理的酶进行比较,发现损失小于 5%[1]。
- 基于超滤的抑制试验: 1. 将纯化的 TEM-1 (1 μM) 与 5 μM 阿维巴坦在 37°C 下孵育 5 分钟。 2. 通过两次连续的超滤步骤(5 kDa 截留分子量)去除未结合的抑制剂。 3. 使用硝基头孢菌素作为底物测量残余酶活性。 4. 与阿维巴坦结合的TEM-1显示出<5%的残余活性,证实了共价抑制[1,5] - KPC-2抑制动力学: 1. 将KPC-2 (0.1 μM) 与不同浓度的阿维巴坦 (0.1–10 μM) 在Tris缓冲液中孵育。 2. 使用亚胺培南作为底物,通过分光光度法 (λ=486 nm) 监测抑制情况。 3. IC50 = 38 nM,解离速率较慢 (0.045 ± 0.022 min⁻¹),表明酶的占据时间较长 [1,5] 酰化动力学:将 TEM-1 (2.5 nM) 与阿维巴坦 (60 nM 至 50 μM) 和硝基头孢菌素 (200 μM) 混合于 100 mM 磷酸盐缓冲液 (pH 7.0) 中,于 37°C 下进行反应。使用常规分光光度法和停流分光光度法监测 460–490 nm 处的吸光度。数据拟合采用两步可逆抑制模型。 [1] - 脱酰基化(解离速率)测定:将 TEM-1 (1 μM) 与阿维巴坦 (5 μM) 在 37°C 下孵育 5 分钟,然后用含硝基头孢菌素 (400 μM) 的测定缓冲液稀释 4000 倍。在 490 nm 处监测活性恢复情况,并拟合公式 1 以获得 koff 值。[1] - 水解/核磁共振:将 40 μM 阿维巴坦与 4 μM TEM-1 在 37°C 下孵育长达 24 小时,并用 ¹H Carr-Purcell-Meiboom-Gill 核磁共振分析样品。[1] - 质谱分析:蛋白质样品经变性后,用电喷雾电离质谱分析以确认共价加合物。 [1] - 平衡解离 (Kd):将酰基-TEM-1 (1 μM) 进行系列稀释,并在 37°C 下平衡 2 小时。通过活性测定、蛋白质质谱和小分子质谱对游离酶进行定量。数据拟合到紧密结合模型。[1] - 等温滴定量热法 (ITC):使用先前报道的可逆配体进行竞争性滴定以测定 Kd。[1] - 酰基酶交换:将酰化供体酶(TEM-1、CTX-M-15、KPC-2、PP9、AmpC)与脱辅基受体酶(各 1 μM)在 37°C 下混合,并取等分试样进行质谱分析。[1] |
| 细胞实验 |
将过夜肉汤培养物中的细胞(约 10⁹ cfu)涂布于添加了以下两种溶液的 Mueller-Hinton 琼脂平板上:(i) 头孢洛林加阿维巴坦(1 或 4 mg/L),浓度为最低抑菌浓度 (MIC) 的 1-16 倍;(ii) 头孢洛林(1 或 4 mg/L)加阿维巴坦,浓度为将头孢洛林 MIC 降低至 1 或 4 mg/L 所需浓度的 1-8 倍。过夜培养后计数菌落,并保留代表性菌落[2]。采用微量肉汤稀释法分析最低抑菌浓度 (MIC)。对 16 株 KPC-2 型和 1 株 OXA-232 型产碳青霉烯酶肺炎克雷伯菌进行不同浓度头孢他啶-阿维巴坦的时间-杀菌曲线试验。本研究采用棋盘格法,对28株NDM菌株和2株NDM合并KPC碳青霉烯酶肺炎克雷伯菌菌株进行了体外协同杀菌作用的测定。根据计算等级,选择具有协同杀菌作用的药物作为抑菌浓度指数。对其中12株菌株进行了头孢他啶-阿维巴坦联合阿维巴坦的体外杀菌试验。[3] 目的:头孢洛林+阿维巴坦(NXL104)是一种新型抑制剂组合,对产A类和C类β-内酰胺酶的肠杆菌科细菌具有活性。我们研究了其耐药突变风险。方法:从肠杆菌科细菌中筛选并鉴定出具有超广谱β-内酰胺酶(ESBLs)、AmpC β-内酰胺酶和KPC β-内酰胺酶的单步和多步突变体。结果:在含有低MIC倍数头孢洛林+阿维巴坦的琼脂培养基上,细菌过度生长,但单步突变体的频率低于10⁻⁹。大多数突变体不稳定,仅有三个突变体在传代培养后仍保持耐药性。其中一个突变体来自CTX-M-15阳性的大肠杆菌,其对头孢洛林+阿维巴坦的MIC值升高,但该菌对头孢洛林的耐药性降低,并丧失了对其他氧亚氨基头孢菌素的耐药性。当将突变体bla(CTX-M-15)克隆到大肠杆菌DH5α中时,这种耐药性特征仍然存在。测序结果显示,CTX-M-15变体中存在Lys237Gln氨基酸替换。另外两个稳定的单步突变体来自AmpC去抑制的阴沟肠杆菌菌株;这些突变体对其他β-内酰胺类抗生素的耐药性未发生改变或略有降低。这两个突变体均缺失了AmpC Ω环中的213-226位氨基酸。通过多步筛选,从AmpC诱导型和去抑制型阴沟肠杆菌中获得了更多稳定突变体,这些突变体表现出OmpC和OmpF表达降低,和/或AmpC中Asn366His/Ile氨基酸替换。结论:稳定耐药突变体的筛选较为困难。来自AmpC去抑制型阴沟肠杆菌的突变体存在孔蛋白缺失或AmpC结构改变,包括Ω环缺失。 CTX-M-15 中的 Lys237Gln 取代赋予了耐药性,但基本消除了 ESBL 活性。[2]
- 细菌生长抑制: 1. 将肺炎克雷伯菌 (10⁶ CFU/mL) 与头孢他啶 (0.5–256 mg/L) ± 阿维巴坦 (0.5–16 mg/L) 在 Mueller-Hinton 肉汤中孵育。 2. 在 37°C 孵育 24 小时后测定 MIC 终点。 3. 阿维巴坦将表达 KPC-2 的菌株的头孢他啶 MIC90 从 >256 mg/L 降低至 8 mg/L [4,5] - 突变体筛选方案: 1. 将大肠杆菌培养物暴露于头孢洛林 + 阿维巴坦(1× MIC)中 7 天,每日进行传代培养。 2. 对存活菌落进行孔蛋白缺失(例如,结晶紫排除法)和 β-内酰胺酶突变(测序)的筛选。 3. 筛选出的突变体对阿维巴坦组合的 MIC 值提高了 2-8 倍 [2] |
| 动物实验 |
动物模型:6周龄BALB/c小鼠(雌性),肺炎克雷伯菌Y8株感染模型[4]
剂量:0.375 mg/g,与头孢他啶联合使用 给药途径:皮下注射,感染后4小时给药,之后每8小时给药一次,持续10天 结果:感染组小鼠在4天内死亡70%,PBS组小鼠在13天内全部死亡。感染后每8小时给予抗生素治疗,持续10天,治疗组小鼠全部存活;然而,停止抗生素治疗后,对照组小鼠在4天内全部死亡。与感染组相比,治疗组小鼠肝脏和脾脏中的菌落形成单位(CFU)计数降低。 - 中性粒细胞减少小鼠大腿感染模型: 1. 用环磷酰胺(200 mg/kg,腹腔注射)抑制BALB/c小鼠(6-8周龄)的免疫功能。 2. 肌内注射肺炎克雷伯菌(10⁷ CFU/只)。 3. 感染后4小时皮下注射头孢他啶(1024 mg/kg)±阿维巴坦(256 mg/kg)。 4. 24小时后采集大腿组织进行细菌计数[4,5] - 大鼠腹腔脓肿模型: 1. 将肺炎克雷伯菌(10⁸ CFU/mL)与琼脂珠混合,腹腔内植入。 2. 每8小时静脉注射头孢他啶(100 mg/kg)+阿维巴坦(25 mg/kg),持续52小时。 3. 无菌抽取脓肿,接种于培养皿进行菌落形成单位(CFU)计数[4] 雌性CD-1小鼠(20-25 g,7-8周龄)通过腹腔注射环磷酰胺(第-4天150 mg/kg,第-1天100 mg/kg)诱导中性粒细胞减少。 [3] - 大腿感染模型:将0.05 mL细菌悬液(~10⁶–10⁷ CFU)肌内注射至每侧大腿。[3] - 肺部感染模型:在轻度异氟烷麻醉下,经鼻给予0.05 mL细菌悬液。[3] - 感染后2小时,单次皮下注射头孢他啶和阿维巴坦(剂量均为1–128 mg/kg,以不同组合给药)。[3] - 给药后0至360分钟,在12个时间点采集血液和支气管肺泡灌洗液(BALF)。[3] - 使用尿素稀释法测定BALF中上皮衬液(ELF)的浓度。[3] - 使用液相色谱-串联质谱法(LC-MS/MS)测定血浆和ELF中阿维巴坦的浓度。 [3] - 药代动力学参数采用非房室模型分析法获得。[3] 雌性 CD-1 小鼠(20–25 g,7–8 周龄)经腹腔注射环磷酰胺(第 -4 天 150 mg/kg,第 -1 天 100 mg/kg)诱导中性粒细胞减少。[3] - 大腿感染模型:每只小鼠大腿肌内注射 0.05 mL 细菌悬液(~10⁶–10⁷ CFU)。[3] - 肺部感染模型:在轻度异氟烷麻醉下,经鼻内给予 0.05 mL 细菌悬液。[3] - 感染后 2 小时,皮下注射单剂量头孢他啶和阿维巴坦(各 1–128 mg/kg,以不同组合给药)。 [3] - 在给药后0至360分钟的12个时间点采集血液和支气管肺泡灌洗液(BALF)。[3] - 使用尿素稀释法,通过BALF计算上皮衬液(ELF)浓度。[3] - 采用液相色谱-串联质谱法(LC-MS/MS)测定血浆和ELF中阿维巴坦的浓度。[3] - 通过非房室模型分析得出药代动力学参数。[3] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
阿维巴坦和头孢他啶主要经肾脏排泄。阿维巴坦和头孢他啶的稳态分布容积分别为22.2 L和17 L。阿维巴坦和头孢他啶的清除率分别约为12 L/h和7 L/h。代谢/代谢物:在人肝脏制剂中未观察到阿维巴坦的代谢。未代谢的阿维巴坦是人血浆和尿液中主要的药物成分。80-90%的头孢他啶以原形排出。生物半衰期:头孢他啶-阿维巴坦的半衰期约为2.7-3.0小时。 - 吸收:皮下注射后迅速吸收,小鼠生物利用度为 80% [3] - 分布:组织渗透性高,在感染肺和股部的支气管肺泡灌洗液 (ELF) 中浓度可达血浆浓度的 60-70%。分布容积 = 1.18 L/kg [3,5] - 消除:经肾脏以原形排泄,小鼠终末半衰期为 0.24 小时。清除率 = 3.4 L/h/kg [3] 阿维巴坦在血浆和 ELF 中均表现出线性剂量比例药代动力学特征。[3] - 平均终末血浆半衰期:0.24 ± 0.04 小时。[3] - 分布容积:1.18 ± 0.34 L/kg。 [3] - 肺泡上皮衬液与血浆AUC比值(总药物):0.20 ± 0.02。[3] - 肺泡上皮衬液与血浆AUC比值(游离药物):0.22 ± 0.02。[3] - 大腿感染小鼠和肺部感染小鼠的药代动力学未见显著差异。[3] - 未观察到与头孢他啶的药代动力学相互作用。[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
阿维巴坦与血浆蛋白的结合率为5.7%–8.2%,而头孢他啶与血浆蛋白的结合率低于10%。 |
| 参考文献 |
|
| 其他信息 |
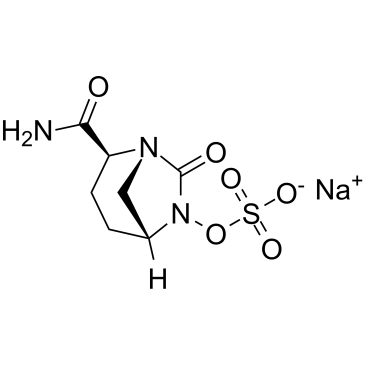
阿维巴坦钠是一种有机钠盐,是阿维巴坦的单钠盐。它与头孢他啶五水合物联合使用,用于治疗复杂性尿路感染,包括肾盂肾炎。它是一种EC 3.5.2.6(β-内酰胺酶)抑制剂、抗菌剂和抗微生物剂。它含有阿维巴坦(1-)结构域。阿维巴坦属于氮杂双环烷类化合物,其化学名称为(2S,5R)-7-氧代-1,6-二氮杂双环[3.2.1]辛烷-2-甲酰胺,其中6位上的氨基氢被磺氧基取代。它(以钠盐形式)与头孢他啶五水合物联合使用,用于治疗复杂性尿路感染,包括肾盂肾炎。它是一种抗菌剂、抗菌剂和EC 3.5.2.6(β-内酰胺酶)抑制剂。它是一种单羧酸酰胺,属于脲类、氮杂双环烷烃和羟胺O-磺酸。它是阿维巴坦(1-)的共轭酸。阿维巴坦是一种非β-内酰胺酶抑制剂,可与头孢他啶(Avycaz)联合使用。该组合于2015年2月25日获得FDA批准,用于与甲硝唑联合治疗复杂性腹腔内感染,以及治疗由耐药病原体(包括多重耐药革兰氏阴性菌)引起的复杂性尿路感染(包括肾盂肾炎)。由于临床安全性和有效性数据有限,Avycaz应保留用于18岁及以上且其他治疗选择有限的患者。阿维巴坦是一种β-内酰胺酶抑制剂。阿维巴坦的作用机制是作为β-内酰胺酶抑制剂。
药物适应症 AVYCAZ(头孢他啶-阿维巴坦)与甲硝唑联合使用,适用于治疗由以下敏感微生物引起的复杂性腹腔内感染:大肠杆菌、肺炎克雷伯菌、奇异变形杆菌、普罗维登斯菌属、阴沟肠杆菌、产酸克雷伯菌和铜绿假单胞菌,适用于18岁及以上患者。 AVYCAZ 也适用于治疗由以下敏感微生物引起的复杂性尿路感染,包括肾盂肾炎:大肠杆菌、肺炎克雷伯菌、科氏柠檬酸杆菌、产气肠杆菌、阴沟肠杆菌、弗氏柠檬酸杆菌、变形杆菌属和铜绿假单胞菌,适用于 18 岁及以上患者。 FDA标签 作用机制 阿维巴坦是一种非β-内酰胺酶抑制剂,它通过独特的共价可逆机制灭活某些β-内酰胺酶(包括肺炎克雷伯菌碳青霉烯酶在内的Ambler A β-内酰胺酶、Ambler C β-内酰胺酶和部分Ambler D β-内酰胺酶),从而保护头孢他啶免受某些β-内酰胺酶的降解。阿维巴坦可迅速到达细菌周质空间,并达到足以恢复头孢他啶对耐头孢他啶、产生β-内酰胺酶菌株活性的浓度。阿维巴坦不会降低头孢他啶对头孢他啶敏感菌的活性。 阿维巴坦是一种β-内酰胺酶抑制剂,目前与β-内酰胺类药物联合用于治疗革兰氏阴性菌感染,并处于临床开发阶段。阿维巴坦属于一类结构抑制剂,这类抑制剂不具有β-内酰胺核心结构,但能够共价酰化其β-内酰胺酶靶标。我们利用TEM-1酶,通过测定酰化反应的结合速率和脱酰化反应的解离速率来表征阿维巴坦的抑制作用。脱酰化反应的解离速率为0.045 min⁻¹,这使我们能够研究TEM-1的脱酰化途径。我们利用核磁共振(NMR)和质谱(MS)证实,脱酰化是通过完整阿维巴坦的再生而非水解实现的。除TEM-1外,我们还发现其他四种具有临床意义的β-内酰胺酶在酰化后也能释放完整的阿维巴坦。我们发现阿维巴坦是一种共价、缓慢且可逆的抑制剂,这在β-内酰胺酶抑制剂中是一种独特的抑制机制。[1] 背景:近年来,耐碳青霉烯类肠杆菌科细菌(CRE)感染的发生率迅速增加。由于CRE菌株通常对大多数抗菌药物耐药,因此该感染患者的死亡率往往很高。这给临床感染管理带来了严峻挑战。本研究旨在探讨头孢他啶-阿维巴坦单独使用或与氨曲南联合使用对产KPC或NDM碳青霉烯酶肺炎克雷伯菌的体外和体内杀菌活性,并探索耐药菌株感染的新临床治疗方案。[3] 方法:采用微量肉汤稀释法测定最低抑菌浓度(MIC)。本研究对16株KPC-2菌株和1株OXA-232型产碳青霉烯酶肺炎克雷伯菌进行了不同浓度头孢他啶-阿维巴坦的时间-杀菌曲线试验。此外,本研究采用棋盘格法测定了头孢他啶-阿维巴坦联合氨曲南对28株NDM菌株和2株NDM-KPC型产碳青霉烯酶肺炎克雷伯菌的体外协同杀菌作用。根据计算的等级,筛选出具有协同杀菌作用的药物,并以抑制浓度指数(ICI)作为指标。对其中12株菌株进行了头孢他啶-阿维巴坦联合氨曲南的体外杀菌试验。在小鼠模型中,研究了头孢他啶-阿维巴坦对KPC型碳青霉烯酶肺炎克雷伯菌Y8菌株感染的疗效。 [3] 结果:时间-杀菌曲线试验表明,浓度为2MIC、4MIC和8MIC的头孢他啶-阿维巴坦均对耐药菌株表现出显著的杀菌活性。然而,在28株NDM菌株和2株NDM-KPC碳青霉烯酶肺炎克雷伯菌中,仅有7株对头孢他啶-阿维巴坦敏感,其MIC50和MIC90分别为64 mg/L和256 mg/L。头孢他啶-阿维巴坦联合氨曲南的抗菌药物敏感性试验结果显示,两种药物在90%(27/30)的菌株中具有协同作用,在3.3%(1/30)的菌株中具有相加作用,在6.6%(2/30)的菌株中无显著作用。未发现拮抗作用。后续的杀菌试验也证实了上述结果。头孢他啶-阿维巴坦对小鼠肺炎克雷伯菌Y8株感染的治疗效果显示,感染组小鼠的死亡率在4天内达到70%,所有小鼠在13天内全部死亡。细菌载量检测结果显示,感染组和治疗组小鼠血液中的细菌数量无显著差异。然而,与感染组相比,治疗组小鼠脾脏和肝脏中的菌落形成单位(CFU)计数较低,表明头孢他啶-阿维巴坦对细菌具有显著的杀菌作用,并具有一定的治疗效果。[3] 结论:本研究表明,头孢他啶-阿维巴坦对产生KPC-2和OXA-232碳青霉烯酶的肺炎克雷伯菌具有显著的杀菌作用。与氨曲南联用时,阿维巴坦对产生NDM碳青霉烯酶的肺炎克雷伯菌表现出更强的协同杀菌作用。[3] - 作用机制:阿维巴坦独特的双环磺酸核心结构模拟β-内酰胺类抗生素,并与β-内酰胺酶的活性位点结合,形成可逆的酰基-酶复合物。该复合物阻断底物接近,同时允许缓慢水解以再生活性酶。[1] - 临床适应症:获准与头孢他啶联用,用于治疗由多重耐药革兰氏阴性菌引起的复杂性泌尿道/腹腔内感染。[5] - 耐药机制:外膜孔蛋白(例如OmpC/F)的缺失或β-内酰胺酶(例如TEM-1 A237V)的突变会降低阿维巴坦的疗效。这些突变是在长期药物胁迫下选择的。[2,4] 阿维巴坦(曾用名NXL-104)是一种二氮杂双环辛烷(DBO)类非β-内酰胺类β-内酰胺酶抑制剂。[1] - 目前,它正与头孢洛林和头孢他啶联合用于治疗革兰氏阴性菌感染,处于临床开发阶段。[1] - 与β-内酰胺类抑制剂不同,阿维巴坦通过氨甲酰键酰化丝氨酸β-内酰胺酶,并通过可逆脱酰化作用完整释放,无需水解或重排。[1] - 其机制涉及两步可逆抑制:E + I ⇌ EI → EI,其中酰化步骤是起效的限速步骤,而脱酰化(环化)步骤缓慢且可逆。 [1] - 该机制与其他β-内酰胺酶抑制剂不同,并使其对A类和C类β-内酰胺酶具有广谱活性。[1] |
| 分子式 |
C7H10N3NAO6S
|
|---|---|
| 分子量 |
287.22
|
| 精确质量 |
287.018
|
| 元素分析 |
C, 29.27; H, 3.51; N, 14.63; Na, 8.00; O, 33.42; S, 11.16
|
| CAS号 |
1192491-61-4
|
| 相关CAS号 |
Avibactam free acid;1192500-31-4;Avibactam sodium hydrate;2938989-90-1;Avibactam sodium dihydrate
|
| PubChem CID |
24944097
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
0.453
|
| tPSA |
142.44
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
18
|
| 分子复杂度/Complexity |
462
|
| 定义原子立体中心数目 |
2
|
| SMILES |
C1C[C@H](N2C[C@@H]1N(C2=O)OS(=O)(=O)[O-])C(=O)N.[Na+]
|
| InChi Key |
RTCIKUMODPANKX-JBUOLDKXSA-M
|
| InChi Code |
InChI=1S/C7H11N3O6S.Na/c8-6(11)5-2-1-4-3-9(5)7(12)10(4)16-17(13,14)15;/h4-5H,1-3H2,(H2,8,11)(H,13,14,15);/q;+1/p-1/t4-,5+;/m1./s1
|
| 化学名 |
sodium (2S,5R)-2-carbamoyl-7-oxo-1,6-diazabicyclo[3.2.1]octan-6-yl sulfate
|
| 别名 |
NXL104; NXL-104; NXL 104; Avibactam;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO :30~57 mg/mL ( 104.45 ~198.44 mM )
Water : 50 ~57 mg/mL(~174.08 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.75 mg/mL (9.57 mM) (饱和度未知) in 5% DMSO + 40% PEG300 + 5% Tween80 + 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
*生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.75 mg/mL (9.57 mM) (饱和度未知) in 5% DMSO + 95% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (7.24 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: ≥ 2.08 mg/mL (7.24 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将100μL 20.8mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 5 中的溶解度: ≥ 0.55 mg/mL (1.91 mM) (饱和度未知) in 1% DMSO 99% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 6 中的溶解度: 5% DMSO+40% PEG300+5% Tween-80+50% Saline: ≥ 2.75 mg/mL (9.57 mM) 配方 7 中的溶解度: 140 mg/mL (487.41 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4817 mL | 17.4083 mL | 34.8165 mL | |
| 5 mM | 0.6963 mL | 3.4817 mL | 6.9633 mL | |
| 10 mM | 0.3482 mL | 1.7408 mL | 3.4817 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04402359 | COMPLETED | Drug: meropenem Drug: ceftazidime 2 grams and avibactam 500 Device: ventilator |
Ventilator Associated Pneumonia | King Abdul Aziz Specialist Hospital | 2018-07-05 | |
| NCT04040621 | TERMINATEDWITH RESULTS | Drug: Ceftazidime-avibactam | Hospitalized Children With Suspected or Confirmed Nosocomial Pneumonia | Pfizer | 2020-06-15 | Phase 1 |
| NCT05340530 | UNKNOWN STATUS | Drug: The injectable TQD3606 Drug: meropenem Drug: Avibactam Sodium Drug: Placebo |
Infections | Chia Tai Tianqing Pharmaceutical Group Co., Ltd. | 2022-04 | Phase 1 |
| NCT06051513 | RECRUITING | Drug: treatment with or without colistin | Carbapenem-Resistant Enterobacteriaceae Infection | Southeast University, China | 2023-09-21 | Not Applicable |
| NCT03580044 | TERMINATEDWITH RESULTS | Combination Product: ATM-AVI Drug: BAT |
Serious Bacterial Infection | Pfizer | 2020-12-25 | Phase 3 |
|
|
|