| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
DNA-PKcs (IC50 = 91.3 nM); PI3Kγ (IC50 = 1.37 μM); ATM (IC50 = 117.93 μM)
|
|---|---|
| 体外研究 (In Vitro) |
AZD7648 在 A549 非小细胞肺癌 (NSCLC) 细胞中抑制 IR 诱导的 DNA-PK S2056 自动磷酸化,IC50 = 92 nM。 DNA-PK S2056 自磷酸化,IC50 值为 92 nM。停滞在细胞周期 G2/M 期的细胞数量显着增加,微核形成增加 4 倍,H2AX、pATM S1981 和 53BP1 焦点形成诱导 3 倍当 AZD7648 (1 M) 与 2Gy IR 结合 48 小时时,所有这些都是在 A549 细胞中引起的[2]。
研究人员开发了一种高效和选择性的DNA-PK抑制剂AZD7648,它在A549非小细胞肺癌(NSCLC)细胞中以IC50=92nM抑制IR-诱导的DNA-PKS2056自动磷酸化。AZD7648是一种强效的放射增敏剂,其中与IR联合治疗导致A549和H1299 NSCLC细胞集落存活能力的浓度依赖性降低(DEF37在100 nM时分别为1.7和2.5)。在A549细胞中,与单独使用IR相比,AZD7648(≥1µM)与2Gy IR联合使用48小时,导致细胞明显积聚在细胞周期的G2/M期,微核形成增加4倍,γH2AX、pATM S1981和53BP1病灶形成诱导增加3倍。在应用Loewe加性模型时,在一组卵巢和三阴性乳腺癌症(TNBC)细胞系的细胞生长抑制试验中,AZD7648也被发现与阿霉素协同结合(协同得分4-35)。[2]
这种优化产生了AZD7648,它是DNA-PK的强效抑制剂(生化测定中为0.6 nM,A549细胞中为89 nM),在Thermofisher选择性面板中对396种其他激酶的选择性大于100倍。此外,AZD7648在临床前物种中具有良好的晶体溶解性、代谢稳定性和可预测的药代动力学。 |
| 体内研究 (In Vivo) |
AZD7648 是一种有效的、高选择性的 DNA-PK 抑制剂,具有良好的结晶溶解度、渗透性和代谢稳定性,在临床前物种中具有良好的生物利用度和可预测的药代动力学,与奥拉帕尼或放疗联合使用时,可有效敲低 pRPA 并在小鼠异种移植模型中实现回归[1 ]。
在小鼠异种移植物模型中,使用pRPA(S4/8)评估PD,并有效抑制PD(体内IC50=52 nM)。AZD7648作为单一疗法观察到肿瘤生长抑制,与奥拉帕尼或放疗联合使用观察到消退。AZD7648与奥拉帕尼联合使用时观察到的疗效与体内IC90的自由覆盖有关。AZD7648是一种强效、高选择性的DNA-PK抑制剂,具有良好的结晶溶解性、渗透性和代谢稳定性,在临床前物种中具有良好的生物利用度和可预测的药代动力学,与奥拉帕尼或辐射联合使用时,在小鼠异种移植物模型中具有强效的pRPA敲除和回归作用。这些特征使AZD7648成为一种合适的临床候选药物,并计划在2019年进行临床研究,评估其作为潜在的癌症治疗方法。[1]
在体内,AZD7648与IR(5x 2Gy)的组合以剂量依赖的方式诱导H1299和A549 NSCLC异种移植物的肿瘤消退(分别为84%和11%的消退),而单药治疗仅实现了肿瘤生长抑制。在这两种模型中,AZD7648治疗抑制了IR对三种主要DNA-PK药效标志物pDNAPK(S2056)、pRPA32(S4/8)和γH2AX的激活增加(IR+AZD7648治疗2小时后抑制率为70-90%)。类似地,在BT474c ER+乳腺癌症异种移植物模型和TNBC PDX模型中,脂质体阿霉素(每周2.5 mg/kg)与AZD7648(37.5 mg/kg bid)联合诱导肿瘤消退(分别为63%和33%消退),而单药治疗仅实现肿瘤生长抑制。这些数据证实,AZD7648对DNA-PK的抑制增强了一系列体外和体内DSB诱导剂的疗效,为其临床研究提供了明确的理论基础[2]。 AZD7648在异种移植物和PDX模型中的一系列剂量和方案中增强了奥拉帕尼的疗效,实现了持续的肿瘤消退,并为其临床研究提供了明确的理论基础[4]。 |
| 细胞实验 |
细胞药理学[4]
通过测量Ser2056上的DNA-PKcs自磷酸化,在IR后在A549细胞中评估AZD7648对DNA-PK活性的主要效力。在其他细胞试验中评估了AZD7648对HT29中ATM(pATM Ser1981)、HT29中ATR(pCHK1 Ser345)、MDA-MB-468中mTOR(pAKT Ser473)和BT474(PI3Kα)、MDAM-B-468(PI3Kβ)、RAW-264(PI3Kγ)和JEKO-1(PI3Kδ)细胞中PI3K亚型(pAKT Thr308)的选择性。IC50定义为使每种相应激酶的下游靶标磷酸化减少50%所需的浓度。 高含量免疫荧光成像和分析[4] 在A549和OAW42细胞中进行了高含量成像分析,以分别评估AZD7648与IR和阿霉素联合治疗的细胞反应。将细胞固定并进行γH2AX、53BP1和pATM Ser1981染色,并在CV7000高含量成像平台上成像。 |
| 动物实验 |
Immunocompromised SCID (C.B-17/IcrHan®Hsd-Prkdcscid) or Hsd:Athymic Nude-Foxn1nu female mic were used for tumour implantation. AZD7648 was formulated in 0.5% hydroxypropyl methylcellulose/0.1% Tween80 (HPMC/T) and orally dosed (4–100 mg kg−1). When dosed twice daily, the time between the morning and evening doses was 8 h. Targeted irradiation of 2 Gy was delivered over 2 min daily over the first 5 days of treatment. Liposomal doxorubicin was diluted in physiological saline and intravenously dosed at 2.5 or 5 mg kg−1 once per week. Olaparib was formulated in 10% DMSO/30% Kleptose and orally dosed at 100 mg kg−1 once daily. All three combinations were dosed 1 h after the morning dose of AZD7648 or its vehicle HPMC/T. Tumour growth inhibition from start of treatment was assessed by comparison of the mean change in tumour volume for the control and treated groups, using the Mousetrap application and represented as TGI. Statistical significance was evaluated using a one-tailed t-test. All in vivo studies complied with all relevant ethical regulations for animal testing and research, followed AstraZeneca’s global bioethics policy and received ethical approval from the AstraZeneca ethical committee. HBCx-17 PDX study was carried out at XenTech, France in accordance with French regulatory legislation concerning the protection of laboratory animals. [4]
|
| 参考文献 | |
| 其他信息 |
DNA-PK抑制剂AZD7648是一种口服生物利用度高的ATP竞争性DNA依赖性蛋白激酶(DNA-PK)抑制剂,具有潜在的化疗/放疗增敏和抗肿瘤活性。口服后,DNA-PK抑制剂AZD7648选择性地靶向、结合并抑制DNA-PK的活性,从而干扰非同源末端连接(NHEJ)过程,并阻止电离辐射或化疗引起的DNA双链断裂(DSB)的修复。这增强了化疗和放疗的细胞毒性,从而促进肿瘤细胞死亡。AZD7648还可以增强聚(ADP-核糖)聚合酶(PARP)抑制剂的作用,并可能作为单药疗法用于治疗因其他DNA修复途径缺陷而导致内源性DNA损伤水平高的肿瘤。肿瘤细胞修复DSB的能力增强是肿瘤细胞对化疗和放疗产生耐药性的主要原因。 DNA-PK在非同源末端连接(NHEJ)通路和DNA双链断裂(DSB)修复中发挥关键作用。DNA依赖性蛋白激酶(DNA-PK)是DNA损伤反应(DDR)的关键参与者,也是用于检测和修复DNA双链断裂(DSB)的非同源末端连接(NHEJ)通路的重要组成部分。我们证明,高效且高选择性的DNA-PK抑制剂AZD7648可有效增强辐射和阿霉素诱导的DNA损伤,在异种移植和患者来源的异种移植(PDX)模型中,二者联合使用可诱导持续的损伤消退。利用ATM缺陷细胞,我们证明AZD7648与PARP抑制剂奥拉帕尼联合使用可增加基因组不稳定性,从而抑制细胞生长并诱导细胞凋亡。在异种移植和PDX模型中,AZD7648增强了奥拉帕尼在不同剂量和给药方案下的疗效,实现了持续的肿瘤消退,并为其临床研究提供了明确的理论依据。AZD7648作为一种NHEJ抑制剂,其作用机制独特,可作为现有DDR靶向药物的补充,并有望与这些药物联合使用,从而获得更深层次的疗效。[4]
|
| 分子式 |
C18H20N8O2
|
|---|---|
| 分子量 |
380.4038
|
| 精确质量 |
380.17
|
| 元素分析 |
C, 56.83; H, 5.30; N, 29.46; O, 8.41
|
| CAS号 |
2230820-11-6
|
| 相关CAS号 |
2230820-11-6
|
| PubChem CID |
135151360
|
| 外观&性状 |
Off-white to light yellow solid powder
|
| LogP |
1
|
| tPSA |
101
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
28
|
| 分子复杂度/Complexity |
588
|
| 定义原子立体中心数目 |
0
|
| SMILES |
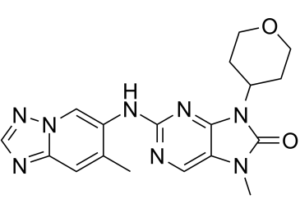
CC1=CC2=NC=NN2C=C1NC3=NC=C(N(C)C(N4C5CCOCC5)=O)C4=N3
|
| InChi Key |
XISVSTPEXYIKJL-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C18H20N8O2/c1-11-7-15-20-10-21-25(15)9-13(11)22-17-19-8-14-16(23-17)26(18(27)24(14)2)12-3-5-28-6-4-12/h7-10,12H,3-6H2,1-2H3,(H,19,22,23)
|
| 化学名 |
7-methyl-2-[(7-methyl-[1,2,4]triazolo[1,5-a]pyridin-6-yl)amino]-9-(oxan-4-yl)purin-8-one
|
| 别名 |
AZD7648; AZD 7648; 2230820-11-6; AZD7648; 7-methyl-2-[(7-methyl-[1,2,4]triazolo[1,5-a]pyridin-6-yl)amino]-9-(oxan-4-yl)purin-8-one; 7-Methyl-2-((7-methyl-[1,2,4]triazolo[1,5-a]pyridin-6-yl)amino)-9-(tetrahydro-2H-pyran-4-yl)-7H-purin-8(9H)-one; 97A09L5JCK; 7,9-Dihydro-7-methyl-2-[(7-methyl[1,2,4]triazolo[1,5-a]pyridin-6-yl)amino]-9-(tetrahydro-2H-pyran-4-yl)-8H-purin-8-one; compound 16 [PMID: 31851518]; AZD-7648
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 8.3~9 mg/mL (21.9~23.7 mM)
Ethanol: ~3 mg/mL (~7.9 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 10 mg/mL (26.29 mM) in 0.5% HPMC 0.1%Tween80 (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6288 mL | 13.1441 mL | 26.2881 mL | |
| 5 mM | 0.5258 mL | 2.6288 mL | 5.2576 mL | |
| 10 mM | 0.2629 mL | 1.3144 mL | 2.6288 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03907969 | Completed | Drug: AZD7648 Drug: PLD |
Advanced Malignancies | AstraZeneca | October 9, 2019 | Phase 1 Phase 2 |