| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 500μg |
|
||
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
ATPase family AAA domain-containing protein 2 (ATAD2) (IC50 = 166 nM)
|
|---|---|
| 体外研究 (In Vitro) |
在 TR-FRET 测试中,BAY-850 的 IC50 为 166 nM,表明其与单乙酰化组蛋白 H4 N 端肽在结合 ATAD2 BD 方面具有竞争性。 BAY-850 取代四乙酰化肽,IC50 为 157 nM,KD 为 115 nM。 BAY-850 显着的亚型特异性意味着与传统 BD 抑制剂相比具有独特的作用机制 [1]。
在TR-FRET测试中,BAY-850的IC50为166 nM,表明其与单乙酰化组蛋白H4 N端肽在结合ATAD2 BD方面具有竞争力。BAY-850以157 nM的IC50和115 nM的KD替代了四乙酰化肽。与传统的BD抑制剂相比,BAY-850的显著亚型特异性暗示了一种不同的作用机制[1] BAY-850与单乙酰化组蛋白H4 N端肽与ATAD2 BD的结合竞争,TR-FRET测定的IC50为166 nM(图2A)。在类似条件下,该化合物以22nM的IC50取代了四乙酰化H4肽。对于所有测试的相关化合物,观察到两种检测方法之间存在类似的变化(支持信息图4A)。这与K12单乙酰化肽在该试验中先前已被证明具有更高结合效力的事实是一致的。4在正交结合竞争试验中,如Alphacreen和BROMOscan,BAY-850分别以157 nM和115 nM的IC50取代了四乙酰化肽,证实了该化合物显示的效果与用于测量它们的读出技术无关(图2A)。此外,该化合物抑制了四乙酰化H4肽与包括ATP酶结构域的较大ATAD2构建体的结合(支持信息图4D)。阴性对照化合物BAY-460在所有测试中的浓度相同时均无活性[1]。 接下来,我们开始通过生物物理技术检测化合物与ATAD2的直接结合来确认BAY-850的生化活性。首先,蛋白质观察到的核磁共振波谱证实了BAY-850的一个同源物与ATAD2的特异性结合(支持信息图3)。在微尺度热泳(MST)试验中,BAY-850对ATAD2水合壳表现出剂量依赖性、可饱和效应(图2B),由此计算出KD为85 nM。该值与上述效力一致,这一特征适用于所有用MST分析的化合物(支持信息图4B)。此外,在热转移试验(TSA)中,与BAY-460不同,BAY-850以剂量依赖的方式提高了ATAD2的熔化温度(图2C)。该测定还显示,随着同一化学系列成员的生化效力的增加,热稳定性有增强的趋势(支持信息图4C)。BAY-850和BAY-460的选择性特征最初在BROMOscan面板中进行了研究,其中第一种化合物只与ATAD2结合,但令人惊讶的是,没有与ATAD2B密切相关,而后者在相同浓度下没有显示出显著的效果(图2D和支持信息图5A)。这些结果在TSA小组中得到了证实,当在10μM下测试化合物时,没有观察到BAY-850对BD家族其他成员ATAD2热稳定性的影响(图2E和支持信息图5B)。此外,BAY-850在354种激酶中没有显示出抑制活性,在高浓度下对少数GPCR只有适度的影响(支持信息表2和表3)[1]。 BAY-850前所未有的异构体选择性表明,其作用方式与经典BD抑制剂不同。等温量热法(ITC)分析(支持信息图4E)强化了这一解释,其中只有在37°C时才能记录到相互作用的弱热信号,与立构配体相比,化学计量是不典型的。1对TSA中BAY-850剂量滴定的更仔细检查表明,随着化合物浓度的增加,ATAD2熔解曲线从单相转变为两相形状,这表明在BAY-850饱和时出现了具有不同熔解曲线的新蛋白质物种(图2C)。这些观察结果促使我们使用非变性或天然质谱(MS)对BAY-850结合模式进行了深入研究,这是一种研究蛋白质-配体相互作用的成熟方法,10通过质谱中的电荷态分布提供有关蛋白质多聚体特征和构象的信息。无标签ATAD2的天然质谱主要由两个信号主导,这两个信号分别来自电荷态为+6和+7的单体ATAD2,两个次要信号分别来自带电态为+9和+10的二聚体ATAD2和1100至2000 m/z范围内部分展开的ATAD2的信号(图3A)。接下来,我们获得了与BAY-850一起孵育的ATAD2的天然质谱。令我们惊讶的是,光谱主要由一个BAY-850分子与ATAD2二聚体结合的复合物产生的信号主导(图3B),没有观察到单体ATAD2的结合。相比之下,非活性对照BAY-460没有与单体或二聚体ATAD2结合。BAY-850的二聚体诱导作用是浓度依赖性的,表明了一个特定的过程(图3C和支持信息图6A)。这些观察结果得到了分析尺寸排阻色谱(SEC)分析的证实,在该分析中,我们观察到化合物在洗脱曲线中从ATAD2单体转变为ATAD2二聚体形式(图3D)。重要的是,当用GST标记的ATAD2进行实验时,BAY-850不能诱导GST二聚体的进一步多聚化(图3D,插图),证实这种效应源于化合物与ATAD2之间的相互作用,而不是与GST标签的相互作用。竞争性天然MS实验表明,单个单乙酰化组蛋白H4肽分子与抑制剂结合的ATAD2二聚体的结合较弱。相比之下,在没有BAY-850的情况下,观察到同一肽与单体ATAD2的1:1结合和与二聚体ATAD2的2:2结合(支持信息图6B)[1]。 敲除实验表明,一些癌症细胞系的存活可能依赖于ATAD2。因此,我们研究了BAY-850、BAY-460和几种具有广泛生物化学活性的相关化合物对三种癌症细胞系的抗增殖作用。我们观察到生化效力和生长抑制之间的相关性较弱,BAY-850和类似效力的化合物的GI50在个位数微摩尔范围内,而BAY-460在测试的最高浓度下没有疗效(图4D)。由于生长抑制仅在高化合物浓度下发生,并且细胞系之间没有特别的区别,我们继续比较BAY-850和BAY-460在正常上皮细胞和癌症细胞中的活性。在这里,再次观察到两种化合物之间的明显分化,但BAY-850对未转化和癌症细胞具有类似的活性(图4E)。因此,我们得出结论,BAY-850显示的细胞毒性作用不能与ATAD2-BD抑制明确相关。基因表达研究提供了观察到的生长抑制与ATAD2 BD抑制之间脱节的进一步证据,其中BAY-850治疗不影响一些先前鉴定的ATAD2靶基因的表达(支持信息图7)。一致地,尽管在活细胞中使用ATAD2 BD,但最近发表的其他ATAD2 BD抑制剂也未能证明对靶基因表达和低于20μM的癌症细胞存活有显著影响。最近观察到SMARCA2/4蛋白在含多结构域的蛋白质中BD的潜在可选择性,其中观察到整个蛋白质的敲除与其BD功能的特异性抑制之间存在差异。根据这些报告,到目前为止,还没有令人信服的ATAD2 BD在癌症细胞存活中的结构域特异性遗传验证,至少在白血病结构域聚焦的CRISPR/Cas9筛选中,没有显示出对ATAD2 BD的依赖性[1]。 |
| 酶活实验 |
时间分辨荧光共振能量转移(TR-FRET)结合竞争分析[1]
在室温(RT)下在384孔低容量黑色微量滴定板中进行测定,最终体积为5µL。使用Precision液体处理机器人将测试化合物在DMSO(3.5倍,12点,0-20µM)中连续稀释,并用蜂鸟毛细管分配器以测试浓度的100倍将50 nl分配到平板上。接下来,将2µl 10 nM GST-ATAD2 BD[在50 mM Hepes pH 7.5、100 mM NaCl、50 mM KF、0.25 mM CHAPS、0.05%牛血清白蛋白(BSA)和1 mM二硫曲糖醇(DTT)的测定缓冲液中]与Multidrop一起加入,并将平板温育15分钟。最后,分配3µl 50 nM的C端生物素化合成乙酰化肽,来源于组蛋白H4 a.1-25(K12单乙酰化或K5,8,12,16四乙酰化)和检测试剂(10 nM抗6His-XL665),2.5 nM链霉抗生物素Eu,均在测定缓冲液内),并进一步温育至少1分钟。h.用Viewlux或Pherastar微量滴定板读数器获取与平衡中蛋白质-肽复合物数量相对应的TRFRET信号。通过基于四参数方程[最小值、最大值、IC50、Hill;Y=Max+(Min-Max)/(1+(X/IC50)^ Hill]的回归分析,使用Screener软件计算化合物浓度增加时在330-350nm激发后在665nm和620-622nm处的荧光发射的标准化比率,以计算IC50值。 [1] AlphaScreen®结合竞争分析[1] 通过使用AlphaScreen®组氨酸(镍螯合物)或FLAG(M2)检测试剂盒从Hexa-His标记的ATAD2 BD或FLAG标记的ATAD2(342-1390)蛋白中置换四乙酰化生物素化肽来确定化合物结合。使用Echo 525液体处理器将化合物从DMSO原液中分配到测定板中。在25°C下,在25 mM HEPES pH7.4、100mM NaCl、0.1%BSA、0.05%CHAPS的缓冲液中,在20µl的体积内进行了检测,缓冲液中含有25 nM肽(SGRGK(ac)GGK(ac)GLGK(ac)GGAK(ac)RHRK(生物素)-酸)、100 nM ATAD2、0.2%DMSO。将肽和蛋白质预先混合,加入复合板中并孵育30分钟,然后加入AlphaScreen®珠粒至终浓度为6µg/ml。将检测板孵育60分钟,然后使用Pherastar FS测量发光。 ADP-Glo®ATP酶活性测定[1] 根据制造商的说明,使用ADP-Glo®试剂盒进行ATP酶测定。使用Echo 525液体处理器(Labcyte)将化合物和ATP分配到测定板中。在25°C下,在20 mM HEPES pH7.4、50 mM NaCl、0.5 mM TCEP、1 mM MgCl2和0.1%BSA的缓冲液中,以4µl的体积进行检测。通过加入100 nM ATAD2蛋白(342-1390)引发反应,并孵育三小时。然后通过加入4µl ADP-Glo®试剂终止反应,以耗尽未水解的ATP,然后在25°C下孵育一小时。然后通过加入4µl ADP-Glo®检测试剂引发萤光素酶/萤光素反应,然后加入该试剂,在25°C下孵育一小时,然后在BMG Pherastar FSX上读取测定板。 微尺度热泳(MST)[1] 对于荧光标记蛋白的实验,根据制造商的说明,使用RED-NHS试剂盒标记GST-ATAD2-BD。或者,Alexa Fluor 647通过NHS偶联共价连接到蛋白质的N-末端伯胺基团上。实验在Monolith NT.115仪器上使用RED探测器进行。当选择Nano Temper专有标记时,使用20 nM的蛋白质浓度和含有25 mM HEPES pH7.4、150 mM NaCl、0.05%吐温20和0.5 mM TCEP的缓冲液。对于使用Alexa Fluor 647标记的实验,GST-ATAD2 BD的浓度为50 nM,缓冲液为50 mM Hepes pH 7.5,补充了150 mM NaCl和0.05%Pluronic。从100μM化合物浓度开始,手动或使用Echo 525液体处理器,以12点三倍连续稀释的方式筛选化合物,直至0.5 nM。孵育30分钟后,将蛋白质和化合物样品在14000 rpm下离心5分钟,然后装入Monolith™NT.115系列MST高级涂层毛细管中。MST实验使用20%或40%的LED功率和40%或80%的MST功率进行(取决于使用Nanotempate专有或Alexa Fluor 647标记),热泳发生时间超过30秒。KD值用Nanotempate的MO亲和分析软件v2.1测定。使用GST-ATAD2 BD浓度为500 nM的无标记检测器在Monolith NT.Automatic仪器上进行未修饰蛋白质的实验。从500μM 26化合物浓度开始,以12点两倍的连续稀释筛选化合物,直至244 nM。该测定在含有150 mM NaCl、50 mM HEPES 7.5、0.05%Pluronic的缓冲液中进行。孵育30分钟后,将样品装入Monolith™NT。自动零背景MST高级涂层毛细管芯片,并使用Monolith NT进行MST实验。自动(LED功率50%,MST功率80%)。KD值用Nanotempate的MO亲和分析软件v2.1测定。 等温滴定量热法(ITC)[1] 实验在37°C的NanoITC微量热计(TA Instruments)上在20 mM HEPES pH 7.5、50 mM NaCl、0.5 mM TCEP、5%甘油中进行。通过透析将ATAD2蛋白溶液缓冲交换到ITC缓冲液中。实验在反向滴定模式下进行。注射器中的蛋白质浓度为200μM,细胞中的BAY-850抑制剂浓度为40μM。使用ΔG=ΔH-TΔS=-RTlnKB计算热力学参数,其中ΔG、ΔH和ΔS分别是使用单结合位点模型计算的自由能、焓和结合熵的变化。 热位移分析(TSA)/差示扫描荧光法(DSF)[1] 使用ViiATM实时PCR仪在384孔板上进行了GST标记和未标记ATAD2-BD的热熔实验。在5.3µM的蛋白质浓度下,在环境敏感荧光探针SYPRO Orange的存在下,使用含有20 mM HEPES pH7.5的缓冲液,从供应的原料中稀释1:625,获得熔解曲线;200 mM氯化钠;10%甘油;0.5mM TCEP。对于结合实验,将连续稀释的配体(0.049µM至100µM,5倍)加入混合物中,作为对照使用1%DMSO。SYPRO 27橙色染料的激发和发射滤光片分别设置为465和590 nm,以4°C/min的速率在25°C至95°C的范围内测量扫描。为了评估BAY-850的溴结构域选择性,使用Mx3005p机器进行了热熔实验。蛋白质在10 mM HEPES、pH 7.5、500 mM NaCl中缓冲,并在96孔板中以20μL体积中2μM的终浓度进行测定BAY-850以获得10μM的终浓度,并从供应的原料中以1:1000的稀释度加入SYPRO Orange。SYPRO Orange染料的激发和发射滤光片分别设置为465和590 nm。以每分钟3°C的速度将温度从25°C升高到96°C,并在每个时间间隔读取荧光读数 天然质谱[1] 使用分子量截止值为10kDa的Slide-A-Lyzer透析盒,通过透析用100mM乙酸铵(pH 6.8)和1mM DTT交换ATAD2样品缓冲液。使用NanoDrop 2000分光光度计通过280nm处的吸光度测定透析后的蛋白质浓度。对于滴定实验,ATAD2蛋白质样品用100 mM乙酸铵稀释至10µM,并与1.25至50µM的配体浓度一起孵育,最终DMSO浓度为1%。肽竞争实验是通过将10µM ATAD2蛋白与10µM肽一起孵育,随后以1.2%的DMSO终浓度增加配体浓度(1.25-50µM)来进行的。在Waters SYNAPT G2-S四极杆飞行时间质谱仪上收集了28个纳米电喷雾质谱数据,该质谱仪连接到基于Triversa NanoMate芯片的纳米ESI源,在正离子模式下以1.7 kV的芯片喷嘴电压和导电移液管尖端后部2.7巴的压力运行。源温度保持在室温。所有测量均在三种不同的锥电压(50、75和100 V)下进行,以找到在不破坏非共价蛋白质-配体相互作用的情况下获得窄峰形状的最佳条件。使用碘化钠簇(2µg/µL,溶于2-丙醇:水;1:1)对仪器进行校准,最高可达m/z 3500。为了提高信噪比,质谱累积1-2分钟。使用MassLynx软件版本4.1控制仪器并评估数据。 尺寸排阻色谱法(SEC)[1] 为了通过BAY-850评估ATAD2溴结构域二聚,将ATAD2和GST-ATAD2制剂分别等分为两个样品;其中一个用摩尔比为1:1的BAY-850(50mM DMSO储备溶液)孵育,而另一个用相同量的DMSO而不是化合物(apo样品)孵育。然后使用16/600 HiLoad Superdex200制备级柱和缓冲液B通过SEC分析样品。使用商业凝胶过滤标准进行柱校准。 |
| 细胞实验 |
渗透性测定。[1]
从DSMZ购买的Caco2细胞以每孔4.5 x 104个细胞的密度接种,并在含有典型补充剂的DMEM中生长15天。细胞在37°C的湿度为5%的二氧化碳环境中保存。在进行渗透试验之前,用不含FCS的Hepes碳酸盐转运缓冲液(pH 7.2)代替培养基。为了评估单层完整性,测量了跨上皮电阻。将试验化合物预先溶解在DMSO中,并以2µM的终浓度加入顶端或基底外侧室。在37°C下孵育2小时前后,从两个隔室中取样。用甲醇沉淀后,通过LC/MS/MS分析进行化合物含量分析。在心尖至基底外侧(A→B)和基底外侧至心尖(B→A)方向计算渗透率(Papp)。通过将Papp B-A除以Papp A-B来计算基底外侧(B)与顶端(A)的流出比。平行分析参考化合物作为测定对照。 肝细胞的代谢稳定性。[1] 将各物种的肝细胞悬浮液通过无菌纱布在50 mL Falcon管中过滤,并在室温下以50×g离心3分钟。将细胞颗粒重新悬浮在30 mL WME中,并通过Percoll®梯度在100×g下离心两次。再次用WME洗涤肝细胞,并将其重新悬浮在含有5%FCS的培养基中。肝细胞以1.0×106个活细胞/mL的密度分布在含有5%FCS的WME玻璃瓶中。加入终浓度为1µM的BAY-850和BAY-460。在孵育过程中,以580rpm连续摇动肝细胞悬浮液,并在2、8、16、30、45和90分钟时取等分试样,立即向其中加入等体积的冷甲醇。将样品33在-20°C下冷冻过夜,然后在3000 rpm下离心15分钟,通过LC/MS/MS分析上清液。根据浓度-时间图确定BAY-850和BAY-460的半衰期。根据半衰期计算固有清除率。 肝微粒体的代谢稳定性。[1] 通过在pH 7.4的100 mM磷酸盐缓冲液(NaH2PO4 x H2O+Na2HPO4 x 2H2O)中以1µM浓度在肝微粒体悬浮液中孵育化合物,并在37°C下以0.5 mg/mL的蛋白质浓度孵育化合物来测定体外代谢稳定性。通过加入含有8mM葡萄糖-6-磷酸盐、4mM MgCl2的辅因子混合物来激活微粒体;0.5 mM NADP和1 IU/mL G-6-P-脱氢酶在pH 7.4的磷酸盐缓冲液中。随后不久,通过向培养液中加入最终体积为1 mL的BAY-850或BAY460开始代谢测定。在培养过程中,以580 rpm的速度连续摇动微粒体悬浮液,并在2、8、16、30、45和60分钟时取等分试样,立即向其中加入等体积的冷甲醇。将样品在-20°C下冷冻过夜,然后在3000 rpm下离心15分钟,通过LC/MS/MS分析上清液。根据浓度-时间图确定BAY-850和BAY-460的半衰期。根据半衰期计算体外血液清除率。 |
| 药代性质 (ADME/PK) |
BAY-850 和 BAY-460 具有总体可接受的理化性质和体外药代动力学特征,且渗透性中等(通过 Caco-2 细胞渗透性测定,见补充信息表 4)。这些特性使得我们能够确定其在细胞内的靶点结合情况。我们采用光漂白后荧光恢复 (FRAP) 法,利用我们之前描述的优化方法4,测量了化合物对 MCF7 细胞中标记的全长 ATAD2 从染色质上的置换作用(图 3A-C)。用 1 μM 的 BAY-850 处理后,GFP 标记的全长野生型 ATAD2 的半衰期 (t1/2) 缩短。BAY-460 未观察到此效应,且与 ATAD2 BD 的突变作用相当(图 4B、C)。该方法使我们能够证明 BAY-850 是一种具有细胞活性的 ATAD2 BD 抑制剂,在 1 μM 浓度下具有最大的靶向细胞活性[1]。
|
| 参考文献 | |
| 其他信息 |
ATAD2 (ANCCA) 是一种表观遗传调控因子和转录辅助因子,其过表达与多种癌症的进展相关。本文报道了一种基于 DNA 编码文库筛选的化合物 BAY-850,它是一种高效且具有亚型选择性的 ATAD2 溴结构域抑制剂,能够特异性地诱导 ATAD2 溴结构域二聚化,并抑制其在体外与乙酰化组蛋白的相互作用,以及在细胞内与染色质的相互作用。这些特性使得 BAY-850 成为研究 ATAD2 生物学特性的化学探针。[1]
总之,我们利用 DNA 编码文库的亲和力筛选方法,发现了一类新型的高效且具有亚型选择性的 ATAD2 溴结构域抑制剂。这些特性,以及其良好的溶解性和渗透性,使得 BAY-850 及其非活性对照化合物 BAY-460(在非细胞毒性浓度下给药)成为进一步研究 ATAD2 生物学特性的宝贵工具。此外,我们的结果表明,BAY-850 的作用机制可能与蛋白质二聚体的诱导有关,这一特性可能代表了一种抑制蛋白质-蛋白质相互作用的新方法。18 利用该化合物,我们证实了 ATAD2 BD 在基因表达调控中并非必需。这些发现,结合 ATAD2 基因在基因敲低研究中的作用,使得 ATAD2 特别适合用于靶向蛋白质降解策略。我们的工作为进一步的化合物开发奠定了基础,例如,开发具有更高效力和更优药代动力学特性的 PROTAC“弹头”,这最终可能促成体内探针和新型治疗药物的诞生。[1] |
| 分子式 |
C38H44CLN5O3
|
|---|---|
| 分子量 |
654.240668296814
|
| 精确质量 |
653.313
|
| 元素分析 |
C, 69.76; H, 6.78; Cl, 5.42; N, 10.70; O, 7.34
|
| CAS号 |
2099142-76-2
|
| 相关CAS号 |
2099142-77-3 (isomer); 2099142-76-2; 2561471-14-3 (HCl);
|
| PubChem CID |
129196931
|
| 外观&性状 |
White to light yellow solid powder
|
| LogP |
5.9
|
| tPSA |
125
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
7
|
| 可旋转键数目(RBC) |
13
|
| 重原子数目 |
47
|
| 分子复杂度/Complexity |
1000
|
| 定义原子立体中心数目 |
2
|
| SMILES |
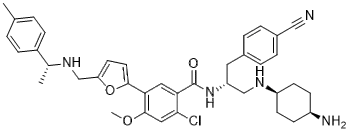
ClC1=CC(=C(C2=CC=C(CN[C@@H](C)C3C=CC(C)=CC=3)O2)C=C1C(N[C@@H](CC1C=CC(C#N)=CC=1)CNC1CCC(CC1)N)=O)OC
|
| InChi Key |
BSISGUIVBKDTQO-JLXKDNNHSA-N
|
| InChi Code |
InChI=1S/C38H44ClN5O3/c1-24-4-10-28(11-5-24)25(2)42-23-32-16-17-36(47-32)34-19-33(35(39)20-37(34)46-3)38(45)44-31(18-26-6-8-27(21-40)9-7-26)22-43-30-14-12-29(41)13-15-30/h4-11,16-17,19-20,25,29-31,42-43H,12-15,18,22-23,41H2,1-3H3,(H,44,45)/t25-,29?,30?,31-/m1/s1
|
| 化学名 |
N-[(2R)-1-[(4-Aminocyclohexyl)amino]-3-(4-cyanophenyl)propan-2-yl]-2-chloro-4-methoxy-5-[5-({[(1R)-1-(4-methylphenyl)ethyl]amino}methyl)-2-furyl]benzamide
|
| 别名 |
BAY-850; BAY850; BAY-850; 2099142-76-2; CHEMBL4536031; N-[(2R)-1-[(4-aminocyclohexyl)amino]-3-(4-cyanophenyl)propan-2-yl]-2-chloro-4-methoxy-5-[5-[[[(1R)-1-(4-methylphenyl)ethyl]amino]methyl]furan-2-yl]benzamide; N-[(2R)-1-[(4-aminocyclohexyl)amino]-3-(4-cyanophenyl)propan-2-yl]-2-chloro-4-methoxy-5-[5-({[(1R)-1-(4-methylphenyl)ethyl]amino}methyl)furan-2-yl]benzamide; trans-BAY-850; SCHEMBL18930553; SCHEMBL21144877;
BAY 850
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~62.5 mg/mL (~95.53 mM)
H2O : < 0.1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 6.25 mg/mL (9.55 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 62.5 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 6.25 mg/mL (9.55 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 62.5 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.5285 mL | 7.6425 mL | 15.2849 mL | |
| 5 mM | 0.3057 mL | 1.5285 mL | 3.0570 mL | |
| 10 mM | 0.1528 mL | 0.7642 mL | 1.5285 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Discovery of BAY-850.
Cellular target engagement and mechanistic activity of BAY-850.ACS Chem Biol. 2017 Nov 17;12(11):2730-2736. |
Characterization of BAY-850’s mode of action.ACS Chem Biol. 2017 Nov 17;12(11):2730-2736. |
Potency and selectivity of BAY-850.ACS Chem Biol. 2017 Nov 17;12(11):2730-2736. |