| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 2g |
|
||
| 5g |
|
||
| 10g |
|
||
| Other Sizes |
|
| 靶点 |
Cyclooxygenase-1 (COX-1) (IC50 = 0.5 μM) [3]
- Cyclooxygenase-2 (COX-2) (IC50 = 0.1 μM) [3] |
|---|---|
| 体外研究 (In Vitro) |
在 HLEC-B3 中,溴芬酸(0-80 μg/mL;24 h)可以浓度依赖性方式阻断转化生长因子-β2 触发的上皮间质转化[2]。在人前囊中,转化生长因子-β2 诱导的上皮-间质转化受到溴芬酸(80 μg/Ml;48 小时)的抑制[2]。
Bromfenac Sodium(AHR 10282R) 对COX-2表现出强效抑制活性(IC50 = 0.1 μM),对COX-1具有中等抑制作用(IC50 = 0.5 μM),对COX-2具有优先选择性[3] - 在人晶状体上皮细胞(LECs)中,Bromfenac Sodium(0.1–10 μM)以剂量依赖性方式抑制细胞增殖。10 μM浓度下,增殖抑制率达78%;5 μM时,Western blot检测显示α-平滑肌肌动蛋白(α-SMA)和I型胶原蛋白表达分别降低65%和58%[2] - 该化合物(1–10 μM)在体外抑制LECs迁移,划痕实验中10 μM浓度下迁移能力降低62%[2] |
| 体内研究 (In Vivo) |
在大鼠中,溴芬酸(0.0032-3.16%;100 或 200 μL;局部应用)在剂量低至 0.1%(治疗前 4 小时)或 0.32%(治疗前 18 小时)时具有显着的抗炎作用[3]。当局部应用于爪子时,溴芬酸(0.032-3.16%;100 μL)对大鼠具有剂量依赖性抗炎作用[3]。将溴芬酸(0.032-1.0%;50 μL)直接涂抹在暴露于紫外线的豚鼠皮肤区域,其预防红斑的效果是吲哚美辛的 26 倍[3]。当将溴芬酸(0.0032-0.1%;50 μL)涂抹到未注射的爪子上,每周 5 天,每天 4 小时,大鼠双后肢的爪子体积会以剂量和时间依赖性方式减少[3] 。当局部应用于腹部时,溴芬酸(0.32%;50 μL)可显着抑制小鼠响应乙酰胆碱挑战而出现的腹部收缩[3]。当作为滴眼剂使用时,每天两次使用 1 μL (0.09%) 溴芬酸,持续 4 周,可部分减少角膜染色,到第四周时角膜染色变得不那么明显[4]。
家兔眼部局部给予Bromfenac Sodium(0.1%滴眼液,每日4次,连续7天)后,视网膜脉络膜组织中可检测到药物浓度。脉络膜中药物峰浓度在给药后1小时达2.8 ng/g,视网膜中在2小时达1.6 ng/g,表明其能有效渗透至眼后段[1] - 在大鼠后发性白内障(PCO)模型中,植入载Bromfenac Sodium的人工晶状体(载药量:50 μg/晶状体)可显著抑制PCO形成。植入后8周,PCO分级从对照组的3.2降至1.1,后囊膜上增殖的LECs数量减少72%[2] - 在角叉菜胶诱导的大鼠足肿胀模型中,局部涂抹Bromfenac Sodium(1%、2%软膏)以剂量依赖性方式抑制肿胀。2%软膏在角叉菜胶注射后4小时的最大抑制率达68%[3] - 在乙酸诱导的小鼠扭体实验中,腹腔注射Bromfenac Sodium(5、10 mg/kg)产生镇痛作用,抑制率分别为45%和70%;甩尾实验中,10 mg/kg(腹腔注射)较对照组延长甩尾潜伏期52%[3] - 在肉毒杆菌毒素B诱导的小鼠干燥性角结膜炎模型中,局部给予Bromfenac Sodium(0.1%滴眼液,每日2次,连续14天)可减轻眼表炎症,角膜荧光素染色评分降低55%,泪液分泌量增加42%[4] |
| 酶活实验 |
COX-1/COX-2抑制活性测定:COX-1来源于绵羊精囊,COX-2为人类重组酶。反应体系包含酶、花生四烯酸(底物)及不同浓度的Bromfenac Sodium(0.01–10 μM),37°C孵育15分钟后,采用酶联免疫试剂盒定量前列腺素E2(PGE2)生成量,通过非线性回归分析计算IC50值[3]
|
| 细胞实验 |
细胞活力测定[2]
细胞类型:经转化生长因子-β2 处理的人前囊。 测试浓度: 80 μg/mL 孵育时间: 48 小时 实验结果: 抑制转化生长因子-β2 诱导初级晶状体上皮细胞 (LEC) 的上皮-间质转化。 细胞迁移测定 [2] 细胞类型: HLEC-B3 细胞 测试浓度: 0、20、40、60、和 80 μg/ mL 孵育时间:24 小时 实验结果:抑制 HLEC-B3 中转化生长因子-β2 诱导的细胞迁移细胞,并显示出对上皮间质转化标记物过度表达的抑制。 LEC增殖测定:人LECs以每孔3×103个细胞接种到96孔板,过夜培养后用Bromfenac Sodium(0.1–10 μM)处理48小时。采用CCK-8法检测细胞活力,计算增殖抑制率[2] - α-SMA和I型胶原蛋白Western blot分析:LECs接种到6孔板,用Bromfenac Sodium(1–10 μM)处理72小时后裂解细胞,蛋白提取物经SDS-PAGE分离并转膜,用α-SMA、I型胶原蛋白和β-肌动蛋白抗体孵育,图像分析软件定量条带强度[2] - LEC迁移测定:LECs接种到6孔板培养至融合,用移液管尖端制造划痕损伤,加入Bromfenac Sodium(1–10 μM)处理,在0小时和24小时显微镜下测量划痕面积并计算伤口愈合率[2] |
| 动物实验 |
动物/疾病模型:雄性SD(Sprague-Dawley)大鼠(150-250克)注射角叉菜胶[2]
剂量:0.0032、0.01、0.032、0.1、0.32、1.0、3.16%(100或200微升) 给药途径:注射角叉菜胶前1-72小时涂抹于背部 实验结果:在0.32%角叉菜胶刺激前1、2和4小时涂抹,可产生显著的抗炎活性。在角叉菜胶攻击前 1 或 4 小时使用有效,但在角叉菜胶攻击前 24 小时(或更长时间)使用无效(0.2%)。 兔视网膜脉络膜渗透研究:将新西兰白兔随机分为对照组和溴芬酸钠组(每组 n=6)。将药物配制成 0.1% 的滴眼液,每日局部滴眼 4 次,连续 7 天。在末次给药后 1、2、4、8、12 和 24 小时,处死兔子,并解剖视网膜和脉络膜。药物浓度采用高效液相色谱法 (HPLC) 测定 [1] - 大鼠后囊膜混浊 (PCO) 模型:Sprague-Dawley 大鼠接受超声乳化术,并植入载有溴芬酸钠的人工晶状体(载药量:25、50、100 μg/晶状体)或空白晶状体(对照)。术后 2、4、6 和 8 周,处死大鼠,摘除眼球,进行 PCO 和晶状体上皮细胞 (LEC) 增殖的组织学分析 [2] - 啮齿动物抗炎和镇痛模型:对于爪水肿模型,Wistar 大鼠在右后爪局部涂抹溴芬酸钠(1%、2% 软膏),30 分钟后皮下注射角叉菜胶(1% 生理盐水)。分别于注射角叉菜胶后 1、2、4 和 6 小时测量爪体积。为进行镇痛实验,ICR 小鼠在注射醋酸(0.6% 生理盐水,腹腔注射)前 30 分钟腹腔注射溴芬酸钠(5、10 mg/kg),并记录 15 分钟内的扭体次数。在另一组小鼠中,于给药后 60 分钟测量甩尾潜伏期 [3]。 - 小鼠干眼症模型:C57BL/6 小鼠泪腺内注射 B 型肉毒杆菌毒素(10 mU/眼)以诱导干眼。三天后,小鼠每天两次使用溴芬酸钠(0.1% 眼药水)治疗,持续 14 天。采用酚红线法测量泪液分泌量,并在基线和第 14 天对角膜荧光素染色进行评分[4] |
| 药代性质 (ADME/PK) |
在兔眼中,局部滴用溴芬酸钠(0.1%滴眼液)后,药物在脉络膜的平均停留时间(MRT)为3.8小时,在视网膜的平均停留时间为4.2小时。脉络膜和视网膜的浓度-时间曲线下面积(AUC0-24h)分别为8.6 ng·h/g和5.8 ng·h/g [1]。该药物能迅速被眼部组织吸收,给药后1-2小时内达到峰值浓度,并维持在可检测水平长达24小时 [1]。
|
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概要 口服常用剂量溴芬酸钠后,乳汁中的药物浓度可能较低,但注射较高剂量后尚未测量乳汁中的药物浓度。哺乳期妇女使用溴芬酸钠时应谨慎,尤其是注射剂。 母亲使用溴芬酸钠滴眼液预计不会对母乳喂养的婴儿造成任何不良影响。为了大幅减少使用滴眼液后进入母乳的药物量,请按压眼角泪管至少 1 分钟,然后用吸水纸巾吸去多余的药液。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 兔子局部使用 0.1% 溴芬酸钠滴眼液 7 天后,未观察到明显的眼毒性,未出现角膜上皮损伤、结膜充血或前房炎症[1]。 - 在植入溴芬酸钠洗脱型人工晶状体(每片晶状体最高 100 μg)的大鼠中,未检测到全身毒性,包括体重、血清 ALT 等无显著变化。植入后 8 周的 AST 或肌酐水平 [2] - 在大鼠身上局部应用溴芬酸钠软膏(浓度高达 2%)不会引起皮肤刺激,例如用药部位出现发红、水肿或糜烂 [3] |
| 参考文献 |
|
| 其他信息 |
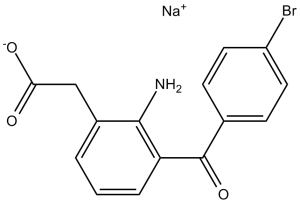
溴芬酸钠是溴芬酸的钠盐。请注意,“溴芬酸钠”通常指的是倍半水合物(CAS号:120638-55-3),即无水形式。它是一种非甾体类抗炎药和非麻醉性镇痛药。它含有溴芬酸(1-)基团。
溴芬酸钠是溴芬酸的钠盐形式,溴芬酸是一种具有镇痛和抗炎作用的非甾体类抗炎药(NSAID)。眼用后,溴芬酸与环氧合酶II(COX II)结合并抑制其活性。COX II是一种将花生四烯酸转化为环状内过氧化物(前列腺素(PG)的前体)的酶。溴芬酸通过抑制前列腺素(PG)的生成,能够抑制PG诱导的炎症,从而预防血管舒张、白细胞增多、血-房水屏障破坏、血管通透性增加和眼内压(IOP)升高。 另见:溴芬酸(含有活性成分)。 药物适应症 治疗成人白内障摘除术后眼部炎症。 溴芬酸钠(AHR 10282R)是一种非甾体抗炎药(NSAID),它通过抑制环氧合酶发挥抗炎和镇痛作用,从而减少前列腺素的合成[3]。 - 局部给药后,其能够渗透到眼后部组织,因此适用于治疗眼内炎症和预防后囊膜混浊(PCO)[1][2]。 - 该化合物对……具有优先选择性。与非选择性非甾体抗炎药相比,COX-2 抑制 COX-1 活性,这可能有助于降低全身性副作用的风险[3] - 除了抗炎和镇痛作用外,它还能抑制 LEC 增殖和迁移,这是其预防多囊卵巢综合征 (PCOS) 的关键机制[2] |
| 分子式 |
C15H11BRNO3.NA
|
|
|---|---|---|
| 分子量 |
356.15
|
|
| 精确质量 |
354.981
|
|
| CAS号 |
91714-93-1
|
|
| 相关CAS号 |
Bromfenac sodium hydrate;120638-55-3;Bromfenac;91714-94-2;Bromfenac-d4 sodium;2749400-35-7
|
|
| PubChem CID |
23693301
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 沸点 |
562.2ºC at 760 mmHg
|
|
| 熔点 |
285ºC
|
|
| 闪点 |
293.8ºC
|
|
| 蒸汽压 |
1.77E-13mmHg at 25°C
|
|
| LogP |
2.135
|
|
| tPSA |
83.22
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
4
|
|
| 重原子数目 |
21
|
|
| 分子复杂度/Complexity |
372
|
|
| 定义原子立体中心数目 |
0
|
|
| InChi Key |
HZFGMQJYAFHESD-UHFFFAOYSA-M
|
|
| InChi Code |
InChI=1S/C15H12BrNO3.Na/c16-11-6-4-9(5-7-11)15(20)12-3-1-2-10(14(12)17)8-13(18)19;/h1-7H,8,17H2,(H,18,19);/q;+1/p-1
|
|
| 化学名 |
2-Amino-3-(4-bromobenzoyl)benzeneacetic acid sodium
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮和光照。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1.14 mg/mL (3.20 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 11.4 mg/mL澄清DMSO储备液加入到400 μL PEG300中并混合均匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.14 mg/mL (3.20 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 11.4 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.8078 mL | 14.0390 mL | 28.0781 mL | |
| 5 mM | 0.5616 mL | 2.8078 mL | 5.6156 mL | |
| 10 mM | 0.2808 mL | 1.4039 mL | 2.8078 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05107921 | Recruiting | Drug: Bromfenac Sodium | Familial Exudative Vitreoretinopathies | Seoul National University Hospital | November 1, 2021 | Phase 2 |
| NCT01387464 | Completed Has Results | Drug: ISV-303 Drug: Bromday™ |
Cataract | Sun Pharmaceutical Industries Limited | July 2011 | Phase 2 |
| NCT01576952 | Completed Has Results | Drug: ISV-303 Other: DuraSite Vehicle |
Ocular Inflammation | Sun Pharmaceutical Industries Limited | July 2012 | Phase 3 |
| NCT01310127 | Completed Has Results | Drug: Bromfenac Drug: Nepafenac |
Inflammation Pseudophakia |
Toyos Clinic | November 2010 | Phase 4 |
|
|
|