| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
IKKβ; COX2
Dehydrocostus Lactone (DHE) targets IKKβ by binding to its ATP-binding site, thereby inhibiting the NF-κB/COX-2 signaling pathway. The study does not provide IC₅₀, Ki, or EC₅₀ values for binding to IKKβ. - Directly targets IKKβ (Inhibitor of Nuclear Factor Kappa-B Kinase subunit beta) by binding to its ATP-binding site, as demonstrated by molecular docking studies. [2] - Inhibits the phosphorylation of IKKα/β, IκBα, and p65 (NF-κB subunit). [2] - Downregulates COX-2 (Cyclooxygenase-2) expression at both mRNA and protein levels. [2] - Modulates apoptosis-related proteins: decreases Bcl-2, increases BAX and cleaved caspase-3/9, and promotes cytochrome c release. [2] |
|---|---|
| 体外研究 (In Vitro) |
脱氢木香内酯(DHE)可在体外抑制PGE2的合成。它能显著降低COX-2的表达,但对COX-1的表达无影响[1]。DHE处理后,胶质母细胞瘤(U118、U251或U87)细胞的活力、增殖和迁移能力均显著降低。DHE诱导线粒体介导的细胞凋亡的另一种途径是释放细胞色素c至胞质溶胶,从而激活caspase信号通路。DHE通过靶向ATP结合位点阻断IKK磷酸化,并阻止NF-κB与COX-2启动子的结合和p300的募集,从而显著降低COX-2的表达。 DHE抑制胶质母细胞瘤细胞的迁移和集落形成能力,并通过线粒体途径诱导细胞凋亡[2]。
脱氢木香内酯通过多种机制在多种胶质母细胞瘤细胞系中表现出显著的抗胶质瘤作用。 1. 抑制细胞活力:在U118、U251和U87胶质母细胞瘤细胞中,DHE(0-100 μM)以剂量和时间依赖性方式(12、24、36、48 h)抑制细胞活力。48 h时的IC₅₀值分别为17.16 ± 2.11 μM (U118)、22.33 ± 1.93 μM (U251)和26.42 ± 2.84 μM (U87)。 [2] 2. 抑制克隆形成:用DHE(10和20 μM)处理3小时后,U87和U251细胞形成的克隆数量呈剂量依赖性显著减少。[2] 3. 抑制细胞迁移(伤口愈合实验):在U118和U251细胞中,用DHE(10和20 μM)处理48小时后,与对照组相比,细胞迁移率显著降低(P < 0.01)。[2] 4. 诱导线粒体凋亡:在U87细胞中,用DHE处理(48小时)后,细胞色素c从线粒体释放到胞质溶胶(共聚焦显微镜和Western blot)。它还降低了抗凋亡蛋白Bcl-2/BAX的比值,并以剂量依赖的方式增加了procaspase-9和procaspase-3的裂解。[2] 5. COX-2表达下调:如Western blot和RT-PCR所示,DHE(10、20、30 μM;48 h)以剂量依赖的方式抑制U87和U251细胞中COX-2蛋白的表达以及COX-2 mRNA的水平。[2] 6. NF-κB转录活性抑制:在U87细胞中进行的ChIP和链霉亲和素-琼脂糖下拉实验表明,DHE以剂量依赖的方式抑制p300的募集以及p50/p65 NF-κB与COX-2启动子的结合。 Western blot 和免疫荧光实验证实,DHE 降低了 p300、p65 和 p50 的核转位。[2] 7. IKKβ/NF-κB 信号通路的抑制:在 U87 和 U251 细胞中进行的 Western blot 分析显示,DHE(10、20、30 μM;48 h)呈剂量依赖性地降低了 IKKα/β、IκBα 和 p65 的磷酸化水平,而对 IKKα、IKKβ、IκBα 和 p65 的总蛋白水平没有影响。[2] 8. 分子对接(IKKβ 结合):分子建模研究预测,DHE 与 IKKβ 的 ATP 结合位点结合,并通过其内酯环与 Cys99 形成氢键,该内酯环延伸至口袋的疏水腔内。 [2] |
| 体内研究 (In Vivo) |
脱氢木香内酯可抑制无胸腺小鼠体内结肠癌细胞系colo205移植的结直肠癌异种移植瘤的生长。抑制作用与剂量呈正相关[1]。脱氢木香内酯可穿过血脑屏障(BBB)。在异种移植裸鼠模型中,DHE治疗显著降低了肿瘤的重量和体积,且未观察到明显的不良反应,这些作用可能是通过抑制IKKβ/NF-κB/COX-2信号通路介导的[2]。
脱氢木香内酯在异种移植裸鼠模型中表现出显著的抗肿瘤疗效,且无明显毒性。 1. 血脑屏障穿透性:腹腔注射DHE(100 mg/kg)1小时后,对SD大鼠脑脊液进行LC-MS/MS分析,结果显示只有一个峰,表明DHE可以快速穿过血脑屏障。 [2] 2. 异种移植模型中肿瘤生长的抑制:将携带 U87 皮下异种移植瘤的裸鼠分别用 DHE(10 或 20 mg/kg/d,腹腔注射)或 PBS 治疗 14 天。与对照组相比,两种剂量的 DHE 均显著降低了肿瘤体积和重量。[2] 3. 无全身毒性:在整个实验过程中,DHE 治疗组和对照组小鼠的体重无显著差异,表明在所测试的剂量下未观察到明显的副作用。 [2] 4. 体内抑制 IKKβ/NF-κB/COX-2 通路:肿瘤异种移植的免疫组织化学染色显示,DHE 处理呈剂量依赖性地降低了 COX-2、磷酸化 p65 (p-p65) 和磷酸化 IKKβ (p-IKKβ) 的表达。[2] |
| 酶活实验 |
未对纯化酶进行直接酶活性测定。IKKβ靶向的主要证据来自分子对接研究。
1. 分子对接:本研究采用分子对接模拟DHE与IKKβ的相互作用。使用SurflexDock将DHE的优化结构对接至IKKβ的活性位点(PDB代码:4KIK)。结果预测DHE与ATP结合位点结合,并与Cys99形成氢键。采用MOLCAD表面分析可视化结合模式。[2] |
| 细胞实验 |
为了获得70%汇合度的单层细胞,对U118(6×10³个细胞/孔)、U251(8×10³个细胞/孔)和U87(7×10³个细胞/孔)细胞进行计数,并使其贴壁。然后用指定浓度的DHE处理细胞。分别孵育12、24、36或48小时后,向每个孔中加入10 μL MTT(5 mg/ml),并继续孵育4小时。为了溶解甲臜晶体,用100 μL DMSO替换培养基。使用酶标仪在570 nm处测量吸光度。每个实验至少重复三次。通过剂量反应曲线外推法确定IC50值。
采用多种基于细胞的检测方法来表征脱氢木香内酯对胶质母细胞瘤细胞的影响。 1. 细胞活力(MTT法):将U118、U251和U87细胞接种于96孔板中,用不同浓度的DHE处理12-48小时,加入MTT孵育4小时,并在570 nm处测量吸光度以计算IC₅₀值。[2] 2. 克隆形成实验:将U87和U251细胞接种于6孔板中,用DHE处理3小时,然后在新鲜培养基中培养15天。固定克隆,用结晶紫染色,并进行计数。 [2] 3. 伤口愈合实验:用移液器吸头划伤汇合的U118和U251细胞单层,在无血清培养基中加入DHE处理48小时,然后对伤口愈合情况进行成像和定量分析。[2] 4. 免疫荧光:将生长在盖玻片上的U87细胞用DHE处理,固定、透化后,分别与针对细胞色素c、p300、p65或p50的一抗孵育,随后与荧光二抗孵育。用DAPI进行细胞核复染,并通过共聚焦显微镜采集图像。 [2] 5. Western Blot:制备细胞裂解液或核提取物,经SDS-PAGE分离后转移至PVDF膜,并用针对目标蛋白(例如,裂解型caspase-3/9、COX-2、p-IKK、p-p65)的特异性抗体进行检测。蛋白条带通过ECL显色并进行定量。[2] 6. RT-PCR:提取细胞总RNA,进行逆转录,并使用COX-2和GAPDH的特异性引物进行PCR。PCR产物通过琼脂糖凝胶电泳进行分析。[2] 7. 染色质免疫沉淀(ChIP):用甲醛交联U87细胞,超声处理,并与针对p300、p65、p50或IgG的抗体孵育。纯化DNA,并使用COX-2启动子特异性引物进行PCR分析。 [2] 8. 链霉亲和素-琼脂糖下拉实验:将U87细胞的核提取物与生物素标记的COX-2启动子探针和链霉亲和素-琼脂糖珠孵育。通过Western blot分析结合的p300、p65和p50蛋白。[2] |
| 动物实验 |
雌性无胸腺裸鼠(4-6周龄)和Sprague Dawley大鼠(8-10周龄)
10和20 mg/kg 腹腔注射 本研究采用了两种主要的体内实验方案:血脑屏障穿透的药代动力学研究和异种移植模型中的疗效/毒性研究。 1. **血脑屏障穿透研究:** - **动物:**雄性Sprague Dawley大鼠(200-220 g)。[2] - **给药:**大鼠腹腔注射DHE(100 mg/kg)。[2] - **样本采集:**注射后1小时,对大鼠进行麻醉,并从枕大池采集脑脊液(CSF)。 [2] - **样品制备与分析:** 将脑脊液与乙腈混合,离心,上清液在氮气下干燥。残渣复溶后,采用液相色谱-串联质谱法(LC-MS/MS)检测二氢麦角胺(DHE)。[2] 2. **异种移植瘤模型(疗效和毒性):** - **动物:** 雌性无胸腺裸鼠(4-6周龄)。[2] - **肿瘤接种:** 将U87细胞(1 × 10⁷)皮下注射到每只小鼠的左侧腋窝。 [2] - **治疗方案:**两周后,将小鼠随机分为三组(每组n=6),分别每日腹腔注射PBS(对照组)、DHE(10 mg/kg)或DHE(20 mg/kg),持续14天。[2] - **监测:**每2天记录小鼠体重和肿瘤体积(计算公式为V = 1/2 × 长 × 宽²)。[2] - **终点操作:**第30天,处死小鼠。切除肿瘤,称重并拍照。将肿瘤组织固定于福尔马林中,用于COX-2、p-p65和p-IKKβ的免疫组织化学分析。 [2] 本研究采用了两种主要的体内实验方案:血脑屏障穿透的药代动力学研究和异种移植模型中的疗效/毒性研究。 1. 血脑屏障穿透研究: - 动物:雄性 Sprague Dawley 大鼠(200-220 g)。[2] - 给药:大鼠腹腔注射二氢麦角胺(DHE)(100 mg/kg)。[2] - 样本采集:注射后 1 小时,对大鼠进行麻醉,并从枕大池采集脑脊液(CSF)。[2] - 样本制备和分析:将脑脊液与乙腈混合,离心,并将上清液在氮气下干燥。将残余物复溶,并通过液相色谱-串联质谱法(LC-MS/MS)分析以检测二氢麦角胺(DHE)。 [2] 2. 异种移植瘤模型(疗效和毒性): - 动物:雌性无胸腺裸鼠(4-6周龄)。[2] - 肿瘤接种:将U87细胞(1 × 10⁷)皮下注射到每只小鼠的左侧腋窝。[2] - 治疗方案:两周后,将小鼠随机分为三组(每组n=6),分别每日腹腔注射PBS(对照组)、DHE(10 mg/kg)或DHE(20 mg/kg),持续14天。[2] - 监测:每2天记录一次小鼠的体重和肿瘤体积(计算公式为V = 1/2 × 长 × 宽²)。[2] - 处死程序:第30天,处死小鼠。肿瘤被切除、称重并拍照。肿瘤组织用福尔马林固定,用于COX-2、p-p65和p-IKKβ的免疫组织化学分析。[2] |
| 药代性质 (ADME/PK) |
该研究提供了脑渗透的证据,但未提供详细的药代动力学参数。
- 血脑屏障渗透:腹腔注射(100 mg/kg)1 小时后,在大鼠脑脊液中检测到了DHE,表明其能够快速穿过血脑屏障。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
该研究提供了异种移植模型的初步安全性数据。
- 体内毒性(异种移植模型):在携带 U87 异种移植瘤的裸鼠中,连续 14 天每日腹腔注射 10 和 20 mg/kg 的 DHE,与对照组相比,未引起体重显著变化,表明这些剂量下未观察到明显的全身毒性或副作用。[2] |
| 参考文献 | |
| 其他信息 |
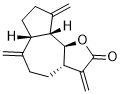
脱氢金烯内酯是一种有机杂三环化合物,属于愈创木烷倍半萜内酯家族。其结构为丙烯酸2位被4-羟基-3,8-双(亚甲基)癸基肼-5-基取代,其中羟基和羧基发生缩合反应生成相应的γ-内酯。它可用作代谢物、锥虫杀灭剂、抗肿瘤剂、环氧合酶2抑制剂、抗分枝杆菌药物和细胞凋亡诱导剂。它是一种倍半萜内酯、愈创木烷倍半萜化合物、有机杂三环化合物和γ-内酯。据报道,脱氢金烯内酯存在于单花艾菊(Ainsliaea uniflora)、姜科植物(Costus)和其他具有相关数据的生物体中。另见:牛蒡根(部分)。
脱氢木香内酯 (DHE) 是一种天然倍半萜内酯,提取自旋覆花 (Inula helenium L.) 和风毛菊 (Saussurea lappa) 等药用植物。传统上,它因其抗炎、抗溃疡和免疫调节特性而被使用。本研究首次全面探讨了其抗胶质瘤作用及其潜在机制。主要研究结果表明,DHE 能有效抑制体外和体内胶质母细胞瘤细胞的生长、增殖、迁移和存活。其主要作用机制是直接靶向 IKKβ 的 ATP 结合位点,从而抑制经典的 NF-κB 通路。这导致IκBα磷酸化和降解减少,p50/p65 NF-κB核转位降低,共激活因子p300向COX-2启动子的募集减少,最终导致COX-2表达下调。DHE还能诱导线粒体介导的细胞凋亡。重要的是,该研究首次证实DHE能够穿过血脑屏障,这对于脑肿瘤治疗至关重要。在异种移植模型中,DHE显著抑制了肿瘤生长,且未观察到明显的毒性。这些发现表明DHE有望成为治疗胶质母细胞瘤的先导化合物。[2] |
| 分子式 |
C15H18O2
|
|---|---|
| 分子量 |
230.307
|
| 精确质量 |
230.13
|
| 元素分析 |
C, 78.23; H, 7.88; O, 13.89
|
| CAS号 |
477-43-0
|
| 相关CAS号 |
477-43-0
|
| PubChem CID |
73174
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
383.7±42.0 °C at 760 mmHg
|
| 熔点 |
59 °C
|
| 闪点 |
161.2±25.3 °C
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
| 折射率 |
1.536
|
| LogP |
3.4
|
| tPSA |
26.3
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
0
|
| 重原子数目 |
17
|
| 分子复杂度/Complexity |
432
|
| 定义原子立体中心数目 |
4
|
| SMILES |
O1C(C(=C([H])[H])[C@]2([H])C([H])([H])C([H])([H])C(=C([H])[H])[C@]3([H])C([H])([H])C([H])([H])C(=C([H])[H])[C@]3([H])[C@@]12[H])=O
|
| InChi Key |
NETSQGRTUNRXEO-XUXIUFHCSA-N
|
| InChi Code |
InChI=1S/C15H18O2/c1-8-4-7-12-10(3)15(16)17-14(12)13-9(2)5-6-11(8)13/h11-14H,1-7H2/t11-,12-,13-,14-/m0/s1
|
| 化学名 |
(3aS,6aR,9aR,9bS)-3,6,9-trimethylidene-3a,4,5,6a,7,8,9a,9b-octahydroazuleno[4,5-b]furan-2-one
|
| 别名 |
(-)-Dehydrocostus lactone; Dehydrocostus Lactone
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 46~250 mg/mL (199.7~1085.5 mM)
Ethanol: 15~46 mg/mL (65.1 mM~199.7) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (9.03 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (9.03 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (9.03 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.3420 mL | 21.7099 mL | 43.4197 mL | |
| 5 mM | 0.8684 mL | 4.3420 mL | 8.6839 mL | |
| 10 mM | 0.4342 mL | 2.1710 mL | 4.3420 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|