| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Autophagy
|
|---|---|
| 体外研究 (In Vitro) |
EACC 不影响内溶酶体活性,但会抑制自噬体-溶酶体融合 [1]。通过阻止 SNARE Stx17 加载自噬体,EACC 限制了自噬体融合 [1]。 RAB、系绳和溶酶体功能性 SNARE 不受 EACC 影响,尽管 EACC 阻止它们与 LC3 和 Stx17 相互作用 [1]。
自噬是一种进化上保守的细胞内溶酶体降解途径。这是一个涉及双膜自噬体从头形成的多步骤过程,自噬体捕获细胞质成分(货物)并最终与溶酶体融合,其中货物被降解,从而产生更简单的生物分子被循环利用。除了自噬功能外,一些自噬相关蛋白还在其他囊泡运输途径的界面上起作用。因此,开发不干扰内溶酶体运输的特异性自噬调节剂具有独特的挑战。在本文中,我们报道了一种新的小分子EACC,它通过阻断自噬体与溶酶体的融合来抑制自噬通量。引人注目的是,与其他晚期抑制剂不同,EACC对溶酶体特性或内吞介导的EGF受体降解没有任何影响。EACC影响SNAREs Stx17和SNAP29在自噬体上的易位,但不阻碍自噬体的完成。EACC处理还降低了Stx17与HOPS亚基VPS33A和同源溶酶体R-SNARE VAMP8的相互作用。有趣的是,尽管EACC的这种作用非常强大,但它是可逆的,因此EACC可以用作研究自噬体SNARE运输的工具。我们的研究结果提出了一种通过阻断自噬体SNAREs的作用来阻断自噬通量的新方法。 [1] |
| 细胞实验 |
CellTiter-Glo细胞活力测定[1]
采用CellTiter-Glo细胞活力法检测化合物的毒性。对HeLa细胞进行计数,等量(1500个/孔)接种于384孔板中的生长培养基中。第二天,在饥饿培养基中混合100 nM ~ 100 μM范围内不同浓度的EACC,加入到细胞中,孵育5小时。5小时后,每孔加入CellTiter-Glo Reagent,使用Varioskan Flash测量发光。 EGFR贩运[1] HeLa细胞被镀在六孔板上并允许附着。第二天,用PBS洗涤细胞,然后在DMEM(无血清培养基)中饥饿3小时。用<强>EACC预处理1小时,然后用100 ng/ml EGF脉冲细胞,并在0,1 -,2-和3-h间隔收集样本。 |
| 参考文献 |
[1]. Vats S, et al. A reversible autophagy inhibitor blocks autophagosome-lysosome fusion by preventing Stx17 loading onto autophagosomes. Mol Biol Cell. 2019 Aug 1;30(17):2283-2295.
|
| 其他信息 |
EACC介导的自噬通量阻断最显著的特征是Stx17向自噬体的装载受损。据我们所知,目前尚无其他报道指出存在任何能够选择性阻止Stx17转位从而使自噬体“丧失融合能力”的自噬化学调节剂。Stx17转位至完整自噬体的确切机制尚不十分清楚。最近的一项研究表明,Stx17通过与小GTP酶IRGM和哺乳动物ATG8蛋白相互作用而被募集到自噬体上(Kumar等,2018)。虽然我们尚未验证EACC是否会影响Stx17与IRGM的相互作用,但我们认为,在EACC存在或不存在的情况下鉴定Stx17的结合蛋白,可能有助于揭示EACC的靶点,并有助于鉴定可能参与Stx17募集到自噬体上的其他辅助因子。此外,我们还证明EACC的作用是可逆的。洗脱EACC后,自噬通量的阻滞消失,因为Stx17此时能够转位至自噬体并参与进一步的融合事件。因此,由于其作用的可逆性,EACC可作为研究Stx17转运的有效工具。[1]
为了测定自噬通量,通常使用溶酶体抑制剂,例如BafA1和氯喹。然而,这些处理方法并不理想,因为它们不仅会损害溶酶体功能,还会阻碍包括内吞-溶酶体转运在内的所有其他溶酶体途径。我们的结果还表明,EACC的作用特异性地针对自噬体,并不影响溶酶体的pH值、功能或内吞转运。它也不影响溶酶体SNARE或RAB的定位。此外,即使是像渥曼青霉素和3-甲基腺嘌呤这样已知的早期自噬抑制剂也具有非特异性,因为它们会阻断所有磷脂酰肌醇3-激酶依赖的信号通路,从而导致一系列副作用。在这种情况下,使用EACC抑制Stx17转位,从而特异性地阻断自噬,可能是进行自噬通量实验的一种更精确的方法。事实上,沉默Stx17的表达被认为是选择性抑制自噬通量的理想方法(Hegedus等人,2013)。总之,像EACC这样的分子可以填补该领域因缺乏特异性自噬抑制剂而存在的空白。[1] |
| 分子式 |
C13H11N3O6S2
|
|---|---|
| 分子量 |
369.372940301895
|
| 精确质量 |
369.008
|
| 元素分析 |
C, 42.27; H, 3.00; N, 11.38; O, 25.99; S, 17.36
|
| CAS号 |
864941-31-1
|
| PubChem CID |
3704668
|
| 外观&性状 |
Typically exists as Light yellow to yellow solid at room temperature
|
| LogP |
3.3
|
| tPSA |
187
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
24
|
| 分子复杂度/Complexity |
526
|
| 定义原子立体中心数目 |
0
|
| SMILES |
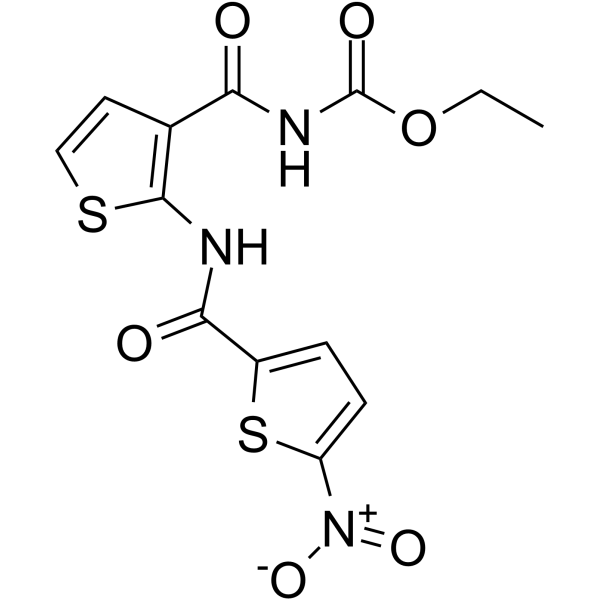
O=C(OCC)NC(C1=C(NC(C2=CC=C([N+]([O-])=O)S2)=O)SC=C1)=O
|
| InChi Key |
ISLJZDYAPAUORR-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C13H11N3O6S2/c1-2-22-13(19)15-10(17)7-5-6-23-12(7)14-11(18)8-3-4-9(24-8)16(20)21/h3-6H,2H2,1H3,(H,14,18)(H,15,17,19)
|
| 化学名 |
ethyl N-[2-[(5-nitrothiophene-2-carbonyl)amino]thiophene-3-carbonyl]carbamate
|
| 别名 |
EACC; 864941-31-1; ethyl (2-(5-nitrothiophene-2-carboxamido)thiophene-3-carbonyl)carbamate; Ethyl N-[2-[(5-nitrothiophene-2-carbonyl)amino]thiophene-3-carbonyl]carbamate;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~16.88 mg/mL (~45.70 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 1.69 mg/mL (4.58 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 16.9 mg/mL澄清的DMSO储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80 +,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.7073 mL | 13.5366 mL | 27.0731 mL | |
| 5 mM | 0.5415 mL | 2.7073 mL | 5.4146 mL | |
| 10 mM | 0.2707 mL | 1.3537 mL | 2.7073 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。