| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| Other Sizes |
|
| 靶点 |
Voltage-Dependent Calcium Channels (VDCCs, L-type and N-type) (10 μM inhibits L-type Ca²⁺ current by 62% and N-type Ca²⁺ current by 58% in rat cerebellar granule cells) [1]
NMDA Receptor (NR2B subtype) (acts as a non-competitive antagonist) [1] Human Ether-à-go-go-Related Gene (hERG) Channel (IC50 = 3.2 μM, patch-clamp assay in hERG-expressing HEK293 cells) [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Eliprodil(以前称为 SL-820715)是一种非竞争性 NR2B-NMDA 受体拮抗剂,IC50 值为 1 uM,对包含 NR2A 和 NR2C 的受体效力较低,IC50 > 100 uM。 NMDA 受体在介导谷氨酸诱导的兴奋性毒性中发挥关键作用,因此人们相信 NMDA 拮抗剂在中风或其他创伤性脑损伤后具有神经保护作用。 Eliprodil 保护海马切片中的锥体神经元免受缺氧或缺血性损伤。 Eliprodil 还可刺激中枢神经系统髓鞘形成,并可能具有治疗多发性硬化症的潜力。激酶测定:NR2B-NMDA 拮抗剂人 N 型 Ca2+ 通道电流被艾芬地尔和依利普地尔抑制,IC50 值分别为 50 µM 和 10 µM,而 P 型 Ca2+ 通道电流被艾芬地尔和依利普地尔可逆抑制,IC50 值约为 60分别为μM和9μM。 eliprodil (1 microm) 产生适度的反向速率依赖性动作电位持续时间延长(在周期长度为 300、1000 和 5000 ms 时分别为 7.4+/-1.5、8.9+/-2.1 和 9.9+/-1.8%; n=9)。细胞测定:在 HEK293 细胞中重组表达人 α 1B-1 α 2b beta 1-3 Ca2+ 亚基,产生 omega-芋螺毒素敏感的神经元 N 型电压依赖性 Ca2+ 通道和 omega-Aga IVA 敏感的 Ca2+ 通道 (P -型)在急性分离的小脑浦肯野神经元中被艾芬地尔和埃利普地尔可逆地抑制。
1. 抑制电压依赖性钙通道:Eliprodil(0.1-100 μM)以剂量依赖性方式抑制大鼠小脑颗粒细胞和背根神经节神经元的L型和N型钙电流(全细胞膜片钳)。10 μM剂量下,L型钙电流降低62%,N型钙电流降低58%,对T型钙通道无显著抑制(10 μM时抑制率<10%)[1] 2. NMDA受体拮抗作用:Eliprodil(1-30 μM)非竞争性抑制大鼠海马神经元中NMDA诱导的电流(膜片钳),10 μM时使NMDA最大反应降低45%,且不偏移NMDA浓度-反应曲线,提示结合于变构位点(优先靶向含NR2B亚型的NMDA受体)[1] 3. 延长心脏复极化:Eliprodil(0.1-10 μM)剂量依赖性抑制hERG表达HEK293细胞的hERG介导钾电流(IKr),IC50=3.2 μM。在豚鼠心室肌细胞中,10 μM Eliprodil使90%复极化时动作电位时程(APD90)延长38%,在离体灌流心脏中使QT间期延长25%[2] 4. 抗兴奋性毒性神经保护作用:Eliprodil(1-10 μM)降低NMDA诱导的大鼠皮质神经元死亡(MTT实验),10 μM剂量下细胞活力从NMDA单独处理组的42%升高至78%;5 μM时减少NMDA诱导的细胞内钙超载55%(荧光钙指示剂实验)[1] |
| 体内研究 (In Vivo) |
1. 沙鼠全脑缺血模型中的神经保护作用:60-80 g雄性蒙古沙鼠通过双侧颈总动脉夹闭5分钟诱导全脑缺血,Eliprodil(1、3、10 mg/kg)腹腔注射给药(缺血前30分钟或再灌注后立即给药)。缺血后72小时,3 mg/kg预处理组脑梗死体积减少40%(TTC染色),神经功能改善(转棒实验:坠落潜伏期从22秒增至58秒,vs溶媒组);10 mg/kg剂量无额外获益,但会增强镇静作用[1]
2. 复极化储备降低兔模型中的促心律失常风险:2-2.5 kg新西兰白兔先用亚治疗剂量索他洛尔(1 mg/kg,静脉注射)预处理以降低复极化储备,随后给予Eliprodil(0.3、1 mg/kg,静脉注射)。联合用药组(1 mg/kg Eliprodil)QT间期延长42%,3/6只兔诱发尖端扭转型室速(TdP);而Eliprodil单独给药(1 mg/kg)仅使QT间期延长15%,无TdP发生。正常白兔中未观察到显著心律失常[2] |
| 酶活实验 |
1. 电压依赖性钙通道(VDCC)电流实验:大鼠小脑颗粒细胞或背根神经节神经元接种于盖玻片,37℃下采用铯基电极内液和含钠/钙的细胞外液进行全细胞膜片钳记录。Eliprodil(0.1-100 μM)加入细胞外液,通过特异性电压 protocol 诱发L型(从-80 mV去极化至0 mV)和N型(从-80 mV去极化至+10 mV)钙电流,电流振幅按细胞电容标准化并计算抑制率[1]
2. NMDA受体电流实验:大鼠海马神经元培养14-21天,采用钾基电极内液进行全细胞膜片钳记录。加入100 μM NMDA激活受体,共孵育Eliprodil(1-30 μM)评估抑制效果,通过有无Eliprodil存在时的NMDA浓度-反应曲线判断竞争/非竞争性结合模式[1] 3. hERG通道电流实验:hERG稳定表达的HEK293细胞接种于盖玻片,35℃下采用钾基电极内液和含镁的细胞外液进行全细胞膜片钳记录。Eliprodil(0.01-30 μM)加入细胞外液,通过电压 protocol (从-80 mV静息电位去极化至+40 mV持续2秒,复极化至-50 mV持续5秒)诱发hERG电流,测量电流密度并通过剂量-反应曲线推导IC50值[2] |
| 细胞实验 |
1. 皮质神经元兴奋性毒性实验:分离大鼠胚胎皮质神经元,培养7-10天后用Eliprodil(1-10 μM)预处理1小时,再暴露于100 μM NMDA 24小时。MTT法检测细胞活力(570 nm吸光度),荧光钙指示剂(激发488 nm,发射525 nm)测定细胞内钙水平[1]
2. 豚鼠心室肌细胞动作电位实验:酶解法分离豚鼠心室肌细胞,维持在生理缓冲液中。全细胞膜片钳技术测量Eliprodil(0.1-10 μM)存在下的动作电位时程(APD20、APD50、APD90),电压 protocol 为从-80 mV静息电位给予2毫秒去极化脉冲至阈电位,刺激频率1 Hz[2] |
| 动物实验 |
1. Gerbil global cerebral ischemia model: Male Mongolian gerbils (60-80 g) were anesthetized with pentobarbital sodium (50 mg/kg, i.p.). Bilateral common carotid arteries were occluded with microclips for 5 minutes to induce ischemia, followed by reperfusion. Gerbils were randomly divided into 5 groups (n=8/group): sham-operated, vehicle (saline), Eliprodil 1 mg/kg (i.p.), 3 mg/kg (i.p.), 10 mg/kg (i.p.). Drugs were administered 30 minutes before ischemia or immediately after reperfusion. At 72 hours post-ischemia, gerbils were subjected to rotarod test (neurological function) and sacrificed. Brains were sectioned and stained with TTC to measure infarct volume [1] 2. Rabbit proarrhythmia model: New Zealand White rabbits (2-2.5 kg) were anesthetized with ketamine (50 mg/kg, i.m.) + xylazine (5 mg/kg, i.m.), intubated, and instrumented with ECG leads and venous catheters. Rabbits were randomly divided into 4 groups (n=6/group): vehicle (saline), Eliprodil 0.3 mg/kg (i.v.), Eliprodil 1 mg/kg (i.v.), sotalol (1 mg/kg, i.v.) + Eliprodil 1 mg/kg (i.v.). Drugs were infused over 10 minutes. ECG was continuously recorded for 2 hours, and QT intervals were measured. Torsades de pointes (TdP) was defined as a polymorphic ventricular tachycardia with QT prolongation [2] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 急性毒性:在沙鼠中,单次腹腔注射高达 30 mg/kg 的 Eliprodil 不会在 72 小时内造成显著死亡,但 10 mg/kg 会引起轻度镇静(运动活性降低),持续 4-6 小时 [1]
2. 致心律失常毒性:在复极储备降低的兔子(索他洛尔预处理)中,Eliprodil(1 mg/kg,静脉注射)在 50% (3/6) 的动物中诱发尖端扭转型室性心动过速 (TdP),并使 QT 间期延长 42%。在正常兔中,未观察到尖端扭转型室性心动过速(TdP),但1 mg/kg剂量下QT间期延长了15%[2] 3. 细胞毒性:浓度高达30 μM的Eliprodil不影响未刺激皮层神经元的活力(MTT法),表明其固有细胞毒性较低[1] |
| 参考文献 |
|
| 其他信息 |
Eliprodil 是一种外消旋体,由等摩尔量的 (R)- 和 (S)-eliprodil 组成。它是一种非竞争性 N-甲基-D-天冬氨酸 (NMDA) 受体拮抗剂和抗缺血药物,具有神经保护作用。它可作为抗衰老药、NMDA 受体拮抗剂、神经保护剂和钙通道阻滞剂。它包含 (R)-eliprodil 和 (S)-eliprodil。
Eliprodil 已用于帕金森病和运动障碍治疗的研究试验。 1. Eliprodil 是一种具有双重作用机制的神经保护药物:非竞争性拮抗含 NR2B 亚基的 NMDA 受体和选择性抑制 L 型/N 型电压依赖性钙通道 (VDCC)。这些作用减少了兴奋性毒性钙离子流入神经元,从而保护大脑免受缺血性损伤[1] 2. 它在急性缺血性中风中表现出潜在的治疗作用,如沙鼠全脑缺血模型中梗死体积减少和神经功能改善所证明的那样。然而,其临床开发受到致心律失常风险的限制,尤其是在心脏复极储备降低的患者中(例如,同时使用延长QT间期的药物、电解质紊乱)[1][2] 3. 依利普地尔的致心律失常作用归因于其对hERG钾通道(IKr)的抑制,这会延长心脏复极(QT间期),并增加易感个体发生尖端扭转型室性心动过速(TdP)的风险[2] 4. 依利普地尔对NR2B亚型NMDA受体和L/N型Ca²⁺通道具有选择性,最大限度地减少了对其他受体/通道亚型的脱靶效应。其神经保护作用在脑缺血发生前或发生后立即给药时最为显著,这凸显了其在急性卒中治疗中较窄的治疗窗口[1] |
| 分子式 |
C₂₀H₂₃CLFNO
|
|
|---|---|---|
| 分子量 |
347.85
|
|
| 精确质量 |
347.145
|
|
| CAS号 |
119431-25-3
|
|
| 相关CAS号 |
|
|
| PubChem CID |
60703
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 密度 |
1.205 g/cm3
|
|
| 沸点 |
474.1ºC at 760 mmHg
|
|
| 闪点 |
240.5ºC
|
|
| 蒸汽压 |
8.57E-10mmHg at 25°C
|
|
| 折射率 |
1.58
|
|
| LogP |
4.405
|
|
| tPSA |
23.47
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
3
|
|
| 可旋转键数目(RBC) |
5
|
|
| 重原子数目 |
24
|
|
| 分子复杂度/Complexity |
359
|
|
| 定义原子立体中心数目 |
0
|
|
| InChi Key |
GGUSQTSTQSHJAH-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C20H23ClFNO/c21-18-5-3-17(4-6-18)20(24)14-23-11-9-16(10-12-23)13-15-1-7-19(22)8-2-15/h1-8,16,20,24H,9-14H2
|
|
| 化学名 |
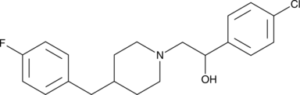
1-(4-chlorophenyl)-2-[4-[(4-fluorophenyl)methyl]piperidin-1-yl]ethanol
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 1.43 mg/mL (4.11 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 14.3 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 1.43 mg/mL (4.11 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 14.3 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.8748 mL | 14.3740 mL | 28.7480 mL | |
| 5 mM | 0.5750 mL | 2.8748 mL | 5.7496 mL | |
| 10 mM | 0.2875 mL | 1.4374 mL | 2.8748 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 Effect of eliprodil on the APD (APD90) in canine right ventricular papillary muscle.Br J Pharmacol.2004 Sep;143(1):152-8 |
|---|
 Effect of eliprodil on the APD (APD90) in the presence ofIK1block by BaCl2(10μm) in canine right ventricular papillary muscle.Br J Pharmacol.2004 Sep;143(1):152-8 |
(a) Effect of 1μmeliprodil on QTcinterval of the volume-conducted ECG recorded in isolated Langendorff-perfused rabbit heart in the absence and presence of 10μmBaCl2(b) The percentage change of the eliprodil-evoked QTclengthening in normal and in attenuated repolarisation reserve preparations.Br J Pharmacol.2004 Sep;143(1):152-8 |
Proarrhythmic effect of 1μmeliprodil after the administration of 10μmBaCl2on volume-conducted ECG recorded in isolated Langendorff-perfused rabbit heart.Br J Pharmacol.2004 Sep;143(1):152-8 |
|---|
 Lack of effect of 1μmeliprodil in canine ventricular myocytes on the inward rectifier potassium current (IK1) measured as the steady-state current at the end of the test pulse in the voltage range between −80 to 0 mV (a), on the transient outward current (Ito) (b) and on the slow component of the delayed rectifier potassium current (IKs).Br J Pharmacol.2004 Sep;143(1):152-8 |
 Effect of 1μmeliprodil on the rapid component of the delayed rectifier potassium current (IKr) in canine ventricular myocytes. (Left panel) Original current traces under control conditions and after application of 1μmeliprodil. (Right panel) The current–voltage relationship ofIKrunder control conditions and in the presence of 1μmeliprodil (mean±s.e.m.).Br J Pharmacol.2004 Sep;143(1):152-8 |