| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Neurokinin-1 receptor
Fosaprepitant (MK-0517, L-758,298) is a phosphoryl prodrug for aprepitant. A corticosteroid and a 5-HT 3 receptor antagonist are approved as combination therapies with the selective substance P (NK-1 receptor) antagonist aprepitant to prevent acute and delayed chemotherapy-induced nausea and vomiting. [1] Neurokinin-1 (NK-1) receptor antagonist . [1] |
|---|---|
| 体外研究 (In Vitro) |
Fosaprepitant (MK-0517, L-758,298) 是阿瑞匹坦的磷酰基前药。皮质类固醇和 5-HT 3 受体拮抗剂被批准与选择性 P 物质(NK-1 受体)拮抗剂阿瑞吡坦联合治疗,以预防化疗引起的急性和迟发性恶心和呕吐。 [1]
|
| 体内研究 (In Vivo) |
福沙匹坦二葡胺(30 mg/kg;腹腔注射;每天;持续7天)在绳中解除对吗啡的耐受性并增加抗损伤作用[1]。 动物模型:Sprague-Dawley大鼠[1] 剂量:30 mg/kg 给药:腹腔注射,每天,持续 7 天 结果:与对照组相比,吗啡的镇痛作用增强。
在雪貂动物模型中,fosaprepitant (阿瑞匹坦的水溶性磷酸化前药) 抑制了顺铂引起的急性和延迟性呕吐。顺铂前单次给药可在72小时内减少呕吐,每日给药则在整个72小时观察期内消除呕吐。当与地塞米松或5-HT3受体拮抗剂昂丹司琼联用时,其止吐活性似乎增强。[1] 在一项接受顺铂化疗的初治患者临床研究中,单次静脉注射fosaprepitant 与昂丹司琼相比,对急性呕吐的控制效果相似,但在控制延迟性呕吐方面明显更优 (完全控制率72% vs 30%)。[1] 在另一项临床研究中,在地塞米松基础上加用第1天静脉注射fosaprepitant (随后第2-5天口服阿瑞匹坦或安慰剂),与昂丹司琼加地塞米松方案相比,改善了延迟性呕吐的控制 (63-68%无呕吐 vs 41%无呕吐),但对急性呕吐的控制效果较差。[1] 在雪貂动物模型中,fosaprepitant (阿瑞匹坦的水溶性磷酸化前药) 抑制了顺铂引起的急性和延迟性呕吐。顺铂前单次给药可在72小时内减少呕吐,每日给药则在整个72小时观察期内消除呕吐。当与地塞米松或5-HT3受体拮抗剂昂丹司琼联用时,其止吐活性似乎增强。[1] 在一项接受顺铂化疗的初治患者临床研究中,单次静脉注射fosaprepitant 与昂丹司琼相比,对急性呕吐的控制效果相似,但在控制延迟性呕吐方面明显更优 (完全控制率72% vs 30%)。[1] 在另一项临床研究中,在地塞米松基础上加用第1天静脉注射fosaprepitant (随后第2-5天口服阿瑞匹坦或安慰剂),与昂丹司琼加地塞米松方案相比,改善了延迟性呕吐的控制 (63-68%无呕吐 vs 41%无呕吐),但对急性呕吐的控制效果较差。[1] |
| 动物实验 |
Sprague-Dawley大鼠连续7天注射吗啡(10 mg/kg,每日两次)和/或福沙匹坦(30 mg/kg,每日一次)。采用热板试验评估疼痛阈值。通过免疫组织化学方法评估这些大鼠脊髓中P物质(SP)和降钙素基因相关肽(CGRP)的表达。[2]
福沙匹坦(也称为MK-0517和L-758,298)是阿瑞匹坦的水溶性磷酸前药,静脉注射后,在普遍存在的磷酸酶的作用下,可在30分钟内转化为阿瑞匹坦。由于福沙匹坦能迅速转化为活性形式(阿瑞匹坦),115 mg 福沙匹坦的 AUC 值与口服 12 mg 阿瑞匹坦的 AUC 值相同,预计福沙匹坦的止吐效果也与阿瑞匹坦相似。临床研究表明,福沙匹坦可作为阿瑞匹坦口服胶囊的静脉替代疗法。一项针对健康受试者的研究表明,在最终药物浓度为 1 mg/ml 时,115 mg 福沙匹坦的耐受性良好,且其 AUC 值与 125 mg 阿瑞匹坦具有生物等效性。美国FDA、欧盟和澳大利亚当局已批准在为期3天的口服阿瑞吡坦治疗方案的第1天给予115毫克福沙吡坦,并在第2天和第3天继续口服阿瑞吡坦。福沙吡坦可能是一种有效的口服阿瑞吡坦的肠外给药替代方案。需要进一步研究以明确福沙吡坦在预防化疗引起的恶心呕吐(CINV)方面的作用,并确定可替代口服阿瑞吡坦的最佳给药方案[2]。 在一项雪貂顺铂诱导呕吐模型研究中,研究人员给予了福沙吡坦。该方案包括在顺铂给药前单次给药或每日给药,并在72小时的观察期内监测呕吐情况。该研究评估了福沙吡坦单独使用以及与其他止吐药(如地塞米松或昂丹司琼)联合使用的效果。 [1] 在一项雪貂顺铂诱导呕吐模型研究中,研究人员给予了福沙匹坦。该方案包括在顺铂给药前单次给药或每日给药,并在72小时的观察期内监测呕吐情况。该研究评估了福沙匹坦单独使用以及与其他止吐药(如地塞米松或昂丹司琼)联合使用的效果。[1] |
| 药代性质 (ADME/PK) |
福沙匹坦二葡甲胺是阿瑞匹坦的水溶性磷酰前药。静脉注射后,它在磷酸酶的作用下于30分钟内迅速转化为活性药物阿瑞匹坦。[1]
阿瑞匹坦(以及转化后的福沙匹坦)的药代动力学呈非线性。达到最大血浆浓度的时间(Tmax)约为4小时。[1] 阿瑞匹坦主要在肝脏中通过细胞色素P450酶CYP3A4代谢,少量通过CYP1A2和CYP2C19代谢。[1] 阿瑞匹坦的血浆半衰期为9至13小时,主要以代谢物的形式排出体外。给予标记的福沙匹坦后,尿液(57%)和粪便(45%)中回收了放射性物质。 [1] 阿瑞吡坦是CYP3A4的中度抑制剂和诱导剂,也是CYP2C9的诱导剂。与经CYP3A4代谢的药物(例如,地塞米松、甲泼尼龙、咪达唑仑)合用可增加其血浆浓度。与CYP2C9底物(例如,华法林)合用可能降低其血浆浓度。[1] CYP3A4抑制剂可增加阿瑞吡坦的血浆浓度,而CYP3A4诱导剂可降低其血浆浓度。[1] 在一项健康受试者的研究中,115 mg静脉注射的福沙吡坦在AUC(药时曲线下面积)方面与125 mg口服阿瑞吡坦具有生物等效性。 [1] 福沙匹坦二葡甲胺是阿瑞匹坦的水溶性磷酰前药。静脉注射后,它会在磷酸酶的作用下于30分钟内迅速转化为活性药物阿瑞匹坦。[1] 阿瑞匹坦(以及转化后的福沙匹坦)的药代动力学呈非线性。达到最大血浆浓度的时间(Tmax)约为4小时。[1] 阿瑞匹坦主要在肝脏中通过细胞色素P450酶CYP3A4代谢,少量通过CYP1A2和CYP2C19代谢。[1] 阿瑞匹坦的血浆半衰期为9至13小时,主要以代谢物的形式消除。服用标记的福沙匹坦后,尿液(57%)和粪便(45%)中均检测到放射性物质。[1] 阿瑞匹坦是CYP3A4的中度抑制剂和诱导剂,也是CYP2C9的诱导剂。与经CYP3A4代谢的药物(例如,地塞米松、甲泼尼龙、咪达唑仑)合用可增加其血浆浓度。与CYP2C9底物(例如,华法林)合用可能降低其血浆浓度。[1] CYP3A4抑制剂可增加阿瑞匹坦的血浆浓度,而CYP3A4诱导剂可降低其血浆浓度。 [1] 在一项针对健康受试者的研究中,115 mg 静脉注射的福沙匹坦在 AUC(曲线下面积)方面与 125 mg 口服的阿瑞匹坦具有生物等效性。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
在临床试验中,与阿瑞吡坦方案(福沙吡坦可转化为阿瑞吡坦)相关的最常见不良事件(发生率>10%)包括乏力/疲倦、厌食、便秘、腹泻、恶心和呃逆。[1]
静脉输注福沙吡坦后观察到静脉刺激,且其程度与总剂量、浓度和输注速率有关。浓度为1 mg/mL,输注时间为15-30分钟时,耐受性良好。较高浓度(25 mg/mL)快速输注(超过30秒)则与静脉刺激相关。[1] 在一项生物等效性研究中,剂量为100-150 mg(1 mg/mL)的福沙吡坦耐受性良好,未报告严重不良事件。最常见的不良事件是轻度至中度头痛和输注部位症状。[1] 阿瑞吡坦可能会降低口服避孕药的疗效;建议采用其他避孕方法。[1] 在轻度至中度肝肾功能不全的患者中,未发现具有临床意义的药代动力学差异,因此这些人群无需调整剂量。[1] 在临床试验中,与阿瑞吡坦方案(福沙吡坦可转化为阿瑞吡坦)相关的最常见不良事件(发生率>10%)包括乏力/疲倦、厌食、便秘、腹泻、恶心和呃逆。[1] 观察到静脉输注福沙吡坦后出现静脉刺激,且发现其与总剂量、浓度和输注速率有关。浓度为 1 mg/mL,输注时间为 15-30 分钟时,耐受性良好。较高浓度(25 mg/mL)快速输注(30 秒内)则与静脉刺激相关。[1] 在一项生物等效性研究中,福沙匹坦剂量为 100-150 mg(1 mg/mL)时耐受性良好,未报告严重不良事件。最常见的不良事件是轻度至中度头痛和输注部位症状。[1] 阿瑞匹坦可能会降低口服避孕药的疗效;建议采用其他避孕方法。[1] 在轻度至中度肝肾功能不全的患者中,未发现具有临床意义的药代动力学差异,因此这些人群无需调整剂量。[1] |
| 参考文献 |
[1]. Expert Opin Investig Drugs. 2007 Dec;16(12):1977-85. [2]. Role of fosaprepitant, a neurokinin Type 1 receptor antagonist, in morphine-induced antinociception in rats. Indian J Pharmacol. 2016 Jul-Aug; 48(4): 394-398.[3]. Fosaprepitant: a neurokinin-1 receptor antagonist for the prevention of chemotherapy-induced nausea and vomiting. Expert Rev Anticancer Ther . 2008 Nov;8(11):1733-42. |
| 其他信息 |
福沙匹坦二甲葡胺是福沙匹坦的二甲葡胺盐形式,福沙匹坦是阿瑞匹坦的水溶性N-磷酸化前药,具有止吐活性。静脉注射后,该药物迅速转化为阿瑞匹坦,并选择性地与中枢神经系统(CNS)中的人P物质/神经激肽1(NK1)受体结合。这抑制了内源性P物质与受体的结合,从而预防P物质引起的呕吐。
福沙匹坦二甲葡胺是阿瑞匹坦的前药,其开发目的是为了替代口服阿瑞匹坦胶囊,用于预防化疗引起的恶心和呕吐(CINV)。[1] 它通常与5-HT3受体拮抗剂和皮质类固醇(例如地塞米松)联合使用,作为联合止吐方案的一部分。 [1] 所提出的作用机制涉及拮抗中枢神经系统(例如,孤束核等脑干核团)以及可能在外周神经系统中的神经激肽-1 (NK-1) 受体上的 P 物质,从而阻断参与呕吐反射的关键通路,尤其对化疗引起的恶心呕吐 (CINV) 的延迟期有效。[1] 临床研究表明,在含有 5-HT3 受体拮抗剂和地塞米松的方案中加入阿瑞吡坦/福沙吡坦,可显著改善高致吐性化疗(例如,大剂量顺铂)后急性及延迟性 CINV 的控制。[1] 对于中度致吐性化疗,加入阿瑞吡坦/福沙吡坦可提高 24 小时内的完全缓解率以及 120 小时内的总体缓解率,但并未持续改善恶心控制。 [1] 115 mg 静脉注射的福沙匹坦(fosaprepitant)已提交 FDA 批准,作为 3 天止吐疗程第一天口服 125 mg 阿瑞匹坦(aprepitant)的替代方案。[1] 福沙匹坦二葡甲胺(fosaprepitant dimeglumine)是阿瑞匹坦的前体药物,其研发目的是为了替代口服阿瑞匹坦胶囊,用于预防化疗引起的恶心和呕吐(CINV)。[1] 它通常与 5-HT3 受体拮抗剂和皮质类固醇(例如地塞米松)联合使用,作为联合止吐方案的一部分。 [1] 所提出的作用机制涉及拮抗中枢神经系统(例如,孤束核等脑干核团)以及可能在外周神经系统中的神经激肽-1 (NK-1) 受体上的 P 物质,从而阻断参与呕吐反射的关键通路,尤其对化疗引起的恶心呕吐 (CINV) 的延迟期有效。[1] 临床研究表明,在含有 5-HT3 受体拮抗剂和地塞米松的方案中加入阿瑞吡坦/福沙吡坦,可显著改善高致吐性化疗(例如,大剂量顺铂)后急性及延迟性 CINV 的控制。[1] 对于中度致吐性化疗,加入阿瑞吡坦/福沙吡坦可提高 24 小时内的完全缓解率以及 120 小时内的总体缓解率,但并未持续改善恶心控制。 [1] 115毫克静脉注射的福沙匹坦已提交FDA批准,作为3天止吐疗程第一天口服125毫克阿瑞匹坦的替代方案。[1] |
| 分子式 |
C37H56F7N6O16P
|
|---|---|
| 分子量 |
1004.8337
|
| 精确质量 |
1004.34
|
| 元素分析 |
C, 44.23; H, 5.62; F, 13.23; N, 8.36; O, 25.48; P, 3.08
|
| CAS号 |
265121-04-8
|
| 相关CAS号 |
Fosaprepitant; 172673-20-0; Fosaprepitant-d4 dimeglumine
|
| PubChem CID |
136086851
|
| 外观&性状 |
White solid powder
|
| tPSA |
366.08
|
| 氢键供体(HBD)数目 |
9
|
| 氢键受体(HBA)数目 |
21
|
| 可旋转键数目(RBC) |
13
|
| 重原子数目 |
54
|
| 分子复杂度/Complexity |
1130
|
| 定义原子立体中心数目 |
7
|
| SMILES |
P(N1C(N([H])C(C([H])([H])N2C([H])([H])C([H])([H])O[C@@]([H])([C@]2([H])C2C([H])=C([H])C(=C([H])C=2[H])F)O[C@]([H])(C([H])([H])[H])C2C([H])=C(C(F)(F)F)C([H])=C(C(F)(F)F)C=2[H])=N1)=O)(=O)(O[H])O[H].O([H])[C@]([H])([C@]([H])(C([H])([H])N([H])C([H])([H])[H])O[H])[C@@]([H])([C@@]([H])(C([H])([H])O[H])O[H])O[H].O([H])[C@]([H])([C@]([H])(C([H])([H])N([H])C([H])([H])[H])O[H])[C@@]([H])([C@@]([H])(C([H])([H])O[H])O[H])O[H]
|
| InChi Key |
VRQHBYGYXDWZDL-OOZCZQCLSA-N
|
| InChi Code |
InChI=1S/C23H22F7N4O6P.2C7H17NO5/c1-12(14-8-15(22(25,26)27)10-16(9-14)23(28,29)30)40-20-19(13-2-4-17(24)5-3-13)33(6-7-39-20)11-18-31-21(35)34(32-18)41(36,37)38;2*1-8-2-4(10)6(12)7(13)5(11)3-9/h2-5,8-10,12,19-20H,6-7,11H2,1H3,(H,31,32,35)(H2,36,37,38);2*4-13H,2-3H2,1H3/t12-,19+,20-;2*4-,5+,6+,7+/m100/s1
|
| 化学名 |
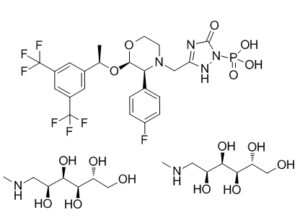
[3-[[(2R,3S)-2-[(1R)-1-[3,5-bis(trifluoromethyl)phenyl]ethoxy]-3-(4-fluorophenyl)morpholin-4-yl]methyl]-5-oxo-4H-1,2,4-triazol-1-yl]phosphonic acid;(2R,3R,4R,5S)-6-(methylamino)hexane-1,2,3,4,5-pentol
|
| 别名 |
MK0517; MK 0517; MK-0517; Fosaprepitant dimeglumine; Fosaprepitant dimeglumine salt; Ivemend; Fosaprepitant meglumine; MK-0517; Fosaprepitant (dimeglumine); UNII-D35FM8T64X; Emend; Inemend
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 该产品在溶液状态不稳定,请现配现用。 (2). 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O: ~50 mg/mL (~49.8 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (99.52 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 0.9952 mL | 4.9760 mL | 9.9519 mL | |
| 5 mM | 0.1990 mL | 0.9952 mL | 1.9904 mL | |
| 10 mM | 0.0995 mL | 0.4976 mL | 0.9952 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Efficacy and Safety of Fosaprepitant Dimeglumine in Preventing Chemotherapy-Induced Nausea and Vomiting (MK-0517-031)
CTID: NCT01594749
Phase: Phase 3 Status: Completed
Date: 2018-09-04
|