| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
FLT3 (IC50 = 0.29 nM); LTK (IC50 = 0.35 nM); AXL (IC50 = 0.73 nM); EML4-ALK (IC50 = 1.2 nM); c-KIT (IC50 = 230 nM)
The targets of Gilteritinib (ASP2215) are Fms-like tyrosine kinase 3 (FLT3) and AXL receptor tyrosine kinase; it is a type I tyrosine kinase inhibitor with high selectivity for FLT3 and AXL, and weak activity against c-KIT. [2] Gilteritinib (ASP2215) inhibits mutated forms of FLT3 including internal tandem duplication (FLT3-ITD), FLT3-D835Y point mutation, and FLT3-F691 mutation (inhibitory activity against FLT3-F691 is weaker); [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:在体外测试的 78 种酪氨酸激酶中,1 nM 浓度的 Gilteritinib 可抑制 FLT3、白细胞酪氨酸激酶 (LTK)、间变性淋巴瘤激酶 (ALK) 和 AXL 激酶超过 50%,IC50 值为 0.29 nM对于 FLT3,其效力比 c-KIT 强约 800 倍。 Gilteritinib 在 1 nM(FLT3、LTK、ALK 和 AXL)或 5 nM(TRKA、ROS、RET 和 MER)浓度下对 78 种测试激酶中的 8 种抑制超过 50%。 FLT3 的 IC50 值为 0.29 nM,AXL 的 IC50 值为 0.73 nM。 Gilteritinib 抑制 FLT3 的 IC50 浓度比抑制 c-KIT 所需浓度 (230 nM) 强约 800 倍。 Gilteritinib 的抗增殖活性是针对内源性表达 FLT3-ITD 的 MV4-11 和 MOLM-13 细胞进行评估。治疗 5 天后,Gilteritinib 抑制 MV4-11 和 MOLM-13 细胞的生长,平均 IC50 分别为 0.92 nM (95% CI: 0.23-3.6 nM) 和 2.9 nM (95% CI: 1.4-5.8 nM)。 。 MV4-11 细胞的生长抑制伴随着 FLT3 磷酸化的抑制。相对于载体对照细胞,用 0.1 nM、1 nM 和 10 nM Gilteritinib 处理 2 小时后,磷酸化 FLT3 水平分别为 57%、8% 和 1%。此外,低至 0.1 nM 或 1 nM 的剂量会导致磷酸化 ERK、STAT5 和 AKT 的抑制,所有这些都是 FLT3 激活的下游靶标。为了研究 Gilteritinib 对 AXL 抑制的影响,用 Gilteritinib 处理表达外源 AXL 的 MV4-11 细胞。在 1 nM、10 nM 和 100 nM 浓度下持续 4 小时,Gilteritinib 治疗可使磷酸化 AXL 水平分别降低 38%、29% 和 22%。激酶测定:Gilteritinib 在一组 78 个测试激酶中进行了测试,使用的 ATP 浓度大约等于 TK-ELISA 或片外迁移率变动测定中每种激酶的 Km 值。最初,测试了两种浓度的 Gilteritinib(1 nM 和 5 nM),以评估每种化合物对 TK 活性的抑制作用。然后使用 Gilteritinib 的剂量范围进行进一步的研究,以确定激酶的 IC50 值,其中 1 nM Gilteritinib 以及 c-KIT 的活性被抑制 > 50%。 TK-ELISA 和 MSA 测定用于进行 FLT3、LTK、AXL 和 c-KIT 的 IC50 研究; HTRF KinEASE-TK 测定用于评估棘皮动物微管相关蛋白样 4-ALK (EML4-ALK) 的 IC50 值。细胞测定:用DMSO或增加浓度的gilteritinib处理的MV4-11细胞孵育2小时。对磷酸化 FLT3 和总 FLT3 进行免疫沉淀和免疫印迹。
1. AML细胞系抗增殖活性:在携带FLT3突变的MV4-11、MOLM-13 AML细胞系,以及表达突变型FLT3(FLT3-ITD、FLT3-D835Y、FLT3-ITD-D835Y)的Ba/F3细胞中测试Gilteritinib (ASP2215)的作用。MV4-11细胞经DMSO或递增浓度的吉瑞替尼处理5天后,采用CellTiter-Glo法检测细胞活力,结果显示吉瑞替尼以剂量依赖方式抑制细胞生长(均值±标准误,四重复实验,三次独立实验的代表性结果);MOLM-13细胞经相同方式处理后,也观察到一致的剂量依赖性生长抑制[2] 2. 抑制FLT3磷酸化及下游信号通路:MV4-11细胞经DMSO或递增浓度的Gilteritinib (ASP2215)处理2小时后,免疫沉淀和蛋白质印迹分析显示,吉瑞替尼以剂量依赖方式降低FLT3的磷酸化水平(印迹下方标注光密度值,三次重复实验);此外,蛋白质印迹分析证实吉瑞替尼可降低FLT3下游靶点AKT、ERK、STAT5的磷酸化水平(三次重复实验)[2] 3. 抑制不同FLT3突变体:Gilteritinib (ASP2215)在细胞实验中对FLT3-ITD和FLT3-D835Y突变体表现出强效抑制活性,对FLT3-F691突变体的抑制活性较弱[2] |
| 体内研究 (In Vivo) |
口服Gilteritinib 10 mg/kg 4天后,肿瘤(MV4-11异种移植小鼠)中Gilteritinib的浓度比血浆中的浓度高20倍。 Gilteritinib 治疗 28 天会导致 MV4-11 肿瘤生长的剂量依赖性抑制,并在超过 6 mg/kg 时诱导肿瘤完全消退。此外,Gilteritinib 可降低骨髓中的肿瘤负荷,并延长静脉移植 MV4-11 细胞的小鼠的存活时间。
1. MV4-11异种移植模型的血浆与肿瘤分布:给荷MV4-11皮下移植瘤的裸鼠单次口服Gilteritinib (ASP2215)(1 mg/kg、6 mg/kg、10 mg/kg),采用高效液相色谱-串联质谱(HPLC-MS/MS)测定血浆和肿瘤中的药物浓度。结果显示吉瑞替尼在肿瘤组织中分布水平高,数据以均值±标准差呈现(血浆:2或3只动物;肿瘤:3只动物)[2] 2. 抑制移植瘤中FLT3/STAT5磷酸化:给荷MV4-11移植瘤的雄性小鼠口服溶媒对照或递增浓度的Gilteritinib (ASP2215),24小时内收集肿瘤组织蛋白裂解液:(1)ELISA法测定磷酸化FLT3/总FLT3的比值,结果以磷酸化蛋白水平相对溶媒对照组的归一化比值呈现;(2)蛋白质印迹法测定磷酸化STAT5/总STAT5的比值,采用相同归一化方法[2] 3. MV4-11异种移植模型的抗肿瘤活性:给荷MV4-11移植瘤的雄性小鼠口服溶媒对照或递增浓度的Gilteritinib (ASP2215)(1 mg/kg、3 mg/kg、6 mg/kg、10 mg/kg),持续28天。吉瑞替尼以剂量依赖方式降低肿瘤体积(均值±标准误,每组6只小鼠;第28天与对照组相比,P < 0.05、P < 0.01、P < 0.001,Dunnett检验),且小鼠体重无显著变化,提示无明显毒性[2] 4. FLT3突变体移植瘤模型的肿瘤消退:给荷表达FLT3-ITD、FLT3-D835Y或FLT3-ITD-D835Y的Ba/F3细胞移植瘤的雄性裸鼠,在肿瘤确认生长后,每日一次口服Gilteritinib (ASP2215)(10 mg/kg或30 mg/kg),持续7天。吉瑞替尼在三种模型中均诱导显著的肿瘤消退(均值±标准误,每组5只小鼠;第7天与对照组相比,P < 0.01、P < 0.001,Dunnett检验)[2] 5. 骨髓内移植模型降低白血病负荷并改善生存:给移植MV4-11-luc细胞的雌性NOD-SCID小鼠,从第15天开始每日一次口服溶媒或30 mg/kg Gilteritinib (ASP2215),持续56天。活体成像显示吉瑞替尼显著降低MV4-11-luc细胞的骨髓浸润(均值±标准误,每组10只小鼠;第42天与对照组相比,P < 0.001,Student’s t检验);Kaplan–Meier分析证实吉瑞替尼显著改善小鼠生存率(与对照组相比,P < 0.001,Log-rank检验)[2] |
| 酶活实验 |
TK-ELISA 或片外迁移率变化测定用于测试 Gilteritinib 对一组 78 种测试激酶的激酶抑制活性,其中 ATP 浓度大致相当于每种激酶的 Km 值。最初,在两种浓度的 Gilteritinib(1 nM 和 5 nM)下评估每种化合物对 TK 活性的抑制作用。接下来,使用一系列 Gilteritinib 剂量进行了其他研究,以确定 c-KIT 和激酶的 IC50 值,这些激酶的活性在 1 nM Gilteritinib 时被抑制一半以上。 FLT3、LTK、AXL 和 c-KIT IC50 研究是使用 TK-ELISA 和 MSA 测定进行的; HTRF KinEASE-TK 测定用于测定棘皮动物微管相关蛋白样 4-ALK (EML4-ALK) 的 IC50 值[2]。
开展初始激酶活性实验以评估Gilteritinib (ASP2215)的选择性。实验体系包含纯化的FLT3、AXL、c-KIT及其他酪氨酸激酶 ;将吉瑞替尼与激酶在ATP和特异性底物存在下,于优化的反应条件(未指定温度、孵育时间)下孵育;采用未指定的检测方法测定激酶活性,以确定吉瑞替尼对各激酶的抑制作用。结果证实吉瑞替尼对FLT3和AXL具有高选择性,对c-KIT活性弱 [2] |
| 细胞实验 |
CellTiter-Glo 发光细胞活力测定用于评估 gelderitinib 对 MV4-11 和 MOLM-13 细胞的影响。进一步研究调查 quizartinib 和 gilteritinib 对表达 FLT3-ITD、FLT3-D835Y、FLT3-ITD-D835Y、FLT3-ITD-F691 L 或 FLT3-ITD-F691I 的 Ba/F3 细胞的影响。连续五天,将 DMSO 或增加浓度的 Gilteritinib(0.01、0.1、1、10 和 100 nM)应用于 MV4-11 和 MOLM-13 细胞。 CellTiter-Glo 用于测量细胞的活力[2]。
1. AML细胞活力实验: - 步骤1:将MV4-11和MOLM-13 AML细胞以特定密度(未指定)接种至适宜培养板,在标准条件下培养,确保细胞贴壁并处于对数生长期; - 步骤2:用DMSO(对照)或系列浓度的Gilteritinib (ASP2215)处理细胞,孵育5天; - 步骤3:采用CellTiter-Glo法(未指定检测原理)量化细胞活力,四重复收集数据并以均值±标准误呈现;实验重复三次,报道代表性结果[2] 2. FLT3磷酸化的免疫沉淀与蛋白质印迹实验: - 步骤1:将MV4-11细胞在完全培养基中培养至所需汇合度(未指定),用DMSO或递增浓度的Gilteritinib (ASP2215)处理2小时; - 步骤2:收集细胞并裂解(裂解液组分未指定),测定蛋白浓度(方法未指定); - 步骤3:用FLT3特异性抗体从细胞裂解液中免疫沉淀FLT3蛋白,将免疫沉淀物进行SDS-PAGE电泳(凝胶浓度未指定); - 步骤4:将分离的蛋白转膜(膜类型未指定),用磷酸化FLT3和总FLT3一抗孵育,再加入二抗; - 步骤5:检测蛋白条带(方法未指定),光密度分析量化条带强度(值标注于印迹下方);实验重复三次[2] 3. FLT3下游信号蛋白的蛋白质印迹实验: - 步骤1:按上述方法用DMSO或递增浓度的Gilteritinib (ASP2215)处理MV4-11细胞2小时; - 步骤2:制备细胞裂解液,取等量蛋白进行SDS-PAGE电泳、转膜,用磷酸化AKT、ERK、STAT5及其总蛋白一抗孵育(未指定内参); - 步骤3:检测并分析蛋白条带(三次重复实验)[2] |
| 动物实验 |
小鼠:在移植了MV4-11 AML细胞的裸鼠中评估抗肿瘤活性。此外,还检测了异种移植小鼠的药代动力学。作为治疗的一部分,对MV4-11异种移植小鼠口服吉瑞替尼(10 mg/kg),疗程为4天。吉瑞替尼治疗28天,剂量大于6 mg/kg时可导致肿瘤完全消退,并呈剂量依赖性地抑制MV4-11肿瘤的生长[1]。
1. MV4-11皮下异种移植模型(药代动力学分析): - 步骤1:将特定数量的MV4-11 AML细胞皮下注射到裸鼠(性别/年龄未指定)体内(未指定),以建立异种移植模型。 - 步骤2:当肿瘤达到一定体积(未指定)时,小鼠单次口服1 mg/kg、6 mg/kg或10 mg/kg的吉瑞替尼(ASP2215)(药物溶出配方/载体未指定)。 - 步骤3:给药后在预定时间点(未指定)采集血液和肿瘤样本。 - 步骤4:测定血浆和肿瘤中吉瑞替尼的浓度。采用高效液相色谱-串联质谱法(HPLC-MS/MS)测定吉瑞替尼的浓度,数据以均值±标准差(SD)表示(血浆样本取2或3只动物,肿瘤样本取3只动物)[2]。 2. MV4-11皮下异种移植模型(药效学和疗效分析): - 步骤1:将MV4-11细胞皮下植入雄性裸鼠(每组n=6)体内,建立异种移植模型。 - 步骤2:肿瘤形成后(具体体积未指定),小鼠每日口服给予载体对照或吉瑞替尼(ASP2215),剂量分别为1 mg/kg、3 mg/kg、6 mg/kg或10 mg/kg,连续28天(药物制剂未指定)。 - 步骤3:药效学分析:收集24小时内的肿瘤组织,制备蛋白裂解液,并计算……测定磷酸化FLT3/总FLT3(ELISA)和磷酸化STAT5/总STAT5(免疫印迹)的比值。 - 步骤4:疗效分析:在28天的治疗期间定期测量肿瘤体积和体重(间隔未指定),并在第28天进行统计分析(Dunnett检验)[2] 3. Ba/F3-FLT3突变皮下异种移植模型: - 步骤1:将表达FLT3-ITD、FLT3-D835Y或FLT3-ITD-D835Y的Ba/F3细胞皮下注射到雄性裸鼠(每组n=5)体内,建立异种移植模型。 - 步骤2:确认肿瘤生长后(具体体积未指定),分别口服给予小鼠载体对照、10 mg/kg或30 mg/kg吉瑞替尼。 (ASP2215)每日一次,最多持续7天(药物制剂未指定)。 - 步骤3:在指定时间点(未指定)测量肿瘤体积,并在第7天进行统计分析(Dunnett检验)[2] 4. AML骨髓内移植模型: - 步骤1:将MV4-11-luc细胞(表达荧光素酶的MV4-11细胞)通过骨髓内注射移植到雌性NOD-SCID小鼠体内(注射部位/细胞数量未指定)。 - 步骤2:从移植后第15天开始,小鼠(每组n=10)口服给予载体对照或30 mg/kg吉瑞替尼(ASP2215),每日一次,持续56天(药物制剂未指定)。 - 步骤3:进行全身生物发光成像在指定时间点(例如,第 21 天、第 42 天)进行检测,以监测 MV4-11-luc 细胞的骨髓浸润情况(成像参数未指定)。 - 步骤 4:记录小鼠存活率,并进行 Kaplan-Meier 分析(Log-rank 检验)以评估吉瑞替尼对存活率的影响 [2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在临床前试验中,口服吉瑞替尼后2小时血浆浓度达到峰值,随后在4-8小时后肿瘤内浓度达到峰值。最大浓度和AUC均随剂量相应变化,分别为374 ng/ml和6943 ng·h/ml。给药后15天内达到稳态血浆浓度,生物蓄积量约为10倍。据报道,空腹状态下,人体达峰时间(tmax)为4-6小时。与高脂餐同时摄入后,Cmax 和 AUC 分别降低了 26% 和 10%,且 tmax 延迟 2 小时。 吉瑞替尼主要经粪便排泄,占给药剂量的 64.5%,其余 16.4% 以原药或其代谢物的形式经尿液排出。 估计的表观中心和外周分布容积分别为 1092 L 和 1100 L。该值表明吉瑞替尼具有广泛的组织分布。 吉瑞替尼的估计清除率为 14.85 L/h。 代谢/代谢物 吉瑞替尼主要在肝脏中通过 CYP3A4 代谢。其代谢主要由 N-去烷基化和氧化反应驱动,生成代谢物 M17、M16 和 M10。根据血浆浓度,主要形式为原形药物。 生物半衰期 据报道,吉瑞替尼的中位半衰期约为 45-159 小时。 1. 吸收和分布:吉瑞替尼 (ASP2215)经口服给药于携带 MV4-11 异种移植瘤的裸鼠,结果显示其吸收迅速(未提供 Tmax 数据)且在异种移植瘤内分布广泛。单次口服给药(1 mg/kg、6 mg/kg、10 mg/kg)后,采用 HPLC-MS/MS 法测定血浆和肿瘤浓度,观察到肿瘤内药物浓度较高;[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
吉瑞替尼治疗期间,血清转氨酶水平升高较为常见,78% 的患者会出现这种情况,其中 12% 的患者转氨酶水平超过正常值上限的 5 倍。吉瑞替尼的临床应用有限,但尚未发现与伴有症状或黄疸的急性肝损伤病例相关。由于 FLT3 抑制剂的临床应用经验有限,其引起肝损伤的可能性尚不明确。 可能性评分:E(未经证实,但怀疑是临床上明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无吉瑞替尼在哺乳期用药的信息。吉瑞替尼与血浆蛋白的结合率为 94%,因此乳汁中的含量可能很低;然而,其半衰期较长,约为 113 小时。制造商建议在吉瑞替尼治疗期间以及末次给药后 2 个月内停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 据报道,吉瑞替尼与血浆蛋白高度结合,占剂量的 94%。根据这一比例,主要的蛋白结合物是血清白蛋白。 1. 小鼠模型体内毒性:在接受吉瑞替尼 (ASP2215)治疗的小鼠模型中未观察到明显的毒性。在MV4-11异种移植模型中,使用吉瑞替尼(1-10 mg/kg,每日一次)治疗28天后,小鼠体重未发生显著变化,表明其具有良好的耐受性[2] |
| 参考文献 | |
| 其他信息 |
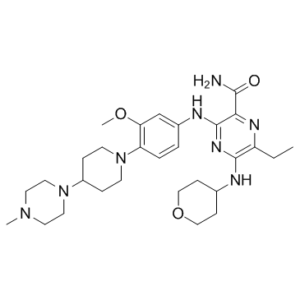
吉瑞替尼属于吡嗪类化合物,其结构为吡嗪-2-甲酰胺,在3、5和6位分别被{3-甲氧基-4-[4-(4-甲基哌嗪-1-基)哌啶-1-基]苯基}亚硝基、(氧杂环己烷-4-基)亚硝基和乙基取代。它是FLT3和AXL酪氨酸激酶受体的强效抑制剂(IC50分别为0.29 nM和0.73 nM)。吉瑞替尼已获FDA批准用于治疗携带FLT3基因突变的急性髓系白血病患者。它具有诱导细胞凋亡、抑制EC 2.7.10.1(受体蛋白酪氨酸激酶)和抗肿瘤的双重作用。它是一种N-甲基哌嗪类化合物,属于哌啶类、仲氨基化合物、单甲氧基苯类化合物、吡嗪类化合物、伯羧酰胺类化合物、芳香胺类化合物和氧杂环己烷类化合物。
吉瑞替尼(Gilteritinib),又名ASP2215,是一种FLT3酪氨酸激酶抑制剂小分子,与其他同类药物相比,具有更高的选择性和效力。它是一种吡嗪羧酰胺衍生物,对FLT3具有高度选择性,可避免其他疗法中观察到的c-Kit介导的骨髓抑制。吉瑞替尼由安斯泰来制药公司研发,并于2018年11月28日获得美国食品药品监督管理局(FDA)批准。该药物最初被设计为孤儿药,并获得了快速通道和优先审评资格。吉瑞替尼是一种口服小分子FMS样酪氨酸激酶3(FLT3)抑制剂,用于治疗携带FLT3突变的急性髓系白血病,是一种抗肿瘤药物。吉瑞替尼治疗期间血清转氨酶升高发生率中等,并可能引起罕见的临床表现明显的急性肝损伤。 吉瑞替尼是一种口服生物利用度高的受体酪氨酸激酶(RTK)抑制剂,包括FMS样酪氨酸激酶3(FLT3;STK1;FLK2)、AXL(UFO;JTK11)、间变性淋巴瘤激酶(ALK;CD246)和白细胞受体酪氨酸激酶(LTK),具有潜在的抗肿瘤活性。给药后,吉瑞替尼可与FLT3、AXL、ALK和LTK的野生型和突变型结合并抑制其活性。这可能导致FLT3、AXL、ALK和LTK介导的信号转导通路受到抑制,并降低过度表达这些RTK的癌细胞的增殖。 FLT3、AXL、ALK 和 LTK 在多种癌细胞类型中过度表达或发生突变,在肿瘤细胞的生长和存活中发挥关键作用。 另见:富马酸吉瑞替尼(有盐形式)。 药物适应症 吉瑞替尼适用于治疗经 FDA 批准的检测方法检测到 FLT3 突变的复发性或难治性急性髓系白血病成人患者。该适应症已扩展至伴随诊断试剂,例如 LeukoStrat CDx FLT3 突变检测,以包含与吉瑞替尼联合使用。急性髓系白血病是一种快速进展的、影响血液和骨髓的癌症。这种疾病会导致正常血细胞数量减少,需要持续输血。 Xospata适用于治疗伴有FLT3突变的复发或难治性急性髓系白血病(AML)成人患者,可作为单药疗法。 作用机制 吉瑞替尼是一种强效选择性抑制剂,可抑制FLT3受体的两种突变:内部串联重复(ITD)和酪氨酸激酶结构域(TKD)。同时,吉瑞替尼还能抑制AXL和ALK酪氨酸激酶。FLT3和AXL是参与癌细胞生长的分子。吉瑞替尼的作用机制是抑制FLT3及其下游靶点(如STAT5、ERK和AKT)的磷酸化。当研究报告显示约30%的急性髓系白血病患者存在突变激活的FLT3亚型时,人们对FLT3跨膜酪氨酸激酶的兴趣日益浓厚。此外,ITD突变与患者预后不良相关,而TKD突变会产生对FLT3酪氨酸激酶抑制剂的耐药机制,AXL酪氨酸激酶则倾向于产生对化疗的耐药机制。 1. 背景和分类:吉瑞替尼(ASP2215)是一种新型I型酪氨酸激酶抑制剂,对FLT3和AXL具有高度选择性。FLT3是急性髓系白血病(AML)中最常见的突变基因之一,FLT3突变与较差的总生存期相关;AXL在FLT3激活和AML发病机制中发挥作用[2] 2.作用机制:吉瑞替尼 (ASP2215) 通过抑制突变型 FLT3 及其下游信号通路(AKT、ERK、STAT5)的磷酸化发挥抗白血病活性,从而抑制 AML 细胞增殖并在体内诱导肿瘤消退 [2]。 3. 临床应用潜力:临床前研究表明,吉瑞替尼 (ASP2215) 在 FLT3 突变型 AML 细胞系和小鼠模型(异种移植和骨髓内移植模型)中具有显著的抗白血病活性,且无明显毒性。这些结果表明,吉瑞替尼可能是一种重要的下一代 FLT3 抑制剂,用于治疗 FLT3 突变阳性 AML [2]。 4. 计算机模型:对吉瑞替尼 (ASP2215) 与野生型 FLT3 的结合进行了计算机模型构建。吉瑞替尼被建模为球棍模型,原子按元素类型着色;蛋白质表面按静电势着色。门控残基F691被突出显示,吉瑞替尼与FLT3的结合模式被可视化[2] |
| 分子式 |
C29H44N8O3
|
|---|---|
| 分子量 |
552.71
|
| 精确质量 |
552.353
|
| 元素分析 |
C, 63.02; H, 8.02; N, 20.27; O, 8.68
|
| CAS号 |
1254053-43-4
|
| 相关CAS号 |
Gilteritinib hemifumarate;1254053-84-3;Gilteritinib-d8;2377109-74-3
|
| PubChem CID |
49803313
|
| 外观&性状 |
Yellow solid powder
|
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
696.9±55.0 °C at 760 mmHg
|
| 闪点 |
375.3±31.5 °C
|
| 蒸汽压 |
0.0±2.2 mmHg at 25°C
|
| 折射率 |
1.627
|
| LogP |
4.35
|
| tPSA |
121.11
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
10
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
40
|
| 分子复杂度/Complexity |
785
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O(C([H])([H])[H])C1C([H])=C(C([H])=C([H])C=1N1C([H])([H])C([H])([H])C([H])(C([H])([H])C1([H])[H])N1C([H])([H])C([H])([H])N(C([H])([H])[H])C([H])([H])C1([H])[H])N([H])C1C(C(N([H])[H])=O)=NC(C([H])([H])C([H])([H])[H])=C(N=1)N([H])C1([H])C([H])([H])C([H])([H])OC([H])([H])C1([H])[H]
|
| InChi Key |
GYQYAJJFPNQOOW-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C29H44N8O3/c1-4-23-28(31-20-9-17-40-18-10-20)34-29(26(33-23)27(30)38)32-21-5-6-24(25(19-21)39-3)37-11-7-22(8-12-37)36-15-13-35(2)14-16-36/h5-6,19-20,22H,4,7-18H2,1-3H3,(H2,30,38)(H2,31,32,34)
|
| 化学名 |
6-ethyl-3-[3-methoxy-4-[4-(4-methylpiperazin-1-yl)piperidin-1-yl]anilino]-5-(oxan-4-ylamino)pyrazine-2-carboxamide
|
| 别名 |
ASP-2215; ASP2215; ASP 2215; Gilteritinib; Trade name: Xospata
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 10 mg/mL (18.09 mM) in 50% PEG300 50% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
*生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 5%DMSO+40%PEG300+5%Tween80+50%ddH2O: 0.2mg/ml 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8093 mL | 9.0463 mL | 18.0927 mL | |
| 5 mM | 0.3619 mL | 1.8093 mL | 3.6185 mL | |
| 10 mM | 0.1809 mL | 0.9046 mL | 1.8093 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04336982 | Active Recruiting |
Drug: Gilteritinib Drug: Azacitidine |
Leukemia, Myeloid, Acute | Celgene | August 5, 2020 | Phase 1 Phase 2 |
| NCT03836209 | Active Recruiting |
Drug: Gilteritinib Drug: Midostaurin |
Acute Myeloid Leukemia | PrECOG, LLC. | December 6, 2019 | Phase 2 |
| NCT02421939 | Active Recruiting |
Drug: gilteritinib Drug: Azacitidine |
Leukemia, Acute Myeloid (AML) | Astellas Pharma Global Development, Inc. |
October 20, 2015 | Phase 3 |
| NCT05791890 | Completed | Drug: Gilteritinib | Acute Myeloid Leukemia | University of Rome Tor Vergata | May 31, 2022 | |
| NCT04027309 | Active Recruiting |
Drug: Gilteritinib Drug: Midostaurin |
Myelodysplastic Syndrome With Excess Blasts-2 Acute Myeloid Leukemia |
Stichting Hemato-Oncologie voor Volwassenen Nederland |
December 20, 2019 | Phase 3 |
Gilteritinib inhibits cell growth in AML cells and blocks phosphorylation of FLT3 and its downstream targets.Invest New Drugs.2017 Oct;35(5):556-565. |
|---|
Antitumor activity of gilteritinib in an MV4–11 xenograft AML mouse model.Invest New Drugs.2017 Oct;35(5):556-565. |
Gilteritinib significantly decreases leukemic burden and increases survival in an intra-bone marrow transplantation model of AML.Invest New Drugs.2017 Oct;35(5):556-565. |
Computational modeling of gilteritinib binding to wild-type FLT3.Invest New Drugs.2017 Oct;35(5):556-565. |
|---|
Gilteritinib induces regression of FLT3 mutant-expressing tumors in a mouse xenograft model.Invest New Drugs.2017 Oct;35(5):556-565. |
Antitumor Effect of Gilteritinib in Combination with Azacitidine in Mice Xenografted with MV4-11 Cells.Blood. 2016, 128:2830. |