| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|

| 靶点 |
Glucosylceramide synthase
|
|---|---|
| 体外研究 (In Vitro) |
在未经处理的 WT 细胞中,Ibiglustat(1 μM,15 天;法布里病 (FD) 细胞)产生的 GL-3 水平几乎达到生理水平,表明 Ibiglustat 进一步抑制 GL-3 积累,并可以增强 FD 细胞中 GL-3 的存在。这种鞘脂的很大一部分[4]
|
| 体内研究 (In Vivo) |
编码溶酶体酶葡糖脑苷酶(GCase)的基因GBA的突变是发展包括帕金森病(PD)在内的突触核蛋白疾病的最大遗传风险因素。此外,携带突变GBA等位基因的帕金森病患者发病较早,运动和非运动症状的疾病进展加快。对突触核蛋白病小鼠模型的临床前研究表明,使用中枢神经系统渗透剂小分子通过抑制葡糖神经酰胺合酶(GCS)来调节鞘脂代谢途径可能是突触核蛋白疾病的潜在治疗方法。在这里,我们的目的是通过抑制GCase的主要糖脂底物葡糖基神经酰胺(GlcCr)的从头合成来减轻脂质储存负担。我们之前已经表明,系统性GCS抑制减少了GlcCr和葡糖基鞘氨醇(GlcSph)的积累,减缓了海马中α-突触核蛋白的积累,并改善了认知缺陷。在这里,我们研究了脑渗透临床候选GCS抑制剂venglustat在GBA相关突触核蛋白病小鼠模型中的疗效,包括更紧密地复制典型GBA-PD患者基因型的杂合GBA小鼠模型。总之,这些数据支持了调节GCase相关鞘脂代谢作为治疗GBA相关突触核蛋白病的治疗策略的基本原理[1]。
|
| 酶活实验 |
糖脂水平的测量[1]
通过液相色谱法和串联质谱法(LC–MS/MS)对鞘脂进行定量分析28。简言之,将脑组织在10体积的水(w/v)中匀浆。用1ml提取溶液(50∶50乙腈/甲醇)通过蛋白质沉淀提取10微升匀浆或血浆。如前所述,通过液-液提取法提取小鼠CSF鞘脂37。使用Waters Acquity UPLC和Cortecs HILIC柱(2.1mm × 100毫米、2.7微米颗粒),并通过API 5000三重四极质谱仪以MRM模式进行分析。通过Waters Acquity UPLC和BEH HILIC柱(2.1mm × 100毫米,1.7微米颗粒),并通过API 6500三重四极质谱仪以MRM模式进行分析。GlcCr和GlcSph标准品分别购自Matreya,LLC和Avanti Polar Lipids。所有程序都是在不了解基因型或治疗的情况下进行的。 |
| 细胞实验 |
为了暴露不溶性α-突触核蛋白聚集体,一些组织在室温下用蛋白酶K(1:4稀释)预处理7分钟以消化可溶性α-突触蛋白23。在室温下用10%(vol/vol)正常驴血清封闭脑切片1小时,并与以下抗体孵育:小鼠抗泛素(1:300;猫#MAB1510)、兔抗α-突触核蛋白(1:300)和小鼠抗τ(1:500,tau-5)。然后将脑切片与驴抗小鼠Alexa Fluor-488(1:250稀释液)或驴抗兔生物素化第二抗体(1:200稀释液)孵育1小时。对于α-突触核蛋白聚集物的定量,使用花青3-酪酰胺信号扩增试剂盒。细胞核用4’,6-二氨基-2-苯基吲哚(DAPI)复染。切片用aqua-poly/mount覆盖,CA1海马细胞体层外部的放射层用SPOT相机(SPOT Imaging)与配备有20 × 物镜,如前所述22。对每只动物的两到三个切片进行成像,并通过MetaMorph软件上的阈值荧光区域定量测量免疫荧光。所有程序都是在不了解治疗或基因型的情况下进行的,阈值面积百分比表示为平均值 ± SE.[1]
|
| 动物实验 |
葡糖基神经酰胺合成酶抑制剂的给药:venglustat 和工具化合物 GZ667161[1]
部分动物通过颗粒饲料分别以 0.03% 或 0.033% (w/w) 的比例接受葡糖基神经酰胺合成酶抑制剂 venglustat(又名 GZ402671)或 GZ667161。在每个实验中,性别和同胞均随机匹配分组。靶点结合和暴露确认研究包括对 GbaD409V/D409V 或 GbaD409V/WT 小鼠连续两周(从约 4 月龄开始)给予 venglustat。参与持续 GCS 抑制研究的小鼠在断奶后(约 4 周龄)接受 GZ667161 或 venglustat 给药。野生型、基线和对照组饲喂载体啮齿动物饲料。在进行尸检和组织采集之前,小鼠持续喂食含GCS抑制剂和载体的饲料。 脑脊液采集[1] 在将动物固定于手术耳杆装置之前,先通过腹腔注射10:1的氯胺酮/赛拉嗪混合液进行麻醉。沿头部中线切开一小块皮肤后,使用电凝笔切开脂肪和肌肉层,暴露颅底和枕骨嵴。然后去除剩余组织,暴露枕大池膜。使用拉制玻璃吸管刺破枕大池膜,使脑脊液通过毛细作用自由流入吸管。收集约10-20 μL脑脊液后,将其转移至干净的低蛋白吸附管中。脑脊液样本中若可见血液污染,则不纳入分析。 动物灌注、组织和血液采集[1] 采集全血前,小鼠经腹腔注射200 μL戊巴比妥钠麻醉。待足底捏压和角膜反射消失后,使用玻璃毛细管从眼眶后静脉窦采集约250 μL全血至含有K2 EDTA抗凝剂的Microtainer®管中。采集的全血样本立即置于冰上。在4℃下以8000 rpm离心5分钟后分离血浆。采血后立即以18 mL/min的流速经心脏灌注冷磷酸盐缓冲液(PBS),持续2分钟。将大脑沿中线矢状切开后,将左半球显微解剖成不同区域,液氮速冻后保存于−80 °C直至使用。右半球用10%中性缓冲福尔马林固定48–72小时。之后,右半球用1×PBS洗涤三次,并转移至30%蔗糖溶液中浸泡24–48小时。最后,将右半球包埋于OCT包埋剂中,并使用冰冻切片机切成20 µm厚的切片,具体方法如前所述。 |
| 参考文献 |
|
| 其他信息 |
Venglustat 正在临床试验 NCT01674036(Genz-682452 在健康男性中的安全性、耐受性和药代动力学)中进行研究。
药物适应症 治疗常染色体显性多囊肾病 治疗半乳糖唾液酸沉积症、GM1 神经节苷脂沉积症、GM2 神经节苷脂沉积症、唾液酸沉积症 治疗多囊肾病 治疗帕金森病 |
| 分子式 |
C20H24FN3O2S
|
|---|---|
| 分子量 |
389.4869
|
| 精确质量 |
389.157
|
| 元素分析 |
C, 61.68; H, 6.21; F, 4.88; N, 10.79; O, 8.22; S, 8.23
|
| CAS号 |
1401090-53-6
|
| 相关CAS号 |
Ibiglustat (L-Malic acid);1629063-79-1 (HCl); 1629063-78-0 (malate; Ibiglustat succinate;1629063-80-4; 1401090-53-6; 1629063-80-4 (succinic acid)
|
| PubChem CID |
60199242
|
| 外观&性状 |
White to off-white solid
|
| 密度 |
1.3±0.1 g/cm3
|
| 折射率 |
1.613
|
| LogP |
4.13
|
| tPSA |
82.7Ų
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
5
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
533
|
| 定义原子立体中心数目 |
1
|
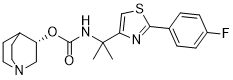
| SMILES |
S1C(C2C([H])=C([H])C(=C([H])C=2[H])F)=NC(=C1[H])C(C([H])([H])[H])(C([H])([H])[H])N([H])C(=O)O[C@]1([H])C([H])([H])N2C([H])([H])C([H])([H])C1([H])C([H])([H])C2([H])[H]
|
| InChi Key |
YFHRCLAKZBDRHN-MRXNPFEDSA-N
|
| InChi Code |
InChI=1S/C20H24FN3O2S/c1-20(2,17-12-27-18(22-17)14-3-5-15(21)6-4-14)23-19(25)26-16-11-24-9-7-13(16)8-10-24/h3-6,12-13,16H,7-11H2,1-2H3,(H,23,25)/t16-/m1/s1
|
| 化学名 |
(3S)-1-azabicyclo[2.2.2]octan-3-yl N-{2-[2-(4-fluorophenyl)- 1,3-thiazol-4-yl]propan-2-yl}carbamate
|
| 别名 |
Venglustat; SAR402671; GZ402671; Genz-682452-AA; SAR-402671; GZ402671; Ibiglustat; SAR 402671; GZ-402671; GZ-452; Genz-682452
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~128.37 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.42 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.42 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.42 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5675 mL | 12.8373 mL | 25.6746 mL | |
| 5 mM | 0.5135 mL | 2.5675 mL | 5.1349 mL | |
| 10 mM | 0.2567 mL | 1.2837 mL | 2.5675 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
A Study of the Safety, Tolerability, and Bioavailability of Orally Administered Venglustat in Healthy Adult Participants
CTID: NCT06418620
Phase: Phase 1 Status: Completed
Date: 2024-05-17