| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Apical sodium-dependent bile acid transporter (ASBT) (IC50 = 42±3 nM for human ASBT)
Apical Sodium-Dependent Bile Acid Transporter (ASBT, also known as IBAT) (no definite IC₅₀, Ki, or EC₅₀ data provided; described as a "highly potent" inhibitor) [1] Apical Sodium-Dependent Bile Acid Transporter (ASBT) (used to study its regulatory role in hepatic cysteine sulfinic acid decarboxylase (CSAD) expression) [2] Apical Sodium-Dependent Bile Acid Transporter (ASBT) (target for treating pruritus in Primary Biliary Cholangitis (PBC)) [3] Linerixibat (GSK2330672) is a highly potent and nonabsorbable inhibitor of the apical sodium-dependent bile acid transporter (ASBT), also referred to as the ileal bile acid transporter (IBAT). This transporter is responsible for reabsorbing bile salts from the lumen of the gastrointestinal tract. By inhibiting ASBT in the ileum, linerixibat reduces the enterohepatic circulation of bile acids, leading to decreased serum bile acid levels and increased fecal bile acid excretion. No IC50 or Ki values are provided in the available search results. |
|---|---|
| 体外研究 (In Vitro) |
化合物 56 也称为两性离子、非吸湿性结晶盐形式,在 pH 7.4 下具有良好的溶解度 (>7 mg/mL)、良好的热稳定性,并且不会产生伪影或反应性 [1]。GSK2330672是一种高效、不可吸收的ASBT抑制剂,具有优异的水溶性、选择性和可开发性,可用于安全性研究,最终用于人类。GSK2330672将是一种有价值的临床工具,用于探索非吸收性ASBT抑制剂对2型糖尿病患者的治疗效用。
Linerixibat (GSK2330672) 通过从第一代抑制剂 264W94 开始的广泛构效关系研究被鉴定出来。先导化合物优化工作集中于鉴定一种高效、不可吸收的 ASBT 抑制剂,并具有良好的开发性能。该化合物在2型糖尿病动物模型中显示出降低血糖的作用。现有搜索结果中未提供详细的体外实验数据。 |
| 体内研究 (In Vivo) |
在 2 型糖尿病动物模型中,使用 Linerixibat(GSK2330672;0.05–10 mg/kg;侧壁灌胃;每天两次,持续 14 天;重量分析 ZDF 含量)治疗可降低糖尿病水平 [1]。
GSK2330672在大鼠中导致ASBT的有效抑制和非常低的口服吸收。GSK2330672显示出强大的小鼠和大鼠ASBT活性,并且在GI稳定性测定中是稳定的。GSK2330672在啮齿类动物的胃肠道中是稳定的,并能有效诱导小鼠的粪便胆汁酸排泄,这使我们选择这三种化合物分别用于瘦大鼠和Zucker糖尿病脂肪(ZDF)大鼠的体内机制和疗效研究[1]。 1. 2型糖尿病动物模型的降糖作用:Linerixibat(GSK2330672)作为强效非吸收性ASBT抑制剂,在2型糖尿病动物模型中可显著降低血糖水平,证实其治疗2型糖尿病的潜在价值[1] 2. 小鼠肝脏CSAD表达的调控作用:雄性C57BL/6J小鼠通过灌胃给予Linerixibat(GSK2330672)(2 mg/kg,每日两次),持续1周。小鼠过夜禁食后收集组织,检测显示Linerixibat(GSK2330672)可显著诱导肝脏CSAD的mRNA和蛋白表达,表明ASBT抑制可上调小鼠肝脏CSAD表达[2] 3. PBC患者中的疗效与安全性(IIb期研究):Linerixibat(GSK2330672)正处于IIb期研究阶段,用于治疗PBC患者的瘙痒症状。该研究旨在确定改善瘙痒的最佳剂量和给药频率,并评估其对PBC基础疾病的影响。前期小型研究显示,药物总体耐受性良好,无严重不良事件报告;药物被开发为片剂,通过阻断肠道胆汁酸重吸收,促进致瘙痒化学物质随粪便排出[3] 在服用二甲双胍的2型糖尿病患者中,linerixibat (GSK2330672) 90 mg每日两次、连续14天治疗后,与安慰剂相比,空腹血糖降低-1.21 mmol/L(95% CI: -2.14, -0.28),加权平均血糖AUC0-24h降低-1.33 mmol/L(95% CI: -2.30, -0.36)。空腹和加权平均胰岛素AUC0-24h也降低。Linerixibat 使 LDL 胆固醇降低约40%,同时降低非 HDL 胆固醇、总胆固醇和载脂蛋白 B 浓度。HDL 胆固醇无变化,但观察到空腹甘油三酯水平有升高趋势。 在针对原发性胆汁性胆管炎瘙痒患者的 Phase 2b GLIMMER 试验中(N=147),linerixibat 组在第16周时平均最差每日瘙痒评分较基线降低≥2分;然而,在意向治疗分析中与安慰剂的差异不显著。对治疗期间每月瘙痒评分较基线变化的事后分析显示,安慰剂与 linerixibat 180 mg每日一次(P = .0424)、40 mg每日两次(P = .0105)和90 mg每日两次(P = .0370)之间存在显著差异。在符合方案人群中观察到总日剂量与反应之间的显著关系(P = .0542)。 |
| 酶活实验 |
测定人、小鼠和大鼠ASBT抑制作用的方法[1]
在准备测量表达ASBT的细胞对胆汁酸的吸收时,将HEK293细胞在补充有10%FBS的DMEM/F12中培养。在进行实验前24小时,在80–90%的汇合处收获细胞。将细胞以50000个细胞/孔接种在聚d-赖氨酸包被的平板中,并加入ASBT Bacmam病毒,使得每个孔含有3.67×106pfu(73.4pfu/细胞)。用Breathe Easy Seal覆盖每个测定板,并将其放置在培养箱中24小时,以使转运蛋白表达。 在摄取实验当天,将10mM HEPES加入Hank’s Balanced Salt Solution,并用TRIS(HBSSH)将pH调节至7.4。将100pM[3H]-牛磺胆酸盐和10μM冷牛磺胆酸钠加入室温HBSSH中制备测定缓冲液。通过向HBSSH中加入10μM冷牛磺胆酸盐(每个测定板~30mL)制备单独的洗涤缓冲液,并放置在冰上。使用100%DMSO,从200μM开始制备每种测试化合物的8点3倍稀释曲线。类似地,从1.8mM开始,制备对照化合物1的8点剂量-反应曲线。通过将每种浓度的3μL添加到v底96孔板中,然后用177μL的测定缓冲液稀释60倍,形成药物板。将培养皿从培养箱中取出,冷却至25°C。抽吸培养基,并用300μL HBSSH洗涤一次孔。然后,将50μL的每种剂量-反应曲线浓度一式三份逐柱加入到测定板中,保留第10列用于对照(测定缓冲液+1.67%DMSO),第11和12列用于对照化合物。将平板在环境温度下孵育90分钟,然后抽吸平板,然后用300μL洗涤缓冲液洗涤1倍。然后向每个孔中加入220μL Microscint 20,并将板密封。第二天使用微板闪烁计数器对细胞裂解物中[3H]-牛磺胆酸盐的量进行定量。 使用以下公式测定每种药物浓度下的摄取抑制百分比:100×(1-((T1–C2)/(C1–C2));其中T1是试验化合物的平均cpm,C1是在不存在任何添加的抑制剂的情况下观察到的平均cpm,C2是在存在已知引起100%摄取抑制的物质(30μM对照化合物)的情况下观测到的平均cpm。IC50可以使用公式y=(Vmax×xn)/(Kn+xn)生成。 |
| 细胞实验 |
MDCK渗透率的测定方法[1]
使用在与肠道吸收相关的条件下孵育的稳定转染的人多药耐药性1–Madin–Darby犬肾(hMDR1-MDCK)细胞在体外测量被动通透性。简言之,将hMDR1-MDCK细胞以6.6×105个细胞/孔的速度接种到孔径为0.4μm的12孔聚碳酸酯Transwells滤膜上,并在37°C、5%CO2和95%相对湿度的环境中保持在含有10%胎牛血清(DMEM-FBS)的Dulbecco改良Eagle培养基中。三天后,从心尖和基底外侧腔中取出培养基,并用最终浓度为2μM的含有P-gp抑制剂GF120918A的转运缓冲液(含有25mM葡萄糖和25mM HEPES的HBSS)代替。在30分钟的平衡后,从心尖腔中取出运输缓冲液,并用含有3μM测试化合物、2μM GF120918A、25mM葡萄糖和250μM路西法黄CH的禁食状态模拟肠液(FaSSIF)代替。接下来,从基底外侧腔中取出运输缓冲液,用含有1%(w/v)人血清白蛋白和2μM GF 120918A的运输缓冲液代替。 在37°C下孵育60分钟后,从根尖(供体)和基底外侧(受体)室收集样品,并加入乙腈(分别为1:1和1:2(v/v))中。然后对受试者样品进行离心,去除上清液并通过LC-MS/MS进行分析。 所有剂量溶液中的最终DMSO浓度为0.3%(v/v)。每次治疗重复进行。普萘洛尔(一种高渗透性标记化合物)和安非那韦(一种P-gp活性的标记化合物)被包括在单独的孔中作为测定的对照。通过基于荧光的测定法测量路西法黄转运来评估细胞单层完整性。 大鼠灯具内容物稳定性测定[1] 如下制备在磷酸盐缓冲盐水(PBS,pH 7.4)中的来自大鼠盲肠和结肠的管腔内容物的10%(w/v)匀浆。 将两只雄性SD大鼠禁食过夜,并通过CO2窒息实施安乐死,然后放血。从两只动物身上取下大肠和盲肠,并纵向切开。取出管腔内容物,合并到预先称重的50mL锥形管中,用PBS(10mL/g样品重量)稀释,并通过倒置轻轻混合。将匀浆置于湿冰上直至使用。 将试验化合物(10μM终浓度)加入4 mL玻璃螺旋盖小瓶中,该小瓶含有3 mL大鼠盲肠和结肠管腔内容物的匀浆。加入受试化合物后,立即轻轻混合小瓶,取出3×100μL等分试样(t=0),并将其放入含有400μL停止溶液(80%乙腈/20%甲醇)的96深孔板中。接下来,将玻璃小瓶在温和的氮气流下吹扫约30秒,加盖,并放置在37°C的振荡水浴中。在t=2、4和24小时时,从小瓶中取出3×100μL等分试样,并将其放入含有400μL停止溶液的96深孔板中。小瓶在温和的氮气流下吹扫约30 s,加盖,并在每个时间点后放置在37°C的振荡水浴中。覆盖样品并在−10°C下储存,直到进行LC-MS/MS分析。 |
| 动物实验 |
动物/疾病模型:雄性 Zucker 糖尿病肥胖 (ZDF) 大鼠 [1]
\n剂量:0.05 mg/kg、0.1 mg/kg、0.5 mg/kg、1 mg/kg、5 mg/kg、10 mg/kg,每日两次;持续14天的结果:糖化血红蛋白(HbA1c)降低了1.30-1.64%,非空腹血糖降低了50%以上,低于200 mg/dL,血浆胰岛素显著升高。 \\n大鼠口服吸收试验[1] \n\\n雄性Sprague-Dawley (SD)大鼠(271-303 g;查尔斯河实验室,北卡罗来纳州罗利市)除非另有说明,否则可自由摄取标准饲料(PMI 5002块状饲料)和水。静脉注射治疗组的动物通过手术植入颈静脉和股静脉插管。口服治疗组的动物通过手术植入颈静脉和门静脉插管。给药前一晚,大鼠禁食,给药后约4小时恢复喂食。\n口服给药组通过灌胃给予以0.5% HPMC/0.1% Tween配制的均质悬浮液形式的测试化合物,剂量为10 mg/kg。分别于给药后0.25、0.5、1、2、4和8小时,从颈静脉和门静脉插管采集血样。制备血浆样本,并储存于−70 °C直至分析。 \n\n大鼠粪便药物回收率[1] \n\n粪便回收率[1] \n\n雄性SD大鼠(查尔斯河实验室,北卡罗来纳州罗利市)通过灌胃给予以0.1% HPMC:0.5% Tween配制的均质悬浮液形式的测试化合物,剂量为10 mg/kg。粪便样本采集时间点如下:给药后0–6、6–12、12–24、24–36、36–48、48–60和60–72小时。每次采集后,样本加盖并储存于−70 °C直至分析。分析前,样本用5倍体积的20%乙醇:80%水溶液稀释,于10 °C浸泡过夜,然后使用Polytron手持式均质器进行均质。均质液用3倍体积的乙腈提取,然后在4 °C、2304 g下离心15分钟。取各乙腈上清液分装至干净的96孔板中,并用等体积的水稀释。药物浓度通过 LC-MS/MS 进行定量分析。 \\n\\n\\n\\n \\n \n\n\n查看更多\\n\\n用于疗效研究的动物[1] \\n\\n小鼠粪便收集[1] \n\\n雄性C57BL/6J小鼠分别于上午7:00和下午3:00接受赋形剂(0.5%羟丙基甲基纤维素(HPMC),0.1%吐温80)或六个剂量(0.0001、0.001、0.01、0.1、1和10 mg/kg)的化合物给药,持续一天,并收集24小时(上午7:00至次日上午7:00)的粪便样本。每只动物最多用于五项研究,研究之间间隔一周的洗脱期。 \\n\\n大鼠粪便收集[1] \n\\n雄性ZDF大鼠于七周龄(±3天)到达。经过一周的适应期后,根据基线葡萄糖/载体(0.5%羟丙基甲基纤维素(HPMC),0.1%吐温80;每种化合物设置一个载体组)和化合物20、45和56的六个剂量(0.05、0.1、0.5、1、5和10 mg/kg),将大鼠分配到不同的治疗组(每组n = 6-8只)。所有治疗均通过灌胃法给药,每日两次。在治疗的第7天收集24小时的粪便样本。 \\n\\nZDF大鼠的代谢效应[1] \n\\n雄性ZDF大鼠在7周龄(±3天)时到达。经过一周的适应期后,大鼠用异氟烷(Abbott Laboratories,IL)麻醉,并在上午9:00采集尾静脉血样,无需禁食。为确保各治疗组均衡,根据基线葡萄糖/载体(0.5%羟丙基甲基纤维素(HPMC),0.1%吐温80)和选定的化合物剂量(化合物20为0.05、0.1、0.5、1、5和10 mg/kg,化合物45和56分别为0.001、0.01、0.1、1和10 mg/kg),将ZDF大鼠分为六个治疗组。所有药物均通过灌胃法给药,每日两次。随后对动物进行为期两周的观察,并在第14天上午9:00采集尾静脉血样,无需禁食。血浆样本储存于−80 °C,以备后续分析。 \n\n临床化学参数测定[1] \n\n使用奥林巴斯AU640临床化学分析仪测定粪便提取液中的血浆葡萄糖和胆汁酸。葡萄糖检测试剂由贝克曼库尔特公司生产。胆汁酸检测试剂由Trinity Biotech公司生产。使用Primus Affinity Ultra2高效液相色谱系统和Primus Affinity Assay试剂盒测定糖化血红蛋白(HbA1c)。胰岛素、总GLP-1(tGLP-1)、PYY和GIP的测定采用Meso Scale Discovery(MSD)试剂盒。采用 MSD 总 Glp-1 检测试剂盒测定总 Glp-1,并在 MSD Sector Imager 6000 上进行分析。 \n\n粪便胆汁酸提取[1] \n\n粪便样本风干 5 天,然后在 60 °C 下用甲醇-KOH (300 mM) 提取 24 小时。将粪便提取物与 150 mM Mg2SO4 (1:1) 混合。离心后,收集上清液,并按上述方法进行胆汁酸测定。\n\n \n1. 2 型糖尿病动物模型实验:使用特定动物物种(例如,小鼠、大鼠)建立 2 型糖尿病模型。 Linerixibat (GSK2330672)通过合适的给药途径(可能是口服,这与其不吸收的特性以及后续的片剂制剂相符)给药。给药频率和持续时间根据降血糖效果进行设定。在特定时间点测量血糖水平以评估治疗效果[1] \n2. 小鼠肝脏CSAD调控实验:使用雄性C57BL/6J小鼠(每组n=5)。Linerixibat (GSK2330672)溶解于合适的溶剂(未具体说明)中,以2 mg/kg的剂量,每日两次,通过灌胃给药,持续1周。治疗结束后,小鼠禁食过夜,然后处死,并收集肝组织。肝组织样本用于mRNA检测(例如,RT-PCR)和蛋白质检测(例如,Western blot),以分析CSAD的表达水平[2] |
| 药代性质 (ADME/PK) |
1. 不可吸收特性:Linerixibat (GSK2330672) 被明确描述为一种“不可吸收”的抑制剂。口服后,它不被吸收进入体循环,主要留在胃肠道内,对ASBT发挥局部抑制作用,无全身分布[1]
2. 胃肠道局部作用:由于其不可吸收的特性,该药物特异性地作用于位于肠上皮细胞顶膜的ASBT,阻断胆汁酸从肠腔的重吸收。它主要经粪便排泄(根据其不可吸收的特性推断)[1] Linerixibat (GSK2330672) 被设计为不可吸收的化合物,全身暴露极低。在一项健康日本志愿者接受10-180 mg单次口服给药的 Phase 1 研究中,大多数受试者的血浆中检测不到该药物。这一药代动力学特征与其依赖于胃肠道局部活性的作用机制一致。现有搜索结果中未报告 Cmax、Tmax、AUC、半衰期、清除率或分布容积的具体数值,尽管这些参数已在临床试验中测量。该化合物通过口服给药,剂型为溶液剂或稀释于溶媒中的粉末。 |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 临床研究中的不良事件:在先前一项针对原发性胆汁性胆管炎 (PBC) 患者的小型研究中,利奈昔巴 (GSK2330672) 最常见的不良事件是腹泻(药物组 7 例,安慰剂组 1 例),而头痛在安慰剂组更为常见(安慰剂组 7 例,药物组 6 例)。未报告严重不良事件 [3]
在一项健康日本志愿者的 Phase 1 研究中(单次口服剂量10-180 mg),linerixibat (GSK2330672) 未出现严重不良事件,也无导致研究终止或退出的不良事件。药物相关不良事件均为轻度且无需干预即可缓解,包括胃肠道症状(主要为腹泻)和粪便潜血阳性。 在针对 PBC 患者的 Phase 2b GLIMMER 试验中(n=147),与其作用机制一致,腹泻是最常见的不良事件,发生率随剂量增加而增加。 在2型糖尿病患者的 Phase 1/2 研究中,与 GSK2330672 相关的最常见不良事件为胃肠道反应,主要为腹泻(发生率22-100%),且似乎与剂量无关。 在一项首次人体 Phase 1 研究中,排除标准包括筛选时粪便潜血阳性、炎症性肠病、慢性腹泻、克罗恩病或与吸收不良综合征相关的腹泻病史。QTc ≥450 msec 的受试者也被排除。所有可用研究中均未报告死亡或严重毒性事件。 |
| 参考文献 |
|
| 其他信息 |
GSK2330672 已被研究用于治疗 2 型糖尿病。
药物适应症 治疗原发性胆汁性胆管炎 1. 治疗适应症:Linerixibat (GSK2330672) 最初是为治疗 2 型糖尿病而开发的,其靶点是 ASBT,用于调节葡萄糖代谢[1];后来,它被重新用于治疗原发性胆汁性胆管炎 (PBC) 的瘙痒,以满足 PBC 患者对有效止痒治疗的未满足需求(因为一线 PBC 治疗药物熊去氧胆酸对止痒无效)[3] 2. 作用机制:Linerixibat (GSK2330672) 抑制肠腔内 ASBT 介导的胆汁酸重吸收。对于 2 型糖尿病,这种抑制作用可调节肝脏胆固醇代谢和葡萄糖稳态;对于原发性胆汁性胆管炎 (PBC) 相关瘙痒,它通过促进胆汁酸随粪便排出,减少全身胆汁酸蓄积(瘙痒的主要原因之一)[1, 3] 3. 药物研发现状:Linerixibat (GSK2330672) 于 2019 年 9 月获得美国食品药品监督管理局 (FDA) 授予的“孤儿药资格”。孤儿药资格授予针对罕见病的药物,可缩短研发周期,加快患者用药。该药物正在开发为口服片剂,并在一项 IIb 期研究中进行评估,以确定中重度瘙痒的原发性胆汁性胆管炎 (PBC) 患者的最佳剂量、给药频率、安全性和耐受性 [3] 4. 临床研究设计(IIb 期):Linerixibat (GSK2330672) 的 IIb 期研究包括 7 次现场访视和 1 次最终电话随访,由研究医生/护士进行。在加拿大,该研究在 5 个研究中心(蒙特利尔、温尼伯、卡尔加里、埃德蒙顿和伦敦)进行。参与者将获得两次访视的差旅费报销和餐费/茶点补偿(每次访视时长:2-5 小时)[3] 5. 在胆汁酸代谢研究中的作用:Linerixibat (GSK2330672) 被用作研究胆汁酸重吸收与肝脏牛磺酸生成之间联系的工具。它诱导小鼠肝脏 CSAD 表达,证实 ASBT 抑制将胆汁酸代谢与牛磺酸合成偶联 [2] Linerixibat (GSK2330672) 是通过从第一代 ASBT 抑制剂 264W94 开始进行的先导化合物优化工作发现的。广泛的构效关系研究最终鉴定出该化合物,其显示出良好的开发性能,可用于评估不可吸收的 ASBT 抑制剂在2型糖尿病患者中的潜在治疗价值。该化合物已在多项临床试验中进行研究,包括首次人体研究(NCT01416324)、服用二甲双胍的2型糖尿病患者研究(NCT02202161)、原发性胆汁性胆管炎瘙痒患者研究(NCT01899703)以及 Phase 2b GLIMMER 试验(NCT02966834)。药效学效应包括随剂量增加总血清胆汁酸减少和血清胆汁酸合成关键中间体 C4 增加。已确定了用于 PBC 胆汁淤积性瘙痒 Phase 3 研究的良好耐受剂量。 |
| 分子式 |
C28H38N2O7S
|
|---|---|
| 分子量 |
546.675527095795
|
| 精确质量 |
546.24
|
| 元素分析 |
C, 61.52; H, 7.01; N, 5.12; O, 20.49; S, 5.87
|
| CAS号 |
1345982-69-5
|
| PubChem CID |
53492727
|
| 外观&性状 |
Typically exists as white to off-white solids at room temperature
|
| LogP |
5.708
|
| tPSA |
150.41
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
13
|
| 重原子数目 |
38
|
| 分子复杂度/Complexity |
870
|
| 定义原子立体中心数目 |
2
|
| SMILES |
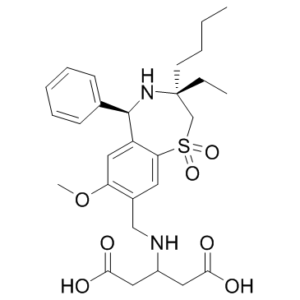
O=C(O)CC(NCC1=C(OC)C=C(C2=C1)[C@@H](C3=CC=CC=C3)N[C@](CC)(CCCC)CS2(=O)=O)CC(O)=O
|
| InChi Key |
CZGVOBIGEBDYTP-VSGBNLITSA-N
|
| InChi Code |
InChI=1S/C28H38N2O7S/c1-4-6-12-28(5-2)18-38(35,36)24-13-20(17-29-21(14-25(31)32)15-26(33)34)23(37-3)16-22(24)27(30-28)19-10-8-7-9-11-19/h7-11,13,16,21,27,29-30H,4-6,12,14-15,17-18H2,1-3H3,(H,31,32)(H,33,34)/t27-,28-/m1/s1
|
| 化学名 |
3-[[(3R,5R)-3-butyl-3-ethyl-7-methoxy-1,1-dioxo-5-phenyl-4,5-dihydro-2H-1lambda6,4-benzothiazepin-8-yl]methylamino]pentanedioic acid
|
| 别名 |
1345982-69-5; Linerixibat; GSK2330672; GSK-2330672; Iinerixibat; Linerixibat [USAN]; CHEMBL2387408; Linerixibat (USAN);
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~91.46 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (4.57 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.57 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.57 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8292 mL | 9.1461 mL | 18.2922 mL | |
| 5 mM | 0.3658 mL | 1.8292 mL | 3.6584 mL | |
| 10 mM | 0.1829 mL | 0.9146 mL | 1.8292 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。