| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
| 靶点 |
Calcium ionophore
|
|---|---|
| 体外研究 (In Vitro) |
聚合链霉菌产生抗生素和钙离子载体离子霉素[1]。当 LCLC 103H 细胞中添加 2 μM 离子霉素时,细胞内 Ca2+ 浓度暂时从 50 nM 增加至 180 nM。在离子霉素处理的培养物中,DNA 和蛋白质分析显示 DNA 和 PARP 探针发生片段化,其中存在 caspase 介导的细胞消毒特征的 85 kDa 片段。大约 1-5% 的离子霉素处理细胞具有台北细胞。在整个细胞中激活 caspase 后,观察到离子霉素处理后抗 Ac-DEVD-amc 活性增加 [2]。离子霉素介导的间质和外泌体释放。离子霉素处理后,SKOV3ip 细胞条件培养基中携带 L1-32 切片的外泌体数量增加 [4]。此外,离子霉素通过 Ca2+ 的 SOCE 流入磷酸化 p38 MAPK,从而防止 TNF-α 产生的 NF-κB 磷酸化 [5]。
研究了一种新型抗生素离子霉素/Ionomycin的离子载体特性。发现抗生素能够将钙离子从水相主体中提取到有机相中。抗生素还充当移动离子载体,将阳离子运输穿过溶剂屏障。通过离子竞争实验确定的离子霉素的二价阳离子选择性顺序为:Ca大于Mg大于Sr=Ba,其中抗生素对锶和钡的结合微不足道。抗生素也在一定程度上结合La3+,但它与单价碱金属离子的络合作用可以忽略不计。离子霉素与Ca2+结合的测量表明,离子霉素以一比一的化学计量比复合和运输钙离子。[1] 我们研究了可能是Ca2+离子载体离子霉素诱导T细胞有丝分裂特性的信号机制。离子霉素诱导高度纯化的静息人T细胞在单核细胞存在下增殖,并伴随IL-2R表达和IL-2合成。用离子霉素处理T细胞会引发磷酸肌醇的水解,水解副产物磷脂酸和肌醇磷酸盐的积累证明了这一点。离子霉素还诱导蛋白激酶C(PKC)的激活,如PKC的自身磷酸化和PKC靶蛋白CD4和CD8的磷酸化所示。离子霉素与PMA协同增强PKC的激活。结论是,离子霉素除了激活Ca2+/钙调素依赖的信号通路外,还诱导人T细胞中磷酸肌醇的水解和PKC的激活。离子霉素与佛波酯在触发T细胞活化方面的协同作用可能至少部分与PKC的增强活化有关。[2] 普遍存在的钙蛋白酶(μ-calpain和m-calpain)一再与细胞凋亡有关,但其潜在机制仍有待阐明。我们检测了来自人类大细胞肺癌的LCLC 103H细胞中离子霉素诱导的细胞死亡。我们检测到细胞凋亡的标志,如膜起泡、核凝聚、DNA梯状结构形成、胱天蛋白酶激活和聚ADP核糖聚合酶切割。细胞与钙蛋白酶抑制剂乙酰钙蛋白酶抑制剂27肽和半胱氨酸天冬氨酸蛋白酶抑制剂Z-DEVD-fmk预孵育可防止细胞凋亡,表明钙蛋白酶和半胱氨酸天冬酶都参与了凋亡过程。凋亡事件与Bid和Bcl-2的减少以及半胱氨酸天冬氨酸蛋白酶-9、-3和-7的激活呈可抑制的钙调素相关。在体外,两种普遍存在的钙蛋白酶都在截断其N端区域的单个位点切割重组Bcl-2、Bid和Bcl-x(L)。结合研究表明,钙蛋白酶截短的Bcl-2和Bid与固定的完整Bcl-2家族蛋白的相互作用减弱。此外,钙蛋白酶切割Bcl-2,Bid诱导分离线粒体释放细胞色素c。我们得出结论,离子霉素/Ionomycin诱导的钙蛋白酶激活促进了Bcl-2蛋白的减少,从而触发了内在的凋亡途径。[3] 外泌链脱落是一种蛋白水解机制,通过这种机制,跨膜分子转化为可溶性形式。切割由金属蛋白酶介导,以组成型或诱导型方式进行。尽管人们认为这是一个细胞表面事件,但越来越多的证据表明,切割可以发生在细胞内的隔室中。然而,尚不清楚裂解的可溶性分子是如何进入细胞外空间的。通过分析卵巢癌细胞中的L1(CD171)和CD44,我们在本文中表明,Ionomycin/离子霉素、APMA(4-氨基苯汞醋酸盐)或MCD(甲基β-环糊精)诱导的切割是在内体室中启动的,随后以外泌体的形式释放。钙内流增强了含有功能活性形式的ADAM10(一种去整合素和金属蛋白酶10)和ADAM17[TACE(肿瘤坏死因子α转换酶)]以及CD44和L1细胞质切割片段的外泌体的释放。切割也可以在释放的外泌体中进行,但只有小干扰RNA消耗ADAM10才能在组成型和诱导条件下阻断切割。相比之下,响应PMA的L1切割发生在细胞表面,并由ADAM17介导。我们得出结论,不同的ADAM参与不同的细胞隔室,ADAM10负责囊泡中的脱落。我们的发现开辟了外泌体作为外结构域脱落平台和可溶性分子细胞输出载体的可能性。[4] 通过储存操作钙进入(SOCE)的钙内流在调节绝大多数细胞生理事件中起着重要作用。MAPK信号传导也是许多细胞功能的另一个关键调节因子。然而,SOCE和MAPK之间的关系尚不清楚。在这项研究中,我们阐明了SOCE参与了Gαq/11蛋白介导的肠上皮细胞系HT-29/B6中p38 MAPK的激活。在该细胞系中,我们之前的研究表明,刺激M3毒蕈碱乙酰胆碱受体(M3 mAChR)而不是组胺H1受体(H1R)会导致p38 MAPK磷酸化,从而通过ADAM17蛋白酶介导的TNF受体-1(TNFR1)的脱落抑制肿瘤坏死因子-α(TNF-α)诱导的NF-κB信号传导。首先,我们发现对M3-mAChR和蛋白酶激活的受体-2(PAR-2)的刺激,而不是对H1R的刺激,通过SOCE诱导了胞浆Ca2+浓度的持续上调。M3-mAChR或PAR-2的激活也抑制了TNF-α诱导的NF-κB磷酸化,这依赖于p38 MAPK活性。时间过程实验表明,M3 mAChR刺激可诱发细胞内钙依赖性早期p38 MAPK磷酸化和细胞外钙依赖性晚期p38 MAPK磷酸化。这种由M3-mAChRs或PAR-2引起的后期p38 MAPK磷酸化通过抑制SOCE而被消除。Thapsigargin或Ionomycin/离子霉素也通过SOCE的Ca2+内流磷酸化p38 MAPK,从而抑制TNF-α诱导的NF-κB磷酸化。最后,我们发现p38 MAPK对于thapsigargin诱导的TNFR1切割和TNF-α诱导的NF-κB磷酸化的抑制至关重要。总之,SOCE对p38 MAPK磷酸化很重要,并参与TNF-α信号抑制[5]。 |
| 体内研究 (In Vivo) |
离子霉素治疗挽救了BMSC特异性条件性alpl敲除小鼠的骨质疏松症[6]
为了进一步确定BMSCs中ALPL缺乏是否会导致体内成骨和脂肪生成改变,我们评估了BV/TV和Tb。我们发现,与对照组alplf/f同窝小鼠相比,3个月大的Prrx1 alpl-/-小鼠的氮含量显著降低(图7a,b)。用抹了面粉的alpl同窝伙伴(alplf/f)作为对照。显微CT和组织学分析显示,BMD、BV/TV和Tb。与Prrx1-alpl-/-小鼠相比,用离子霉素治疗的3个月大Prrx1-alpl-/-鼠的N显著增加(图7a,b)。为了进一步检测BMSCs中成骨/成脂谱系分化的变化,我们检测了用离子霉素治疗的alplf/f、Prrx1-alpl-/-小鼠和Prrx1-alpl-/-鼠骨髓中的脂肪细胞数量。油红O染色显示,与对照alplf/f同窝小鼠相比,Prrx1-alpl-/-骨髓中的脂肪细胞数量显著增加(图7c)。然而,与Prrx1-alpl-/-小鼠相比,离子霉素治疗后Prrx1-alpl-/-骨髓中的脂肪细胞数量显著减少(图7c)。钙黄绿素双重标记分析显示,与对照alplf/f小鼠相比,Prrx1-alpl-/-小鼠的骨形成率降低(图7d)。离子霉素治疗逆转了Prrx1-alpl-/-小鼠受损的成骨作用。此外,通过ELISA评估,RANKL和OPG的血清水平没有显著变化(图S7c,d),这表明破骨细胞在Prrx1-alpl-/-小鼠中可能没有改变。与对照组BMSCs相比,alpl-/-BMSCs的细胞内Ca2+水平降低,离子霉素处理提高了alpl-/-BMSCs细胞内的Ca2+水平(图7e)。此外,与alplf/f小鼠的BMSC相比,Prrx1-alpl-/-小鼠的BMSCs显示出成骨分化降低和成脂分化增加(图7f-i)。用离子霉素处理的Prrx1-alpl-/-小鼠的BMSC显示出成骨分化增加和成脂分化减少(图7f-i)。这些结果表明,骨髓间充质干细胞中ALPL缺乏会诱导与年龄相关的骨质疏松症表型,离子霉素治疗逆转了这一表型。 |
| 细胞实验 |
活细胞中的蛋白酶活性[3]
分别用荧光底物Suc-LLVY-amc(160μm)或Ac-DEVD-amc(200μm)测量全细胞中钙蛋白酶或胱天蛋白酶样活性。将底物离子霉素、依托泊苷和AC27P混合在适当的HEPES缓冲无血清生长培养基中。将LCLC 103H细胞铺在24孔板上(105个细胞/孔),并在37°C的加湿5%CO2培养箱中与底物预孵育30分钟。使用荧光读取系统(Fluoroskan上升)监测37°C下的底物水解,激发波长设置为355±20 nm,发射波长设置为460±20 nm。在添加离子霉素之前和之后,以及在37°C下用50μm AC27P或20μm Z-DEVD-fmk预孵育细胞1小时后,每5分钟(最多400分钟)收集一次荧光读数。 凋亡细胞的FACS分析[3] 通过流式细胞术同时监测膜联蛋白V结合和碘化丙啶摄取来评估细胞存活率。将LCLC 103H细胞铺在内径10cm的培养板上,在37°C下用指定的抑制剂/抑制剂处理,重新悬浮在2ml膜联蛋白V结合缓冲液中,最后在室温下用膜联蛋白V-荧光素和碘化丙啶(9:1)处理5分钟。使用FACS Calibur Sort通过530/30带通滤光片测量20000个细胞的荧光,以监测膜联蛋白荧光素磷脂酰丝氨酸结合,并通过585/42滤光片监测碘化丙啶摄取。 游离钙浓度的测量[3] 在添加2μm离子霉素前后测定LCLC 103H细胞中的游离钙浓度。这些测量和Fura-2荧光的校准是根据标准方案进行的(31)。简而言之,用FluoronicR F-127稀释的5μm Fura-2 AM装载细胞1小时。盖玻片用含有20 mmHEPES、5.6 mm葡萄糖、137 mm NaCl、0.8 mm KCl、0.5 mm CaCl2、1.0 mm MgCl2、2 mm EDTA、pH 7.4的溶液冲洗,放置在成像室中,并安装在37°C的平台上,放置在尼康数码相机的载物台上。使用75瓦氙气光源和滤光轮(Ludl)在340和380纳米的交替波长下激发Fura-2。发射波长在增强型CCD相机检测之前通过510nm滤光片组。在用pH 7.4的20 mm HEPES中的10 mm CaCl2溶液冲洗和预孵育细胞后,测量饱和钙浓度,该溶液含有5.6 mm葡萄糖、137 mm NaCl、0.8 mm KCl、1.0 mm MgCl2、2 mm EDTA,随后两次添加2μm离子霉素,间隔5分钟。之后,通过加入2ml pH 8.0的80mm EGTA来测量钙的缺失。使用IonWizard软件存储和处理数据。 膜囊泡的分离[4] 细胞在无血清培养基中培养过夜,然后用或不用离子霉素(1μM)、APMA(50μM),MCD(10 mM)或PMA(50 ng/ml)处理指定时间。收集组织培养上清液,在300 g下离心10分钟,在10000 g下离心20分钟,以去除细胞碎片。使用Beckman SW40转子在4°C下以100000 g离心2小时,收集膜囊泡。将囊泡直接溶解在SDS样品缓冲液[30%蔗糖、80 mM Tris/HCl(pH 8.8)、3%SDS和0.01 mg/ml溴酚蓝]中,或进一步进行梯度离心处理(见下文)。 |
| 动物实验 |
离子霉素治疗[6]
离子霉素溶于DMSO。体内治疗中,将离子霉素腹腔注射给12周龄的alpl+/−小鼠和alpl−/− CKO小鼠,剂量为1 mg·kg−1/天,持续28天。对照组小鼠仅注射溶剂。离子霉素治疗后,所有组别的小鼠均健康。 体内油红O染色[6] 为了评估骨小梁区域的脂肪组织,将股骨固定于4%多聚甲醛溶液中,并用5% EDTA(pH 7.4)脱钙,然后进行冰冻切片。切片用油红O染色,在显微镜下对阳性区域进行定量,结果以占总面积的百分比表示。简而言之,切片先用60%异丙醇洗涤,然后在室温下用新鲜的油红O染色液孵育15分钟,最后用苏木精复染。所有油红O染色试剂均购自Sigma-Aldrich公司。 |
| 毒性/毒理 (Toxicokinetics/TK) |
小鼠皮下注射LD50为28 mg/kg,《抗生素杂志》,31(815),1978 [PMID:711623]
6446270 小鼠口服LD50为650 mg/kg,《柯克-奥斯默化学技术百科全书》,第3版,M. Grayson和D. Eckroth主编,纽约,John Wiley & Sons出版社,1978,3(47),1978 6446270 小鼠腹腔注射LD50为12 mg/kg,《柯克-奥斯默化学技术百科全书》,第3版,M. Grayson和D. Eckroth主编,纽约,John Wiley & Sons出版社,1978,3(47),1978 |
| 参考文献 | |
| 其他信息 |
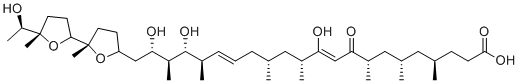
离子霉素是一种极长链脂肪酸,其化学名为二十二碳-10,16-二烯酸,其4、6、8、12、14、18和20位被甲基取代,11、19和21位被羟基取代,21位被(2',5-二甲基八氢-2,2'-联呋喃-5-基)乙醇基团取代。离子霉素是由球形链霉菌(Streptomyces conglobatus)产生的一种离子载体,在研究中用于提高细胞内Ca²⁺水平,并作为一种研究工具来了解Ca²⁺跨生物膜的转运。它既是一种代谢产物,也是一种钙离子载体。它是一种烯醇、环醚、极长链脂肪酸和多不饱和脂肪酸。
已有报道称链霉菌(Streptomyces conglobatus)中存在离子霉素,并有相关数据。 离子霉素是一种聚醚类抗生素,从新种链霉菌(Streptomyces conglobatus sp. nov. Trejo)中分离得到,具有抗肿瘤活性。离子霉素是一种钙离子载体,可提高细胞内Ca++水平,这可能与淋巴细胞内切酶活化、Bcl-2/Bax比值降低以及最终导致细胞凋亡有关。此外,该药物还用于研究细胞内钙在细胞过程中的作用。(NCI) 一种二价钙离子载体,被广泛用作研究细胞内钙在细胞过程中作用的工具。 ALPL基因的功能缺失突变会导致低磷酸酯酶症(HPP),这是一种先天性代谢紊乱,会导致骨骼矿化缺陷。在成人中,主要临床特征包括乳牙或恒牙早期脱落、骨质疏松、骨痛、软骨钙化和骨折。然而,目前尚无针对成人低磷酸血症(HPP)的治疗指南。本研究表明,ALPL缺陷导致细胞内Ca2+内流减少,进而引起人骨髓间充质干细胞(BMSCs)骨质疏松表型,这是由于成骨分化下调和成脂分化上调所致。在人骨髓间充质干细胞和小鼠骨髓间充质干细胞中,使用离子霉素提高BMSCs的细胞内钙水平可以挽救alpl+/-小鼠和BMSC特异性(Prrx1-alpl-/-)条件性alpl敲除小鼠的骨质疏松表型。机制研究表明,ALPL对于维持细胞内Ca2+内流至关重要,它通过与α2δ亚基结合来调节L型Ca2+通道的转运,从而调控L型Ca2+通道的内化。 Ca2+ 内流减少会使 Akt/GSK3β/β-catenin 信号通路失活,而该通路调控骨髓间充质干细胞 (BMSC) 的谱系分化。本研究揭示了胞外酶 ALPL 在维持钙通道转运、调控干细胞谱系分化和骨稳态方面此前未知的作用。通过离子霉素治疗加速 L 型 Ca2+ 通道的 Ca2+ 内流可能是一种有前景的治疗成人低磷酸血症 (HPP) 的方法。[6] |
| 分子式 |
C41H72O9
|
|---|---|
| 分子量 |
709.0050
|
| 精确质量 |
708.518
|
| 元素分析 |
C, 69.46; H, 10.24; O, 20.31
|
| CAS号 |
56092-81-0
|
| 相关CAS号 |
Ionomycin calcium;56092-82-1
|
| PubChem CID |
6912226
|
| 外观&性状 |
Colorless to light yellow liquid
|
| 密度 |
1.072 g/cm3
|
| 沸点 |
817.2ºC at 760 mmHg
|
| 闪点 |
235.2ºC
|
| 折射率 |
1.512
|
| LogP |
7.799
|
| tPSA |
153.75
|
| 氢键供体(HBD)数目 |
5
|
| 氢键受体(HBA)数目 |
9
|
| 可旋转键数目(RBC) |
22
|
| 重原子数目 |
50
|
| 分子复杂度/Complexity |
1120
|
| 定义原子立体中心数目 |
14
|
| SMILES |
O1[C@](C([H])([H])[H])([C@@]([H])(C([H])([H])[H])O[H])C([H])([H])C([H])([H])[C@]1([H])[C@]1(C([H])([H])[H])C([H])([H])C([H])([H])[C@@]([H])(C([H])([H])[C@@]([H])([C@]([H])(C([H])([H])[H])[C@@]([H])([C@@]([H])(/C(/[H])=C(\[H])/C([H])([H])[C@@]([H])(C([H])([H])[H])C([H])([H])[C@@]([H])(C([H])([H])[H])/C(=C(\[H])/C([C@@]([H])(C([H])([H])[H])C([H])([H])[C@@]([H])(C([H])([H])[H])C([H])([H])[C@]([H])(C([H])([H])[H])C([H])([H])C([H])([H])C(=O)O[H])=O)/O[H])C([H])([H])[H])O[H])O[H])O1
|
| InChi Key |
PGHMRUGBZOYCAA-OJFQOPKISA-N
|
| InChi Code |
InChI=1S/C41H72O9/c1-25(21-29(5)34(43)24-35(44)30(6)22-27(3)20-26(2)14-15-38(46)47)12-11-13-28(4)39(48)31(7)36(45)23-33-16-18-41(10,49-33)37-17-19-40(9,50-37)32(8)42/h11,13,24-33,36-37,39,42-43,45,48H,12,14-23H2,1-10H3,(H,46,47)/b13-11+,34-24-/t25-,26-,27+,28-,29-,30+,31+,32-,33?,36+,37?,39-,40+,41+/m1/s1
|
| 化学名 |
(4R,6S,8S,10Z,12R,14R,16E,18R,19R,20S,21S)-11,19,21-trihydroxy-22-((2S,5'S)-5'-((R)-1-hydroxyethyl)-2,5'-dimethyloctahydro-[2,2'-bifuran]-5-yl)-4,6,8,12,14,18,20-heptamethyl-9-oxodocosa-10,16-dienoic
acid
|
| 别名 |
SQ23377; ionomycin; 56092-81-0; Ionomycin free acid; SQ-23377; CHEBI:63954; 54V905V6AT; (4R,6S,8S,10Z,12R,14R,16E,18R,19R,20S,21S)-11,19,21-trihydroxy-22-[(2S,5S)-5-[(2R,5S)-5-[(1R)-1-hydroxyethyl]-5-methyloxolan-2-yl]-5-methyloxolan-2-yl]-4,6,8,12,14,18,20-heptamethyl-9-oxodocosa-10,16-dienoic acid; UNII-54V905V6AT; SQ-23377; SQ 23377
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~141.04 mM)
Ethanol : ~100 mg/mL (~141.04 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (3.53 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (3.53 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (3.53 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: ≥ 2.5 mg/mL (3.53 mM) (饱和度未知) in 10% EtOH + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,您可以将 100 μL 25.0 mg/mL 澄清乙醇储备液添加到 900 μL 玉米油中并充分混合。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.4104 mL | 7.0521 mL | 14.1042 mL | |
| 5 mM | 0.2821 mL | 1.4104 mL | 2.8208 mL | |
| 10 mM | 0.1410 mL | 0.7052 mL | 1.4104 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03678610 | COMPLETED | Other: Doing ICSI I a medium supplemented with Ionomycin and Latrunculin A |
Infertility | Ibn Sina Hospital | 2018-09-25 | Not Applicable |
| NCT06106412 | RECRUITING | Drug: Ionomycin SIGMA Drug: A23187 |
Infertility, Female | Instituto Valenciano de Infertilidad, IVI VALENCIA | 2024-01-01 | Not Applicable |
| NCT02045914 | UNKNOWN STATUS | Other: calcium ionophore solution | Fertilization Failure | Baskent University | 2014-01 | Not Applicable |
| NCT05706714 | COMPLETED | Lysinuric Protein Intolerance Urea Cycle Disorder |
Istanbul University - Cerrahpasa (IUC) | 2021-04-06 | ||
| NCT00657891 | COMPLETED | Drug: Omalizumab Drug: Placebo |
Asthma | Creighton University | 2007-03 | Phase 4 |
|
|
|