| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Natural Polyphenols
|
|---|---|
| 体外研究 (In Vitro) |
在我们继续努力寻找有效的天然来源药物治疗糖尿病并发症的过程中,我们从八成EtOH的Brandisia hanei茎和叶提取物中分离出五种咖啡因化苯丙苷,毛蕊花苷(1),异毛蕊花苷(2),poliumo苷(3),brandioside(4)和phelipo苷(5)。这些分离物(1-5)进行了体外生物测定,以评估其对晚期糖基化终产物形成和大鼠晶状体醛糖还原酶活性的抑制活性。与阳性对照氨基胍(IC50=1,056µM)和槲皮素(IC50=28.4µM)相比,所有化合物均表现出明显的晚期糖基化终产物形成抑制作用,IC50值为4.6-25.7µM。[1]
异牛皮苷抑制COX-2、iNOS、TNF-α、IL-6和IL-1β的表达。此外,异acto苷通过降低磷酸化的i -κB -α和IKK水平以及NF-κB/p65核易位来减弱lps诱导的NF-κB转录活性。此外,异乳糖苷通过降低磷酸化JNK1/2和p38MAPK的水平,抑制lps诱导的AP-1转录活性。异牛皮苷阻断了lps诱导的TLR4二聚化,导致MyD88和含tir结构域的适配器诱导干扰素-β (TRIF)的募集减少,TGF-β活化激酶-1 (TAK1)的磷酸化减少。[2] 皂苷对卵巢癌细胞具有剂量依赖性和时间依赖性的生长抑制作用,孵育24h时IC50值为15µM。异牛皮苷诱导这些细胞的早期和晚期凋亡。异牛皮苷还导致亚g1期细胞周期阻滞,并表现出强烈的剂量依赖性。异牛皮苷处理还能抑制细胞迁移和细胞侵袭。[3] |
| 体内研究 (In Vivo) |
在大鼠晶状体醛糖还原酶实验中,与阳性对照3,3-四亚甲基戊二酸(IC50=4.03µM)和槲皮素(IC50=7.2µM)相比,毛蕊花苷、异毛蕊花苷和白藜芦醇苷对大鼠晶状体醛糖还原酶的抑制作用更强,IC50分别为0.83、0.83和0.85µM。此外,还研究了毛苷对高糖诱导的斑马鱼幼鱼视网膜血管扩张的影响。与高糖处理的对照组相比,毛蕊花苷在10µM时使高糖诱导的玻璃体视网膜血管直径减小69%,在20µM时使其直径减小81%。上述结果提示,韩菖蒲及其有效成分可能具有治疗和预防糖尿病血管并发症的作用。[1]
异核苷预处理小鼠能有效抑制二甲苯致耳部水肿和脂多糖致内毒素死亡,并对脂多糖致AKI有保护作用。 结论和意义:异牛油果苷阻断TLR4二聚化,激活MyD88-TAK1-NF-κB/MAPK信号级联和TRIF通路。我们的数据表明,异牛皮苷是治疗炎症性疾病的潜在先导化合物。[2] 结果显示,与对照组相比,异核苷组明显抑制OVCAR-3肿瘤的生长。在5周治疗期结束时,未治疗组的平均肿瘤生长和体积明显高于治疗组。 结论:综上所述,本研究提示异牛油果苷在体外和体内均具有抑制卵巢癌细胞生长的巨大潜力,可作为一种潜在的抗癌药物。[3] |
| 酶活实验 |
isoacteoside与TLR4复合物的对接[2]
使用Ledock中的分子建模软件包进行了isoacteoside与TLR4复合物(PDB代码:3FXI)的对接模拟(http://www.lephar.com). TLR4复合晶体结构从RCSB蛋白质数据库(PDB代码:3FXI)获得(Park等人,2009)。 |
| 细胞实验 |
MTT实验[2]
将RAW264.7细胞以每孔105个细胞的密度接种到96孔板中过夜。然后,用isoacteoside(20、40或80μM)处理细胞24小时,并根据我们之前的报告(Gao等人,2015)使用MTT法测定细胞毒性。 亚硝酸盐和NO的测定[2] RAW264.7细胞以每孔5×105的密度在24孔板上过夜。用isoacteoside(20、40或80μM)预处理细胞1小时后,将LPS(1μg·mL-1)加入含isoacteoside的培养基中并培养24小时。根据制造商的方案,使用Griess试剂测定培养基中的亚硝酸盐水平。 收集处理过的细胞,用DAF-FM(1μM)再染色1小时。使用FITC通道通过FACScan流式细胞术测定荧光信号。 ELISA[2] 用异丙交酯(20、40或80μM)预处理1小时后,BMDM和RAW264.7细胞与LPS(1μg·mL-1)孵育24小时。收集培养基,根据制造商的说明使用ELISA试剂盒测定TNF-α、IL-6和IL-1β的分泌水平。 免疫荧光[2] NF-κB/p65的免疫荧光分析如前所述进行(Gao等人,2016)。简而言之,将2×105个RAW264.7细胞接种到35毫米玻璃底SPL共聚焦培养皿中过夜。将细胞用isoacteoside(80μM)预处理1小时,用LPS(1μg·mL-1)刺激2小时后,应用抗NF-κB/p65(1:50)的第一抗体和山羊抗兔Alexa Fluor 568(1:200)的第二抗体。细胞被固定并用Hoechst 33 342(1μM)染色以进行成像。成像在Leica TCS SP8激光共聚焦显微镜下进行,放大倍数为60倍,激发/发射波长为588/615-690 nm。 瞬时转染和萤光素酶测定[2] 将HEK293T细胞以106个细胞的密度接种到培养皿(10cm,i.d.)中,并放置过夜。使用TurboFect转染试剂将从Addgene获得的TLR4-HA和TLR4-Flag质粒共转染24小时。将转染的细胞以5×105个细胞的密度接种到培养皿(5cm,i.d.)中,并放置过夜。细胞在收获前用isoacteoside(80μM)预处理1小时,用LPS(1μg·mL-1)刺激24小时。 根据制造商的说明,将在96孔板中培养过夜的RAW264.7细胞瞬时共转染piNOS-luc、pNF-κB-luc或pAP-1-luc质粒和pRL-TK质粒,分别检测iNOS、NF-κB或AP-1转录活性。pRL-TK质粒用作参考对照。转染48小时后,细胞用isoacteoside(80μM)预处理1小时,用LPS(1μg·mL-1)刺激16小时。根据制造商的说明,使用Dual-Glo萤光素酶检测系统试剂盒测定萤光素酶活性。 通过Western印迹、定量实时PCR或ELISA评估NF-κB通路、MAPK通路、iNOS、TNF-α、IL-6和IL-1β的表达。通过用TLR4质粒转染HEK293T细胞来测定TLR4二聚化。[2] MTT法用于研究化合物对细胞存活率的细胞毒性作用。通过流式细胞术评估对细胞凋亡和细胞周期阻滞的影响。采用体外伤口愈合试验和基质凝胶试验分别研究了异丙交酯对细胞迁移和细胞侵袭的影响。非癌卵巢细胞系SV-40作为对照。3. 采用Western blotting、实时荧光定量PCR或ELISA法检测NF-κB通路、MAPK通路、iNOS、TNF-α、IL-6、IL-1β的表达。用TLR4质粒转染HEK293T细胞,检测TLR4二聚化。[2] 采用MTT法研究该化合物对细胞活力的细胞毒作用。流式细胞术观察其对细胞凋亡和细胞周期阻滞的影响。采用体外创面愈合实验和基质实验分别研究isoacteoside对细胞迁移和细胞侵袭的影响。非癌性卵巢细胞系SV-40作为对照 MTT试验[3] MTT法检测卵巢癌细胞和正常细胞的增殖情况。简单地说,将细胞以每孔5×104个细胞的密度在96孔的平板微滴培养板中培养,并在不同浓度的isoacteoside处理24小时。然后加入新鲜的MTT溶液,在37℃下再孵育4小时。然后加入二甲基亚砜溶解甲醛晶体。最后,使用微孔板读取器在570 nm处测量吸光度。 基质侵袭试验[3] 利用Matrigel®涂层侵袭室评估侵袭情况。isoacteoside处理和未处理的到达膜下表面的OVCAR-3细胞用结晶紫(CV)染色,并拍摄CV染色细胞的图像。将形成的结晶紫配合物溶解在10%的乙酸中,用分光光度计测量所得溶液在600 nm处的吸光度,测定其对细胞的侵袭。 |
| 动物实验 |
采用二甲苯诱导的小鼠耳水肿、LPS诱导的内毒素休克和LPS诱导的内毒素血症相关急性肾损伤(AKI)模型,测定了异阿司匹林苷的体内抗炎作用。[2]
动物实验和伦理声明:BALB/c小鼠(雄性,6-8周龄,体重18-22克)饲养于塑料笼中(每笼≤5只),在标准条件下(无特定病原体)自由摄食饮水,并进行空气过滤(22±2℃,12小时光照/12小时黑暗)。对于二甲苯诱导的小鼠耳水肿模型(Ma et al., 2013),腹腔注射异阿司匹林(100 mg·kg−1)。2 小时后,在小鼠右耳的后表面和前表面涂抹 30 μL 二甲苯(≥98.5%)。左耳不进行任何处理,作为对照。1 小时后,在乙醚麻醉下,通过颈椎脱臼处死小鼠,并采集两个耳部组织样本(内径 7 mm)称重。通过比较左右耳组织样本重量的增加来评估水肿程度。收集耳部组织,并在室温下用 10% 甲醛固定至少 24 小时。经不同浓度的酒精脱水后,将组织包埋于石蜡中并切片。切片经苏木精-伊红 (H&E) 染色后,在光学显微镜下成像。 对于内毒素休克模型(Chen et al., 2015b),通过腹腔注射脂多糖 (LPS,20 mg·kg−1) 诱导小鼠内毒素血症。在注射 LPS 前 2 小时,小鼠预先腹腔注射异阿司匹林 (100 mg·kg−1)。地塞米松 (DEX,5 mg·kg−1,腹腔注射) 用作阳性对照,因为它具有优异的抗炎作用(Zeng et al., 2015; Qin et al., 2016),并且已在临床研究中用于治疗内毒素休克(Zhang et al., 2003)。连续监测 132 小时的存活率。 132小时后,剩余小鼠在乙醚麻醉下通过颈椎脱臼处死。 对于AKI模型(Zarjou和Agarwal,2011),小鼠被随机分为六组:对照组、异阿司匹林组(25、50和100 mg·kg⁻¹,腹腔注射)、LPS组(10 mg·kg⁻¹,腹腔注射)和阳性对照地塞米松组(5 mg·kg⁻¹,腹腔注射)。在LPS注射前2小时,小鼠接受异阿司匹林预处理。12小时后,在乙醚麻醉下通过眼眶后静脉丛取血采集血清样本,并根据制造商的说明使用ELISA试剂盒检测细胞因子(TNF-α、IL-6和IL-1β)。小鼠随后通过颈椎脱臼处死。使用罗氏P800型分析仪测定血清尿素氮(BUN)和肌酐水平。此外,收集肾脏组织并用10%甲醛固定。经不同浓度酒精脱水后,将组织包埋于石蜡中并切片。切片经苏木精-伊红(H&E)染色后,在光学显微镜下成像。[2] >体内研究[3] 本研究中,将5×10⁶个OVCAR-3细胞皮下注射到4周龄雌性小鼠左侧腹部。然后将小鼠随机分为两组。当肿瘤出现后,一组小鼠(n=5)腹腔注射溶于100 μL生理盐水中的0.1%二甲基亚砜(DMSO)溶液(30 mg/kg体重),并将此时间点作为实验的第一天。实验组小鼠每周三次接受异阿司匹林注射,对照组小鼠仅接受溶于生理盐水的0.1%二甲基亚砜(DMSO)注射。5周后,处死小鼠并取出肿瘤组织,用于评估肿瘤生长情况及其他相关研究。 |
| 参考文献 |
|
| 其他信息 |
异肉桂酸苷是一种羟基肉桂酸。
据报道,异肉桂酸苷存在于无刺萼花(Acanthus ebracteatus)、厚朴(Magnolia officinalis)以及其他有相关数据的生物体中。 另见:钩果草(Harpagophytum zeyheri)的根(部分)。 |
| 分子式 |
C29H36O15
|
|---|---|
| 分子量 |
624.5872
|
| 精确质量 |
624.205
|
| CAS号 |
61303-13-7
|
| PubChem CID |
6476333
|
| 外观&性状 |
White to yellow solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
942.9±65.0 °C at 760 mmHg
|
| 熔点 |
220-230℃
|
| 闪点 |
306.1±27.8 °C
|
| 蒸汽压 |
0.0±0.3 mmHg at 25°C
|
| 折射率 |
1.689
|
| LogP |
2.58
|
| tPSA |
245.29
|
| 氢键供体(HBD)数目 |
9
|
| 氢键受体(HBA)数目 |
15
|
| 可旋转键数目(RBC) |
11
|
| 重原子数目 |
44
|
| 分子复杂度/Complexity |
936
|
| 定义原子立体中心数目 |
10
|
| SMILES |
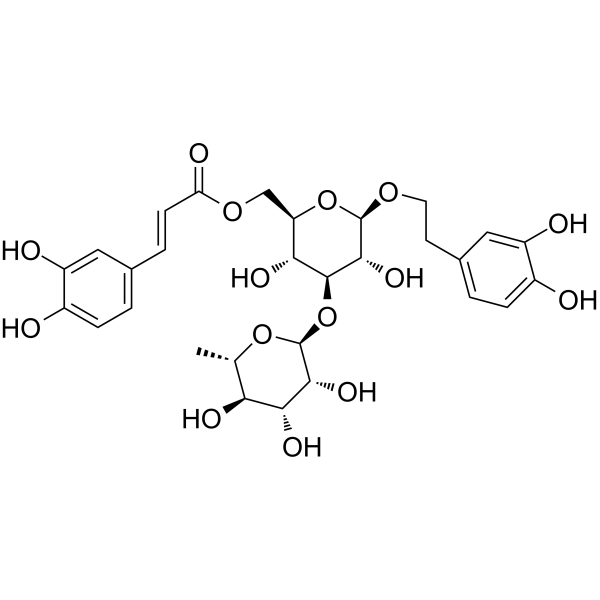
O([C@@]1([H])[C@@]([H])([C@@]([H])([C@]([H])([C@]([H])(C([H])([H])[H])O1)O[H])O[H])O[H])[C@]1([H])[C@]([H])([C@]([H])(OC([H])([H])C([H])([H])C2C([H])=C([H])C(=C(C=2[H])O[H])O[H])O[C@]([H])(C([H])([H])OC(/C(/[H])=C(\[H])/C2C([H])=C([H])C(=C(C=2[H])O[H])O[H])=O)[C@@]1([H])O[H])O[H]
|
| InChi Key |
FNMHEHXNBNCPCI-QEOJJFGVSA-N
|
| InChi Code |
InChI=1S/C29H36O15/c1-13-22(35)24(37)25(38)29(42-13)44-27-23(36)20(12-41-21(34)7-4-14-2-5-16(30)18(32)10-14)43-28(26(27)39)40-9-8-15-3-6-17(31)19(33)11-15/h2-7,10-11,13,20,22-33,35-39H,8-9,12H2,1H3/b7-4+/t13-,20+,22-,23+,24+,25+,26+,27-,28+,29-/m0/s1
|
| 化学名 |
[(2R,3R,4S,5R,6R)-6-[2-(3,4-dihydroxyphenyl)ethoxy]-3,5-dihydroxy-4-[(2S,3R,4R,5R,6S)-3,4,5-trihydroxy-6-methyloxan-2-yl]oxyoxan-2-yl]methyl (E)-3-(3,4-dihydroxyphenyl)prop-2-enoate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~250 mg/mL (~400.26 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (3.33 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (3.33 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (3.33 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.6011 mL | 8.0053 mL | 16.0105 mL | |
| 5 mM | 0.3202 mL | 1.6011 mL | 3.2021 mL | |
| 10 mM | 0.1601 mL | 0.8005 mL | 1.6011 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。