| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
Cdk1/cyclin B (IC50 = 0.4 μM); cdk2/cyclin A (IC50 = 0.68 μM); CDK5/p35 (IC50 = 0.85 μM); CDK2/cyclinE (IC50 = 7.5 μM); GSK-3β (IC50 = 0.023 μM); erk1 (IC50 = 20 μM); erk2 (IC50 = 9 μM); c-raf (IC50 = 38 μM)
CDK1/Cyclin B (IC₅₀ = 0.4 μM) [1, 2] - CDK2/Cyclin A (IC₅₀ = 0.68 μM) [1, 2] - CDK5/p35 (IC₅₀ = 0.85 μM) [1, 2] - GSK-3β (IC₅₀ = 0.023 μM) [1, 2] - LCK (IC₅₀ = 0.6 μM) [2] - Casein Kinase 1 (CK1) (IC₅₀ = 10-100 μM) [2] - Aurora Kinase A (IC₅₀ = 10-100 μM) [2] |
|---|---|
| 体外研究 (In Vitro) |
与 kenpaullone 长时间孵育可显着降低 HEK-293 细胞中 Tyr279 上内源 GSK3α 的磷酸化量。此外,虽然不太显着,内源性 GSK3β 的磷酸化也会下降。在 PC12 和 SH-SY5Y 细胞中,kenpaullone 还会导致两种 GSK3 亚型去磷酸化。无论 GSK3 是在 Sf21 细胞还是大肠杆菌中表达,kenpaullone (20μM) 在体外都能强烈抑制 GSK3β 在 Tyr216 处的自磷酸化[2][3]。
1. 激酶抑制作用: - 对多种蛋白激酶具有ATP竞争性抑制作用,对GSK-3β(IC₅₀ = 23 nM)和CDK1(IC₅₀ = 0.4 μM)的抑制活性最高 [1, 2] - 选择性特征: 对CDK1/GSK-3β的选择性比对ERK1/2、JNK、PKB等激酶高100倍以上 [2] - 对CDK家族成员(CDK2、CDK5)有相似的抑制活性 [2] - 对LCK(Src家族激酶)有中等抑制活性(IC₅₀ = 0.6 μM) [2] - 在神经元细胞中抑制GSK-3β和CDK5介导的tau蛋白磷酸化 [2] 2. 抗增殖作用: - 抑制多种癌细胞系增殖(IC₅₀ = 1-10 μM),通过诱导G1/S或G2/M期细胞周期阻滞实现 [1, 2] - 阻止视网膜母细胞瘤蛋白(pRb)磷酸化并下调细胞周期蛋白D1表达 [2] - 通过激活caspase-3和-9通路诱导癌细胞凋亡 [2] - 通过降低肿瘤细胞中VEGF表达抑制血管生成 [2] 3. 其他细胞效应: - 增强TGF-β/Smad3信号通路并促进Foxp3转录,诱导调节性T细胞分化 [1] - 通过增加酪氨酸酶表达和活性(EC₅₀ = 2.5-5 μM)刺激B16黑色素瘤细胞和人黑色素细胞合成黑色素 [2] - 通过抑制CDK5活性抑制小鼠纹状体切片中DARPP-32的磷酸化 [2] - 促进神经祖细胞的神经元分化 [2] |
| 酶活实验 |
激酶测定在 30°C 下进行 10 分钟,最终体积为 30 ml,加入 1 mg/mL 组蛋白 H1,并加入 15 μM [g-32P]ATP (3000 Ci/μmol ;1 mCi/mL)。它是通过纯化、分析或抑制其他激酶来完成的。动力学实验中ATP浓度范围为50~400μM,kenpaullone浓度范围为1~4μM,组蛋白H1浓度降低至3.5mg/mL。
1. CDK1/Cyclin B激酶活性测定: - 将重组CDK1(100 nM)和cyclin B(200 nM)与10 μM ATP、50 μM底物肽(SAMS)、10 mM MgCl₂和不同浓度的Kenpaullone在激酶缓冲液(25 mM Tris-HCl, pH 7.5, 0.1 mM EGTA, 1 mM DTT)中30°C孵育30分钟 [2] - 加入EDTA至20 mM终止反应 - 通过[γ-³²P]ATP掺入底物的量来测量磷酸化,使用P81滤纸过滤和闪烁计数 - 通过绘制抑制百分比与抑制剂浓度的关系曲线确定IC₅₀值 [2] 2. GSK-3β激酶活性测定: - 将重组GSK-3β(50 nM)与10 μM ATP、50 μM底物肽(GSK-3共有序列)、10 mM MgCl₂和不同浓度的Kenpaullone在激酶缓冲液(25 mM Tris-HCl, pH 7.5, 0.1 mM EGTA, 1 mM DTT)中30°C孵育30分钟 [2] - 反应终止和磷酸化测量同上 - 从剂量-反应曲线计算IC₅₀值 [2] 3. LCK激酶活性测定: - 将重组LCK(100 nM)与10 μM ATP、50 μM底物肽(Src共有序列)、10 mM MgCl₂和不同浓度的Kenpaullone在激酶缓冲液(25 mM Tris-HCl, pH 7.5, 0.1 mM EGTA, 1 mM DTT)中30°C孵育30分钟 [2] - 通过[γ-³²P]ATP掺入底物的量来测量磷酸化,使用P81滤纸过滤和闪烁计数 - 确定IC₅₀值的方法同上 [2] |
| 细胞实验 |
1. 细胞增殖测定:
- 将人癌细胞(1×10⁴ cells/well)接种于96孔板,用不同浓度的Kenpaullone(0.1-10 μM)处理72小时 [2] - 通过MTT还原法或结晶紫染色法测量细胞活力 - 通过绘制抑制百分比与抑制剂浓度的关系曲线计算IC₅₀值 [2] 2. 细胞周期分析: - 用Kenpaullone(1-5 μM)处理细胞(5×10⁵)24-48小时 - 收集细胞,用70%乙醇固定,碘化丙啶(50 μg/mL)含RNase A(100 μg/mL)染色,流式细胞术分析 - 确定细胞在G1、S和G2/M期的分布 [2] 3. 凋亡测定: - 用Kenpaullone(1-5 μM)处理细胞(5×10⁵)24-48小时 - 通过annexin V-FITC/PI染色和流式细胞术测量凋亡,或使用荧光底物(DEVD-AFC)测量caspase-3/7活性 [2] 4. 黑色素合成测定: - 用Kenpaullone(0.1-10 μM)处理B16黑色素瘤细胞(1×10⁴ cells/well)48-72小时 - 细胞用PBS洗涤,用含10% DMSO的1 N NaOH裂解,80°C加热1小时 - 通过测量405 nm处的吸光度确定黑色素含量 [2] - 酪氨酸酶活性测定:将细胞裂解物与L-多巴(0.05%)在磷酸盐缓冲液(pH 6.8)中37°C孵育20分钟,测量475 nm处的多巴醌形成 [2] |
| 动物实验 |
1. Xenograft tumor model:
- Human cancer cells (5×10⁶) were subcutaneously injected into nude mice (BALB/c nu/nu) - When tumors reached 100-200 mm³, mice were treated with Kenpaullone (10-30 mg/kg, p.o. or i.p.) daily for 14 days - Tumor volume was measured every 3 days using calipers (Volume = length × width² × 0.5) - Body weight was monitored daily to assess toxicity [1, 2] 2. Neuropathic pain model: - Sprague-Dawley rats (200-250 g) underwent spinal nerve ligation to induce neuropathic pain - After 7 days, Kenpaullone (1-10 mg/kg, p.o.) was administered daily for 7 days - Mechanical allodynia was assessed by measuring paw withdrawal threshold using von Frey filaments - Thermal hyperalgesia was measured by paw withdrawal latency in a hot plate test (50°C) [2] |
| 药代性质 (ADME/PK) |
吸收:啮齿动物口服给药后迅速吸收(半衰期 T₁/₂ = 0.5-1 小时)[2]
- 分布:广泛分布于组织中,肝脏、肾脏和脑组织浓度最高(由于可穿透血脑屏障)[2] - 血浆蛋白结合率:>95% [2] - 代谢:主要通过 9 位羟基化和甲基硫基氧化代谢[2] - 消除: - 大鼠半衰期:2-3 小时[2] - 约 60% 的剂量在 24 小时内经粪便排出,30% 经尿液排出[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
急性毒性:小鼠 LD₅₀ >2000 mg/kg(口服)[2]
- 亚慢性毒性: - 大鼠每日剂量高达 100 mg/kg,连续给药 14 天,未观察到明显毒性[2] - 高剂量下出现轻微胃肠道反应(恶心、呕吐)[2] - 特定器官效应: - 治疗剂量下未观察到明显肝毒性或肾毒性[2] - 高剂量下啮齿动物出现短暂性血小板减少症[2] |
| 参考文献 | |
| 其他信息 |
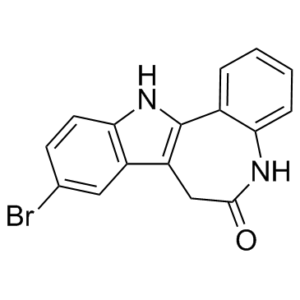
Kenpaullone是一种吲哚并氮杂卓类化合物,其结构与paullone类似,只是9位上的氢原子被溴取代。它是一种ATP竞争性抑制剂,可抑制细胞周期蛋白依赖性激酶(CDK)和糖原合成酶激酶3β(GSK3β)。Kenpaullone具有抗衰老、抑制EC 2.7.11.26(tau蛋白激酶)、心脏保护和抑制EC 2.7.11.22(细胞周期蛋白依赖性激酶)等多种活性。它是一种吲哚并氮杂卓类化合物、内酰胺类化合物和有机溴化合物。它在功能上与泡桐酮相关。
1. 化学结构和性质: - 9-溴-7,12-二氢吲哚并[3,2-d][1]苯并氮杂卓-6(5H)-酮 (C₁₆H₁₁BrN₂O, MW = 327.18) - 固体粉末,溶于DMSO (≥30 mg/mL),微溶于乙醇,不溶于水[1] - 在-20°C下至少稳定2年[1] 2. 作用机制: - ATP竞争性抑制剂,与蛋白激酶的ATP结合口袋结合 - 对GSK-3β和CDK的选择性归因于与“守门员”残基(GSK-3β中的Thr148,CDK1中的Thr14)和其他保守残基的特异性相互作用激酶结构域中的残基[2] 3. 治疗潜力: - 肿瘤学:作为单一药物或与化疗药物联合使用,具有治疗多种癌症(胶质母细胞瘤、乳腺癌、肺癌、结肠癌)的潜力[1, 2] - 神经系统疾病:具有治疗阿尔茨海默病(抑制tau蛋白磷酸化)、帕金森病和神经性疼痛的潜力[2] - 自身免疫性疾病:具有治疗银屑病、类风湿性关节炎和炎症性肠病(通过诱导Treg细胞)的潜力[1] - 皮肤病学:由于其刺激黑色素生成的作用,具有治疗色素减退性疾病(白癜风)的潜力[2] 4. 构效关系: - 9位溴取代基对于抑制CDK和GSK-3β的活性至关重要[1, 2] - 吲哚并[3,2-d][1]苯并氮杂卓核心结构对于激酶抑制活性至关重要[1] - 吲哚环2位上的修饰可以增强对特定激酶靶点的选择性[2] |
| 分子式 |
C16H11BRN2O
|
|---|---|
| 分子量 |
327.1753
|
| 精确质量 |
326.005
|
| 元素分析 |
C, 58.74; H, 3.39; Br, 24.42; N, 8.56; O, 4.89
|
| CAS号 |
142273-20-9
|
| 相关CAS号 |
237430-03-4 (Alsterpaullone)
|
| PubChem CID |
3820
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.6±0.1 g/cm3
|
| 沸点 |
613.0±45.0 °C at 760 mmHg
|
| 熔点 |
>300ºC (dec.)
|
| 闪点 |
324.5±28.7 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.730
|
| LogP |
4.02
|
| tPSA |
44.89
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
1
|
| 可旋转键数目(RBC) |
0
|
| 重原子数目 |
20
|
| 分子复杂度/Complexity |
402
|
| 定义原子立体中心数目 |
0
|
| SMILES |
BrC1C([H])=C([H])C2=C(C=1[H])C1C([H])([H])C(N([H])C3=C([H])C([H])=C([H])C([H])=C3C=1N2[H])=O
|
| InChi Key |
QQUXFYAWXPMDOE-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C16H11BrN2O/c17-9-5-6-14-11(7-9)12-8-15(20)18-13-4-2-1-3-10(13)16(12)19-14/h1-7,19H,8H2,(H,18,20)
|
| 化学名 |
9-bromo-7,12-dihydro-5H-indolo[3,2-d][1]benzazepin-6-one
|
| 别名 |
1-azakenpaullone; Kenpaullone; NSC664704; NSC 664704; NSC-664704; 9-Bromopaullone
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~65 mg/mL (~198.7 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (7.64 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2% DMSO+50% PEG 300+5% Tween 80+ddH2O: 2.5mg/mL 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.0564 mL | 15.2821 mL | 30.5642 mL | |
| 5 mM | 0.6113 mL | 3.0564 mL | 6.1128 mL | |
| 10 mM | 0.3056 mL | 1.5282 mL | 3.0564 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 Inhibition of CDK1/cyclin B by paullones.A, dose-response curves for several paullones.B, kinetic analysis of inhibition by kenpaullone.Cancer Res.1999 Jun 1;59(11):2566-9. |
|---|
 Effect of kenpaullone and 10-bromo-paullone on cell cycle progression.Cancer Res.1999 Jun 1;59(11):2566-9. |
 Schematic drawing of CDK2-kenpaullone interactions. |