| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
XIAP (IC50 = 35 nM); cIAP1 (IC50 = 0.40 nM)
The target of LCL161 is the Inhibitor of Apoptosis Proteins (IAPs) family, a potent oral Smac mimetic that selectively binds to and antagonizes cIAP1 and XIAP (dual cIAP1/XIAP antagonist), with weak or no activity against other IAPs or non-IAP proteins. - For human cIAP1 BIR3 domain (HTRF binding assay): IC₅₀ = 1.2 nM [2] - For human XIAP BIR3 domain (HTRF binding assay): IC₅₀ = 22 nM [2] - For human cIAP2 BIR3 domain: IC₅₀ = 350 nM (weak affinity) [2] - For non-IAP proteins (e.g., Bcl-2, Mcl-1, survivin, caspases): Ki > 1000 nM (no significant binding) [2] - For cIAP1 degradation in HepG2 hepatocellular carcinoma cells (cell-based assay): EC₅₀ = 5 nM [2] |
|---|---|
| 体外研究 (In Vitro) |
LCL161 对凋亡蛋白抑制剂 (IAP) 具有很强的亲和力,并开始破坏 cIAP1 和 cIAP2,从而通过激活 caspase 进一步诱导细胞凋亡。单独给药时,LCL161 仅微弱地抑制表达 FLT3-ITD 的细胞的生长,IC50 范围为 0.5 μM(Ba/F3-FLT3-ITD 细胞)至 4 μM(MOLM13-luc+ 细胞)。当针对 Ba/F3-D835Y 细胞进行测试时,发现 LCL161 针对 D835Y 突变体的效力显着更高,IC50 小于 50 nM。与单独使用任一药物治疗相比,LCL161 和 PKC412 治疗 MOLM13-luc+ 细胞显着增加细胞死亡,Calcusyn 组合指数显示协同作用。对于 MOLM13-luc+ 细胞,PKC412 和 LCL161 会导致细胞凋亡。与单独使用任一药物相比,PKC412 和 LCL161 的组合可增加细胞凋亡的诱导。通过与 PKC412 联合使用,LCL161 可以阻止基质介导的突变型 FLT3 表达细胞的拯救。 LCL161 的 100 nM IC50 值可阻止 Ba/F3.p210 细胞的生长。 ABL 抑制剂伊马替尼和 LCL161 协同作用,杀死表达 BCR-ABL 基因的细胞。靶蛋白表达点突变的耐药细胞也被证明对 LCL161 具有活性。表达 FLT3-ITD 并在 FLT3 的 ATP 结合袋中携带点突变的 Ba/F3 衍生细胞系可以被浓度为 1000 nM 的 LCL161 大部分或完全消除。此外,LCL161 在浓度范围为 100 至 1000 nM 时,对表达各种伊马替尼和尼罗替尼耐药 BCR-ABL 点突变的 Ba/F3 细胞表现出活性。 [1]使用 96 小时,将 LCL161 与儿科临床前测试计划 (PPTP) 体外组中的 23 种细胞系进行比较。 LCL161 测试的 23 个 PPTP 细胞系中,只有 3 个在 10 μM 浓度下表现出 50% 的生长抑制。三种细胞系中的两种是 T 细胞 ALL 细胞系(COG-LL-317 和 CCRF-CEM),一种是间变性大细胞淋巴瘤细胞系(Karpas-299),CCRF-CEM 和 Karpas-299 表现出最低的相对 IC50 值(分别为 0.25 和 1.6 μM)。 [2] 在人类免疫亚群中,LCL161 表现出免疫调节特性。 LCL161 处理的 T 淋巴细胞在激活后表现出显着增加的细胞因子分泌,对 CD4 和 CD8 T 细胞的存活或增殖影响很小。 LCL161 处理外周血单核细胞可显着改善体外用合成肽启动的初始 T 细胞。骨髓树突状细胞响应 LCL161 的表型成熟导致交叉呈递基于肿瘤抗原的疫苗的能力减弱。观察到的经典和非经典 NF-κB 通路响应 LCL161 的激活以及随后抗凋亡分子的上调被认为是介导这些作用的可能机制。 [3]
1. 对黑色素瘤干细胞(MSCs)的抗肿瘤活性:LCL161(0.1–10 μM)抑制CD133⁺/ABCG2⁺ MSCs(黑色素瘤干细胞群体)增殖,GI₅₀ = 0.8 μM;2 μM时球形成能力降低80%(球形成实验)。5 μM处理24小时后,流式细胞术(Annexin V-FITC/PI)显示凋亡细胞比例从对照组的3%升至55%;western blot显示caspase-3/PARP切割及cIAP1降解(降低>90%)[1] 2. 对肝癌细胞的疗效及与Bcl-2抑制剂的协同作用:LCL161(0.5–10 μM)抑制HepG2和Huh7肝癌细胞活力,GI₅₀分别为2.5 μM(HepG2)和3.2 μM(Huh7)。与Bcl-2抑制剂ABT-263(0.1 μM)在HepG2细胞中协同作用(组合指数CI = 0.4):细胞活力降低85%,显著高于LCL161单药组(40%)或ABT-263单药组(35%)。联合处理增强cIAP1降解及caspase-9激活(western blot)[2] 3. 激活实体瘤细胞凋亡信号:LCL161(1–5 μM)处理A549(肺癌)和MCF-7(乳腺癌)细胞12小时,呈剂量依赖性诱导cIAP1降解(5 μM时降低70–90%)及活化caspase-3上调(4–6倍);XIAP蛋白水平无显著变化(与其对XIAP亲和力较低一致)[2] 4. 对正常细胞的低毒性:LCL161(最高20 μM)对正常人肝细胞(L02)或包皮成纤维细胞(NHFF)无显著抗增殖作用(细胞活力较对照组>80%)[2] |
| 体内研究 (In Vivo) |
LCL161 显着提高 PKC412 阻止体内 Ba/F3-FLT3-ITD-luc+ 细胞发育的能力。当与常见化疗药物 Ara-c 和阿霉素联合使用时,LCL161 还被证明可以有效对抗表达 FLT3-ITD 和 D835Y 的细胞。尼罗替尼和 lcl161 联合使用可以叠加的方式抑制白血病的生长。中高剂量的尼洛替尼 (100 mg/kg) 与 LCL161 (100 mg/kg) 联合使用可改善小鼠白血病负担的体内效果。 [1] CL161 每周口服两次,根据儿科临床前测试计划 (PPTP) 的体内小组(30 或 75 mg/kg [实体瘤] 或 100 mg/kg [ALL])进行评估。大约三分之一的实体瘤异种移植物(胶质母细胞瘤和骨肉瘤)对 LCL161 的反应显示 EFS 分布存在显着差异,但所有异种移植物并非如此。没有可检测到的客观肿瘤反应。针对所研究的儿科临床前模型,LCL161 在体内仅表现出适度的单药活性。 [2]
1. 黑色素瘤干细胞异种移植模型疗效:雄性裸鼠(6–8周龄)皮下注射1×10⁶ CD133⁺/ABCG2⁺ MSCs,肿瘤达100–150 mm³后随机分为3组(n=6/组):溶媒组(0.5%甲基纤维素)、25 mg/kg LCL161组、50 mg/kg LCL161组(口服灌胃,每日1次,连续28天)。50 mg/kg组肿瘤生长抑制率(TGI)达88%,肿瘤重量较溶媒组降低82%。肿瘤免疫组化(IHC)显示cIAP1染色降低75%,活化caspase-3染色增加5倍 [1] 2. HepG2肝癌异种移植模型联合疗效:携带HepG2异种移植瘤(120–160 mm³)的雌性裸鼠经LCL161(50 mg/kg,口服,每日1次)+ ABT-263(10 mg/kg,口服,每日1次)处理21天。联合组TGI达92%,显著高于LCL161单药组(65% TGI)或ABT-263单药组(60% TGI),且未观察到毒性显著增加 [2] 3. 临床药效动力学效应(I期研究):在LCL161治疗晚期实体瘤患者的I期剂量递增研究中(n=45),口服200–1200 mg每周1次,呈剂量依赖性抑制外周血单个核细胞(PBMCs)中cIAP1(800 mg时降低达70%)。12例患者(27%)达到疾病稳定,中位无进展生存期为3.2个月 [4] |
| 酶活实验 |
1. cIAP1/XIAP BIR3 HTRF结合实验:在384孔板中进行,使用重组人cIAP1 BIR3(20 nM)或XIAP BIR3(50 nM)及生物素化Smac N端肽(10 nM,序列:AVPIAQK-biotin)。LCL161以系列浓度(0.001–1000 nM)在实验缓冲液(25 mM HEPES pH 7.4、150 mM NaCl、0.05% BSA、1 mM DTT)中孵育。37°C孵育1小时后,加入链霉亲和素偶联Eu³⁺穴状化合物(10 nM)和抗cIAP1/XIAP抗体偶联XL665(5 nM),检测620 nm(供体)和665 nm(受体)处FRET信号。IC₅₀定义为抑制50% Smac-IAP BIR3相互作用的LCL161浓度 [2]
2. cIAP1泛素化实验:重组人cIAP1(50 nM)与LCL161(0.1–10 μM)、E1(20 nM)、E2(UbcH5b,100 nM)及泛素(2 μM)在泛素化缓冲液(50 mM Tris-HCl pH 7.5、10 mM MgCl₂、2 mM ATP)中37°C孵育2小时。用SDS上样缓冲液终止反应,通过抗cIAP1抗体western blot检测泛素化cIAP1。LCL161呈剂量依赖性诱导cIAP1多聚泛素化(5 μM时最强)[2] |
| 细胞实验 |
使用 DIMSCAN 进行体外测试。
|
| 动物实验 |
小鼠:使用雄性NCr无胸腺裸鼠(5-7周龄)。每只小鼠背部皮下接种1×10⁶个Huh-7细胞,细胞悬浮于0.1 mL含50% Matrigel的无血清培养基中。当肿瘤生长至200-300 mm³时,小鼠每日一次口服LCL161(50 mg/kg)或SC-2001(10 mg/kg)或两者联合用药。对照组给予载体。每周使用游标卡尺测量肿瘤大小,并使用以下公式计算每个肿瘤的体积:宽度²×长度×0.5²。 LCL161 是一种首创的口服 Smac 模拟物,已证实可在小鼠异种移植模型中诱导 caspase 3 裂解和 cIAP1 降解。
大鼠:LCL161 每周口服一次,疗程 21 天,起始剂量为 10 mg(相当于导致 10% 大鼠出现严重毒性的剂量的十分之一)。在 MDA-MB-231 三阴性乳腺癌异种移植模型中,每周一次和每日两次的 LCL161 给药方案疗效相当。每周一次给药方案耐受性更好,体重减轻更少。 1. 黑色素瘤干细胞异种移植模型:雄性无胸腺裸鼠(6-8 周龄,18-22 g)在实验室(12 小时光照/黑暗循环,22±2°C)适应 7 天。将CD133⁺/ABCG2⁺ MSCs(1×10⁶个细胞溶于0.2 mL PBS/Matrigel 1:1混合液中)皮下注射至小鼠右侧腹部。当肿瘤体积达到100–150 mm³(注射后约14天)时,将小鼠随机分为3组(每组n=6)。LCL161用0.5%甲基纤维素(w/v)去离子水配制,剂量分别为25 mg/kg和50 mg/kg,每日一次灌胃给药,连续28天。对照组灌胃相同体积的0.5%甲基纤维素溶液。每周测量两次肿瘤体积(V = 长×宽²/2)和体重。实验结束时,处死小鼠。切除肿瘤进行免疫组化(cIAP1、cleaved caspase-3)检测[1] 2. HepG2肝细胞癌联合模型:将5×10⁶个HepG2细胞(PBS/Matrigel 1:1)皮下注射到雌性裸鼠体内。当肿瘤体积达到120–160 mm³时,将小鼠分为4组(每组n=6):载体组、LCL161组(50 mg/kg,口服,每日一次)、ABT-263组(10 mg/kg,口服,每日一次)和联合用药组。治疗持续21天。ABT-263溶于0.5%甲基纤维素溶液中。如上所述监测肿瘤体积和体重;在研究结束时,称量肿瘤重量以计算肿瘤生长指数(TGI)[2] |
| 药代性质 (ADME/PK) |
1. 口服生物利用度和人体药代动力学(I期研究):在健康受试者(n=12)中,单次口服LCL161(100–1200 mg)显示出剂量比例药代动力学特征。关键参数:口服生物利用度 (F) = 32%(与静脉微剂量相比计算),Cmax = 8.5 μM (1200 mg),Tmax = 3 小时,末端半衰期 (t₁/₂) = 28 小时。稳态浓度在第 15 天达到(每周一次给药)[3, 4]
2. 血浆蛋白结合:将人血浆 (500 μL) 与LCL161 (0.1–10 μM) 混合,并使用截留分子量为 12–14 kDa 的透析膜在 37°C 下透析 4 小时。采用液相色谱-串联质谱法 (LC-MS/MS) 测定透析液中游离药物浓度。血浆蛋白结合率为 98.2% [3] 3. 代谢和 CYP 相互作用:LCL161 主要在人肝微粒体 (HLM) 中通过 CYP3A4 代谢。体外实验:对 CYP3A4 具有时间依赖性抑制作用 (TDI) (IC₅₀ = 1.8 μM),并能诱导原代人肝细胞中 CYP3A4 mRNA 的表达(10 μM 时增加 2 倍)。在健康受试者中,LCL161 (800 mg) 与咪达唑仑(CYP3A4 探针)联合给药可使咪达唑仑的 AUC 增加 2.3 倍(表明体内 CYP3A4 受到抑制)[3] 4. 小鼠组织分布:小鼠口服 LCL161 (50 mg/kg),并在 3 小时后处死(Tmax)。将组织(肝脏、脾脏、肺、肿瘤、脑)在 PBS 中匀浆;采用 LC-MS/MS 法测定药物浓度。最高浓度:肝脏 (22.5 μM),脾脏 (18.3 μM);肿瘤 (6.8 μM,肿瘤/血浆比值 = 1.2);脑 (0.5 μM,脑/血浆比值 = 0.08) [2] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 临床毒性(I期研究):在45例接受LCL161(每周一次,200-1200 mg)治疗的晚期实体瘤患者中,最常见的治疗相关不良事件(TRAE)为疲乏(47%)、恶心(33%)、腹泻(29%)和呕吐(22%)。剂量限制性毒性(DLT)出现在1200 mg剂量组:3级腹泻(n=2)和3级疲乏(n=1)。未报告4级TRAE或治疗相关死亡[4]
2. 小鼠临床前毒性:接受LCL161(50-100 mg/kg,口服,每日一次,持续28天)治疗的小鼠未出现明显的体重减轻(<5%),且肝脏、肾脏、脾脏或肺脏的组织病理学病变。血清ALT/AST、BUN和肌酐均在正常范围内;全血细胞计数(CBC)显示无骨髓抑制(白细胞、红细胞、血小板计数与对照组相比无变化)[2] 3. 药物相互作用风险:由于LCL161具有CYP3A4抑制/诱导作用,因此存在与CYP3A4底物(例如咪达唑仑、环孢素)相互作用的潜在风险。不建议同时使用强效CYP3A4抑制剂(例如酮康唑)或诱导剂(例如利福平),因为它们可能分别升高或降低LCL161的浓度[3] |
| 参考文献 | |
| 其他信息 |
LCL161 是一种小分子 IAP 抑制剂,对多种实体瘤具有强效的抗肿瘤活性。在肝细胞癌 (HCC) 中,LCL161 治疗的疗效已被证实与 Bcl-2 表达相关。它既是一种抗肿瘤药物,又是一种细胞凋亡诱导剂。LCL161 是一种芳香酮类化合物,属于单氟苯类、N-酰基吡咯烷类、1,3-噻唑类和 L-丙氨酸衍生物。LCL161 已用于多种癌症的治疗临床试验,包括白血病、肿瘤、实体瘤、乳腺癌和卵巢癌等。LCL161 是一种口服生物利用度高的 SMAC 模拟物,也是 IAP(凋亡抑制蛋白)蛋白家族的抑制剂,具有潜在的抗肿瘤活性。 SMAC 模拟物 LCL161 可与 IAP 结合,例如 X 染色体连锁 IAP (XIAP) 和细胞 IAP 1 和 2。由于 IAP 可保护癌细胞免受凋亡过程的影响,因此该药物可能通过激活癌细胞的凋亡信号通路来恢复和促进凋亡的诱导。许多癌细胞类型过度表达 IAP,它们通过结合并抑制活性 caspase-3、-7 和 -9 来抑制凋亡,而 caspase-3、-7 和 -9 在凋亡(程序性细胞死亡)、坏死和炎症中发挥着重要作用。
1. 背景:LCL161 是一种首创的口服双重 cIAP1/XIAP 拮抗剂(Smac 模拟物),用于治疗晚期实体瘤。与静脉注射的Smac模拟物(例如GDC-0152)不同,其口服生物利用度使其能够方便地进行门诊给药,这对于慢性癌症治疗而言是一项关键优势[3, 4] 2. 作用机制:LCL161与cIAP1(高亲和力)和XIAP(中等亲和力)的BIR3结构域结合。它诱导cIAP1的自身泛素化和蛋白酶体降解,释放TRAF2以激活非经典NF-κB通路;它还能将caspase从XIAP上置换下来,解除caspase抑制并激活凋亡信号通路。其双重活性增强了对具有异质性 IAP 表达的肿瘤的疗效[2] 3. 临床开发:LCL161 已完成针对晚期实体瘤患者的 I 期临床试验 (NCT00979123),结果显示其安全性良好且具有初步疗效(27% 的患者病情稳定)[4]。随后,研究人员进一步评估了其与其他抗癌药物(例如 Bcl-2 抑制剂、化疗药物)联合用药以增强疗效,但纳入的文献中未报道 II/III 期临床试验结果[2, 4] 4. 治疗优势:LCL161 可选择性地靶向癌细胞和癌干细胞(例如黑色素瘤干细胞),且对正常细胞无显著毒性。它与 Bcl-2 抑制剂的协同作用可解决内在凋亡抵抗问题,这是实体瘤治疗失败的常见机制 [1, 2]。 5. 局限性:主要局限性包括 CYP3A4 介导的药物相互作用(需要调整剂量或避免使用某些药物)以及 I 期临床试验中单药疗效有限(大多数患者病情稳定,而非客观缓解)。未来的研发重点在于联合用药策略以提高临床获益 [3, 4]。 |
| 分子式 |
C26H33FN4O3S
|
|
|---|---|---|
| 分子量 |
500.63
|
|
| 精确质量 |
500.225
|
|
| 元素分析 |
C, 62.38; H, 6.64; F, 3.79; N, 11.19; O, 9.59; S, 6.40
|
|
| CAS号 |
1005342-46-0
|
|
| 相关CAS号 |
|
|
| PubChem CID |
24737642
|
|
| 外观&性状 |
White to yellow solid powder
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
713.7±60.0 °C at 760 mmHg
|
|
| 闪点 |
385.4±32.9 °C
|
|
| 蒸汽压 |
0.0±2.3 mmHg at 25°C
|
|
| 折射率 |
1.577
|
|
| LogP |
3.78
|
|
| tPSA |
123.13
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
7
|
|
| 可旋转键数目(RBC) |
8
|
|
| 重原子数目 |
35
|
|
| 分子复杂度/Complexity |
757
|
|
| 定义原子立体中心数目 |
3
|
|
| SMILES |
S1C([H])=C(C(C2C([H])=C([H])C(=C([H])C=2[H])F)=O)N=C1[C@]1([H])C([H])([H])C([H])([H])C([H])([H])N1C([C@]([H])(C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H])N([H])C([C@]([H])(C([H])([H])[H])N([H])C([H])([H])[H])=O)=O
|
|
| InChi Key |
UFPFGVNKHCLJJO-SSKFGXFMSA-N
|
|
| InChi Code |
InChI=1S/C26H33FN4O3S/c1-16(28-2)24(33)30-22(17-7-4-3-5-8-17)26(34)31-14-6-9-21(31)25-29-20(15-35-25)23(32)18-10-12-19(27)13-11-18/h10-13,15-17,21-22,28H,3-9,14H2,1-2H3,(H,30,33)/t16-,21-,22-/m0/s1
|
|
| 化学名 |
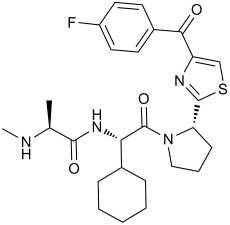
(2S)-N-[(1S)-1-cyclohexyl-2-[(2S)-2-[4-(4-fluorobenzoyl)-1,3-thiazol-2-yl]pyrrolidin-1-yl]-2-oxoethyl]-2-(methylamino)propanamide
|
|
| 别名 |
LCL161; LCL 161; LCL-161
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (4.99 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (4.99 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (4.99 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9975 mL | 9.9874 mL | 19.9748 mL | |
| 5 mM | 0.3995 mL | 1.9975 mL | 3.9950 mL | |
| 10 mM | 0.1997 mL | 0.9987 mL | 1.9975 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT01968915 | Completed | Drug: LCL161 Drug: Paclitaxel |
Neoplasms | Novartis Pharmaceuticals | November 2013 | Phase 1 |
| NCT01617668 | Completed | Drug: LCL161 Drug: Paclitaxel |
Breast Cancer | Novartis Pharmaceuticals | August 2012 | Phase 2 |
| NCT01240655 | Completed | Drug: LCL161 Drug: Paclitaxel |
Solid Tumors | Novartis Pharmaceuticals | April 2011 | Phase 1 |
| NCT01098838 | Completed | Drug: LCL161 | Advanced Solid Tumors | Novartis Pharmaceuticals | April 2011 | Phase 1 |
| NCT03111992 | Completed | Drug: LCL161 Drug: CJM112 |
Multiple Myeloma | Novartis Pharmaceuticals | December 18, 2017 | Phase 1 |
|
|---|
|
 |