| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
GLT-1 (glutamate transporter); EAAT2 (excitatory amino acid transporter 2)
Activator of astroglial glutamate transporter-1 (GLT-1) [1] |
|---|---|
| 体外研究 (In Vitro) |
兴奋性氨基酸转运蛋白2 (EAAT2) 是主要的谷氨酸转运蛋白,其功能是将谷氨酸从突触中清除。研究发现,一种硫代哒嗪衍生物能够提高星形胶质细胞中EAAT2蛋白的水平。结构-活性关系研究表明,该分子的几个组成部分,例如硫醚和哒嗪,对于其活性是必需的。对苄基硫醚进行修饰后,得到了几种衍生物(7-13、7-15和7-17),这些衍生物在浓度低于5 μM的情况下,作用24小时后可使EAAT2水平提高6倍以上。此外,其中一种衍生物(7-22;LDN-212320)在作用24小时后,EC50为0.5 μM时,可使EAAT2水平提高3.5-3.9倍[2]。
|
| 体内研究 (In Vivo) |
腹腔注射LDN-212320(10或20 mg/kg)可显著降低福尔马林诱导的伤害性行为[1]。腹腔注射LDN-212320(10或20 mg/kg)可显著恢复福尔马林损伤的海马依赖性行为。此外,LDN-212320(10或20 mg/kg,腹腔注射)可上调前扣带回皮层(ACC)和海马区域的GLT-1表达[1]。福尔马林诱导的ERK磷酸化(一种伤害感受标志物)在ACC和海马区被LDN-212320(20 mg/kg,腹腔注射)显著降低[1]。
在雄性C57BL/6J小鼠的福尔马林诱导伤害性疼痛模型中,与仅注射福尔马林的小鼠相比,在福尔马林试验前24小时腹腔注射LDN-212320(10或20 mg/kg)可显著减轻福尔马林诱发的舔舐和啃咬行为,且这种减轻呈剂量依赖性。较低剂量5 mg/kg(腹腔注射)则未减轻舔舐和啃咬行为。 [1] - 在福尔马林试验的两个阶段,选择性GLT-1拮抗剂二氢红藻氨酸(DHK,10 mg/kg,腹腔注射)全身给药均能显著逆转LDN-212320(10或20 mg/kg,腹腔注射)的镇痛作用。[1] - 与福尔马林注射组小鼠相比,LDN-212320(20 mg/kg,腹腔注射)显著降低了福尔马林诱导的爪水肿。[1] - 组织学评估显示,福尔马林注射后,LDN-212320(20 mg/kg,腹腔注射)对爪部白细胞浸润无明显影响。 [1] 在Y迷宫测试中,与注射福尔马林的小鼠相比,LDN-212320(20 mg/kg,腹腔注射)显著增加了小鼠在新臂停留的时间和进入新臂的次数,并显著逆转了福尔马林诱导的自发交替行为缺陷。[1] 在物体位置识别测试中,与注射福尔马林的小鼠相比,LDN-212320(10或20 mg/kg,腹腔注射)显著增加了小鼠对被移位物体的偏好。[1] 在高架十字迷宫(EPM)测试中,与注射福尔马林的小鼠相比,LDN-212320(10或20 mg/kg,腹腔注射)显著增加了小鼠进入开放臂的次数,但未显著改变小鼠的运动活性(以进入封闭臂的次数衡量)。 [1] - Western blot 分析显示,与福尔马林注射小鼠相比,LDN-212320(10 或 20 mg/kg,腹腔注射)显著增加了海马和前扣带回皮层 (ACC) 中 GLT-1 的表达。[1] - 免疫荧光染色显示,LDN-212320 不改变海马 CA1 区和齿状回 (DG) 区以及 ACC 中胶质纤维酸性蛋白 (GFAP) 的表达,表明星形胶质细胞数量没有变化。[1] - Western blot 分析表明,LDN-212320(20 mg/kg,腹腔注射)显著逆转了福尔马林诱导的海马和 ACC 中细胞外信号调节激酶 (ERK1/2) 磷酸化水平的升高。 [1] 双重免疫荧光染色显示,LDN-212320 抑制 pERK1/2 表达的作用定位于海马齿状回 (DG)、CA1 区和前扣带回 (ACC) 的神经元(与 NeuN 标记物共定位),而非星形胶质细胞(与 GFAP 标记物共定位)。[1] |
| 酶活实验 |
首先在PA-EAAT2细胞(一种稳定表达EAAT2 mRNA的原代星形胶质细胞系)中评估化合物1的所有衍生物。将化合物(10 μM)孵育4小时和24小时后,收集细胞并通过Western blot分析测定EAAT2蛋白水平。报告EAAT2蛋白水平相对于DMSO对照组的倍数变化。[2]
|
| 细胞实验 |
Western blot分析[1]
Western blot分析按照先前描述的方法进行(Xu et al., 2006),并稍作修改。简而言之,小鼠经快速断头处死;使用小鼠脑立体定位坐标(Franklin and Paxinos, 2008)从1 mm厚的冠状切片中分离出前扣带回皮层(前囟1.18 mm)和海马(前囟-1.7 mm),并保存于-80 °C直至分析。将组织在改良的RIPA缓冲液中匀浆,该缓冲液含有Dulbecco磷酸盐缓冲液(pH 7.4)、1% Igepal CA-630和0.1%十二烷基硫酸钠(SDS)。向RIPA缓冲液中添加蛋白酶抑制剂和磷酸酶抑制剂,并按照制造商的方案使用。样品经离心(16,000 g,4 °C,20 分钟)后收集上清液。采用二喹啉甲酸法测定蛋白质浓度,以白蛋白为标准。取等量蛋白质(60 μg)上样至 10% SDS-PAGE 凝胶进行电泳。分离后的蛋白质在 4 °C 下以 60 V 电压转移至硝酸纤维素膜上过夜。膜用含 5% 脱脂奶粉的 Tris 缓冲盐溶液(TBST)封闭 1 小时。然后,将膜与 GLT-1(1:1000,兔多克隆抗体)、ERK1/2 和 pERK1/2(1:1000,兔多克隆抗体,Cell Signaling Technology,MA,USA)或 β-微管蛋白(E7,1:5000,小鼠单克隆抗体)的一抗在 4°C 下孵育过夜。孵育后,用 TBST 洗涤膜,然后与适当的辣根过氧化物酶标记的二抗(用封闭缓冲液稀释至 1:5000)孵育。用 ECL Prime 试剂检测结合的抗体,并使用密度分析法进行蛋白质定量。[1] 免疫组织化学[1] 免疫组织化学研究按照先前描述的方法进行(Zhang 等,2018),并稍作修改。简而言之,小鼠通过快速断头处死;取出脑组织后,用4%多聚甲醛固定液在室温下固定过夜。然后将脑组织浸入30%蔗糖(溶于0.1 M磷酸盐缓冲液)中,于4℃进行低温保护,直至脑组织沉入液底。之后,将脑组织包埋于Tissue-Tek OCT包埋剂中,并使用Leica CM1850低温恒温切片机切成15 μm厚的切片。每组随机选取3~5张切片,用5%山羊血清(溶于0.3% Triton X-100的1×磷酸盐缓冲液)在室温下封闭1小时,然后在4℃下与pERK1/2(1:500,兔多克隆抗体)或GFAP(1:500,兔多克隆抗体)孵育过夜。对于双重免疫荧光染色,将切片与兔抗p-ERK1/2抗体和鼠单克隆抗神经元特异性核蛋白(NeuN)(神经元标记物,1:200)或鼠单克隆抗胶质纤维酸性蛋白(GFAP)(星形胶质细胞标记物,1:200)的混合物于4℃孵育过夜,随后与AF488或AF647荧光标记的二抗混合物(1:200;ab 150077或ab169348)于室温避光孵育1小时。染色后的切片使用配备DP70数码相机的Olympus AX70荧光显微镜进行观察。免疫荧光定量分析采用ImageJ软件计算积分密度。海马和前扣带回(ACC)的坐标基于Franklin和Paxinos图谱的立体定位图(Franklin和Paxinos,2008);前后(AP)坐标以颅骨囟为参考点,侧向(ML)坐标以正中矢状缝为参考点,腹侧(DV)坐标以颅骨表面为参考点:CA1(AP:-1.70 mm;ML:1.17 mm;DV:1.34 mm),齿状回(DG)(AP:-1.70 mm;ML:0.70 mm;DV:2.04 mm)和前扣带回(ACC)(AP:0.14 mm;ML:0.25 mm;DV:1.00 mm)。 |
| 动物实验 |
动物/疾病模型:小鼠[1]。
剂量:10 或 20 mg/kg。 给药途径:腹腔注射,于注射福尔马林前 24 小时。 实验结果:与注射福尔马林的小鼠相比,在第一阶段和第二阶段,舔舐和啃咬行为均呈剂量依赖性显著减弱。舔舐和啃咬行为显著减少(P < 0.01 或 P < 0.001)。与注射福尔马林的小鼠相比,对被移位物体的偏好显著增加(F3,13 = 28.03,P < 0.01)。与注射福尔马林的小鼠相比,小鼠与移位物体的互动时间显著增加(P < 0.001)。 福尔马林诱导的伤害性疼痛行为[1] 福尔马林诱导的伤害性疼痛模型采用先前描述的方法(Fisher和Coderre,1996;Kim等,1999),并稍作修改。简而言之,将小鼠置于15 × 12 × 10 cm的有机玻璃箱中,每天至少30分钟,连续三天,以适应实验环境。在箱子后方以45°角放置两面镜子,以便清晰地观察小鼠的爪子。在注射福尔马林前24小时,小鼠分别接受(载体,腹腔注射)或(LDN-212320,5、10或20 mg/kg,腹腔注射)处理。对照组动物接受(载体,10 μl,皮下注射 + LDN-212320 20 mg/kg,腹腔注射)。在拮抗剂研究中,于行为学测试前30分钟腹腔注射DHK(10 mg/kg)(Yang等,2011)。随后,使用30号针头Hamilton微量注射器(美国内华达州里诺市)将10 μl 2.5%福尔马林或10 μl载体皮下注射到小鼠后爪背侧。注射后立即将小鼠放回实验箱,开始观察。对于伤害感受反应,通过测量典型双相疼痛行为早期(0-5分钟)和晚期(10-45分钟)两个阶段中舔舐和啃咬注射爪的总持续时间(秒)来监测。 LDN-212320、头孢曲松或DHK的剂量使用方法如前所述(Rasmussen等,2011;Tallarida等,2013)。 LDN-212320溶解于含1%二甲基亚砜(DMSO)和0.5%吐温80的生理盐水(0.9% NaCl)中。 动物:** 使用雄性C57BL/6J小鼠(体重20-30克,5-9周龄)。小鼠以四只为一组饲养于标准实验室条件下(22±2℃,湿度50-60%,12小时光照/黑暗循环),可自由摄取食物和水。 [1] - **药物制备和给药:**LDN-212320溶解于含1%二甲基亚砜(DMSO)和0.5%吐温80的生理盐水(0.9% NaCl)中(溶剂)。所有药物均以10 ml/kg体重的剂量腹腔注射(ip)。[1] - **福尔马林诱导的伤害感受:**小鼠在注射福尔马林前24小时分别接受溶剂或LDN-212320(5、10或20 mg/kg,腹腔注射)处理。在拮抗剂研究中,小鼠在福尔马林试验前30分钟接受DHK(10 mg/kg,腹腔注射)处理。然后,将10 μl 2.5%福尔马林或溶剂皮下注射到小鼠后爪背侧。在早期(0-5分钟)和晚期(10-45分钟)分别测量小鼠舔舐和啃咬注射爪的总持续时间。[1] - **爪水肿测量:**通过足底注射福尔马林(2.5%,10 μl)诱导爪水肿。在注射福尔马林前和注射后60分钟,使用千分尺测量足背-足底厚度。[1] - **Y迷宫测试:**将小鼠置于一个封闭臂(新臂)的Y迷宫中探索15分钟。45分钟后,允许小鼠探索所有三个臂5分钟。记录小鼠进入新臂的次数和停留时间。对于自发交替行为,将小鼠置于所有臂均开放的Y迷宫中5分钟,并计算自发交替行为的百分比。 [1] - **高架十字迷宫 (EPM) 测试:** 将每只小鼠放置在迷宫中心区域,面向开放臂,并录像 5 分钟。分析小鼠进入开放臂和封闭臂的次数。[1] - **物体位置识别测试:** 将小鼠在带有视觉线索的箱中适应 15 分钟。测试当天,将小鼠放入装有三个相同物体的箱中 2 分钟,然后取出。清洁箱后,将其中一个物体移动到新的位置,并将小鼠放回原处。测量小鼠与每个物体互动的时间。[1] - **蛋白质印迹分析:** 将小鼠安乐死,并解剖海马和前扣带回皮层 (ACC)。将组织在含有蛋白酶和磷酸酶抑制剂的 RIPA 缓冲液中匀浆。测定蛋白质浓度后,取等量蛋白质(60 μg)上样至 10% SDS-PAGE 凝胶,转移至硝酸纤维素膜,并用 GLT-1、ERK1/2、pERK1/2 或 β-微管蛋白的一抗进行孵育,随后用 HRP 标记的二抗进行孵育。结合的抗体用 ECL Prime 试剂检测。[1] - **免疫组织化学:** 小鼠安乐死后,取脑组织,用 4% 多聚甲醛进行后固定,用 30% 蔗糖进行低温保护,然后切片(15 μm 厚)。切片封闭后,与一抗(pERK1/2 或 GFAP)孵育过夜。对于双重免疫荧光染色,切片与兔抗 p-ERK1/2 抗体和鼠抗 NeuN 抗体或鼠抗 GFAP 抗体的混合物孵育,随后用荧光标记的二抗进行孵育。染色切片用荧光显微镜观察,并使用 ImageJ 软件进行积分密度定量分析。[1] 动物:使用雄性 C57BL/6J 小鼠(体重 20-30 g,5-9 周龄)。小鼠以四只为一组饲养于标准实验室条件下(22 ± 2°C,湿度 50-60%,12 小时光照/黑暗循环),自由摄取食物和水。[1] - 药物制备和给药:LDN-212320 溶解于含 1% 二甲基亚砜 (DMSO) 和 0.5% Tween 80(溶剂)的生理盐水(0.9% NaCl)中。所有药物均以 10 ml/kg 体重的剂量腹腔注射 (ip)。 [1] - 福尔马林诱导的伤害感受:小鼠在注射福尔马林前24小时分别接受赋形剂或LDN-212320(5、10或20 mg/kg,腹腔注射)处理。在拮抗剂研究中,小鼠在福尔马林试验前30分钟接受DHK(10 mg/kg,腹腔注射)处理。随后,小鼠后爪背侧皮下注射10 μl 2.5%福尔马林或赋形剂。分别在早期(0-5分钟)和晚期(10-45分钟)测量小鼠舔舐和啃咬注射爪的总持续时间。[1] - 爪水肿测量:通过足底注射福尔马林(2.5%,10 μl)诱导爪水肿。在注射福尔马林前和注射后60分钟,使用千分尺测量足背-足底厚度。 [1] - Y迷宫测试:将小鼠置于一个封闭的迷宫臂中探索15分钟(新臂)。45分钟后,允许小鼠探索所有三个臂5分钟。记录小鼠进入新臂的次数和停留时间。对于自发交替行为,将小鼠置于所有臂都开放的Y迷宫中5分钟,并计算自发交替行为的百分比。[1] - 高架十字迷宫(EPM)测试:将每只小鼠置于迷宫中心区域,面向一个开放的臂,并录像5分钟。分析小鼠进入开放臂和封闭臂的次数。[1] - 物体位置识别测试:将小鼠置于带有视觉线索的箱中适应15分钟。测试当天,将小鼠置于装有三个相同物体的箱中2分钟,然后取出。清洁箱后,将其中一个物体移至新位置,并将小鼠放回原处。测量与每个物体互动的时间。[1] - 蛋白质印迹分析:处死小鼠,解剖海马和前扣带回皮层(ACC)。将组织在含有蛋白酶和磷酸酶抑制剂的RIPA缓冲液中匀浆。测定蛋白质浓度,取等量蛋白质(60 μg)上样至10% SDS-PAGE凝胶,转移至硝酸纤维素膜,并用GLT-1、ERK1/2、pERK1/2或β-微管蛋白的一抗进行孵育,随后用HRP标记的二抗进行孵育。用ECL Prime试剂检测结合的抗体。[1] - 免疫组织化学:处死小鼠,将脑组织用4%多聚甲醛固定,在30%蔗糖溶液中进行低温保护,并切片(15 μm厚)。将切片封闭后,与一抗(pERK1/2或GFAP)孵育过夜。对于双重免疫荧光染色,将切片与兔抗p-ERK1/2抗体和鼠抗NeuN抗体或鼠抗GFAP抗体的混合物孵育,随后与荧光标记的二抗孵育。用荧光显微镜观察染色切片,并使用ImageJ软件定量分析积分密度。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
LDN-212320(10 或 20 mg/kg,腹腔注射)并未显著改变高架十字迷宫实验中的运动活性,各组间进入封闭臂的次数无差异。[1]
- LDN-212320 不影响海马 CA1 区和齿状回 (DG) 区以及前扣带回 (ACC) 中星形胶质细胞标志物 GFAP 的表达,表明其不会增加星形胶质细胞的数量。[1] |
| 参考文献 | |
| 其他信息 |
这是首篇报道潜在 GLT-1 激活剂 LDN-212320 在福尔马林诱导疼痛模型中对海马和前扣带回皮层 (ACC) 发挥作用的报告。[1] 研究表明,LDN-212320 通过上调海马和 ACC 中星形胶质细胞 GLT-1 的表达来抑制伤害性疼痛,从而减少谷氨酸溢出和随后的神经元 pERK1/2 信号传导。因此,像 LDN-212320 这样的 GLT-1 激活剂可能成为治疗伤害性疼痛的一种新型疗法。[1]
|
| 分子式 |
C17H15N3S
|
|---|---|
| 分子量 |
293.386101961136
|
| 精确质量 |
293.099
|
| 元素分析 |
C, 61.60; H, 4.68; N, 10.26; O, 15.63; S, 7.83
|
| CAS号 |
894002-50-7
|
| PubChem CID |
7207425
|
| 外观&性状 |
White to gray solid powder
|
| LogP |
4.139
|
| tPSA |
63.97
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
4
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
312
|
| 定义原子立体中心数目 |
0
|
| SMILES |
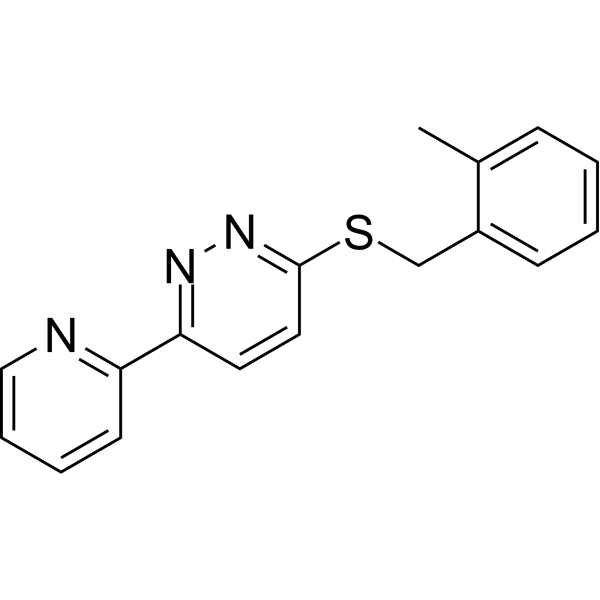
N1C(SCC2C(C)=CC=CC=2)=CC=C(C2C=CC=CN=2)N=1
|
| InChi Key |
DUUQLWDHNYFUPP-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H15N3S/c1-13-6-2-3-7-14(13)12-21-17-10-9-16(19-20-17)15-8-4-5-11-18-15/h2-11H,12H2,1H3
|
| 化学名 |
3-[(2-methylphenyl)methylsulfanyl]-6-pyridin-2-ylpyridazine
|
| 别名 |
LDN-0212320 Maleate
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~170.42 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (8.52 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (8.52 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.4084 mL | 17.0422 mL | 34.0843 mL | |
| 5 mM | 0.6817 mL | 3.4084 mL | 6.8169 mL | |
| 10 mM | 0.3408 mL | 1.7042 mL | 3.4084 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。