| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
PI3Kδ ( IC50 = 11 nM); PI3Kα ( IC50 = 280 nM); PI3Kβ ( IC50 = 480 nM); PI3Kγ ( IC50 = 2.57 μM); DNA-PK ( IC50 = 880 nM)
Leniolisib inhibits phosphorylation of AKT or S6, a pathway activity indicator that is elevated when APDS mutant p110 is expressed in cell lines and patient-derived lymphocytes, in a concentration-dependent manner[1]. |
|---|---|
| 体外研究 (In Vitro) |
Leniolisib 以浓度依赖性方式抑制 AKT 或 S6 的磷酸化,AKT 或 S6 是一种通路活性指标,当 APDS 突变体 p110 在细胞系和患者来源的淋巴细胞中表达时,该磷酸化会升高[1]。
在转染了APDS致病性p110δ突变体(N334K、C416R、E525K、E1021K)的Rat-1成纤维细胞中,leniolisib以浓度依赖性方式降低磷酸化AKT(pAKT)水平,而mTOR抑制剂依维莫司无此作用。[1] 在APDS患者的T细胞母细胞中,leniolisib预处理能剂量依赖性地抑制T细胞受体刺激诱导的AKT和S6磷酸化,且不受特定PIK3CD突变类型影响。[1] |
| 体内研究 (In Vivo) |
口服 leniolisib 可解决免疫失调问题,这也会导致 PI3K/AKT 通路活性呈剂量依赖性下降、循环移行 B 细胞和初始 B 细胞正常化,以及 PD-1+CD4+ 和衰老 CD57+CD8+ T 细胞减少。治疗 12 周后,所有患者的淋巴增殖均有所改善,淋巴结大小和脾脏体积分别减少 39%(平均值,范围,26-57%)和 40%(平均值,范围,13-65%)。 1]。
在一项针对6名APDS患者的12周开放标签、剂量递增临床试验中,口服leniolisib(10、30、70 mg,每日两次)可剂量依赖性地降低B细胞中PI3K/AKT通路活性,使过渡性B细胞和初始B细胞频率恢复正常,减少PD-1⁺CD4⁺和CD57⁺CD4⁻ T细胞,并降低血清IgM及炎症细胞因子/趋化因子水平。[1] 治疗12周后,淋巴结大小平均减少40%,脾脏体积平均减少39%。所有患者的淋巴增殖和血细胞减少症状均得到临床改善。[1] |
| 酶活实验 |
PI3K亚型和其他脂质激酶的生化测定[2]
KinaseGlo Format[2] 使用基于ATP消耗的发光测定法(KinaseGlo),以磷脂酰肌醇(PI)为底物在n-辛基-葡糖苷(OG)中测定激酶对PI3Kα和PI3Kβ的抑制活性。将约50nl的化合物稀释液分配到黑色384孔板(Greiner Cat.7784076)上。将以10mg/ml甲醇溶液形式提供的L-α-磷脂酰肌醇(PI)转移到玻璃管中,并在氮束下干燥。然后通过涡旋将其重悬于3%(v/v)辛基葡糖苷中,并在4°C下储存。加入约4.5μl PI/OG与10nM PI3Kα或0.75μg/ml PI3Kβ的混合物。激酶反应通过加入4.5μl ATP混合物开始,最终体积为9μl,包含以下物质:10mM TRIS HCl pH 7.5、3mM MgCl2或3mM MnCl2、50mM NaCl、0.05%CHAPS、1mM MAKT DTT和1μM ATP。反应在室温(RT)下进行30或60分钟(分别为PI3Kα或PI3Kβ),用9μl激酶Glo停止,10分钟后在Synergy2读取器中使用0.1秒/孔的积分时间读取平板。为了在不添加重组激酶的情况下在激酶缓冲液中产生对激酶反应的100%抑制,使用PI/OG,而在重组激酶存在下通过在水中的溶剂载体(90%v/v)DMSO)给予0%抑制 ADAPTA Format[2] 用于测量PI3Kγ和PI3Kδ活性的激酶测定格式是非放射性的,并监测ADP TR-FRET(ADAPTA)的形成。将约50nl的化合物稀释液分配到白色384孔小体积聚苯乙烯板上。然后,在RT下孵育4.5μl PI3K底物PI和4.5μl ATP(最终测定体积9μl)。Adapta™TR-FRET测定的标准反应缓冲液包含10mM Tris-HCl pH 7.5、3mM MgCl2、50mM NaCl、1mM DTT和0.05%(v/v)CHAPS。在TR-FRET稀释缓冲液中,用4.5μl含有Eu标记的抗ADP抗体和Alexa Fluor®647标记的ADP示踪剂的EDTA混合物停止反应。30到60分钟后,在Synergy2阅读器中读取板(分别为PI3Kγ或PI3Kδ),积分时间为0.4秒,延迟时间为0.05秒。通过用标准反应缓冲液代替PI3K来控制激酶反应的100%抑制。0%抑制的控制通过化合物的溶剂载体(在H2O中的90%DMSO)给出。通过KinaseGlo获得的IC50值和ADAPTA值已被证明是等效的/可比较的 辐射测量 Format[2] 放射性蛋白激酶测定(33PanQinase®活性测定)在来自Perkin Elmer(Boston,MA,USA)的96孔闪板TM中在50μl反应体积中进行。反应混合物按以下顺序分4步移液: •10μl非放射性ATP溶液(在H2O中) •25μl测定缓冲液/[γ-33P]-ATP混合物 •5%二甲基亚砜中的5μl试样 •10μl酶/底物混合物 该测定包含70 mM HEPES NaOH pH 7.5、3 mM MgCl2、3 mM MnCl2、2μM Naorthovanate、1.2 mM DTT、1.0μM ATP、[γ-33P]-ATP(每孔约8 x 1005 cpm)、2.4 nM蛋白激酶和20μg/ml底物(酪蛋白) ProQinase提供的所有蛋白激酶在Sf9昆虫细胞中或在大肠杆菌中以重组GST融合蛋白或His标记蛋白的形式表达,无论是全长还是酶活性片段。所有激酶均由人cDNA产生。激酶通过GSH亲和层析或固定化金属亲和层析纯化。在纯化过程中,从许多激酶中去除了亲和标签。通过SDS-PAGE/考马斯染色检测蛋白激酶的纯度;通过质谱法验证了其身份。将反应混合物在30°C下孵育60分钟。用50μl 2%(v/v)H3PO4停止反应,抽吸板并用200μl 0.9%(w/v)NaCl洗涤两次。用微板闪烁计数器(Microbeta.Wallac)测定33Pi的激酶活性依赖性转移(计数“cpm”)。所有测定均使用BeckmanCoulter Biomek 2000/SL机器人系统进行。对于每种激酶,具有完全反应混合物但没有激酶的三个孔的cpm的中值被定义为“低对照”(n=3)。该值反映了在不存在蛋白激酶但存在底物的情况下放射性与板的非特异性结合。此外,对于每种激酶,具有完全反应混合物但没有任何化合物的其他三个孔的cpm的中值被视为“高对照”,即在没有任何抑制剂的情况下的完全活性(n=3)。高对照和低对照之间的差异被视为每种激酶的100%活性。作为数据评估的一部分,从高控制值以及相应的10个“复合值”中减去特定板的每行的低控制。通过使用以下公式计算特定平板每行每个孔的残余活性(%):Res.activity(%)=100 X[(化合物的cpm-低对照)/(高对照-低控制)]由于针对每种激酶测试了10种不同浓度的每种测试化合物,因此对原始数据的评估得出每种激酶的残余活性的10个值。基于每10个相应的残余活性,使用Prism 5.04 for Windows(Graphpad,San Diego,California,USA;www.Graphpad.com)计算IC50值。使用的数学模型为“Sigmoidal response(variable slope)”,参数“top”固定为100%,“bottom”固定为0%。在基于ATP消耗(KinaseGlo)的n-辛基-葡糖苷(OG)发光测定中,使用PI作为底物,测定了Vps34和PI4Kβ的体外生物化学活性。在抗体依赖性TR-FRET测定中评估了对mTOR的抑制活性,以确定重组mTOR催化的4EBP-1的磷酸化。通过DNA-PK将放射性33P掺入肽底物中来测量对DNA-PK的生物化学活性,并通过液体闪烁计数来测定。 |
| 细胞实验 |
体外B和T细胞活化的细胞测定法[2]
小鼠B细胞活化(CD86表达)和B细胞受体刺激后的增殖。[2] 首先将CDZ173溶解并稀释在DMSO中,然后在培养基中进行1:50稀释。分离Balb/c小鼠的脾细胞,重新悬浮并转移到96孔板(200μl/孔)中。将稀释的化合物或溶剂加入平板(25μl)中,并在37°C下孵育1小时。然后用25μl抗IgM mAb/孔(终浓度30μg/ml)在37°C下刺激培养物24小时,并用抗小鼠CD86-FITC和抗小鼠CD19-PerCP(每孔2μl抗体,均为Becton Dickinson)染色。通过流式细胞术定量CD19阳性B细胞上的CD86表达。基于CD86表达的减少,测定IC50值。为了评估对增殖的影响,在滴定量的化合物存在下,通过抗IgM抗体的B细胞受体刺激小鼠B细胞,并如所述在88小时孵育期的最后16小时内通过掺入放射性3H-胸苷来评估增殖(Julius等1984) 小鼠和人混合淋巴细胞反应(MLR)[2] MLR被认为是体外同种异体T细胞活化的简单模型。对于小鼠MLR,将等量的C57/Bl6和DBA/2小鼠的脾细胞(每个孔4×105个细胞)与在平底组织培养物微量滴定板(Falcon,Becton Dickinson,Basel,Switzerland)中的200ml完全RPMI培养基中的一系列稀释的化合物混合并在37oC的5%CO2中孵育。4天后,将1mCi 3H-胸苷(Amersham,UK)加入每个孔中,并再孵育5小时。随后,用BetaplateTM 96孔采集器在滤纸上采集细胞,并用BetaplateTM计数器测量放射性。根据方程抑制[%]=(高对照-样品)/高对照x100,以百分比计算抑制程度,并确定导致半数最大抑制的浓度(IC50值)。[2] 人类T细胞增殖[2] CDZ173对有或没有CD28共刺激的T细胞受体结合诱导的人类T细胞增殖的影响如简所述进行测量:平底96孔组织培养板在2-8°C下用5μg/ml抗CD3(OKT3)或5μg/ml反CD3(OKT3)和1μg/ml抗CD28(克隆15E8,诺华)抗体溶液包被过夜。如上所述分离人PBMC,并将其置于细胞浓度为2.5x105个细胞/ml的组织培养基中。然后将PBMC与滴定量的CDZ173在37°C、5%CO2下孵育1小时。将抗体溶液从预涂的96孔板上弹开,用200μl/孔PBS洗涤板3次,并去除PBS。然后将细胞悬浮液接种出来(5x104个细胞/孔),并在37°C、5%CO2下孵育56小时。然后用1μCi/孔3H胸苷对细胞进行脉冲处理,在37°C+5%CO2下再孵育16-20小时,并如上所述测量掺入的放射性。 将含APDS相关突变(N334K、C416R、E525K、E1021K)的人PIK3CD cDNA瞬时转染至Rat-1成纤维细胞,用leniolisib或依维莫司处理后,采用均相时间分辨荧光法检测磷酸化AKT(S473)水平。[1] 从APDS患者和健康供者分离的T细胞经抗CD3和抗CD28抗体刺激3天形成T细胞母细胞,再与不同浓度leniolisib孵育,经抗CD3刺激后,通过流式细胞术检测AKT(S473)和S6(S240/244)磷酸化水平。[1] |
| 动物实验 |
大鼠药代动力学/药效学研究[2]
\\n动物[2] \\n药代动力学/药效学实验采用成年雄性Lewis大鼠(LEW/Han/Hsd,德国Charles River公司,体重225-236克)。研究按照瑞士联邦动物保护法进行,并经巴塞尔兽医办公室批准(BS No. 425)。动物饲养于常规卫生条件下(每笼2只,温度20-24℃,相对湿度最低40%,光照/黑暗周期12小时),并自由摄取标准饲料(NAFAG 890 25W16)和饮用水。实验前后,动物均可自由摄取食物和水。 \\n悬浮液载体由0.5% Tween80(Fluka 93781)和0.5%使用羧甲基纤维素水溶液。将溶剂加入化合物中,室温搅拌过夜,制备口服混悬液。所有溶剂和试剂均为分析纯。化合物给药、PK/PD血液采集:CDZ173以4 ml/kg体重的剂量口服给药。采血时,使用Fluvac气流系统以异氟烷麻醉动物。分别于给药前24小时和给药后1、2、4、6、8、10、12和24小时舌下采集全血。药效学分析:每个时间点采集100 μl大鼠血液,置于含30 IU肝素钠(5000 IU/ml)的Eppendorf管中。药代动力学分析:每个时间点采集150 μl大鼠血液,置于EDTA抗凝的Eppendorf管中。猴子[2] \\n\\n动物[2] \\nPK/PD 实验采用 8-9 岁、体重 4.4-6.2 kg 的食蟹猴进行,这些猴子均为圈养繁殖,来自 SICONBREC 公司(n=3,非初次感染:#5517♀、5518♀、5528♂)。它们的血液学、血清/尿液化学检查结果均正常,且结核病、沙门氏菌/志贺氏菌病、病毒感染(B 型疱疹病毒、STLV、SIV、SRV D 型、乙型肝炎病毒)以及体外和体内寄生虫检测结果均为阴性。在研究期间,动物可随时自由摄取食物和水(除在椅子上休息的时间以及给药后两小时的禁食时间外)。每只动物均由 NHP 团队分配的腿部纹身编号或胸部纹身编号进行识别。 NIBR-ATI。在给动物服用测试化合物之前,测量其体重。在7小时的实验过程中,猴子被单独饲养在温度控制在22 ± 2ºC、湿度不低于40%的房间内,笼子均有明显标记。实验结束后,猴子被放回自然光照条件下饲养的群体笼舍。它们的饲料按照诺华标准(灵长类动物颗粒饲料[Kliba Nafag 3446颗粒]、水果和蔬菜)喂养,并且在动物未被束缚时可以自由饮水。动物的处理、护理、药物治疗和血液采样均按照瑞士联邦动物保护法(动物许可证号BS No. 1495)进行。 \\n药物制备和给药[2] \\nCDZ173在给第一只动物给药前一天制备成混悬液,并在给其余两只动物给药前两天制备,然后储存在室温下。将约 225.6 mg CDZ173 溶解于 42.864 ml 0.5% CMC 和 2.256 ml 10% Tween80 的水溶液中。CDZ173 以 10 mg/kg 体重的剂量口服给药。CDZ173 的给药体积为 4 ml/kg 体重。采血时,使用 Fluvac 气流麻醉系统以异氟烷麻醉动物。使用预涂有肝素钠的皮下注射针头的 10 ml 注射器从腹主动脉采集全血。将血液转移至 50 ml Falcon 管中,并将抗凝剂浓度调整至最终浓度为 100 U/ml。 \\n\\n药代动力学研究[2] \\n大鼠体内药代动力学研究[2] \\n雌性野生型 Sprague Dawley 大鼠(Iffa Credo,法国)饲养于符合瑞士动物福利指南的标准笼具和条件下(12 小时光照/黑暗循环,室温 22-24 °C,湿度至少 45% 但 <70%),可自由获取林格氏液(葡萄糖 5%,氯化钠 0.9%,氯化钾 0.5%)和颗粒状啮齿动物饲料。在给予试验物质前96-120小时,用异氟烷麻醉动物,并在严格无菌操作(使用无菌器械和手术材料,并进行局部抗生素预防)下,通过手术将导管植入股动脉和股静脉。导管引出颈部,连接至哈佛旋转系统(Harvard Instruments),并注入含100 U·mL⁻¹肝素的0.9%生理盐水。麻醉苏醒后,将动物单独饲养于特制笼中,并可自由获取食物和自来水,直至实验结束。术后当晚和次日早晨,使用Temgesic®(10 μg/kg,皮下注射,注射体积1 mL/kg)进行镇痛治疗。化合物于早晨(6-8点)给药。在不同时间点,从股动脉导管采集血样至涂有EDTA钠的Eppendorf管中。血液样本立即冷冻于-20℃直至最终处理(最长保存时间为8天)。对同一动物进行静脉和口服给药,两次给药之间间隔48小时的洗脱期。受试物质以1-甲基-2-吡咯烷酮和聚乙二醇200(30:70,v/v)的混合溶液形式静脉注射,剂量为1 mg/kg;以Tween 80和羧甲基纤维素钠(0.5/0.5/99,w/w)的均质水混悬液形式口服,剂量为3 mg/kg。 \\n犬体内药代动力学研究[2] \\n成年雄性比格犬(来自意大利蒙蒂基亚里的马歇尔农场,属于MAP/DMPK永久种群)按照瑞士动物福利指南,在标准条件下饲养于犬舍中(每日喂食一次标准犬粮,研究期间可自由饮用自来水)。给药前禁食12小时,给药后2小时喂食。化合物于上午(7-8点)给药。静脉注射和口服给药均在同一批动物中进行。两次给药之间的洗脱期为一周。受试物质以 1-甲基-2-吡咯烷酮和聚乙二醇 200 (15:85, v/v) 的混合溶液形式静脉注射,剂量为 0.1 mg/kg;以 Tween 80 和羧甲基纤维素钠 (0.5/0.5/99, w/w) 的均质水混悬液形式口服,剂量为 0.3 mg/kg。 \\n食蟹猴体内药代动力学研究[2] \\n两只雄性和一只雌性成年食蟹猴来自 MAP/DMPK 永久种群,饲养于符合瑞士动物福利指南的标准条件下(标准颗粒猴粮,上午加水果,下午加蔬菜,整个研究期间可自由饮用自来水)。在单次给药实验中,直至 7 小时采样时间,动物均单独饲养于实验笼中。实验前后,动物均被群养于大型笼中,仅在需要采集剩余血样时才单独取出。猴子在给药前未禁食,并在给药后2小时喂食。化合物以盒式给药,于早晨使用两种化合物的混合物。静脉注射和口服给药均在同一动物身上进行。两次给药之间的洗脱期为一周。受试物质以1-甲基-2-吡咯烷酮和聚乙二醇200(15:85,v/v)的混合溶液形式静脉注射,剂量为0.1 mg/kg;以吐温80和羧甲基纤维素钠(0.5/0.5/99.5,w/w)的均质水混悬液形式口服,剂量为0.3 mg/kg。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
leniolisib 的全身药物暴露量(AUC 和 Cmax)与剂量成正比。每日两次给药,间隔约 12 小时,leniolisib 达到稳态时,其累积量约为初始值的 1.4 倍(范围为 1.0 至 2.2 倍)。预计约 2 至 3 天后达到稳态药物浓度。Tmax 约为 1 小时。食物对 leniolisib 的全身暴露量影响甚微。 单次口服 70 mg 14C-leniolisib 后 168 小时,14C-leniolisib 总放射性平均回收率为 92.5%。回收剂量中约 67% 和 25.5% 分别存在于粪便和尿液中。尿液中回收的药物剂量中,6.32%为未改变的原药形式,是主要的药物相关物质。 莱尼奥利西布血浆浓度随时间呈双指数衰减,表明其向外周组织的分布存在延迟。莱尼奥利西布在APDS患者中的分布容积估计为28.5 L。 在一项研究中,健康志愿者接受了单次递增剂量至400 mg的莱尼奥利西布,以及多次递增剂量至每日两次,每次140 mg,持续14天。口服药物的血浆清除率(CL/F)为4 L/h。 代谢/代谢物 约60%的莱尼奥利西布在肝脏代谢。莱尼奥利西布主要通过氧化代谢,主要由CYP3A4 (94.5%)介导,CYP3A5 (3.5%)、CYP1A2 (0.7%)和CYP2D6 (0.7%)的参与较少。一项研究对莱尼奥利西布的几种代谢物进行了表征;然而,与母体药物相比,血浆中没有代谢物的浓度较高。其他代谢途径包括脱烷基化、脱甲基化和羟基化。其他可能的排泄途径包括通过BCRP介导的肠道分泌和CYP1A1介导的肝外代谢。 生物半衰期 有效半衰期约为7小时。表观末端消除半衰期约为10小时。 莱尼奥利西布是一种低清除率药物,表观总清除率(CL/F)约为4.2 L/h。 [1] 在每日两次、每次 10–70 mg 的剂量范围内,该药物的药代动力学呈线性关系。[1] 达峰时间 (Tmax) 约为 1 小时,半衰期 (T1/2) 约为 5 小时。[1] 每次增加剂量后 2–3 天达到稳态。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在 leniolisib 上市前针对 APDS 患者的临床试验中,ALT 升高的情况很少见,也没有因肝功能异常而导致肝脏不良事件或停药的报告。未经治疗的 APDS 患者由于细菌、病毒和机会性感染,间歇性肝酶升高并不少见。自 leniolisib 在美国获批以来,尚未有与 leniolisib 治疗相关的临床明显肝损伤病例报告,但该药的临床应用非常有限。 可能性评分:E(不太可能是临床明显肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于 leniolisib 在哺乳期临床应用的信息。由于 leniolisib 与血浆蛋白的结合率为 94.5%,因此其在乳汁中的含量可能很低。制造商建议在接受 leniolisib 治疗期间以及末次给药后 1 周内停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 Leniolisib 与血浆蛋白的结合率为 94.5%。 Leniolisib 在 6 例 APDS 患者中,12 周的耐受性良好。未观察到明显的粒细胞减少症、高甘油三酯血症、高血糖症、胃肠道紊乱、皮疹或肝毒性。[1] 未报告剂量限制性不良反应。[1] 长期使用(扩展研究中超过 9 个月)也未显示明显的不良事件。 [1] 既往报道指出PI3Kδ抑制可能导致基因组不稳定,但本试验并未对此进行评估。[1] |
| 参考文献 |
[2]. Hoegenauer K, et al. Discovery of CDZ173 (Leniolisib), Representing a Structurally Novel Class of PI3K Delta-Selective Inhibitors. ACS Med Chem Lett. 2017 Aug 25;8(9):975-980.
|
| 其他信息 |
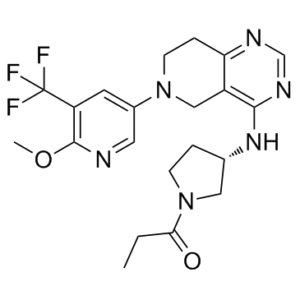
莱尼奥利西布是一种吡啶并嘧啶类化合物,其结构为5,6,7,8-四氢吡啶并[4,3-d]嘧啶,在4位和6位分别被[(3S)-1-丙酰基吡咯烷-3-基]氨基和6-甲氧基-5-(三氟甲基)吡啶-3-基取代。它是一种EC 2.7.1.153(磷脂酰肌醇-4,5-二磷酸3-激酶)抑制剂和免疫调节剂。它是一种芳香醚、吡啶类化合物、有机氟化合物、吡啶并嘧啶类化合物、仲氨基化合物、吡咯烷类化合物和叔酰胺类化合物。
莱尼奥利西布是一种强效且选择性的磷脂酰肌醇3-激酶δ (PI3Kδ) 抑制剂。美国食品药品监督管理局 (FDA) 于 2023 年 3 月 24 日批准了 leniolisib 上市,使其成为首个用于治疗活化磷脂酰肌醇 3-激酶 δ 综合征 (APDS) 的药物。APDS 是一种原发性免疫缺陷病,由编码 PI3Kδ 的基因突变引起,导致 PI3Kδ 活性增强,进而引起免疫功能障碍,并增加感染易感性。Leniolisib 的作用机制是抑制过度活跃的 PI3Kδ。目前正在进行 leniolisib 用于治疗原发性干燥综合征的研究。 Leniolisib 是一种激酶抑制剂。 leniolisib 的作用机制是作为磷脂酰肌醇 3-激酶δ抑制剂、细胞色素 P450 1A2 抑制剂、乳腺癌耐药蛋白抑制剂、有机阴离子转运多肽 1B1 抑制剂和有机阴离子转运多肽 1B3 抑制剂。 Leniolisib 是一种口服激酶抑制剂,用于治疗 12 岁及以上患有活化磷脂酰肌醇-3-激酶δ综合征 (APDS) 的成人和儿童。APDS 是一种极其罕见的遗传性免疫缺陷疾病。莱尼奥利布的临床应用非常有限,但尚未有报道显示其会导致肝酶升高,也未发现与临床上明显的肝损伤事件相关。 另见:莱尼奥利布磷酸盐(活性成分)。 药物适应症 莱尼奥利布适用于治疗12岁及以上成人和儿童患者的活化磷脂酰肌醇3-激酶δ (PI3Kδ) 综合征 (APDS)。 活化磷脂酰肌醇3-激酶δ综合征 (APDS) 的治疗 作用机制 磷脂酰肌醇3-激酶δ (PI3Kδ) 是一种脂质激酶,在免疫细胞中由酪氨酸激酶受体和G蛋白偶联受体下游激活。它介导PI3K/AKT通路,该通路参与细胞增殖、生长和存活。 PI3Kδ是由一个调节亚基(p85α)和一个催化亚基(p110δ)组成的异二聚体,主要表达于造血细胞,例如淋巴细胞和髓系细胞。它能将磷脂酰肌醇-4,5-二磷酸(PIP2)转化为磷脂酰肌醇-3,4,5-三磷酸(PIP3),后者是一种信号分子,可激活下游蛋白,例如AKT激酶,进而激活哺乳动物雷帕霉素靶蛋白(mTOR)复合物I并抑制FOXO家族转录因子。APDS与编码p110δ基因的功能获得性变异或编码p85α基因的功能丧失性变异相关,这两种变异均会导致PI3Kδ过度激活、T细胞功能下降、淋巴结肿大和免疫缺陷。Leniolisib通过阻断p110δ亚基上的活性结合位点来抑制PI3Kδ。在无细胞分离酶活性测定中,Leniolisib 对 PI3K-δ 的选择性高于 PI3K-α(28 倍)、PI3K-β(43 倍)和 PI3K-γ(257 倍),也高于更广泛的激酶组。在基于细胞的测定中,Leniolisib 降低了 pAKT 通路活性,并抑制了 B 细胞和 T 细胞亚群的增殖和活化。Leniolisib 抑制导致 PIP3 生成增加、下游 mTOR/AKT 通路过度激活以及 B 细胞和 T 细胞功能失调的信号通路。 药效学 Leniolisib 通过阻断免疫细胞(如 B 细胞、T 细胞、中性粒细胞、单核细胞、嗜碱性粒细胞、浆细胞样树突状细胞和肥大细胞)的异常 PI3Kδ 依赖性信号通路发挥作用。体外实验表明,在过表达p110δ突变体的细胞系和APDS患者的原代免疫细胞中,leniolisib呈剂量依赖性地抑制PI3Kδ通路过度激活。在APDS患者中,分别以10、30和70 mg每日两次给药,持续四周,对leniolisib在磷酸化Akt (pAkt)阳性B细胞比例中的离体药效学进行了评估。在所研究的剂量范围内,较高的leniolisib血浆浓度通常与pAkt阳性B细胞的更显著降低相关。较高剂量与略高的峰值和更持久的降低相关。每日两次,每次 70 mg 的 leniolisib 治疗达到稳定状态,预计可使 pAkt 阳性 B 细胞的平均减少量约为 80%。 Leniolisib (CDZ173) 是一种选择性口服 PI3Kδ 抑制剂,用于治疗活化 PI3Kδ 综合征 (APDS)。APDS 是一种由 PIK3CD 功能获得性突变引起的原发性免疫缺陷病。[1] 它可抑制过度活跃的 PI3Kδ 信号通路,从而减少淋巴细胞增殖,使免疫细胞亚群恢复正常,并降低炎症标志物水平。[1] 建议的最佳治疗剂量为每日两次,每次 70 mg。[1] 在本文发表时,一项随机、安慰剂对照试验正在进行中 (NCT02435173)。[1] |
| 分子式 |
C21H25F3N6O2
|
|
|---|---|---|
| 分子量 |
450.47
|
|
| 精确质量 |
450.199
|
|
| 元素分析 |
C, 55.99; H, 5.59; F, 12.65; N, 18.66; O, 7.10
|
|
| CAS号 |
1354690-24-6
|
|
| 相关CAS号 |
Leniolisib phosphate;1354691-97-6
|
|
| PubChem CID |
57495353
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
2.96
|
|
| tPSA |
83.48
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
5
|
|
| 重原子数目 |
32
|
|
| 分子复杂度/Complexity |
654
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
FC(C1=C(N=C([H])C(=C1[H])N1C([H])([H])C([H])([H])C2=C(C1([H])[H])C(=NC([H])=N2)N([H])[C@]1([H])C([H])([H])N(C(C([H])([H])C([H])([H])[H])=O)C([H])([H])C1([H])[H])OC([H])([H])[H])(F)F
|
|
| InChi Key |
MWKYMZXCGYXLPL-ZDUSSCGKSA-N
|
|
| InChi Code |
InChI=1S/C21H25F3N6O2/c1-3-18(31)30-6-4-13(10-30)28-19-15-11-29(7-5-17(15)26-12-27-19)14-8-16(21(22,23)24)20(32-2)25-9-14/h8-9,12-13H,3-7,10-11H2,1-2H3,(H,26,27,28)/t13-/m0/s1
|
|
| 化学名 |
(S)-1-(3-((6-(6-methoxy-5-(trifluoromethyl)pyridin-3-yl)-5,6,7,8-tetrahydropyrido[4,3-d]pyrimidin-4-yl)amino)pyrrolidin-1-yl)propan-1-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.55 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.55 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.55 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2199 mL | 11.0995 mL | 22.1990 mL | |
| 5 mM | 0.4440 mL | 2.2199 mL | 4.4398 mL | |
| 10 mM | 0.2220 mL | 1.1100 mL | 2.2199 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05693129 | Not yet recruiting | Drug: Leniolisib | APDS | Pharming Technologies B.V. | August 30, 2023 | Phase 3 |
| NCT05438407 | Rrecruiting | Drug: Leniolisib | APDS | Pharming Technologies B.V. | February 1, 2023 | Phase 3 |
Effective “activated PI3Kδ syndrome”–targeted therapy with the PI3Kδ inhibitor leniolisib.Blood.2017 Nov 23;130(21):2307-2316. |
|---|
PIK3CDmutant transfectants treated with leniolisib or an mTOR inhibitor.Blood.2017 Nov 23;130(21):2307-2316. |
T-cell blast activation in presence or absence of leniolisib.Blood.2017 Nov 23;130(21):2307-2316. |