| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
HIV Reverse transcription (IC50 = 119 nM); NNRTI
Non-nucleoside HIV reverse transcriptase inhibitor (NNRTI) (HIV-1 wild-type reverse transcriptase (RT) IC50 = 0.119 μM) [1] |
|---|---|
| 体外研究 (In Vitro) |
与针对分离 RT 酶的有希望的结果一致,lerivirine 对多种耐药性和野生型 HIV 病毒株显示出出色的功效 [1]。
Lersivirine是第二代NNRTI,正在进行临床开发,用于治疗HIV-1。Lersivirine在结构上与依法韦仑不同,并以一种新的方式结合RT酶[2]。 Lersivirine (UK-453061) 对HIV-1逆转录酶(RT)显示出强效抑制活性,IC50为0.119 μM。[1] Lersivirine (UK-453061) 在细胞培养中对SupT1细胞中感染的HIV-1 RF毒株表现出强效抗病毒活性,IC50(AVE50)为4.9 nM。[1] Lersivirine (UK-453061) 对一系列突变RT酶显示出良好的耐药谱,与野生型RT相比,对几个关键突变如K103N(1.6倍)、Y181C(2.7倍)和F227L(5.0倍)的耐药倍数变化相对较低。[1] Lersivirine (UK-453061) 在SupT1细胞中的细胞毒性浓度(CC50)>30 μM,表明其体外治疗指数较高。[1] |
| 体内研究 (In Vivo) |
Lersivirine 会导致交配的 Crl:CD1(ICR) 小鼠骨骼变异,这与发育迟缓和胎儿骨化减少有关。 Lersivirine(口服管饲;0、150、350 和 500 mg/kg;每天一次;妊娠第 6 至 17 天,随后在妊娠第 18 天进行剖腹产)在前 2 天以 250 mg 诱导肝代谢酶/ kg,然后将剂量增加至 500 mg/kg/天。
产妇和剖宫产观察[2] 治疗对产妇存活、流产或早产没有影响;21、19、18和22只雌性分别以0、150、350和500mg/kg/天的剂量产仔(表1)。Lersivirine/勒西韦林治疗不影响体重和体重增加;在150、350和500mg/kg/天的剂量下,GD 18的体重分别为对照组的100%、99%和102%(表2)。饲料消耗量在350和500mg/kg/天时减少(表2)。在350和500 mg/kg/天的剂量下,整个给药期(GD 6-18)的饲料消耗量明显低于同期对照组的值(p<0.05或p<0.01)(分别为对照组的92%和90%)。 胎儿形态学[2] 母体接受Lersivirine/雷西韦林治疗后,未出现任何外部、内脏或骨骼畸形(表4)。在350mg/kg/天和500mg/kg/天的三个胎儿(1.3%/窝)的外部检查中观察到腭裂内侧裂;然而,鉴于该实验室的背景发病率为每窝3.2%,因此认为该发病率与雷西韦林无关。在0、150、350和500mg/kg/天的剂量下,分别有5只(2.1%/窝)、4只(1.6%/窝),5只(2.1%/窝)和2只(0.7%/窝)出现前肢和/或后肢旋转;然而,鉴于发病率没有剂量反应性增加,这一发现不能归因于雷西韦林。500 mg/kg/天组中发生的唯一骨骼畸形是两个(1.4%/窝)胎儿的腰椎弓融合,鉴于缺乏其他骨骼畸形发生的证据,单窝两个胎儿的这种情况不是由雷西韦林引起的。 |
| 酶活实验 |
逆转录酶(RT)抑制实验测定了化合物对野生型和突变型HIV-1 RT酶的IC50值。实验细节已另行报道。[1]
体外多非利特结合实验用于评估潜在的hERG通道抑制作用,作为离子通道选择性和脱靶药理学指标。[1] |
| 细胞实验 |
抗病毒活性(IC50, AVE50)在细胞培养中使用感染了HIV-1 RF毒株的SupT1细胞进行测定。实验细节已另行报道。[1]
细胞毒性(CC50)在SupT1细胞中进行评估,以确定化合物的潜在毒性作用。[1] |
| 动物实验 |
动物和处理[2]
一百只疑似怀孕的雌性Crl:CD1(ICR)小鼠被随机分为四组,每组25只。另有63只疑似怀孕的小鼠用于毒代动力学样本采集;对照组每组9只,勒西韦林剂量组每组18只。小鼠到达时年龄约为72天,体重约为28克。小鼠单独饲养于不锈钢底笼中。实验动物自由摄取水和饲料,房间采用12小时光照/12小时黑暗循环。 将lersivirine悬浮于含0.1% Tween 80的0.5%甲基纤维素水溶液中,于妊娠第6至17天(妊娠第6-17天)每日一次灌胃给药,剂量分别为0、150、350和500 mg/kg/天,给药体积为10 ml/kg。在最高测试剂量(500 mg/kg/天)下,前两天以250 mg/kg/天的剂量(给药体积为5 ml/kg)给药,之后以500 mg/kg/天的剂量给药。该给药方案可在代谢酶诱导后维持最大耐受暴露量;先前研究表明,勒西韦林可诱导啮齿动物代谢(Walker等,2009)。剂量方案基于一项初步研究,该研究中,妊娠小鼠(每组10只)在妊娠第6天至第17天分别接受150、350和700 mg/kg/天的剂量给药(700 mg/kg/天组在前两天接受350 mg/kg/天的剂量)。在该研究中,700 mg/kg/天组的10只小鼠中有4只因濒死而被实施安乐死;其余所有动物均存活至预定的安乐死时间。因此,估计妊娠小鼠的最大耐受剂量为 500 mg/kg/天(前两天剂量为 250 mg/kg/天)。 勒西韦林暴露量评估[2] 在妊娠第 17 天,处死每组每时间点的三只小鼠后,从其下腔静脉采集血样(约 0.5 ml)。对于勒西韦林治疗组小鼠,分别在给药前以及给药后约 0.5、2、4、8 和 24 小时采集血样。将血样转移至肝素锂涂层试管中,通过离心分离血浆,并在 -20°C 下冷冻保存直至分析。采用经验证的高效液相色谱法 (HPLC) 测定血浆中勒西韦林的浓度。 进行了大鼠药代动力学研究。利西韦林(UK-453061)以2 mg/kg的剂量进行静脉注射(iv)。定期采集血样以测定药代动力学参数。[1] |
| 药代性质 (ADME/PK) |
母体毒代动力学[2]
表6列出了妊娠第6天至第17天给予勒西韦林后,妊娠第17天的勒西韦林血浆浓度。三个剂量组的母体血浆勒西韦林暴露量相似。 在人肝微粒体(HLM)中,勒西韦林(UK-453061)的半衰期(T1/2)大于30分钟。[1] 在人肝细胞实验中,预计游离清除率(CLb)为7 mL/min/kg。 [1] 在以2 mg/kg静脉注射剂量进行的鼠药代动力学研究中,Lersivirine (UK-453061)的清除率(CL)为25.9 mL/min/kg,分布容积(Vd)为1.6 L/kg,半衰期(T1/2)为1.6小时。与之前的先导化合物3相比,这有所改进,后者具有更高的清除率(>100 mL/min/kg)和更短的半衰期(0.1小时)。[1] Lersivirine (UK-453061)具有良好的水溶性和制剂特性。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
勒西韦林是一种第二代非核苷类逆转录酶抑制剂,目前正处于治疗HIV-1的临床开发阶段。本研究开展了一项胚胎-胎儿发育毒性研究,旨在评估勒西韦林对妊娠小鼠的母体和发育毒性。将交配后的Crl:CD1(ICR)小鼠在妊娠第6至17天通过灌胃法每日一次给予0、150、350和500 mg/kg的勒西韦林,并在妊娠第18天进行剖腹产。高剂量组前两天的给药剂量为250 mg/kg,以诱导肝脏代谢酶的表达,之后剂量增加至500 mg/kg/天。这种给药方案能够维持高剂量组的药物暴露量,即使勒西韦林治疗后啮齿动物体内会发生显著的自身诱导。勒西韦林不会导致外部、内脏或骨骼畸形增加。在350和500 mg/kg/天的剂量下,观察到宫内生长迟缓,表现为胎儿体重减轻和与骨骼骨化延迟相关的变异增加。这些研究结果表明,勒西韦林对小鼠无致畸性。[2]
勒西韦林(UK-453061)在SupT1细胞中表现出>30 μM的细胞毒性浓度(CC50)。[1] 在多非替利结合试验中,勒西韦林(UK-453061)的IC50为6%置换率,表明在测试浓度下其对hERG通道的抑制潜力较低。 [1] 利西韦林 (UK-453061) 的微粒体游离分数为 80%,表明在微粒体稳定性测定中,有相当一部分游离药物可用于代谢。[1] |
| 参考文献 | |
| 其他信息 |
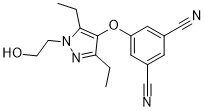
勒西韦林是一种芳香醚。
勒西韦林已用于HIV-1治疗的临床试验。 勒西韦林是一种新一代吡唑类非核苷类逆转录酶抑制剂。勒西韦林对Y181位点发生突变的HIV病毒仍具有活性,而Y181位点突变会导致病毒对依非韦伦、依曲韦林和奈韦拉平产生耐药性。 本研究结果表明,勒西韦林对小鼠无致畸性。此外,勒西韦林对兔也无致畸性(Campion等,同期)。勒西韦林的研究结果,结合其他第一代非核苷类逆转录酶抑制剂(NNRTI)如地拉韦啶和奈韦拉平未见明显的致畸信号(Watts等,2004),支持以下结论:依非韦伦的致畸信号(Lewis-Hall,2005;Mofenson,2005)如果真实存在,则仅限于该化合物,并不代表NNRTI类药物的普遍效应。虽然勒西韦林治疗未导致胎儿畸形,但在接受350和500 mg/kg/天勒西韦林治疗的母亲所生的胎儿中观察到了发育毒性。发育毒性的主要表现是宫内生长迟缓,具体表现为胎儿体重减轻、骨骼变异增加和骨化部位减少。增加的骨骼变异主要与骨化延迟和肋骨发育不全有关。骨骼变异是指在实验物种和品系中常见的、代表可逆性发育延迟或加速的骨骼变化。这与胎儿畸形不同,胎儿畸形是指在该物种和品系中发生率较低的不可逆性改变。宫内生长迟缓的主要指标是胎儿体重。在350和500 mg/kg/天的剂量下,胎儿体重分别比对照组低16%和21%;而在150 mg/kg/天的剂量下,胎儿体重没有变化。除了胎儿体重降低外,在350和500 mg/kg/天的剂量下,母体接受勒西韦林治疗所导致的、提示发育迟缓的骨骼变异还包括:枕上骨、鼻骨、额骨、颈弓、耻骨或坐骨骨化不全,以及枕上骨缺失。此外,在350和500 mg/kg/天剂量组中,舌骨、尾椎、胸骨中心、前肢指骨、后肢跗骨和后肢指骨的骨化程度均有所降低。众所周知,骨化延迟与小鼠胎儿体重下降相关(Deol和Truslove,1957;McLaren和Michie,1958),而胎儿体重下降被认为与结构畸形相关的发病机制无关(Grüneberg,1955)。除宫内生长迟缓外,在500 mg/kg/天剂量组中还发现了两例死胎。未发现其他胎儿存活率受损的证据,各组存活胎儿的数量相当,且勒西韦林治疗与吸收胎儿数量的增加无关。然而,由于死胎发生率历来较低,因此不能排除其与治疗的潜在关联。从妊娠第6天开始每日重复给药,在妊娠第17天,母体血浆中勒西韦林的暴露量在剂量从150 mg/kg/天增加到500 mg/kg/天(约三倍)的过程中基本保持稳定。勒西韦林的特点是清除率和分布容积适中,因此具有良好的口服生物利用度,且全部清除均在肝脏进行(Allan等,2008)。然而,在啮齿动物中,勒西韦林给药会导致肝酶诱导,这种自身诱导会限制稳态下可达到的全身暴露量(Walker等,2009)。自身诱导的程度导致小鼠给药后第1天至第12天之间,0-24小时曲线下面积(AUC)下降8至10倍(Walker等,2009)。因此,虽然第17天(GD 17)各剂量组的暴露量基本持平,但相同剂量范围内第1天的暴露量显示Cmax和AUC(0–24 hr)分别增加了约5倍和10倍(来自一项为期1个月的毒理学研究的未发表数据)。因此,尽管本研究未测量,但在早期器官形成期,该剂量范围内的勒西韦林暴露量可能呈剂量比例增加,而这种增加并未体现在第17天的测量结果中,并且不同剂量水平之间的暴露量差异可能具有毒理学意义。总之,本研究结果表明,勒西韦林治疗不会导致小鼠胎儿畸形。母体暴露于勒西韦林的主要影响是宫内生长迟缓,表现为胎儿体重减轻和与骨化延迟相关的骨骼变异。[2] 我们基于近期报道的3-氰基苯氧基吡唑先导化合物3,制备了三组独立的强效非核苷类HIV逆转录酶抑制剂(NNRTI)。其中几种化合物在体外表现出非常有前景的抗HIV活性、安全性、药代动力学和药理学特性。我们描述了我们选择醇类化合物5(UK-453,061,勒西韦林)进行临床开发的分析和结论。[1] 勒西韦林(UK-453061)是基于其令人信服的体外整体特性而被从一系列吡唑类NNRTI中选为临床开发候选药物的,这些特性包括强效的抗HIV活性、良好的耐药性、良好的代谢稳定性和改善的药代动力学特性。 [1] 该药物旨在对具有临床意义的耐药突变的HIV毒株具有广谱活性,减少服药负担,最大限度地降低副作用和药物相互作用的风险,并提高与现有非核苷类逆转录酶抑制剂(NNRTI)相比的耐受性。[1] 已启动临床试验以评估其治疗HIV感染的潜力。[1] |
| 分子式 |
C17H18N4O2
|
|---|---|
| 分子量 |
310.3504
|
| 精确质量 |
310.142
|
| 元素分析 |
C, 65.79; H, 5.85; N, 18.05; O, 10.31
|
| CAS号 |
473921-12-9
|
| 相关CAS号 |
147362-57-0 (Loviride); 16837-52-8 (Oxymatrine)
|
| PubChem CID |
16739244
|
| 外观&性状 |
Light yellow to khaki solid powder
|
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
455.4±45.0 °C at 760 mmHg
|
| 闪点 |
229.2±28.7 °C
|
| 蒸汽压 |
0.0±1.2 mmHg at 25°C
|
| 折射率 |
1.595
|
| LogP |
3.3
|
| tPSA |
94.86
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
23
|
| 分子复杂度/Complexity |
456
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
MCPUZZJBAHRIPO-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H18N4O2/c1-3-15-17(16(4-2)21(20-15)5-6-22)23-14-8-12(10-18)7-13(9-14)11-19/h7-9,22H,3-6H2,1-2H3
|
| 化学名 |
5-((3,5-diethyl-1-(2-hydroxyethyl)-1H-pyrazol-4-yl)oxy)isophthalonitrile
|
| 别名 |
UK 453061; UK-453061; UK-453,061; UK453,061; Lersivirine; 473921-12-9; 3-CYANO-5-[[3,5-DIETHYL-1-(2-HYDROXYETHYL)-1H-PYRAZOL-4-YL]OXY]BENZONITRILE; UK-453,061; 5-((3,5-diethyl-1-(2-hydroxyethyl)-1H-pyrazol-4-yl)oxy)isophthalonitrile; 5-[3,5-diethyl-1-(2-hydroxyethyl)pyrazol-4-yl]oxybenzene-1,3-dicarbonitrile; R3ZGC15A9A; UK453061; UK 453,061
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~50 mg/mL (~161.11 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 3 mg/mL (9.67 mM) (饱和度未知) in 10% DMSO + 40% PEG300 +5% Tween-80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 30.0 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80 +,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.2222 mL | 16.1108 mL | 32.2217 mL | |
| 5 mM | 0.6444 mL | 3.2222 mL | 6.4443 mL | |
| 10 mM | 0.3222 mL | 1.6111 mL | 3.2222 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。