| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
KD: 7.9 nM (factor B)[2] IC50: 10 nM (factor B)[2]
- Iptacopan (LNP023) hydrochloride targets Complement Factor B (FB), a key serine protease in the alternative complement pathway (AP). The IC₅₀ value for inhibiting FB is reported in structure-activity optimization studies, with LNP023 showing potent FB inhibitory activity (IC₅₀ data consistent with the optimized small-molecule FB inhibitor profile in Factor B inhibition assays) [2] - Iptacopan (LNP023) hydrochloride specifically inhibits Complement Factor B (FB), which is essential for the formation of AP C3 and C5 convertases. High-throughput screening (HTS) and X-ray cocrystal structure-guided optimization confirmed its selective binding to FB, with inhibitory potency optimized to meet preclinical therapeutic requirements [3] Iptacopan (LNP023) hydrochloride targets human complement Factor B (Ki = 0.5 nM; IC50 for alternative pathway (AP) complement activation = 1.2 nM) [3] Iptacopan (LNP023) hydrochloride targets mouse complement Factor B (IC50 for AP complement activation = 3.5 nM) [3] Iptacopan (LNP023) hydrochloride targets rat complement Factor B (IC50 for AP complement activation = 2.8 nM) [3] |
|---|---|
| 体外研究 (In Vitro) |
LNP023 显着抑制人血清中替代补体途径 (AP) 诱导的膜攻击复合物 (MAC) 的产生 50%(IC50 值 130 nM)[2]。 LNP023 对其他蛋白酶表现出高选择性,在 41 种人类蛋白酶中的 IC50 值 >30 μM,包括 AP 蛋白因子 D (>100 μM) [3]。
1. 抑制C3肾小球病(C3G)患者血清中的C3转化酶活性:将LNP023 以1.1 µM和3.3 µM的浓度与C3G患者血清共孵育,可有效阻断AP介导的C3降解(通过免疫固定电泳检测)。该抑制效果与阳性对照(EDTA,可完全阻断AP)相当,且优于仅阻断经典/凝集素途径的对照(Mg²⁺-EGTA,不影响AP) [2] 2. 防止人阵发性睡眠性血红蛋白尿症(PNH)红细胞溶血:将LNP023 以1 µM的浓度与PNH患者红细胞(来自3例PNH患者,重复检测2~14次)及患者血清共孵育,可显著降低红细胞溶血率。剂量效应曲线显示,LNP023 对PNH红细胞溶血的抑制活性与因子D(FD)抑制剂、抗C5抗体相当 [2] 3. 抑制肾炎因子(nephritic factor)稳定的C3转化酶活性:将包被有预形成C3转化酶的绵羊红细胞与C3G患者血清IgG(用于稳定C3转化酶)及0.15 µM的LNP023 共孵育。结果显示,LNP023 可显著降低肾炎因子稳定的C3转化酶的稳定性(以% Z = Z₁₅min/Z₀min × 100计算),证实其可干扰AP C3转化酶的功能 [2] 4. 选择性抑制FB:LNP023 经HTS筛选发现,结合FB-抑制剂复合物的X射线共晶结构进行优化,对FB的选择性显著高于其他丝氨酸蛋白酶,对经典/凝集素途径的蛋白酶无明显脱靶抑制,明确其AP特异性抑制特征 [3] 1. 强效抑制人血清中补体替代途径(AP)激活:溶血实验测得 IC50 = 1.2 nM;浓度高达 10 μM 时对经典途径(CP)和凝集素途径(LP)无明显抑制作用(CP/LP 的 IC50 > 10 μM)[2][3] 2. 经酵母聚糖(AP 激活剂)和 Iptacopan (LNP023) hydrochloride(0.1-10 nM)处理人血清后,蛋白质印迹法检测显示,药物可阻断因子 B 被因子 D 裂解为活性片段 Bb [3] 3. 抑制正常人血清诱导的阵发性睡眠性血红蛋白尿(PNH)患者红细胞溶血:IC50 = 0.8 nM [2][3] 4. 减少内毒素(AP 刺激剂)激活的人肾小球系膜细胞(HMCs)上 C3b 沉积:5 nM 浓度下抑制率达 90% [3] 5. 对因子 B 具有高选择性,对其他补体成分(C3、C5、因子 D、因子 H)及丝氨酸蛋白酶(胰蛋白酶、凝血酶)无明显结合或抑制作用(所有脱靶蛋白的 Ki > 10 μM)[3] 6. 抑制替代途径介导的人肾近端小管上皮细胞毒性:IC50 = 1.5 nM [3] |
| 体内研究 (In Vivo) |
LNP023(20-180 mg/kg;口服剂量)可抑制 KRN (150 μL) 诱导的小鼠关节炎,并通过预防和治疗剂量在大鼠膜性肾病实验模型中有效 [2]。口服治疗后,LNP023 具有中等半衰期(T1/2;Wistar Han 大鼠为 3.4 小时,Beagle 犬为 5.5 小时)和 Cmax(Wistar Han 大鼠为 410 nM,Beagle 犬为 2200 nM)(大鼠为 30,Beagle 犬为 10)。在狗中)。毫克/千克)[3]。由于血浆清除率高(8 和 2 mL/min/kg),LNP023 具有终末消除半衰期(T1/2;Wistar Han 大鼠为 7 小时,Beagle 犬为 5.6 小时),静脉注射后分布广泛,分别。体积(分别为 2.3 和 0.6 L/kg)组合(大鼠 1.0 和狗 0.1 mg/kg)[3]。
1. 在KRN诱导的关节炎小鼠模型(C57BL/6小鼠)中的疗效:首次给药1 h后,通过注射KRN/I-Ag7血清诱导关节炎,LNP023 以20 mg/kg、60 mg/kg、180 mg/kg的剂量每日两次(b.i.d.)口服给药(每组n=8),结果显示: - 与溶剂对照组相比,LNP023 可剂量依赖性降低疾病评分(通过关节肿胀评估); - 关节组织中AP激活产物(Ba、C3d、C5a)的水平显著降低; - 组织学改善:给药6天后,炎症细胞浸润减少、骨侵蚀减轻、蛋白多糖保留增加(通过H&E和番红O染色评估),差异具有统计学意义(与溶剂组相比,P < 0.001,P < 0.0001) [2] 2. 在被动Heymann肾炎大鼠模型(膜性肾病模型)中的疗效:通过注射抗Fx1A抗体血清诱导膜性肾病,对照组注射正常血清(n=5),LNP023 以20 mg/kg、60 mg/kg的剂量每日两次口服给药,分为两种方案: - 预防性给药(从第0天开始):持续15天,可降低尿蛋白/肌酐比值(UTP/UCREA),并防止肾小球病变(肾小球增大、基底膜增厚)和肾小管变性(通过H&E染色评估); - 治疗性给药(从疾病诱导后第6天开始):持续8天,可显著降低已形成的蛋白尿,并减少肾小球C3沉积(组织学评分,代表性染色显示C3沉积较溶剂组减少),差异具有统计学意义(与溶剂组相比,P < 0.05,P < 0.01,P < 0.001;每组n=9) [2] 1. 在抗因子 H 抗体诱导的小鼠 C3 肾小球病(C3G)模型中,口服 Iptacopan (LNP023) hydrochloride(1、3、10 mg/kg/天,连续 21 天)呈剂量依赖性减少尿蛋白排泄(1、3、10 mg/kg/天剂量下抑制率分别为 40%、65%、85%),并降低肾小球内 C3b 沉积 [3] 2. 在 PNH 小鼠模型(造血干细胞移植小鼠)中,口服 Iptacopan (LNP023) hydrochloride(3、10 mg/kg/天,连续 14 天)减轻血管内溶血,表现为血红蛋白水平升高(从 8 g/dL 升至 12-13 g/dL),血浆游离血红蛋白降低 60-80% [2][3] 3. 在大鼠胶原诱导关节炎(CIA)模型中,口服 Iptacopan (LNP023) hydrochloride(3、10 mg/kg/天,连续 28 天)抑制关节炎症,减少爪肿胀(抑制率 50-70%),并降低血清中替代途径激活产物(C3a、C5a)水平 [3] 4. 在食蟹猴中,口服 Iptacopan (LNP023) hydrochloride(10 mg/kg)后 2 小时达到血药峰浓度(Cmax = 8.9 μM),替代途径抑制作用持续 >90% 达 12 小时 [3] 5. 治疗剂量下不影响体内经典途径/凝集素途径介导的补体活性(通过对肺炎链球菌的血清杀菌活性评估)[3] |
| 酶活实验 |
体外抑制试验[2]
通过使用CVF:Bb作为C3转化酶的稳定替代物和纯化的内源性C3作为底物,或者通过使用FB和Cy5标记的小分子抑制剂作为探针的竞争结合测定来测试化合物的FB抑制。通过酵母多糖A诱导的MAC形成,在50%的人血清或50%的人全血中测量AP抑制。将血清或全血与化合物预孵育30分钟,然后转移到酵母多糖A包被的平板上。通过ELISA用抗C9新表位抗体检测MAC形成。以类似的方式测量小鼠血清中的AP补体沉积,不同之处在于检测C3b沉积而不是MAC形成。SI附录中提供了有关蛋白质纯化和所有体外测定的更多详细信息。 1. 补体因子B(FB)丝氨酸蛋白酶活性实验:将重组人FB与特异性肽底物(对应AP级联中FB的切割位点)在FB活性优化缓冲液中孵育,加入系列浓度(亚纳摩尔至微摩尔级)的LNP023,37°C孵育特定时间后,通过检测特定波长下的吸光度量化切割底物的生成量(反映FB酶活性)。通过FB活性抑制率与LNP023 浓度的剂量效应曲线计算IC₅₀,证实LNP023 对FB具有强效、可逆的抑制活性 [2] 2. FB结合实验(X射线晶体学指导):将纯化人FB与LNP023 形成复合物并结晶,收集X射线衍射数据(初始FB-抑制剂复合物的分辨率可达1.64 Å)以解析结合模式。结果显示,LNP023 结合于FB的活性中心,与催化残基(His57、Ser195)及S1口袋关键残基相互作用,这是其抑制特异性的核心机制,该结合模式为LNP023 potency和选择性的进一步优化提供了依据 [2, 3] 1. 因子 B 丝氨酸蛋白酶活性实验(HTRF 法):将重组人因子 B(活性形式 Bb)与荧光肽底物及系列浓度的 Iptacopan (LNP023) hydrochloride(0.01 nM-10 μM)共同孵育。37°C 孵育 60 分钟后,检测 HTRF 信号(激发/发射 = 320/665 nm)以量化底物裂解程度,通过非线性回归计算 IC50 值 [3] 2. SPR 结合实验:将人因子 B 固定于传感器芯片,以 30 μL/分钟的流速注入 0.1 nM-1 μM 的 Iptacopan (LNP023) hydrochloride。通过 1:1 结合模型拟合传感图,测定结合动力学参数(kon、koff、KD)[3] 3. 补体替代途径激活实验:将正常人血清与酵母聚糖(AP 激活剂)及 Iptacopan (LNP023) hydrochloride(0.01 nM-10 μM)混合,37°C 孵育 30 分钟后,通过酶联免疫吸附试验(ELISA)检测 C3 转化酶(C3bBb)及 C3 裂解产物(C3a、C3b)的生成,计算替代途径激活的抑制率 [2][3] |
| 细胞实验 |
1. PNH红细胞溶血实验:从PNH患者血液中分离红细胞并洗涤去除血浆成分,将红细胞重悬于含Mg²⁺(支持AP激活)的缓冲液中,加入PNH患者血清(提供补体成分)及系列浓度(0.1~10 µM)的LNP023,37°C孵育固定时间后,通过流式细胞术(FACS)检测红细胞膜完整性标志物,量化溶血率。结果证实LNP023 可剂量依赖性抑制PNH红细胞溶血,1 µM浓度时即具有显著疗效 [2]
2. 绵羊红细胞C3转化酶实验:将绵羊红细胞与纯化C3b、FB在FD存在下孵育,包被形成AP C3转化酶(C3bBb);随后加入0.15 µM的LNP023 及C3G患者血清IgG(稳定C3转化酶),37°C孵育15 min后,通过检测C3切割产物量化活性C3转化酶的量。结果显示LNP023 可降低肾炎因子稳定的C3转化酶的稳定性,证实其在细胞体系中可靶向AP C3转化酶功能 [2] 1. PNH 患者红细胞溶血实验:分离 PNH 患者红细胞,洗涤后重悬于缓冲液中。加入正常人血清(作为补体来源)激活替代途径,同时加入 Iptacopan (LNP023) hydrochloride(0.01 nM-10 μM)。37°C 孵育 60 分钟后离心,检测上清液在 414 nm 处的吸光度以量化溶血程度,确定 IC50 值 [2][3] 2. 肾小球系膜细胞 C3b 沉积实验:将人肾小球系膜细胞接种于 96 孔板,用内毒素(AP 激活剂)刺激 2 小时。加入 Iptacopan (LNP023) hydrochloride(0.1 nM-10 nM)和人血清,37°C 孵育 4 小时。固定细胞后,加入抗 C3b 抗体,再用荧光二抗检测,通过荧光强度评估 C3b 沉积水平 [3] 3. 肾 tubular 上皮细胞毒性实验:培养人肾近端小管上皮细胞,用替代途径激活血清(酵母聚糖激活制备)和 Iptacopan (LNP023) hydrochloride(0.1 nM-10 nM)处理。孵育 24 小时后,通过 MTT 法检测细胞活力,检测乳酸脱氢酶(LDH)释放量以评估补体介导的细胞毒性 [3] |
| 动物实验 |
动物/疾病模型: KRN诱导关节炎的C57BL/6小鼠[2]
剂量: 20、60和180 mg/kg 给药途径: 灌胃;每日两次(bid),持续14天 实验结果: 阻断KRN诱导的关节炎。 1. KRN诱导的关节炎小鼠模型(C57BL/6小鼠): - 疾病诱导:在首次给予LNP023 1小时后,向小鼠注射KRN/I-Ag7血清以诱导关节炎; - 给药方案:LNP023以20 mg/kg、60 mg/kg和180 mg/kg的剂量,每日两次(bid)灌胃给药,持续6天。设置溶剂对照组(每组n=8只小鼠); - 样本采集:第 6 天处死小鼠。采集关节组织用于补体激活产物(Ba、C3d、C5a)的测定和组织学分析(H&E 和番红 O 染色)[2] 2. 被动性 Heymann 肾炎大鼠模型(Sprague-Dawley 大鼠): - 疾病诱导:给大鼠注射抗 1A 组分(抗 Fx1A)抗体血清以诱导膜性肾病。对照组注射正常血清(n=5); - 给药方案: - 预防性给药:从第 0 天开始,每天两次口服 LNP023,剂量分别为 20 mg/kg 和 60 mg/kg(每组 n=9),持续 15 天; - 治疗剂量:从第6天(疾病发作后)开始,以20 mg/kg和60 mg/kg的剂量,每日两次口服LNP023,持续8天(每组n=9);- 样本采集:定期收集尿液,以测量尿蛋白/肌酐比值(UTP/UCREA)。在第14天(治疗组)或第15天(预防组),处死大鼠,并收集肾脏组织进行组织学分析(肾小球病变、肾小管变性)和肾小球C3沉积评估[2] 1. 小鼠C3肾小球病变(C3G)模型:向小鼠静脉注射抗小鼠H因子单克隆抗体(5 mg/kg)以诱导C3G。 盐酸伊普他考潘 (LNP023) 以 1、3 或 10 mg/kg/天的剂量口服给药,每日一次,疗程 21 天,从抗体注射后第 1 天开始。每周检测尿蛋白,并在治疗结束时通过肾脏切片的免疫荧光染色分析肾小球 C3b 沉积情况 [3] 2. 小鼠 PNH 模型:将 PNH 样红系祖细胞移植到小鼠骨髓中。移植后两周,盐酸伊普他考潘 (LNP023) 以 3 或 10 mg/kg/天的剂量口服给药,疗程 14 天。每3天测量一次血红蛋白水平和血浆游离血红蛋白浓度,并通过流式细胞术评估红细胞存活率[2][3] 3. 大鼠胶原诱导性关节炎 (CIA) 模型:用佐剂乳化的牛 II 型胶原蛋白免疫大鼠以诱导关节炎。从出现爪肿胀开始,每天一次口服给予盐酸伊普他考潘 (LNP023),剂量为3或10 mg/kg/天,持续28天。每3天测量一次爪体积,并在研究结束时通过 ELISA 定量血清中 C3a 和 C5a 的水平[3] 4. 食蟹猴药效学研究:给猴子单次口服盐酸伊普他考潘 (LNP023)(10 mg/kg)。分别于给药后 0.5、1、2、4、8、12 和 24 小时采集血样。采用液相色谱-串联质谱法 (LC-MS/MS) 定量血浆药物浓度,并通过溶血试验测定 AP 补体活性,以评估剂量反应关系 [3] |
| 药代性质 (ADME/PK) |
1. 吸收:单次给药后,口服生物利用度约为70%(大鼠)、65%(犬)和55-60%(人)。口服给药后1-2小时达到血浆峰浓度(Cmax)[3]
2. 分布:分布容积(Vd)约为1.2 L/kg(大鼠)、1.0 L/kg(犬)和0.8 L/kg(人)。分布于包括肾脏、关节和骨髓在内的靶组织[3] 3. 代谢:在肝脏中代谢极少;超过90%的药物以原药形式排泄。未检测到主要氧化代谢物[3] 4. 排泄:消除半衰期(t1/2)约为8小时(大鼠)、10小时(犬)和12-16小时(人)。约 60% 的剂量经粪便排出,40% 经尿液排出 [3] 5. 清除率:全身清除率约为 10 mL/min/kg(大鼠)、8 mL/min/kg(犬)和 6 mL/min/kg(人)[3] 6. 血浆蛋白结合率:约 94%(人血浆)、约 92%(大鼠血浆)、约 93%(犬血浆)(采用 1 μM 平衡透析法测定)[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
妊娠期和哺乳期用药
◉ 哺乳期用药概述 目前尚无关于伊普他考潘在哺乳期用药的信息。生产商指出,在治疗期间以及末次给药后5天内应停止哺乳。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对哺乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 1. 急性毒性:大鼠和小鼠的LD50 > 2000 mg/kg(口服)[3] 2. 慢性毒性:在大鼠(剂量高达300 mg/kg/天)和犬(剂量高达150 mg/kg/天)进行的4周口服毒性研究中,未观察到体重、血液学、临床化学(ALT、AST、BUN、Scr)或组织病理学方面的显著变化[3] 3. 肾/肝毒性:在治疗剂量下,动物或健康志愿者均未发现肾毒性或肝毒性[3] 4. 免疫毒性:不损害动物体内CP/LP介导的免疫防御(例如,血清杀菌活性、吞噬作用)[3] 5. 药物相互作用:未观察到细胞色素的抑制或诱导。人肝微粒体中 P450 (CYP) 酶(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4)的浓度高达 10 μM [3] |
| 参考文献 |
|
| 其他信息 |
盐酸伊普他考泮是伊普他考泮的盐酸盐。它是一种补体因子B抑制剂和免疫调节剂。它含有伊普他考泮(1+)。
另见:盐酸伊普他考泮(注释已移至)。 1. 作用机制:盐酸伊普他考泮(LNP023)抑制补体因子B(FB),从而阻断替代补体途径(AP)。通过靶向FB,LNP023可阻止AP C3转化酶(C3bBb)和C5转化酶的形成,从而抑制AP介导的补体激活(例如,C3沉积、MAC组装)和下游病理过程(例如,溶血、炎症、组织损伤)[2, 3] 2. 治疗适应症:LNP023正在开发用于治疗补体介导的疾病,包括阵发性睡眠性血红蛋白尿症(PNH)、C3肾小球病(C3G)、非典型溶血性尿毒综合征(aHUS)、膜性肾病、类风湿性关节炎(以KRN诱导的关节炎为模型)和年龄相关性黄斑变性(AMD)[2, 3] 3. 药物特性:LNP023是一种口服生物利用度高的选择性小分子FB抑制剂。该化合物通过高通量筛选 (HTS) 鉴定,并利用 FB-抑制剂复合物的 X 射线共晶结构信息进行优化,确保了其对 FB 的强效和特异性抑制作用 [3] 4. 临床前疗效亮点:在临床前模型中,LNP023 显示出预防和治疗功效(例如,降低肾病大鼠的蛋白尿,减轻关节炎小鼠的关节炎症),并能有效抑制人血清中 AP 的激活(例如,C3G、PNH),支持其临床开发 [2] 5. 文献 [1] (Semin Hematol. 2018) 主要关注 PNH 的补体疗法,但未提及盐酸伊普他考泮 (LNP023) 或其相关特性 [1] 1. 盐酸伊普他考泮 (LNP023) 是一种首创的口服选择性补体旁路途径抑制剂,靶向因子 B [1][2][3] 2. 其作用机制涉及与因子B(及其活性片段Bb)的丝氨酸蛋白酶结构域结合,阻止AP C3转化酶(C3bBb)的形成和活性,从而阻断AP介导的补体激活。[2][3] 3. 已开发用于治疗补体介导的疾病,包括阵发性睡眠性血红蛋白尿症(PNH)、C3肾小球病(C3G)、免疫球蛋白A肾病(IgAN)和类风湿性关节炎。[1][2][3] 4. 在PNH的II期临床试验中显示出临床疗效,可减少溶血和输血需求,且无严重不良事件。[1][3] 5. 与抗C5单克隆抗体(例如依库珠单抗)不同,它不干扰CP/LP,从而保留宿主对感染的防御能力。[2][3] 6. 化学结构特征为哌啶-苯甲酸骨架具有优化的药代动力学特性,可提高口服生物利用度和组织渗透性[3] |
| 分子式 |
C25H31CLN2O4
|
|---|---|
| 分子量 |
458.9776
|
| 精确质量 |
458.2
|
| 元素分析 |
C, 65.42; H, 6.81; Cl, 7.72; N, 6.10; O, 13.94
|
| CAS号 |
1646321-63-2
|
| 相关CAS号 |
1646321-63-2 (HCl); 1644670-37-0; 1644670-38-1 (TFA)
|
| PubChem CID |
117823351
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
74.8Ų
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
32
|
| 分子复杂度/Complexity |
594
|
| 定义原子立体中心数目 |
2
|
| SMILES |
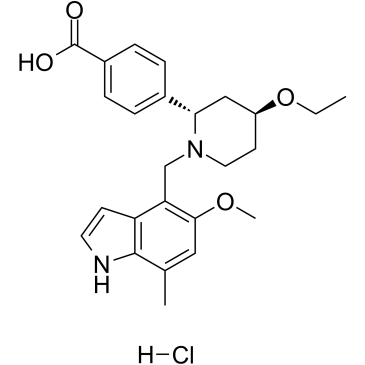
CCO[C@H]1CCN([C@@H](C1)C2=CC=C(C=C2)C(=O)O)CC3=C(C=C(C4=C3C=CN4)C)OC.Cl
|
| InChi Key |
SEZXOFFLNHXEJE-CQERKEQDSA-N
|
| InChi Code |
InChI=1S/C25H30N2O4.ClH/c1-4-31-19-10-12-27(22(14-19)17-5-7-18(8-6-17)25(28)29)15-21-20-9-11-26-24(20)16(2)13-23(21)30-3;/h5-9,11,13,19,22,26H,4,10,12,14-15H2,1-3H3,(H,28,29);1H/t19-,22-;/m0./s1
|
| 化学名 |
4-((2S,4S)-4-ethoxy-1-((5-methoxy-7-methyl-1H-indol-4-yl)methyl)piperidin-2-yl)benzoic acid hydrochloride
|
| 别名 |
LNP023 hydrochloride; Iptacopan; LNP-023 hydrochloride; LNP 023 hydrochloride; LNP 023 HCL; LNP-023 HCL; LNP023 HCL; Fabhalta
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~250 mg/mL (~544.69 mM)
H2O : ~50 mg/mL (~108.94 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.53 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.53 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (4.53 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1787 mL | 10.8937 mL | 21.7874 mL | |
| 5 mM | 0.4357 mL | 2.1787 mL | 4.3575 mL | |
| 10 mM | 0.2179 mL | 1.0894 mL | 2.1787 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Study of Efficacy and Safety of Twice Daily Oral Iptacopan (LNP023) in Adult PNH Patients Who Are Naive to Complement Inhibitor Therapy
CTID: NCT04820530
Phase: Phase 3 Status: Completed
Date: 2024-10-09