| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
| 靶点 |
Human A2B receptor (Ki = 1.39 nM), (Human A2A receptor (Ki = 112 nM), Human A1 receptor (Ki = 157 nM), Human A3 receptor (Ki = 230 nM)
|
|---|---|
| 体外研究 (In Vitro) |
MRS-1706 (0.1-5 μM) 通过剂量依赖性 NECA 拮抗作用抑制野生型腺苷 A2B 受体 [1]。 MRS-1706 (0.1-10000 nM) 可诱导酵母生长抑制。在酵母细胞中,表达七种 CAM 腺苷 A2B 受体。 T42A、T42A/V54A、N36S/T42A 和 F84L、F84S 和 F84L/S95G 的 IC50 值分别为 43、54、40、98、166 和 133 nM[1]。在野生型海绵状条带 (CCS) 中,MRS-1706 (1 μM) 降低 cAMP 水平并抑制腺苷介导的 cAMP 诱导 [2]。
|
| 体内研究 (In Vivo) |
MRS-1706(1-10 μM;海绵体内注射;Ada–/– 动物)可减少镰状细胞病 (SCD) 转基因小鼠和受到电场刺激 (EFS) 诱导的小鼠的 cAMP 水平抑制的量和持续时间海绵体收缩(CCS)[2]。
|
| 酶活实验 |
如前所述,通过用活化的PEG共价修饰纯化的牛ADA来产生PEG-ADA。Ada–/–小鼠在出生时通过筛选血液中的Ada酶活性进行鉴定,如前所述。Ada-/-小鼠从出生后第2天开始接受Ada酶治疗。用ADA酶疗法将小鼠维持至少8周,使其达到生殖成熟。[2]
人腺苷A2B受体属于A类G蛋白偶联受体(GPCR)。在我们之前的工作中,从随机突变库中鉴定出组成型活性突变体(CAM)人腺苷A2B受体。在本研究中,三种已知的A2B受体拮抗剂,4-{2-[7-氨基-2-(2-呋喃基)[1,2,4]三唑并-[2,3-a][1,3,5]三嗪-5-基氨基]乙基}苯酚(ZM241385)、8-环戊基-1,3-二丙基黄嘌呤(DPCPX)和N-(4-乙酰基苯基)-2-[4-(2,3,6,7-四氢-2,6-二氧代-1,3-二丙酰基-1H-嘌呤-8-基)苯氧基]乙酰胺(MRS1706)在酵母生长测定中对具有不同组成活性水平的野生型和九种CAM A2B受体进行了测试。所有三种化合物都证明是腺苷A2B受体的反向激动剂,因为它们能够完全逆转四种低水平组成型活性A2B受体突变体的基础活性,并部分逆转三种中等水平组成型活化A2B受体突变株的基础活性。我们还发现了两种具有高度组成活性的突变体,它们的基础活性不能被三种化合物中的任何一种逆转。使用两态受体模型来解释实验观察结果;拟合得到三种反向激动剂ZM241385、DPCPX和MRS1706的以下相对内在功效:分别为0.14±0.03、0.35±0.03和0.31±0.02。此外,在该模型中,从突变体F84L的0.11到两个高组成活性突变体的999,改变L,活性受体与非活性受体的比率,产生模拟实验曲线的模拟剂量反应曲线。本研究首次描述了人腺苷A2B受体的反向激动剂。此外,使用具有不同组成活性水平的受体突变体使我们能够确定这些反向激动剂的相对内在功效。[2] |
| 细胞实验 |
体外海绵体组织培养。[2]
如上所述制备CCS。然后将分离的CCS浸入37°C下用95%O2鼓泡的标准Krebs溶液(pH 7.4)中。平衡30分钟后,在存在或不存在各种腺苷受体激动剂或拮抗剂或l-NAME的情况下,将条带暴露于不同浓度的腺苷。10分钟后,除去CCSs并立即在液氮中冷冻,用于随后测定cAMP和cGMP水平。在一系列单独的实验中,CCSs暴露于苯肾上腺素(10μM),无论是否用腺苷或l-NAME处理(10分钟)。[2] 主要CCSMC的隔离。[2] 如上所述分离CCS,在PBS中洗涤,并切碎成12-mm3块。将切片在5–10 ml含有0.02%胶原酶A(0.272 U/mg蛋白质)和0.5%弹性蛋白酶(3.73 U/mg蛋白)的酶溶液中于75 mm烧瓶中于37°C下孵育6小时。通过加入补充有10%FCS的10ml DMEM终止酶消化。之后,通过40μm尼龙网过滤悬浮液以分离单个细胞,并以200 g离心10分钟。如前所述(33),使用10 ml补充的血管平滑肌细胞生长培养基(包括抗生素和10%FCS),将细胞颗粒重悬并在75-cm2细胞培养瓶中培养14天。通过α-SMA免疫染色测定,血管平滑肌细胞通常占细胞培养物的约95%。 |
| 动物实验 |
动物/疾病模型: Ada–/– 小鼠 [2]
剂量: 1 和 10 μM 给药途径: 阴茎海绵体内注射 实验结果: 抑制 A2BR 信号传导,降低其强度和持续时间。抑制 cAMP 水平。 Ada–/– 小鼠的构建和基因分型方法如前所述。Ada–/– 小鼠具有 129/sV、C57BL/6 和 FVB/N 品系的混合遗传背景。对照组小鼠(标记为 Ada+)为同窝小鼠,其中野生型 (+/+) 或携带 Ada 无效等位基因的杂合子 (+/–)。杂合子小鼠不表现出表型。所有表型比较均在同窝小鼠之间进行。 A1R–/–小鼠由J. Schnermann(美国国立卫生研究院NIDDK,马里兰州贝塞斯达)提供;A2AR–/–小鼠由J.-F. Chen(美国波士顿大学医学院,马萨诸塞州波士顿)提供;A2BR–/–小鼠由本实验室构建;A3R–/–小鼠由M. Jacobson(美国默克研究实验室,费城西点)提供。所有腺苷受体缺陷小鼠均已回交至C57BL/6背景至少10代,并根据既定方案进行基因分型。仅表达人镰状血红蛋白的SCD转基因小鼠购自杰克逊实验室。所有小鼠的饲养和照护均符合美国国立卫生研究院(NIH)指南,并经德克萨斯大学休斯顿健康科学中心动物护理和使用委员会批准。 |
| 参考文献 |
[1]. Li Q, et, al. ZM241385, DPCPX, MRS1706 are inverse agonists with different relative intrinsic efficacies on constitutively active mutants of the human adenosine A2B receptor. J Pharmacol Exp Ther. 2007 Feb;320(2):637-45.
[2]. Mi T, et, al. Excess adenosine in murine penile erectile tissues contributes to priapism via A2B adenosine receptor signaling. J Clin Invest. 2008 Apr;118(4):1491-501. |
| 分子式 |
C27H29N5O5
|
|---|---|
| 分子量 |
503.56
|
| 精确质量 |
503.217
|
| 元素分析 |
C, 64.40; H, 5.81; N, 13.91; O, 15.89
|
| CAS号 |
264622-53-9
|
| PubChem CID |
5139184
|
| 外观&性状 |
Off-white to yellow solid
|
| LogP |
3.666
|
| tPSA |
128.08
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
10
|
| 重原子数目 |
37
|
| 分子复杂度/Complexity |
837
|
| 定义原子立体中心数目 |
0
|
| SMILES |
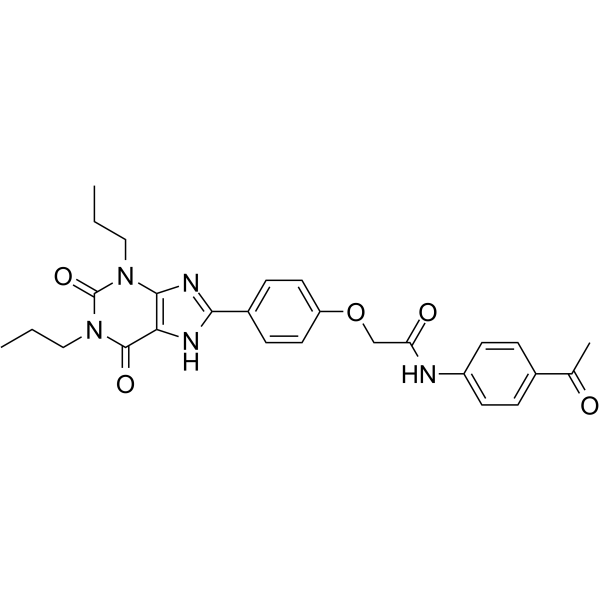
O=C(NC1=CC=C(C(C)=O)C=C1)COC2=CC=C(C3=NC(N(CCC)C(N(CCC)C4=O)=O)=C4N3)C=C2
|
| InChi Key |
ZKUCFFYOQOJLGT-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C27H29N5O5/c1-4-14-31-25-23(26(35)32(15-5-2)27(31)36)29-24(30-25)19-8-12-21(13-9-19)37-16-22(34)28-20-10-6-18(7-11-20)17(3)33/h6-13H,4-5,14-16H2,1-3H3,(H,28,34)(H,29,30)
|
| 化学名 |
N-(4-acetylphenyl)-2-[4-(2,6-dioxo-1,3-dipropyl-1,2,3,6-tetrahydropurin-8-yl)phenoxy]acetamide
|
| 别名 |
MRS-1706; MRS 1706; MRS1706
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~240 mg/mL (~476.62 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 6 mg/mL (11.92 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 60.0 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 6 mg/mL (11.92 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 60.0 mg/mL 澄清 DMSO 储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 0.64 mg/mL (1.27 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9859 mL | 9.9293 mL | 19.8586 mL | |
| 5 mM | 0.3972 mL | 1.9859 mL | 3.9717 mL | |
| 10 mM | 0.1986 mL | 0.9929 mL | 1.9859 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。