| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
MGMT/AGT (O6-alkylguanine-DNA alkyltransferase; DNA repair enzyme)
|
|---|---|
| 体外研究 (In Vitro) |
L3.6pl细胞对O6-苄基鸟嘌呤表现出剂量和时间依赖性敏感性(24-72小时)。 50 μg(48 小时)为 IC50[2]。 O6-苄基鸟嘌呤(50 μg;48 小时)可显着降低 L3.6pl 中的 MGMT 蛋白活性并改变 p53 下游靶标 [2]。
O(6)-苄基鸟嘌呤(O6BG)使胰腺癌症细胞对吉西他滨敏感。在存在O(6)BG的情况下,MGMT、细胞周期蛋白B1、细胞周期素B2、细胞周期因子A和ki-67的蛋白和mRNA表达显著降低。与此形成鲜明对比的是,p21(cip1)的蛋白表达和mRNA信息显著增加。有趣的是,O(6)BG增加p53介导的p21(cip1)转录活性并抑制细胞周期蛋白B1。此外,我们的结果表明p53被招募到p21启动子。此外,p21(cip1)的增加和细胞周期蛋白转录的减少是p53依赖性的[2]。 |
| 体内研究 (In Vivo) |
作为对吉西他滨 (100 mg/kg) 的反应,O6-苄基鸟嘌呤(100 μg;腹膜内注射;每天一次,持续 35 天)抑制胰腺发育并增加胰腺细胞重量 [2]。
研究人员接下来确定了O(6)-benzyl guanine (O6BG)/O(6)-苄基鸟嘌呤(O6BG)(单独或联合)与吉西他滨的体内作用。对来自不同治疗组的肿瘤进行常规组织学和免疫组织化学分析。与单独使用吉西他滨或对照组治疗的肿瘤相比,单独使用O6BG或与吉西他滨联合治疗的小鼠肿瘤的MGMT、细胞周期蛋白B1、细胞周期素B2和细胞周期蛋白a显著降低。与此形成鲜明对比的是,用O6BG治疗的小鼠肿瘤中p21的表达显著增加。 O(6)-苄基鸟嘌呤(O6BG)体内抑制胰腺癌症细胞增殖并诱导肿瘤细胞凋亡[2] 肿瘤细胞凋亡的诱导(TUNEL阳性染色)与增殖(ki-67阳性)呈负相关。TUNEL阳性染色显示,与单独用吉西他滨或对照治疗的小鼠相比,用O6BG(单独或与吉西他滨联合)治疗的小鼠中许多肿瘤细胞发生了凋亡(图5)。与对照组小鼠或吉西他滨治疗的小鼠相比,单独使用O6BG或与吉西他滨联合使用可降低肿瘤细胞增殖。 |
| 酶活实验 |
报告分析[2]
对于报告检测,将L3.6pl细胞(5×10~4)接种在12孔板中,并用MGMT-luc构建体转染。5至6小时后,用或不用O(6)-苄基鸟嘌呤(O6BG)(50μg)处理细胞。在处理后24小时,收集细胞并裂解,按照制造商的方案,使用双荧光素酶报告物测定系统测量荧光素酶活性。使用LipofectAMINE 2000转染细胞,并遵循制造商的转染方案。在另一个实验中,在有或没有wt p53构建体(5μg)的情况下,用MGMT-luc转染L3.6pl细胞(5×104),24小时后收获细胞。在最后一组实验中,将L3.6pl细胞(5×10~4)接种在12孔板中,在有或没有O(6)-苄基鸟嘌呤(O6BG)(50μg)和吉西他滨(1μmol/L)的情况下,用p21-luc构建体和细胞周期蛋白B1-luc构建体转染,并在处理后24小时收获细胞。 染色质免疫沉淀试验[2] 将L3.6pl细胞铺板(2×10~5),24小时后用非特异性和p53 siRNA转染细胞,均为20 nmol/L。48小时后,用或不用O(6)-苄基鸟嘌呤(O6BG)处理细胞,处理24小时后收集细胞并将样品用于染色质免疫沉淀分析(ChIP)。ChIP检测是按照制造商的说明进行的,只做了细微的修改。将L3.6pl细胞铺板(2×10~5),第二天用非特异性(20 nmol/L)和p53 siRNA(20 nmol/L)转染,24小时后用或不用O(6)-苄基鸟嘌呤(O6BG)处理细胞。在处理后48小时收集细胞。将细胞裂解液(400μL)超声处理25次,每次施加10-s脉冲和20-s间隙。离心后,50μL上清液用于检查DNA断裂和输入,剩余的350μL用于染色质免疫沉淀。 |
| 细胞实验 |
蛋白质印迹分析[2]
细胞类型: L3 .6pl 和 PANC1 细胞 测试浓度: 50 μg 孵育时间:48小时 实验结果:O6甲基鸟嘌呤DNA甲基转移酶(MGMT)、cyclin B1、cyclin B2、cyclin A、p53、ki-67的表达减少,而 p21 增加。细胞 C 和 caspase 9 水平升高,而 PARP1 蛋白水平降低。 RT-PCR[2] 细胞类型: L3.6pl 细胞 测试浓度: 50 μg 孵育持续时间:48小时 实验结果:L3.6pl中MGMT转录活性减弱。 |
| 动物实验 |
动物/疾病模型:雄性无胸腺裸鼠(NCI-nu)(携带人胰腺癌L3.6pl细胞)[2]
剂量:100 μg 给药途径:腹腔注射;用于诱导细胞增殖和胰腺癌细胞增殖[2]。每日一次,持续35天 实验结果:肿瘤体积和重量中位数显著降低。 治疗裸鼠胰腺内已建立的人胰腺癌肿瘤[2] 将肿瘤细胞注射到胰腺7天后,处死5只小鼠以确认肿瘤病灶的存在。此时,肿瘤体积中位数为18 mm3。组织学检查证实病灶为活跃生长的胰腺癌。小鼠被随机分为四组(n = 10),具体如下:(a)对照组,每日(MF)腹腔注射1×PBS;(b)每周两次(T、Th)腹腔注射吉西他滨100 mg/kg;(c)每日(MF)腹腔注射O6-苄基鸟嘌呤(O6BG)(100 μg);(d)每周两次腹腔注射吉西他滨联合O6-苄基鸟嘌呤(O6BG)(5天/周)。肿瘤体积采用以下公式计算:0.5 ×(长)×(宽)²。治疗持续5周后,处死小鼠并进行尸检。 |
| 参考文献 |
|
| 其他信息 |
6-O-苄基鸟嘌呤已用于多种疾病的治疗试验,包括HIV感染、成人胶质肉瘤、成人胶质母细胞瘤、I期成人霍奇金淋巴瘤和II期成人霍奇金淋巴瘤等。
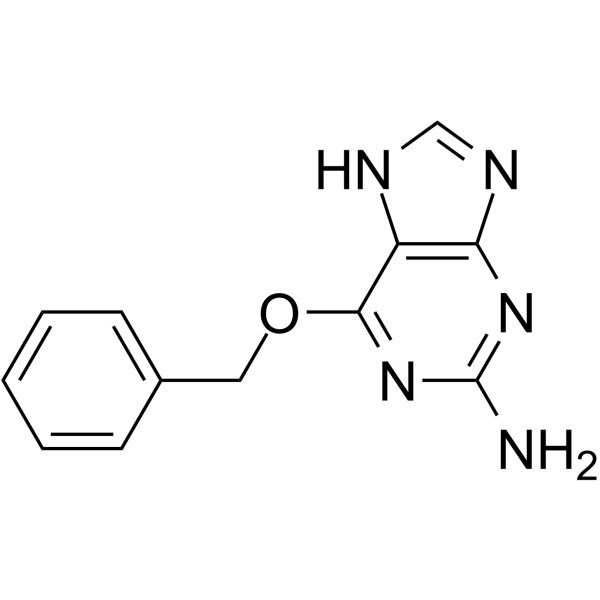
6-O-苄基鸟嘌呤是一种具有抗肿瘤活性的鸟嘌呤类似物。6-O-苄基鸟嘌呤可与DNA修复酶O(6)-烷基鸟嘌呤DNA烷基转移酶(AGT)结合,将苄基转移至活性位点半胱氨酸残基,从而抑制AGT介导的DNA修复。该药物与其他损伤DNA的化疗药物联合使用可增强其疗效。(NCI04) 目的:我们旨在确定单独使用或与吉西他滨联合使用最佳生物剂量的MGMT阻滞剂6-O-苄基鸟嘌呤(O(6)BG)是否能抑制人胰腺癌细胞的生长。实验设计:采用 O(6)BG 单独或联合吉西他滨处理人胰腺癌 L3.6pl 和 PANC1 细胞,并研究这些药物组合的治疗效果和生物活性。结果:O(6)BG 可增强胰腺癌细胞对吉西他滨的敏感性。在 O(6)BG 存在的情况下,MGMT、细胞周期蛋白 B1、细胞周期蛋白 B2、细胞周期蛋白 A 和 Ki-67 的蛋白和 mRNA 表达显著降低。与之形成鲜明对比的是,p21(cip1) 的蛋白表达和 mRNA 表达显著升高。有趣的是,O(6)BG 可增强 p53 介导的 p21(cip1) 转录活性并抑制细胞周期蛋白 B1。此外,我们的结果表明 p53 可募集至 p21 启动子。而且,p21(cip1) 的增加和细胞周期蛋白转录的减少均依赖于 p53。单独使用吉西他滨治疗的小鼠胰腺肿瘤体积减少了27%,单独使用O(6)BG治疗的小鼠胰腺肿瘤体积减少了47%,而联合用药的小鼠胰腺肿瘤体积减少了65%。免疫组织化学分析显示,O(6)BG抑制了MGMT和细胞周期蛋白的表达,并增加了p21(cip1)的表达。此外,肿瘤细胞增殖显著减少,肿瘤细胞凋亡增加。结论:综上所述,我们的结果表明,MGMT表达降低与p53激活相关,并显著抑制了原发性胰腺肿瘤的生长。这些发现提示,O(6)BG单独使用或与吉西他滨联合使用可能为治疗人类胰腺癌提供一种新的有效方法。[2] |
| 分子式 |
C12H11N5O
|
|---|---|
| 分子量 |
241.25
|
| 精确质量 |
241.096
|
| 元素分析 |
C, 59.74; H, 4.60; N, 29.03; O, 6.63
|
| CAS号 |
19916-73-5
|
| 相关CAS号 |
100994-97-6 (sodium); 19916-73-5 (free)
|
| PubChem CID |
4578
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.4±0.1 g/cm3
|
| 沸点 |
621.4±63.0 °C at 760 mmHg
|
| 熔点 |
193(dec.)
|
| 闪点 |
329.6±33.7 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.743
|
| LogP |
1.95
|
| tPSA |
89.71
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
18
|
| 分子复杂度/Complexity |
271
|
| 定义原子立体中心数目 |
0
|
| SMILES |
C1=CC=C(C=C1)COC2=NC(=NC3=C2NC=N3)N
|
| InChi Key |
KRWMERLEINMZFT-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C12H11N5O/c13-12-16-10-9(14-7-15-10)11(17-12)18-6-8-4-2-1-3-5-8/h1-5,7H,6H2,(H3,13,14,15,16,17)
|
| 化学名 |
6-phenylmethoxy-7H-purin-2-amine
|
| 别名 |
CCRIS9383; CCRIS 9383; o6-benzylguanine; 19916-73-5; 6-O-Benzylguanine; 6-(Benzyloxy)-7H-purin-2-amine; O(6)-Benzylguanine; 2-Amino-6-(benzyloxy)purine; 6-(benzyloxy)-9H-purin-2-amine; 2-amino-6-benzyloxypurine; O(6)-Benzylguanine
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~110 mg/mL (~455.96 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.75 mg/mL (11.40 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 27.5 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.75 mg/mL (11.40 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 27.5 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 4.1451 mL | 20.7254 mL | 41.4508 mL | |
| 5 mM | 0.8290 mL | 4.1451 mL | 8.2902 mL | |
| 10 mM | 0.4145 mL | 2.0725 mL | 4.1451 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT05052957
Conditions:Glioblastoma Multiforme|Glioblastoma Multiforme, Adult|Supratentorial Glioblastoma|Supratentorial GliosarcomaLink: https://clinicaltrials.gov/ct2/show/NCT01269424
Conditions:Glioblastoma MultiformeLink: https://clinicaltrials.gov/ct2/show/NCT00669669
Conditions:Glioblastoma|Gliosarcoma
Title:O6-Benzylguanine and Temozolomide in Treating Young Patients With Recurrent or Progressive Gliomas or Brain Stem Tumors
Status:Completed
updateDate:2022-02-11
Ctid:NCT00275002
Link: https://clinicaltrials.gov/ct2/show/NCT00275002
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT02343666
Conditions:Human Immunodeficiency Virus 1 Positive|Stage I Adult Hodgkin Lymphoma|Stage I Adult Non-Hodgkin Lymphoma|Stage II Adult Hodgkin Lymphoma|Stage II Adult Non-Hodgkin Lymphoma|Stage III Adult Hodgkin Lymphoma|Stage III Adult Non-Hodgkin Lymphoma|Stage IV Adult Hodgkin Lymphoma|Stage IV Adult Non-Hodgkin LymphomaLink: https://clinicaltrials.gov/ct2/show/NCT00002971
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00961220
Conditions:Recurrent Primary Cutaneous T-Cell Non-Hodgkin Lymphoma|Stage I Mycosis Fungoides and Sezary Syndrome AJCC v7|Stage II Mycosis Fungoides and Sezary Syndrome AJCC v7Link: https://clinicaltrials.gov/ct2/show/NCT00436436
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT01769911
Conditions:Adult Nasal Type Extranodal NK/T-cell Lymphoma|AIDS-related Diffuse Large Cell Lymphoma|AIDS-related Diffuse Mixed Cell Lymphoma|AIDS-related Diffuse Small Cleaved Cell Lymphoma|AIDS-related Immunoblastic Large Cell Lymphoma|AIDS-related Lymphoblastic Lymphoma|AIDS-related Peripheral/Systemic Lymphoma|AIDS-related Small Noncleaved Cell Lymphoma|Anaplastic Large Cell Lymphoma|Angioimmunoblastic T-cell Lymphoma|Cutaneous B-cell Non-Hodgkin Lymphoma|Extranodal Marginal Zone B-cell Lymphoma of Mucosa-associated Lymphoid Tissue|Hepatosplenic T-cell Lymphoma|HIV-associated Hodgkin Lymphoma|Intraocular Lymphoma|Nodal Marginal Zone B-cell Lymphoma|Noncutaneous Extranodal Lymphoma|Peripheral T-cell Lymphoma|Recurrent Adult Burkitt Lymphoma|Recurrent Adult Diffuse Large Cell Lymphoma|Recurrent Adult Diffuse Mixed Cell Lymphoma|Recurrent Adult Diffuse Small Cleaved Cell Lymphoma|Recurrent Adult Grade III Lymphomatoid Granulomatosis|Recurrent Adult Hodgkin Lymphoma|Recurrent Adult Immunoblastic Large Cell Lymphoma|Recurrent Adult Lymphoblastic Lymphoma|Recurrent Adult T-cell Leukemia/Lymphoma|Recurrent Cutaneous T-cell Non-Hodgkin Lymphoma|Recurrent Grade 1 Follicular Lymphoma|Recurrent Grade 2 Follicular Lymphoma|Recurrent Grade 3 Follicular Lymphoma|Recurrent Mantle Cell Lymphoma|Recurrent Marginal Zone Lymphoma|Recurrent Mycosis Fungoides/Sezary Syndrome|Recurrent Small Lymphocytic Lymphoma|Refractory Hairy Cell Leukemia|Small Intestine Lymphoma|Splenic Marginal Zone Lymphoma|Stage I AIDS-related Lymphoma|Stage II AIDS-related Lymphoma|Stage III AIDS-related Lymphoma|Stage IV AIDS-related Lymphoma|T-cell Large Granular Lymphocyte Leukemia|Testicular Lymphoma|Waldenström MacroglobulinemiaLink: https://clinicaltrials.gov/ct2/show/NCT00020150
Conditions:Brain and Central Nervous System Tumors|Childhood Germ Cell Tumor|Extragonadal Germ Cell Tumor|Kidney Cancer|Liver Cancer|Neuroblastoma|Ovarian Cancer|Sarcoma|Unspecified Childhood Solid Tumor, Protocol SpecificLink: https://clinicaltrials.gov/ct2/show/NCT00005081
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00003766
Conditions:Unspecified Adult Solid Tumor, Protocol SpecificLink: https://clinicaltrials.gov/ct2/show/NCT00253487
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00052780
Conditions:Childhood Central Nervous System Germ Cell Tumor|Childhood Choroid Plexus Tumor|Childhood Craniopharyngioma|Childhood Ependymoblastoma|Childhood Grade I Meningioma|Childhood Grade II Meningioma|Childhood Grade III Meningioma|Childhood High-grade Cerebellar Astrocytoma|Childhood High-grade Cerebral Astrocytoma|Childhood Infratentorial Ependymoma|Childhood Low-grade Cerebellar Astrocytoma|Childhood Low-grade Cerebral Astrocytoma|Childhood Medulloepithelioma|Childhood Mixed Glioma|Childhood Oligodendroglioma|Childhood Supratentorial Ependymoma|Recurrent Childhood Brain Stem Glioma|Recurrent Childhood Cerebellar Astrocytoma|Recurrent Childhood Cerebral Astrocytoma|Recurrent Childhood Ependymoma|Recurrent Childhood Medulloblastoma|Recurrent Childhood Pineoblastoma|Recurrent Childhood Subependymal Giant Cell Astrocytoma|Recurrent Childhood Supratentorial Primitive Neuroectodermal Tumor|Recurrent Childhood Visual Pathway and Hypothalamic GliomaLink: https://clinicaltrials.gov/ct2/show/NCT00005066
Conditions:SarcomaLink: https://clinicaltrials.gov/ct2/show/NCT00006474
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00046878
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00003348
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00005961
Conditions:Melanoma (Skin)Link: https://clinicaltrials.gov/ct2/show/NCT00003765
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00017147
Conditions:Malignant Neoplasms of Eye, Brain and Other Parts of Central Nervous SystemLink: https://clinicaltrials.gov/ct2/show/NCT00086970
Conditions:Unspecified Adult Solid Tumor, Protocol SpecificLink: https://clinicaltrials.gov/ct2/show/NCT00003613
Conditions:Recurrent Cutaneous T-cell Non-Hodgkin Lymphoma|Stage I Cutaneous T-cell Non-Hodgkin Lymphoma|Stage II Cutaneous T-cell Non-Hodgkin LymphomaLink: https://clinicaltrials.gov/ct2/show/NCT00002604
Conditions:Unspecified Adult Solid Tumor, Protocol SpecificLink: https://clinicaltrials.gov/ct2/show/NCT00004072
Conditions:Multiple Myeloma and Plasma Cell NeoplasmLink: https://clinicaltrials.gov/ct2/show/NCT00003567
Conditions:Brain and Central Nervous System Tumors|Lymphoma|Unspecified Adult Solid Tumor, Protocol SpecificLink: https://clinicaltrials.gov/ct2/show/NCT00005981
Conditions:Colorectal CancerLink: https://clinicaltrials.gov/ct2/show/NCT00045721
Conditions:Brain and Central Nervous System TumorsLink: https://clinicaltrials.gov/ct2/show/NCT00004892
Conditions:Brain and Central Nervous System Tumors