| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
hAR (IC50 = hAR )
ODM-201 and its pharmacologically active main metabolite ORM-15341 are novel and structurally distinct from any known antiandrogens including the second-generation antiandrogens enzalutamide and ARN-509. Figure 1A,B show the chemical structures of ODM-201 and ORM-15341. [1] In competitive AR binding assays, the inhibition constant (Ki) values of ODM-201 and ORM-15341 were 11 and 8 nM, respectively, being clearly lower than those of enzalutamide (86 nM) and ARN-509 (93 nM) (Fig. 1C) that were tested under the same conditions. ODM-201 and its major metabolite ORM-15341 are also potent and full antagonists for human AR (hAR) with IC50 values of 26 and 38 nM as shown by transactivation assays in AR-HEK293 cells stably expressing full-length hAR and an androgen-responsive luciferase reporter gene construct. [1] In contrast, in the presence of ODM-201, ORM-15341, enzalutamide, or ARN-509, AR was predominantly cytoplasmic, showing that these antiandrogens inhibit the androgen-induced nuclear translocation of overexpressed AR to same extent[1]. |
|---|---|
| 体外研究 (In Vitro) |
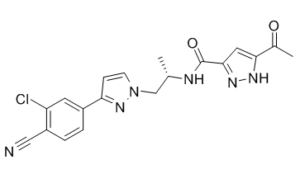
ODM-201及其药理活性主要代谢产物ORM-15341是新颖的,在结构上不同于任何已知的抗雄激素,包括第二代抗雄激素恩杂鲁胺和ARN-509。图1A、B显示了ODM-201和ORM-15341的化学结构。[1]
在竞争性AR结合试验中,ODM-201和ORM-15341的抑制常数(Ki)值分别为11和8 nM,明显低于在相同条件下测试的恩杂鲁胺(86 nM)和ARN-509(93 nM)(图1C)。ODM-201及其主要代谢产物ORM-15341也是人类AR(hAR)的强效完全拮抗剂,IC50值为26和38 nM,如稳定表达全长hAR和雄激素反应性萤光素酶报告基因构建体的AR-HEK293细胞中的转录激活试验所示。[1] 相比之下,在ODM-201、ORM-15341、恩杂鲁胺或ARN-509存在的情况下,AR主要是细胞质的,表明这些抗雄激素在相同程度上抑制了雄激素诱导的过表达AR的核转位[1]。 ORM-15341 是人类野生型雄激素受体 (hAR) 的强效完全拮抗剂,在使用稳定表达全长hAR和雄激素反应性荧光素酶报告基因的AR-HEK293细胞进行的转录激活实验中,其IC50为38 nM。[1] ORM-15341 对导致抗雄激素治疗耐药的临床相关AR突变体具有完全拮抗作用。在使用瞬时转染了突变AR表达载体的U2-OS细胞进行的转录激活实验中,它拮抗了突变体AR(F876L) (IC50 = 51 nM)、AR(W741L) (IC50 = 1160 nM) 和 AR(T877A) (IC50 = 700 nM)。相比之下,恩扎卢胺和ARN-509对F876L突变体表现为激动剂作用。[1] 与ODM-201、恩扎卢胺和ARN-509类似,ORM-15341 能抑制过表达AR的HS-HEK293细胞中睾酮诱导的AR核转位,这一点通过免疫细胞化学和高内涵成像得到了证实。[1] ORM-15341 在体外能抑制VCaP前列腺癌细胞(具有内源性AR基因扩增和过表达)的雄激素诱导性增殖,其IC50为170 nM。在相同条件下,此效果优于恩扎卢胺 (IC50 = 410 nM) 和ARN-509 (IC50 = 420 nM)。[1] ORM-15341(以及ODM-201)的抗增殖作用对AR依赖性细胞具有特异性,因为其对AR阴性的DU-145前列腺癌细胞和H1581肺癌细胞的活力没有影响。[1] |
| 体内研究 (In Vivo) |
为了阐明ODM-201在CRPC小鼠模型中的体内疗效,皮下注射VCaP细胞的去势雄性裸鼠口服ODM-201(50mg/kg)一次(qd)或每日两次(bid),或用恩杂鲁胺(20mg/kg,qd)治疗37天。恩杂鲁胺的剂量是根据之前发表的体内研究9和我们的药代动力学(PK)分析选择的,这些研究表明,在小鼠中,该剂量恩杂鲁酰胺的全身暴露量(AUC0-24)是ODM-201(50mg/kg,bid)的2.5倍。此外,恩杂鲁胺显示出较长的血浆半衰期(18.3小时),而ODM-201在小鼠体内的半衰期不是最佳的(1.6小时),支持恩杂鲁肽每日一次给药和ODM-201的更高剂量和更频繁给药。恩杂鲁胺和ODM-201的PK数据见补充表S1[1]。
|
| 酶活实验 |
使用竞争性结合实验测定ORM-15341与雄激素受体的结合亲和力。从去势大鼠的腹侧前列腺制备胞质裂解物。裂解物经过处理以去除内源性类固醇。实验包括将前列腺胞质制备物、固定浓度的放射性配体[3H]米勃酮与浓度递增的测试化合物在0–4°C下共同孵育过夜。使用包被葡聚糖的活性炭悬浮液分离结合与游离的类固醇。通过液闪计数仪测量上清液中的结合放射性,从而确定抑制常数 (Ki)。[1]
|
| 细胞实验 |
在稳定表达全长人AR和雄激素反应性荧光素酶报告基因的AR-HEK293细胞中,测定ORM-15341对野生型人AR的功能性拮抗活性和效力。在无固醇测定培养基中,用测试化合物和低浓度睾酮 (0.45 nM) 处理细胞。孵育24小时后,裂解细胞,并使用化学发光仪测量荧光素酶活性。[1]
通过转录激活实验研究ORM-15341对突变AR的作用。将人U2-OS骨肉瘤细胞瞬时转染编码特定AR突变体(F876L、T877A或W741L)的表达载体和雄激素反应性荧光素酶报告基因构建体。在无固醇培养基中,用浓度递增的测试化合物和能诱导亚最大报告基因活性的参考激动剂(睾酮或DHT)处理细胞。孵育24小时后,测量荧光素酶活性。[1] 使用过表达AR的HS-HEK293细胞评估ORM-15341对AR核转位的影响。将细胞接种于无固醇培养基中,并用测试化合物 (0.3 μM) 与睾酮 (0.3 nM) 共同处理数小时。然后固定、透化细胞,并用偶联荧光染料的AR抗体进行免疫标记。使用高内涵筛选阅读器定量AR的核定位。[1] 使用VCaP细胞系评估ORM-15341对AR依赖性前列腺癌细胞的抗增殖作用。在无固醇测定培养基中,用亚最大浓度的合成雄激素米勃酮 (0.1 nM) 和浓度递增的测试化合物处理细胞。孵育4天后,使用比色细胞增殖实验 (WST-1) 测量细胞活力。[1] |
| 动物实验 |
在小鼠体内开展了药代动力学研究,评估了ORM-15341的脑渗透性。裸鼠雄性连续7天口服ODM-201(25、50或100 mg/kg,每日两次)。采集血样并分离血浆。将脑组织样本(去除嗅球和延髓)混合并匀浆。采用液相色谱-串联质谱法(LC-MS/MS)测定小鼠血浆和脑匀浆中ORM-15341(ODM-201的代谢物)的浓度。采用非房室模型分析血浆和脑组织浓度-时间数据。基于0至24小时浓度-时间曲线下面积(AUC0-24)计算脑血浆比值。[1]
|
| 药代性质 (ADME/PK) |
ORM-15341 被鉴定为 ODM-201 的主要药理活性代谢物。[1]
ORM-15341 在小鼠体内的脑渗透性极低。基于 AUC0-24 的脑血浆比值在不同剂量水平的母体化合物 ODM-201 中为 1.9%–2.8%,未观察到剂量-反应关系。[1] |
| 参考文献 |
|
| 其他信息 |
酮达罗鲁胺是一种非甾体类抗雄激素(NSAA),是达罗鲁胺的主要活性代谢产物。雄激素受体(AR)的激活对前列腺癌的生长至关重要。值得注意的是,去势抵抗性前列腺癌(CRPC)也依赖于功能性AR,目前已提出多种机制来解释这种依赖性。CRPC的已知病因包括AR基因扩增和过表达以及点突变。本文报道了一种新型AR抑制剂ODM-201的药理学特征。该抑制剂在CRPC患者的I/II期研究中显示出显著的抗肿瘤活性和良好的安全性。ODM-201是一种完全且高亲和力的AR拮抗剂,与第二代抗雄激素恩扎卢胺和ARN-509类似,它能抑制睾酮诱导的AR核转位。重要的是,ODM-201还能阻断抗雄激素疗法诱导产生的突变型雄激素受体(AR)的活性,包括赋予恩扎卢胺和ARN-509耐药性的F876L突变。此外,ODM-201在体外和去势抵抗性VCaP异种移植模型中均能抑制AR过表达的VCaP前列腺癌细胞的生长。与其他抗雄激素药物不同,ODM-201的脑渗透性极低,且不会升高小鼠血清睾酮水平。总之,ODM-201是一种强效的AR抑制剂,它通过拮抗过表达和突变的AR来克服对AR靶向疗法的耐药性。 ODM-201目前正在进行CRPC的III期临床试验。[1]
总之,ODM-201是一种高活性的新一代雄激素受体(AR)抑制剂,可拮抗已知的介导对第一代和第二代抗雄激素耐药性的AR突变体AR(F876L)、AR(W741L)和AR(T877A)。ODM-201在AR过表达细胞中也发挥拮抗作用,并抑制受体的核转位。在CRPC的非临床体外和体内模型中,ODM-201比其他已测试的抗雄激素更有效,并且不会刺激下丘脑-垂体-性腺轴的雄激素反馈环路。综上所述,这些结果表明ODM-201具有独特的特性,可能在CRPC的治疗中优于第一代和第二代抗雄激素。这些非临床研究结果已转化为在转移性 CRPC 男性患者的 1 期和 2 期临床试验中观察到的显著抗肿瘤活性以及良好的耐受性和安全性。28在这些试验中,接受每日两次、每次 700 mg 剂量治疗的初治患者中,86% 的患者出现 PSA 应答(下降 50% 或以上)。[1] ORM-15341 是一种新型化合物,其结构与任何已知的抗雄激素(包括第二代抗雄激素药物恩扎卢胺和 ARN-509)均不同。[1] ORM-15341 是 AR(F876L) 突变的完全拮抗剂,该突变通过将恩扎卢胺和 ARN-509 转化为激动剂而赋予其耐药性。[1] ORM-15341(以及 ODM-201)的脑渗透率极低,表明其通过中枢神经系统机制诱发癫痫的风险较低,而癫痫是某些其他抗雄激素的常见副作用。[1] |
| 分子式 |
C₁₉H₁₇CLN₆O₂
|
|
|---|---|---|
| 分子量 |
396.83
|
|
| 精确质量 |
396.11
|
|
| 元素分析 |
C, 57.51; H, 4.32; Cl, 8.93; N, 21.18; O, 8.06
|
|
| CAS号 |
1297537-33-7
|
|
| 相关CAS号 |
1297537-33-7;
|
|
| PubChem CID |
52919826
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
3.21
|
|
| tPSA |
116.46
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
5
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
28
|
|
| 分子复杂度/Complexity |
637
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
ClC1=C(C#N)C=CC(=C1)C1C=CN(C[C@H](C)NC(C2=CC(C(C)=O)=NN2)=O)N=1
|
|
| InChi Key |
GMBPVBVTPBWIKC-NSHDSACASA-N
|
|
| InChi Code |
InChI=1S/C19H17ClN6O2/c1-11(22-19(28)18-8-17(12(2)27)23-24-18)10-26-6-5-16(25-26)13-3-4-14(9-21)15(20)7-13/h3-8,11H,10H2,1-2H3,(H,22,28)(H,23,24)/t11-/m0/s1
|
|
| 化学名 |
3-acetyl-N-[(2S)-1-[3-(3-chloro-4-cyanophenyl)pyrazol-1-yl]propan-2-yl]-1H-pyrazole-5-carboxamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.30 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: 2.5 mg/mL (6.30 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浊液; 超声助溶。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.30 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5200 mL | 12.5999 mL | 25.1997 mL | |
| 5 mM | 0.5040 mL | 2.5200 mL | 5.0399 mL | |
| 10 mM | 0.2520 mL | 1.2600 mL | 2.5200 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。