| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
TORC1; TORC2
PRT4165 (NSC-600157) is a selective inhibitor of the Polycomb Repressive Complex 1 (PRC1), specifically targeting the E3 ubiquitin ligase activity of RING1B (a core subunit of PRC1). It inhibits RING1B-mediated monoubiquitination of histone H2A (H2Aub1) with an IC50 of ~2.5 μM (measured by in vitro H2A ubiquitination assay) [1] ; - No activity against other E3 ubiquitin ligases (e.g., MDM2, TRAF6) or histone-modifying enzymes (e.g., HDACs, HMTs) was detected at concentrations up to 20 μM [1] . |
|---|---|
| 体外研究 (In Vitro) |
Palomid 529 抑制内皮细胞增殖并增加其凋亡。 Palomid 529 对于 VEGF 驱动的内皮细胞增殖抑制的 IC50 为 20 nM,对于 bFGF 驱动的内皮细胞增殖抑制的 IC50 为 30 nM。 Palomid 529 引起内皮细胞凋亡的能力仍然存在。 Palomid 529 减少 VEGF-A 引起的 pAktS473、pGSK3S9 和 pS6 磷酸化。然而,Palomid 529 抑制 pAktS473 的效果不如 pAktT308 或磷酸化丝裂原激活蛋白激酶 (pMAPK)。 [1] Palomid 529 除了减少缺血性视网膜的增殖反应外,还能增强新形成血管的组织和结构。[1] Palomid 529 除了减少缺血性视网膜的增殖反应外,还能增强发育中血管的结构和组织。 [1] NCI-60 细胞系组证明 Palomid 529 具有强大的抗增殖活性,其生长抑制 50 (GI50) 仅<35 μM。 Palomid 529 也显着改善了放射对前列腺癌细胞 (PC-3) 的抗增殖作用。在 PC-3 细胞上,palomid 529 会产生依赖于浓度的生长抑制作用。 2μM和7μM的剂量分别抑制30%和60%的生长。 palomid 529 会降低 PC-3 中的 Bcl-2/Bax 比率,同时还能抑制辐射诱导的 p-Akt 激活。除了防止辐射引起的 Id-1 和 VEGF 过度表达外,palomid 529 还抑制辐射引起的 MMP-2 和 MMP-9 过度表达。 [2]
PRC1活性抑制(H2Aub1减少): - HeLa细胞经PRT4165(1–10 μM,24小时)处理:Western blot显示H2Aub1呈剂量依赖性减少;10 μM处理使H2Aub1水平较溶媒组降低~80%,而总H2A或RING1B蛋白水平无显著变化 [1] ; - MCF-7细胞(10 μM PRT4165,48小时):免疫荧光染色显示核内H2Aub1焦点较溶媒组减少~70% [1] ; - DNA双链断裂(DSB)修复干扰: - HeLa细胞预先用PRT4165(5 μM,2小时)处理,再给予2 Gy电离辐射(IR):Western blot显示IR后24小时,γH2AX(DSB标志物)水平较单独IR组增加~3倍;免疫荧光检测(IR后48小时)显示53BP1(DSB修复因子)焦点增加~2.5倍 [1] ; - U2OS细胞(5 μM PRT4165,24小时)+ 2 Gy IR:中性彗星实验显示尾矩(未修复DSB指标)较单独IR组增加~60% [1] ; - 抗增殖与促凋亡效应: - HeLa细胞:PRT4165(0.5–20 μM,72小时)抑制增殖,MTT法测得IC50约为5 μM;10 μM处理使克隆形成数减少~75%(克隆形成实验,10天) [1] ; - MCF-7细胞(10 μM PRT4165,48小时):Annexin V-FITC/PI染色显示凋亡率升至~45%,显著高于溶媒组的~5%;Western blot检测到cleaved PARP(凋亡标志物)增加~3倍 [1] ; - 基因表达调控: - qPCR分析(HeLa细胞,10 μM PRT4165,24小时):PRC1抑制的肿瘤抑制基因上调,包括p16INK4a(2.8倍)、p21CIP1(3.2倍)和Bax(2.5倍)(vs. 溶媒组) [1] 。 |
| 体内研究 (In Vivo) |
Palomid 529 治疗可对 Ad-VEGF-A 驱动的血管生成产生剂量依赖性抑制。 Palomid 529 对裸鼠体内 C6V10 神经胶质瘤生长的腹腔注射剂量依赖性抑制。 Palomid 529 减少 AktS473 的信号传导,但不减少 AktT308。 Palomid 529 对裸鼠体内 C6V10 神经胶质瘤生长的腹腔注射剂量依赖性抑制。 Palomid 529 减少 AktS473 的信号传导,但不减少 AktT308。 Palomid 529 降低血管通透性、血管生成和肿瘤生长。 [1] 与未治疗的小鼠相比,Palomid 529 治疗使 PC-3 荷瘤小鼠的肿瘤生长减慢了 57.1%。 [2] Palomid 529 是兔视网膜脱离 (RD) 模型中 Müller 细胞增殖、神经胶质疤痕形成和感光细胞死亡的有效抑制剂。 [3] 通过抑制 Akt 和 mTOR 信号传导,palomid 529 显着减缓小鼠体内 Brca1 缺陷肿瘤的生长。 [4]
|
| 酶活实验 |
这些蛋白质是用兔网织红细胞裂解物产生的。在平行反应中,[35S]甲硫氨酸掺入受体中,然后进行凝胶电泳和胶片曝光,监测表达并凭经验确定每个反应中使用的模板量。在最终体积为 100 mL 的 TEG 缓冲液 [10 mM Tris (pH 7.5)、1.5 mM EDTA、10% 甘油] 中,进行 Palomid 529 和雌激素受体 (ER) 之间的结合反应。每个结合反应都涉及在 0.5 nM [3H]雌二醇 (E2) 存在下使用 5 μL 体外转录翻译受体。 Palomid 529 通常在乙醇中稀释,并在 10−11 至 10−6M 范围内进行测试。通过添加 200 mL 葡聚糖包被的木炭,在 4 °C 下孵育反应过夜后测量结合的 E2。为了通过液体闪烁计数确定 cpm,将管在 4°C 下旋转 15 分钟,离心 10 分钟,并添加 150 mL 上清液。通过仅使用乙醇载体与结合的 E2 竞争,确定最大结合。每个实验使用 5 mL 未编程的兔网织红细胞裂解物作为背景对照。该数量通常代表最大计数的 10% 到 15%,是从所有值中取出的。计算出的 Ki 值绘制在数据上。至少进行了三个单独的实验。
体外H2A泛素化实验(RING1B/BMI1复合物): 1. 制备反应体系(总体积50 μL):0.5 μg重组RING1B/BMI1异二聚体(PRC1核心复合物)、1 μg纯化组蛋白H2A、0.2 μg E1泛素激活酶、0.5 μg E2泛素结合酶(UbcH5c)、2 μM泛素、50 mM Tris-HCl(pH 7.5)、10 mM MgCl₂及2 mM ATP [1] ; 2. 加入系列浓度PRT4165(0.1–20 μM)或溶媒;37°C孵育90分钟 [1] ; 3. 用5×SDS上样缓冲液终止反应(煮沸5分钟);15% SDS-PAGE分离蛋白;转移至PVDF膜;一抗(抗H2Aub1)和HRP标记二抗孵育;ECL底物显影;ImageJ定量条带强度;计算IC50(约2.5 μM) [1] ; - E3泛素连接酶选择性实验: 1. 用重组MDM2(p53 E3连接酶)+ p53底物或TRAF6(TNF信号E3连接酶)+ TRAF6底物替代RING1B/BMI1 + H2A,重复上述泛素化实验 [1] ; 2. 加入PRT4165(最高20 μM)孵育;未检测到MDM2或TRAF6活性的显著抑制(较溶媒组减少<10%) [1] 。 |
| 细胞实验 |
使用的细胞是人脐血管内皮细胞(HUVEC)。将 HUVEC 以每孔 1,000 个细胞的密度接种在 96 孔板中的完全培养基中,以进行增殖测定。 24 小时铺板后,细胞在 0.5% 血清中饥饿 24 小时,然后在含有 10 ng/mL 碱性成纤维细胞生长因子 (bFGF) 或 VEGF 的完全培养基中用 Palomid 529 处理。 48小时后使用比色法测定细胞数。结果以不存在 Palomid 529 时最大 bFGF 或 VEGF 反应的百分比形式呈现。
细胞活力实验(MTT法): 1. HeLa/MCF-7细胞以5×10³细胞/孔接种于96孔板;37°C(5% CO₂)培养过夜 [1] ; 2. 加入系列浓度PRT4165(0.5–20 μM)或溶媒;孵育72小时 [1] ; 3. 每孔加入0.5 mg/mL MTT试剂(20 μL);孵育4小时;去除培养基;加入DMSO(150 μL/孔)溶解甲臜;检测570 nm处吸光度;通过GraphPad Prism计算IC50 [1] ; - Western Blot实验: 1. HeLa/MCF-7细胞以2×10⁵细胞/孔接种于6孔板;用PRT4165(1–10 μM)处理24–48小时(DSB实验中加2 Gy IR) [1] ; 2. 含蛋白酶和磷酸酶抑制剂的RIPA缓冲液裂解细胞;BCA法定量蛋白 [1] ; 3. 每泳道上样30 μg蛋白;10–15% SDS-PAGE分离;转移至PVDF膜;5%脱脂牛奶室温封闭1小时 [1] ; 4. 一抗(H2Aub1、γH2AX、53BP1、cleaved PARP、RING1B、GAPDH)4°C孵育过夜;HRP标记二抗室温孵育1小时;ECL底物显影;ImageJ定量 [1] ; - 免疫荧光实验: 1. HeLa细胞以1×10⁴细胞/盖玻片接种;用PRT4165(5–10 μM)处理24–48小时(±2 Gy IR) [1] ; 2. 4%多聚甲醛室温固定细胞15分钟;0.5% Triton X-100透化20分钟;1% BSA室温封闭1小时 [1] ; 3. 一抗(H2Aub1、53BP1)4°C孵育过夜;Alexa Fluor标记二抗室温避光孵育1小时;DAPI染核5分钟 [1] ; 4. 共聚焦显微镜成像;计数每细胞核焦点数(每组100个细胞);计算较溶媒组的倍数变化 [1] ; - qPCR实验: 1. PRT4165处理的HeLa细胞(10 μM,24小时)用RNA提取试剂提取总RNA;逆转录合成cDNA [1] ; 2. 用基因特异性引物(p16INK4a、p21CIP1、Bax,GAPDH为内参)进行qPCR;2^(-ΔΔCt)法计算相对基因表达量 [1] |
| 动物实验 |
小鼠:在4至6周龄雌性裸鼠皮下注射1×10⁵个C6V10大鼠神经胶质瘤细胞前,先用Palomid 529(200 mg/kg/2d,腹腔注射)预处理1周。在肿瘤生长期间持续给药21天。裸鼠皮下注射U87细胞(3×10⁶/100个AL)。在注射肿瘤细胞后第3天开始,分别用微粉化的Palomid 529(P529)以50 mg和25 mg/kg/2d的剂量进行腹腔注射治疗。对照组小鼠未接受任何药物治疗。U87肿瘤生长24天。在药物治疗期间,使用游标卡尺测量肿瘤体积,并计算公式为长×宽×宽×0.53。动物被安乐死后,取出肿瘤进行免疫组织化学和免疫印迹研究。
|
| 毒性/毒理 (Toxicokinetics/TK) |
对正常细胞的体外毒性:- 人包皮成纤维细胞 (HFF):PRT4165(浓度高达 10 μM,72 小时)导致细胞活力降低 <20%(MTT 检测),表明对正常细胞的毒性较低 [1]
; |
| 参考文献 | |
| 其他信息 |
Palomid 529 已用于研究年龄相关性黄斑变性的治疗试验。
mTORC1/mTORC2 抑制剂 Palomid 529 是一种口服生物利用度高的 mTOR 复合物 1(mTOR 复合物 1;mTORC1;TOR 复合物 1;TORC1)和 mTOR 复合物 2(mTOR 复合物 2;mTORC2;TOR 复合物 2;TORC2)抑制剂,具有潜在的抗肿瘤活性。口服后,mTORC1/mTORC2 抑制剂 Palomid 529 可选择性地靶向并抑制 mTORC1 和 mTORC2,这可能导致表达 mTORC1/2 的肿瘤细胞凋亡和增殖减少。mTOR 是一种丝氨酸/苏氨酸激酶,在某些肿瘤中表达上调;它在PI3K/Akt/mTOR信号通路中发挥重要作用,而该通路在癌细胞中常常失调。 作用机制:PRT4165 (NSC-600157) 与RING1B的RING结构域结合,抑制其E3泛素连接酶活性,并降低H2Aub1的表达——H2Aub1是PRC1介导的基因沉默的关键表观遗传标记。这导致PRT4165抑制的抑癌基因重新激活,干扰DSB修复(通过损害DSB处的泛素信号传导),最终抑制癌细胞增殖并诱导其凋亡[1] ;- 研究背景:PRC1在多种癌症(例如乳腺癌、宫颈癌、肺癌)中经常过表达,并通过沉默抑癌基因促进肿瘤发生。 PRT4165 被开发为一种工具化合物,用于验证 PRC1 作为治疗靶点,并有可能与 DNA 损伤剂(例如放射线、化疗)联合使用 [1] ; |
| 分子式 |
C24H22O6
|
|---|---|
| 分子量 |
406.4279
|
| 精确质量 |
406.141
|
| 元素分析 |
C, 70.92; H, 5.46; O, 23.62
|
| CAS号 |
914913-88-5
|
| 相关CAS号 |
914913-88-5
|
| PubChem CID |
11998575
|
| 外观&性状 |
white solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
614.0±55.0 °C at 760 mmHg
|
| 闪点 |
213.4±25.0 °C
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
| 折射率 |
1.618
|
| LogP |
4.84
|
| tPSA |
78.13
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
6
|
| 重原子数目 |
30
|
| 分子复杂度/Complexity |
574
|
| 定义原子立体中心数目 |
0
|
| SMILES |
O=C1C2C(=CC=C(C(C)O)C=2)C2C(=CC(=C(C=2)OC)OCC2C=CC(OC)=CC=2)O1
|
| InChi Key |
YEAHTLOYHVWAKW-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C24H22O6/c1-14(25)16-6-9-18-19-11-22(28-3)23(12-21(19)30-24(26)20(18)10-16)29-13-15-4-7-17(27-2)8-5-15/h4-12,14,25H,13H2,1-3H3
|
| 化学名 |
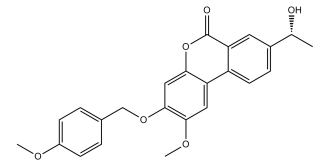
8-(1-hydroxyethyl)-2-methoxy-3-[(4-methoxyphenyl)methoxy]benzo[c]chromen-6-one
|
| 别名 |
SG 00529; -00529; SG00529; Palomid 529; Palomid-529; Palomid529; P529; P 529; P-529
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~81 mg/mL (~199.3 mM)
Water: <1 mg/mL Ethanol: <1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.15 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4604 mL | 12.3022 mL | 24.6045 mL | |
| 5 mM | 0.4921 mL | 2.4604 mL | 4.9209 mL | |
| 10 mM | 0.2460 mL | 1.2302 mL | 2.4604 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT01033721 | Completed | Drug: Palomid 529 | Age-Related Macular Degeneration | Paloma Pharmaceuticals, Inc. | June 2010 | Phase 1 |
| NCT01271270 | Completed | Drug: Palomid 529 | Age-Related Macular Degeneration | National Eye Institute (NEI) | December 20, 2010 | Phase 1 |
P529 is a derivative of a nonsteroidal estrogen antagonist that maintains antiproliferative activity on endothelial cells while no longer inhibiting ER binding. Cancer Res. 2008 Nov 15;68(22):9551-7 |
P529 inhibition of retinal neovascularization. Cancer Res. 2008 Nov 15;68(22):9551-7 |
P529 inhibits glioma cell signaling, tumor growth, and tumor angiogenesis. Cancer Res. 2008 Nov 15;68(22):9551-7 |