| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Adenosine deaminase (Ki = 2.5 pM)
Adenosine deaminase inhibitor (induces T-cell apoptosis through adenosine deaminase inhibition) [1] |
|---|---|
| 体外研究 (In Vitro) |
对于HLA相同和不相同(5/6)的同种异基因HCT,使用ECP、Pentostatin 和600 cGy TBI的联合方案,Miller等人观察到,Pentostatin 和ECP都会导致T细胞和宿主DC耗竭,并使剩余的DC和T细胞群转变为耐受性DC2和T调节群,从而导致GVHD发生率低。[1]
本研究旨在通过实验性感染伊氏锥虫的小鼠,评估3'-脱氧腺苷(虫草素)联合脱氧辅酶霉素(Pentostatin :腺苷脱氨酶抑制剂)在体外治疗的抗锥虫作用。在体外,观察到虫草素对寄生虫具有剂量依赖性的杀锥虫作用[2]。 |
| 体内研究 (In Vivo) |
喷司他丁 (2 mg/kg) 联合虫草素 (2 mg/kg) 对伊氏锥虫感染的小鼠有 100% 的效果。一些生化参数,尤其是肝酶水平的升高,伴随着肝脏和肾脏的组织学病变。喷司他丁单独对感染群体没有作用。所有犬均从第 4 天开始出现粒细胞减少症,粒细胞计数 <500 个细胞/μL。血小板减少症(<20,000 个血小板/μL)在 HCT 后第 7 天开始,最低为 3000 至 14000 个血小板/μL [1]。
在体内试验中,这两种药物分别使用和不同剂量的组合使用。单独使用这些药物对感染的小鼠没有疗效。然而,虫草素(2 mg kg-1)和戊唑醇(2 mg kg-1)的组合在伊氏锥虫感染组中是100%有效的。一些生化参数水平升高,特别是肝酶,伴有肝脏和肾脏的组织学病变。基于这些结果,我们得出结论,使用3'-脱氧腺苷与脱氧辅酶霉素的联合治疗对感染伊氏锥虫的小鼠具有疗效。然而,所测试的治疗方案导致了肝肾损伤,表现为肝毒性和肾毒性[2]。 体外光凝术(ECP)和嘌呤类似物Pentostatin 具有强大的免疫调节作用。我们评估了在用920 cGy TBI预处理后,在无关犬白细胞Ag错配造血细胞移植的犬模型中使用这些治疗方式预防GVHD的效果。我们之前在该模型中表明,36/40只狗在移植后仅接受MTX作为免疫抑制移植,40只狗中有25只患有严重的GVHD,中位生存期为21天。在目前的研究中,9只狗接受了920 cGy TBI的预处理和移植后MTX,或在-2至-1天单独使用ECP(n=5),或在-6和-5天使用ECP联合两剂Pentostatin (-4至-3天)(n=4)。九只狗中有七只成功植入。六只狗出现了严重的急性移植物抗宿主病(单独使用ECP组有四只,使用Pentostatin /戊司他丁和ECP组两只)。与历史对照犬相比,我们未能证明ECP和Pentostatin 对预防GVHD的积极影响[1]。 在DLA不匹配的犬造血细胞移植模型中,pentostatin在移植前第–4天和第–3天以4 mg/m²的剂量静脉给药,联合ECP和920 cGy TBI,之后给予甲氨蝶呤(MTX)作为移植后免疫抑制。所有犬均发生严重急性GVHD,与历史对照组相比,该联合方案未能预防GVHD。[1] |
| 细胞实验 |
混合白细胞培养(MLC)和自然杀伤(NK)细胞毒性试验[1]
如前所述,使用混合白细胞培养来评估ECP前后狗的细胞免疫功能。为了评估ECP前后NK细胞活性,如前所述进行了铬释放测定。 嵌合体分析[1] 使用基于聚合酶链式反应(PCR)的多态性(CA)n二核苷酸重复的检测方法,使用对信息性微卫星标记特异的引物,评估供体和宿主细胞的嵌合体。提取感兴趣细胞的基因组DNA,并在先前描述的条件下进行PCR。所使用的技术能够检测2.5%至97.5%的供体细胞嵌合体。 Annexin V(Ax)/PI染色检测细胞凋亡[1] 使用Annexin V结合通过流式细胞术评估暴露于ECP的细胞的凋亡,这允许检测凋亡细胞细胞表面上的磷脂酰丝氨酸。简而言之,在37°C的5%加湿气氛中孵育过夜后,根据制造商手册收获细胞,裂解,用PBS洗涤,并用Annexin V-FITC和碘化丙啶(PI)孵育。使用CellQuest Analysis软件通过流式细胞术分析细胞。每个样本至少统计了10000个事件。膜联蛋白V阳性但PI阴性的细胞处于早期凋亡,膜联蛋白Ⅴ和PI双重阳性的细胞处于晚期凋亡。结果以膜联蛋白V-FITC阳性细胞的百分比报告。 |
| 动物实验 |
DLA非相合骨髓移植[1]
所有受体犬均采用直线加速器以7 cGy/分钟的速率进行920 cGy全身照射(TBI)预处理。A1组犬在第-2天和第-1天接受体外光疗(ECP),并在第0天接受TBI;A2组犬在第-6天和第-5天接受ECP,在第-4天和第-3天静脉输注4mg/m2剂量的喷司他丁,并在第0天接受TBI(表1)。在全身麻醉下,通过插入肱骨和股骨的针头抽取DLA不相合供者的骨髓细胞,并将其保存在4°C的肝素化组织培养基中,保存时间不超过6小时。22 在全身照射(TBI)后4小时内,将采集的骨髓细胞以2.9(范围:1.9至6.1)×108个总有核细胞(TNC)/kg的中位剂量静脉输注给受者。骨髓移植当天被指定为第0天。除骨髓移植外,在第1天和第2天,受者还接受了通过白细胞分离术从骨髓供者获得的外周血白细胞层的静脉输注,中位剂量为2.3(范围:1.2至6.9)×108个TNC/kg,以确保造血植入的稳定性。移植后免疫抑制采用甲氨蝶呤(MTX),剂量为0.4 mg/kg,静脉注射,分别于移植后第1、3、6和11天给药,之后每周一次,直至第102天。 戊司他丁在移植前第-4天和第-3天静脉注射,剂量为4 mg/m²,用于接受DLA非相合骨髓移植的犬只,移植前均接受920 cGy全身照射。移植前第-6天和第-5天进行体外光疗(ECP),移植后免疫抑制方案包括MTX。监测犬只的植入情况、移植物抗宿主病(GVHD)和存活情况。[1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
口服不吸收,可穿过血脑屏障。 在人体中,单次静脉输注4 mg/m²的喷司他丁5分钟后,约90%的剂量以原形喷司他丁和/或其代谢物的形式经尿液排出,这是通过腺苷脱氨酶抑制活性测定的。 68 mL/min/m² 在少数晚期难治性癌症患者中,每日直接静脉注射0.25 mg/kg喷司他丁,持续4或5天后,血浆喷司他丁浓度约为3.2-9.7 ng/ml。血浆浓度似乎随剂量呈线性增加;在一项针对白血病患者的研究中,静脉输注0.25或1 mg/kg戊司他丁30分钟后,1小时测得的血浆戊司他丁浓度平均值分别约为0.4或1.26 μg/ml。 尚未发现血浆腺苷或脱氧腺苷的平均或绝对浓度与戊司他丁的治疗或毒性反应之间存在明显的相关性;然而,有限的数据表明,药物反应可能与淋巴母细胞中脱氧腺苷三磷酸与腺苷三磷酸的比值存在相关性。此外,据报道,血浆脱氧腺苷水平的升高与红细胞和淋巴母细胞中脱氧腺苷三磷酸的积累平行,且毒性似乎与红细胞中脱氧腺苷三磷酸与腺苷三磷酸的比值相关。动物研究表明,喷司他丁可迅速分布至所有身体组织,但药物在不同组织中的积累程度似乎因物种而异。小鼠腹腔注射后,肾脏、肝脏和脾脏中的药物浓度最高。犬静脉注射后,喷司他丁的组织浓度与组织腺苷脱氨酶活性成正比,肺、脾脏、胰腺、心脏、肝脏和空肠中的浓度最高。据报道,喷司他丁通过与其他核苷类药物相同的易化转运系统或通过简单扩散进入红细胞;虽然尚未明确药物从细胞中的外排情况,但喷司他汀的作用时间进程(例如,腺苷脱氨酶抑制)在不同类型的细胞(例如,淋巴细胞、红细胞)中有所不同。有限的动物和人体数据表明,喷司他汀在脑脊液中的分布相对较差,脑脊液峰值浓度平均约为同期血浆浓度的10%。在一例6岁白血病患者中,连续3天每日静脉注射0.25 mg/kg喷司他汀,首次给药4小时后,采用酶抑制滴定法测得血清和脑脊液(通过腰椎穿刺)中的喷司他汀浓度分别约为147 ng/ml和19 ng/ml;第三次给药后一小时,相应的血清和脑脊液浓度分别约为 241 ng/ml 和 35 ng/ml。 有关戊司他丁(共 7 种)的更多吸收、分布和排泄(完整)数据,请访问 HSDB 记录页面。 代谢/代谢物 主要在肝脏代谢,但仅有少量代谢。 主要在肝脏代谢,但仅有少量代谢。 消除途径:在人体中,单次静脉输注 4 mg/m² 戊司他丁 5 分钟后,约 90% 的剂量以原形戊司他丁和/或代谢物的形式经尿液排出,通过腺苷脱氨酶抑制活性测定。 半衰期:5.7 小时(范围为 2.6 至 16 小时) 生物半衰期 5.7 小时(范围为 2.6 至 16 小时)在健康个体中,单次静脉注射 4 mg/m² 戊司他丁(5 分钟内),据报道其分布半衰期和末端消除半衰期平均分别为 11 分钟和 5.7 小时。在一项针对少数患者进行的多次给药研究中,36 个疗程的戊司他丁(4 mg/m² 静脉注射)治疗后,据报道其分布半衰期和末端消除半衰期平均分别为 9.6 分钟(范围:3.1-48.5 分钟)和 4.9 小时。 在其他针对少数晚期癌症患者的研究中,单次静脉注射 0.1 或 0.25 mg/kg 戊司他丁后,分布半衰期平均为 17-85 分钟,末端消除半衰期平均为 2.6-15 小时。 在肾功能不全(肌酐清除率小于 60 ml/min)的患者中,戊司他丁的半衰期平均约为 18 小时。 |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
喷司他丁是一种强效的腺苷脱氨酶 (ADA) 过渡态抑制剂,其活性在淋巴系统细胞中最为显著。T 细胞的 ADA 活性高于 B 细胞,T 细胞恶性肿瘤的活性高于 B 细胞恶性肿瘤。抑制腺苷或脱氧腺苷的分解代谢所导致的细胞毒性被认为是由细胞内 dATP 水平升高引起的,dATP 可通过抑制核糖核苷酸还原酶来阻断 DNA 合成。细胞内活化导致 dATP 以假嘌呤碱基的形式掺入 DNA 中。此外,喷司他丁掺入 RNA 也会产生细胞毒性作用。细胞毒性具有细胞周期阶段特异性(S期)。 毒性数据 小鼠(静脉注射):LD50 122 mg/kg LD50=128 mg/kg(小鼠) 相互作用 有限的数据表明,戊司他丁(每2周4 mg/m²)与氟达拉滨(主要为每天10 mg/m²,连续4天,每28天为一个周期)联合治疗,可能与严重的和/或致命的肺毒性(例如,肺炎)有关。在一项研究中,6名接受戊司他丁和别嘌醇联合治疗的难治性慢性淋巴细胞白血病患者中有4名报告出现了此类毒性反应。 尽管单独使用戊司他丁或别嘌醇治疗均与皮疹的发生有关,但有限的证据表明,与单独使用戊司他丁治疗相比,在难治性毛细胞白血病患者中同时使用这两种药物并不会增加皮疹的发生率。然而,在少数同时接受戊司他丁和别嘌醇治疗的患者中观察到了其他毒性反应,包括肾功能或肝功能异常。……据报道,一名患者在同时接受戊司他丁和别嘌醇治疗期间发生了致命的超敏性血管炎;然而,尚未确定与这些药物的因果关系。 喷司他丁可抑制阿糖腺苷的降解,并增强其在细胞培养和实验诱导白血病动物模型中的细胞毒性。此外,有限的急性白血病患者数据表明,与单独使用喷司他丁相比,联合使用这些药物可能导致血浆阿糖腺苷浓度和/或半衰期升高,以及毒性更大。尽管有报道称,少数接受阿糖腺苷和喷司他丁联合治疗的急性T细胞淋巴母细胞白血病患者病情有所改善和/或缓解。 |
| 参考文献 |
|
| 其他信息 |
治疗用途
抗生素;抗肿瘤药;酶抑制剂;免疫抑制剂 抗生素、抗肿瘤药;酶抑制剂;免疫抑制剂 抗肿瘤药 喷司他丁用于治疗对干扰素α治疗反应不佳或病情进展的毛细胞白血病(白血病性网状内皮增生症)。喷司他丁已被美国食品药品监督管理局 (FDA) 认定为治疗该疾病的孤儿药。喷司他丁可使约 80-100% 的毛细胞白血病患者出现具有临床意义的肿瘤消退或病情稳定(完全缓解或部分缓解),包括既往未接受治疗的患者(例如,未接受脾切除术或其他治疗的患者)以及脾切除术和/或其他药物(例如,干扰素、抗肿瘤药物)治疗无效的患者(例如,病情进展的患者)。在干扰素α难治性毛细胞白血病患者的临床研究中,喷司他丁治疗的完全缓解通常定义为:外周血和骨髓中毛细胞清除;器官肿大和淋巴结肿大恢复正常;血红蛋白浓度恢复至至少 12 g/dL,血小板计数恢复至至少 100,000/mm³,粒细胞计数恢复至至少 1500/mm³。部分缓解定义为外周血和骨髓中毛细胞数量减少超过50%,以及器官肿大和淋巴结肿大减少超过50%;部分缓解的血液学参数与完全缓解的相同。据报道,在接受喷司他丁4 mg/m²静脉注射,每两周一次,持续3个月的有限患者中,观察到总体完全缓解率为58%,部分缓解率为28%;缓解的患者继续接受3-9个月的治疗。据报道,这些患者的中位缓解时间为4.7个月(范围:2.9-24.1个月)。据报道,在两项毛细胞白血病患者的临床研究中,喷司他丁治疗的中位缓解持续时间分别超过7.7个月和15.2个月,约15-20%的初始缓解患者出现复发。对于脾切除术后病情进展的患者,由于迄今为止干扰素α的治疗经验更为丰富,喷司他丁通常被视为干扰素α的替代疗法或干扰素难治性疾病的二线治疗方案。然而,两种药物或其他疗法的优劣仍有待确定。 有关喷司他丁(共10种)的更多治疗用途(完整)数据,请访问HSDB记录页面。 药物警告 喷司他丁是一种毒性药物,治疗指数低,如果没有出现毒性反应,则不太可能产生治疗反应。该药必须在具有细胞毒性药物治疗经验的医生的持续监督下使用。大多数(但并非全部)喷司他丁的不良反应如果及时发现是可逆的。如果在喷司他丁治疗期间出现严重不良反应,应停止用药或减少剂量,并采取适当的措施。如果需要重新使用喷司他汀,应谨慎,充分考虑是否还需要继续用药,并注意毒性可能复发。 体能状态较差的患者似乎更容易出现喷司他汀的毒性反应,因此只有在预期获益大于潜在风险时才应使用该药。 在喷司他汀治疗期间和治疗后,必须频繁且仔细地监测血液学功能,尤其是在骨髓抑制风险较高的患者(例如毛细胞白血病患者)的最初几个疗程中。对这类患者启动喷司他汀治疗可能导致严重的骨髓抑制。如果严重的粒细胞减少症持续到喷司他汀治疗的初始疗程之后,应检查患者,包括骨髓检查,以确定其疾病状态。此外,对于患有这种白血病的患者,应定期监测外周血毛细胞的出现情况,以评估患者对治疗的反应。可能需要每隔 2 至 3 个月进行一次骨髓穿刺和活检。 接受喷司他丁治疗的患者应密切观察非血液学(例如神经系统)毒性的迹象。如果出现严重不良反应,应暂停用药并根据指示采取适当的纠正措施。如果患者出现神经系统毒性的证据,应暂时停止或停止喷司他丁治疗。 有关喷司他丁(共 11 条)的更多药物警告(完整)数据,请访问 HSDB 记录页面。 药效学 喷司他丁是一种抗肿瘤抗代谢药物,用于治疗多种类型的白血病,包括急性非淋巴细胞白血病和毛细胞白血病。抗代谢药物会伪装成嘌呤或嘧啶——而嘌呤或嘧啶是 DNA 的组成单元。它们阻止这些物质在细胞周期的“S”期掺入DNA,从而阻止正常的细胞发育和分裂。它是天然存在的嘌呤碱基次黄嘌呤和鸟嘌呤的6-硫嘌呤类似物。细胞内活化会导致其作为假嘌呤碱基掺入DNA。此外,它还会掺入RNA,从而产生细胞毒性作用。细胞毒性具有细胞周期阶段特异性(S期)。 喷司他丁是一种嘌呤类似物,可通过抑制腺苷脱氨酶诱导T细胞凋亡。它已被用于造血干细胞移植的预处理方案中,以清除宿主T细胞并预防移植物排斥反应和移植物抗宿主病(GVHD)。在本研究中,在犬DLA不匹配的移植模型中,喷司他丁与ECP联合使用并未预防严重的急性GVHD。[1] |
| 分子式 |
C11H16N4O4
|
|---|---|
| 分子量 |
268.2691
|
| 精确质量 |
268.117
|
| 元素分析 |
C, 49.25; H, 6.01; N, 20.88; O, 23.86
|
| CAS号 |
53910-25-1
|
| PubChem CID |
439693
|
| 外观&性状 |
White crystals from methanol/water
White to off-white solid |
| 密度 |
1.8±0.1 g/cm3
|
| 沸点 |
673.1±65.0 °C at 760 mmHg
|
| 熔点 |
220-225ºC
|
| 闪点 |
360.9±34.3 °C
|
| 蒸汽压 |
0.0±2.2 mmHg at 25°C
|
| 折射率 |
1.793
|
| LogP |
-2.16
|
| tPSA |
112.13
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
19
|
| 分子复杂度/Complexity |
356
|
| 定义原子立体中心数目 |
4
|
| SMILES |
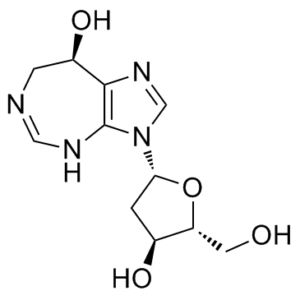
O1[C@]([H])(C([H])([H])O[H])[C@]([H])(C([H])([H])[C@]1([H])N1C([H])=NC2[C@@]([H])(C([H])([H])N=C([H])N([H])C1=2)O[H])O[H]
|
| InChi Key |
FPVKHBSQESCIEP-KDXUFGMBSA-N
|
| InChi Code |
InChI=1S/C11H16N4O4/c16-3-8-6(17)1-9(19-8)15-5-14-10-7(18)2-12-4-13-11(10)15/h4-9,16-18H,1-3H2,(H,12,13)/t6-,7+,8+,9-/m0/s1
|
| 化学名 |
(R)-3-((2S,4S,5R)-4-hydroxy-5-(hydroxymethyl)tetrahydrofuran-2-yl)-3,6,7,8-tetrahydroimidazo[4,5-d][1,3]diazepin-8-ol
|
| 别名 |
Deoxycoformycin; CI825; CI-825; Deoxycoformycin; Nipent; 53910-25-1; 2'-Deoxycoformycin; PD-ADI; Pentostatina; Pentostatine; CI 825; PD81565; PD-81565; PD 81565; covidarabine; deoxycoformycin; pentostatine. brand name: Nipent.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~100 mg/mL (~372.76 mM)
DMSO : ≥ 50 mg/mL (~186.38 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (7.75 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (7.75 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (7.75 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.7276 mL | 18.6379 mL | 37.2759 mL | |
| 5 mM | 0.7455 mL | 3.7276 mL | 7.4552 mL | |
| 10 mM | 0.3728 mL | 1.8638 mL | 3.7276 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。