| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
| 靶点 |
hNav1.7: (IC50 =11 nM); cynNav1.7 (IC50 =12 nM); dogNav1.7 (IC50 =13 nM); ratNav1.7 (IC50 = 171 nM), musNav1.7 (IC50 = 8 nM)
PF-05089771 targets voltage-gated sodium channel Nav1.7 (IC50 = 17 nM for human Nav1.7 in HEK293 cells under fast-inactivated conditions; IC50 = 14 nM for human Nav1.7 in HEK293 cells under slow-inactivated conditions) [2] PF-05089771 targets Nav1.7 [1] PF-05089771 targets Nav1.7[3] |
|---|---|
| 体外研究 (In Vitro) |
研究发现,PF-05089771 对 TTX 敏感 (TTX-S) 通道表现出一系列选择性(Nav1.2 的 10 倍到 Nav1.3 和 Nav1.4 的 900 倍),并且超过 1000-对河豚毒素抗性 (TTX-R) Nav1.5 和 Nav1.8 通道选择性倍数 (IC50 >10 μM)[1]。大部分 TTX-S 电流(75.5 ± 10.5%,n = 5,图 5D)被 PF-05089771 (30 nM) 阻断,而在 100 nM 时实现完全阻断[1]。
1. PF-05089771可强效且选择性抑制稳定表达人Nav1.7的HEK293细胞中的Nav1.7电流,对快失活(IC50=17 nM)和慢失活(IC50=14 nM)状态的Nav1.7通道抑制效价相当;该抑制作用具有电压依赖性,在去极化电位下效价更高 [2] 2. 浓度高达10 μM时,PF-05089771对其他电压门控钠通道亚型(Nav1.1、Nav1.2、Nav1.3、Nav1.4、Nav1.5、Nav1.6、Nav1.8、Nav1.9)仅表现出微弱抑制,证实其对Nav1.7具有高度亚型选择性 [2] 3. 在分离的小鼠背根神经节(DRG)神经元中,PF-05089771(100 nM)可抑制小直径伤害性神经元的动作电位发放,降低轴突传导速度,并抑制DRG-感觉神经元突触处的突触前神经递质释放 [1] 4. PF-05089771(10-1000 nM)以浓度依赖的方式降低小鼠DRG伤害性神经元中Nav1.7介导的钠电流幅度,1000 nM时可完全抑制该电流 [1] |
| 体内研究 (In Vivo) |
与赋形剂相比,口服或吸入PF-05089771在不改变呼吸频率的剂量下可抑制约50-60%的咳嗽[3]。
1. 在豚鼠中,口服给予PF-05089771(3、10、30 mg/kg)可剂量依赖性降低柠檬酸诱导的咳嗽频率(30 mg/kg时最大抑制率达65%,p<0.001 vs 溶媒组);镇咳作用在给药后1小时即可观察到,且持续长达6小时 [3] 2. PF-05089771(30 mg/kg,口服)不影响豚鼠的基线呼吸频率、潮气量或分钟通气量,表明其对呼吸功能无脱靶效应 [3] 3. 在小鼠中,腹腔注射PF-05089771(10 mg/kg)可减轻福尔马林诱导的疼痛模型中的伤害性行为(第一阶段:减少40%,p<0.01;第二阶段:减少55%,p<0.001 vs 溶媒组),并延长热板实验中的痛阈潜伏期(延长80%,p<0.001 vs 溶媒组) [1] 4. PF-05089771(10 mg/kg,腹腔注射)可抑制小鼠外周伤害性轴突中的动作电位传导,该结果通过隐神经电生理记录验证 [1] |
| 酶活实验 |
PF-05089771的抑制谱表明,去极化后结构域IV VSD的构象变化是必要的,并且足以揭示PF-05089781与之相互作用的高亲和力结合位点,将通道稳定在非导电构象中,从该构象恢复缓慢[2]。
1. 对稳定表达人Nav1.7(及其他Nav亚型)的HEK293细胞开展全细胞膜片钳电生理实验,评估PF-05089771对快/慢失活状态Nav1.7通道的抑制作用;将细胞电压钳制在-120 mV,通过500 ms预脉冲至-10 mV诱导快失活,通过10分钟预脉冲至-60 mV诱导慢失活;施加0 mV测试脉冲后检测钠电流峰值幅度,依据浓度-反应曲线计算IC50值 [2] |
| 细胞实验 |
电压钳HEK细胞或小鼠DRG神经元连续超充细胞外溶液(ECS),该溶液含有(mM):30 NaCl、110胆碱Cl、3 KCl、0.8 MgCl2、1.8 CaCl2、0.05 CdCl2、10葡萄糖、10 HEPES、5蔗糖(300–310 mOsm,用TEA-OH滴定至pH 7.4)。贴片移液管(细胞内)溶液(ICS)含有(mM):5 NaCl、135 CsF、10 CsCl、2 MgATP、10 HEPES、5 EGTA(290–300 mOsm,用KOH滴定至pH 7.2)。对于人类DRG记录,使用以下溶液(ECS单位为mM):150 NaCl、4 BaCl、2 CaCl2、1 MgCl2、0.1 CdCl2、10葡萄糖、10 HEPES(用Na-OH滴定至pH 7.3的300-310 mOsm)。ICS(mM):140 CsF、10 NaCl、1 EGTA、1 MgCl2、10 HEPES、10葡萄糖(290–300 mOsm,用Cs-OH滴定至pH 7.3)。串联电阻补偿通常应用于至少75%。采集前,从Vm=-120 mV重复施加20ms至0 mV的脉冲(0.05 Hz),直到获得稳定的电流响应。所有实验均在室温(21-24°C)下进行。在HEK 293细胞系中通过在-120 mV的电压钳位产生IC50值,然后进入失活的V0.5 5秒以积累化合物结合。随后,在20ms测试步骤至0mV之前,100 ms返回至-120 mV。具有大TTX-S电流的细胞(>5 nA小鼠,>8 nA人类)和串联电阻值大于15 MΩ或可变串联电阻的细胞从分析中省略[2]。
1. 分离并培养小鼠DRG神经元;采用全细胞膜片钳记录技术,检测经PF-05089771(10-1000 nM)处理的小直径伤害性神经元的动作电位发放、轴突传导速度和钠电流幅度;通过记录DRG-感觉神经元突触处的兴奋性突触后电流(EPSCs),评估药物处理后的突触传递功能 [1] 2. 培养稳定表达人Nav1.7的HEK293细胞;将细胞接种于玻璃盖玻片,给予1 nM至10 μM浓度的PF-05089771处理10分钟后进行电生理记录;采用电压钳方案区分Nav1.7通道的快失活和慢失活状态 [2] |
| 动物实验 |
豚鼠被随机分为若干组。第一组豚鼠在吸入辣椒素气雾剂(25 μM)5分钟前2.5小时,经口(po)注射NaV1.7抑制剂PF-05089771(15 mg/kg,溶于1 ml水中)或溶剂(DMSO)。药物溶液或溶剂以1 mL的剂量随机经口注射到体重约350 g的豚鼠体内。每次使用前,药物溶液均需涡旋混匀。缓慢给药以确保动物吞服全部剂量的药物溶液。由于本实验采用非配对设计,10天后比较各组在未进行任何干预的情况下,辣椒素诱发的咳嗽情况,结果未观察到显著差异(数据未显示)。在第二组实验中,动物先吸入PF-05089771(100 μM)或溶剂的气溶胶10分钟,再吸入含有PF-05089771(100 μM)或溶剂的辣椒素(25 μM)气溶胶5分钟。该实验采用配对设计,两次咳嗽刺激间隔10天。动物随机接受PF-05089771或溶剂的刺激。我们还设置了第三组较小的动物,采用类似的实验方案,但PF-05089771的浓度较低,为10 μM。为了探究NaV1.7抑制剂对呼吸频率的潜在影响,我们统计了1分钟内的呼吸周期数。呼吸频率的测定时间为PF-05089771吸入后的最后一分钟。在全身口服给药PF-05089771的实验中,由于在吸入辣椒素的第一分钟内16只动物未检测到咳嗽,而4只动物仅检测到一次咳嗽[3],因此测定了吸入辣椒素第一分钟内的呼吸频率。
1. 豚鼠咳嗽模型:使用雄性Dunkin-Hartley豚鼠(250-350 g);将PF-05089771溶解于0.5%甲基纤维素/0.1%吐温80水溶液中,并在柠檬酸刺激前1小时以3、10、30 mg/kg的剂量(体积:10 mL/kg)口服给药;将柠檬酸(0.4 M)雾化10分钟,并在刺激后15分钟内计数咳嗽频率;采用全身容积描记法测量呼吸参数(呼吸频率、潮气量、分钟通气量)[3] 2. 小鼠疼痛模型:使用 C57BL/6 小鼠(20-25 g);将 PF-05089771 溶解于 10% DMSO/90% 生理盐水中,并在注射福尔马林(20 μL 5% 福尔马林注射到后爪)或热板试验(55°C)前 30 分钟腹腔注射 10 mg/kg(体积:10 mL/kg);记录福尔马林诱导的伤害性行为(舔舐/啃咬)60分钟(第一阶段:0-10分钟,第二阶段:15-60分钟),并测量热板潜伏期(最大截断值:60秒)[1] 3. 小鼠轴突传导测定:C57BL/6小鼠用异氟烷麻醉;腹腔注射PF-05089771(10 mg/kg),并在给药后30、60和90分钟进行隐神经动作电位的电生理记录,以测量传导速度和振幅[1] |
| 参考文献 |
[1]. Alexandrou AJ, et al. Subtype-Selective Small Molecule Inhibitors Reveal a Fundamental Role for Nav1.7 in Nociceptor Electrogenesis, Axonal Conduction and Presynaptic Release. PLoS One. 2016 Apr 6;11(4):e0152405.
[2]. Theile JW, et al. The Selective Nav1.7 Inhibitor, PF-05089771, Interacts Equivalently with Fast and Slow Inactivated Nav1.7 Channels. Mol Pharmacol. 2016 Nov;90(5):540-548. [3]. The effect of the voltage-gated sodium channel NaV1.7 blocker PF-05089771 on cough in the guinea pig. Respir Physiol Neurobiol. 2022 May:299:103856. |
| 其他信息 |
PF-05089771 正在进行临床试验 NCT01529671(PF-05089771 在健康受试者和膝骨关节炎患者中的安全性和耐受性研究)。
1. Nav1.7 是一种电压门控钠通道亚型,主要表达于外周伤害性神经元(背根神经节,DRG),其功能障碍与先天性痛觉缺失和慢性疼痛疾病相关[1] 2. PF-05089771 是一种选择性 Nav1.7 抑制剂,可与 Nav1.7 通道的失活状态结合,阻断钠离子内流,从而抑制伤害感受器的电生理、轴突传导和突触前神经递质释放[1] 3. 与大多数 Nav1.7 抑制剂不同,PF-05089771 的相互作用与快速和慢速失活的 Nav1.7 通道等效,这可能有助于其持续的镇痛和止咳作用 [2] 4. Nav1.7 在气道感觉神经中表达,PF-05089771 对 Nav1.7 的抑制作用可降低豚鼠的咳嗽反射敏感性,提示其可能具有治疗慢性咳嗽的潜在用途 [3] 5. PF-05089771 对 Nav1.7 具有高度亚型选择性,最大限度地减少了对心脏 (Nav1.5) 和中枢神经系统 (Nav1.1/1.2/1.6) 钠通道的脱靶效应 [2] |
| 分子式 |
C18H12CL2FN5O3S2
|
|
|---|---|---|
| 分子量 |
500.34
|
|
| 精确质量 |
498.974
|
|
| 元素分析 |
C, 43.21; H, 2.42; Cl, 14.17; F, 3.80; N, 14.00; O, 9.59; S, 12.82
|
|
| CAS号 |
1235403-62-9
|
|
| 相关CAS号 |
PF 05089771 tosylate;1430806-04-4
|
|
| PubChem CID |
46840946
|
|
| 外观&性状 |
White to off-white solid
|
|
| LogP |
6.889
|
|
| tPSA |
159.61
|
|
| 氢键供体(HBD)数目 |
3
|
|
| 氢键受体(HBA)数目 |
9
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
31
|
|
| 分子复杂度/Complexity |
721
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
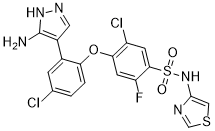
ClC1=C([H])C(=C(C([H])=C1OC1C([H])=C([H])C(=C([H])C=1C1C([H])=NN([H])C=1N([H])[H])Cl)F)S(N([H])C1=C([H])SC([H])=N1)(=O)=O
|
|
| InChi Key |
ZYSCOUXLBXGGIM-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C18H12Cl2FN5O3S2/c19-9-1-2-14(10(3-9)11-6-24-25-18(11)22)29-15-5-13(21)16(4-12(15)20)31(27,28)26-17-7-30-8-23-17/h1-8,26H,(H3,22,24,25)
|
|
| 化学名 |
4-(2-(5-amino-1H-pyrazol-4-yl)-4-chlorophenoxy)-5-chloro-2-fluoro-N-(thiazol-4-yl)benzenesulfonamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (5.00 mM) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.25 mg/mL (4.50 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 22.5 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.25 mg/mL (4.50 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.9986 mL | 9.9932 mL | 19.9864 mL | |
| 5 mM | 0.3997 mL | 1.9986 mL | 3.9973 mL | |
| 10 mM | 0.1999 mL | 0.9993 mL | 1.9986 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|---|
Time course of block by PF-05089771 is independent of the availability of kinetically defined inactivated states.Mol Pharmacol.2016 Nov;90(5):540-548. |
Onset of inhibition develops over similar time course using different conditioning trains with equal time at 0 mV.Mol Pharmacol.2016 Nov;90(5):540-548. |