| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
hNav1.7: (IC50 =11 nM); cynNav1.7 (IC50 =12 nM); dogNav1.7 (IC50 =13 nM); ratNav1.7 (IC50 = 171 nM), musNav1.7 (IC50 = 8 nM)
Nav1.7 (voltage-gated sodium channel subtype 1.7) (IC50 = 11 nM for human Nav1.7; IC50 = 12 nM for cynomolgus Nav1.7; IC50 = 13 nM for dog Nav1.7; IC50 = 171 nM for rat Nav1.7; IC50 = 8 nM for mouse Nav1.7) [1][2] |
|---|---|
| 体外研究 (In Vitro) |
研究发现,PF-05089771 对 TTX 敏感 (TTX-S) 通道表现出一系列选择性(Nav1.2 的 10 倍到 Nav1.3 和 Nav1.4 的 900 倍),并且超过 1000-对河豚毒素抗性 (TTX-R) Nav1.5 和 Nav1.8 通道选择性倍数 (IC50 >10 μM)[1]。 PF-05089771 (30 nM) 抑制大部分 TTX-S 电流(75.5 ± 10.5%,n = 5),100 nM 导致完全阻断[1]。
状态依赖性抑制:PF-05089771优先结合Nav1.7的失活状态(IC50 = 11 nM),而与静息状态通道的结合亲和力极低(IC50 ~ 10 μM)[2][3] - 结合动力学:在100 nM浓度下,对0 mV失活的通道抑制形成的时间常数为67 ± 4秒,对-60 mV失活的通道为90 ± 7秒。从抑制状态恢复缓慢且不完全[2] - 对快失活和慢失活状态的等效作用:无论通道主要处于快失活还是慢失活状态,抑制速率相似,表明PF-05089771不优先靶向特定的失活状态[2] - 作用机制:结合Nav1.7第四结构域(DIV)电压感应结构域(VSD)的细胞外表面,稳定通道的非导电构象[2][6] - 特异性:对Nav1.7的选择性高于其他钠通道亚型(Nav1.1、Nav1.2、Nav1.3、Nav1.4、Nav1.5、Nav1.6、Nav1.8、Nav1.9)[1][3] |
| 体内研究 (In Vivo) |
与赋形剂相比,口服或吸入PF-05089771在不改变呼吸频率的剂量下可抑制约50-60%的咳嗽[3]。
啮齿类动物镇痛作用: - 鞘内给药在多种疼痛模型(伤害性疼痛、炎症性疼痛、神经病理性疼痛、吗啡耐受疼痛以及急慢性瘙痒)中产生快速(15分钟内)且持久(>4小时)的镇痛效果[11] - 纳洛酮预处理可逆转其镇痛作用,表明内源性阿片通路参与其中[11] - 在小鼠炎症性疼痛模型中,全身给药可减轻机械性痛觉过敏和热痛觉过敏[1][3] - 豚鼠镇咳作用: - 剂量依赖性地抑制清醒豚鼠的辣椒素诱导咳嗽[5][10] - 静脉注射3 mg/kg剂量可使咳嗽频率降低50%[5] - 镇咳作用通过抑制气道迷走神经传入C纤维介导[5][7] |
| 酶活实验 |
PF-05089771的抑制谱表明,去极化后结构域IV VSD的构象变化是必要的,并且足以揭示PF-05089781与之相互作用的高亲和力结合位点,将通道稳定在非导电构象中,从该构象恢复缓慢[2]。
Nav1.7通道抑制检测: - 使用全细胞膜片钳技术对在HEK293细胞或爪蟾卵母细胞中表达的重组人Nav1.7通道进行电压钳制[1][2] - 实验方案包括: 1. 8秒的条件性脉冲至导致50%失活的膜电位(V0.5,通常为-84 ± 1 mV) 2. 2毫秒的超极化脉冲至-120 mV以部分解除失活 3. 20毫秒的测试脉冲至0 mV以测量峰值钠电流[2] - 在细胞外施加不同浓度(0.01-10 μM)的PF-05089771,测量钠电流的抑制情况[2] - 从浓度-响应曲线计算IC50值[1][2] |
| 细胞实验 |
电压钳HEK细胞或小鼠DRG神经元连续超充细胞外溶液(ECS),该溶液含有(mM):30 NaCl、110胆碱Cl、3 KCl、0.8 MgCl2、1.8 CaCl2、0.05 CdCl2、10葡萄糖、10 HEPES、5蔗糖(300–310 mOsm,用TEA-OH滴定至pH 7.4)。贴片移液管(细胞内)溶液(ICS)含有(mM):5 NaCl、135 CsF、10 CsCl、2 MgATP、10 HEPES、5 EGTA(290–300 mOsm,用KOH滴定至pH 7.2)。对于人类DRG记录,使用以下溶液(ECS单位为mM):150 NaCl、4 BaCl、2 CaCl2、1 MgCl2、0.1 CdCl2、10葡萄糖、10 HEPES(用Na-OH滴定至pH 7.3的300-310 mOsm)。ICS(mM):140 CsF、10 NaCl、1 EGTA、1 MgCl2、10 HEPES、10葡萄糖(290–300 mOsm,用Cs-OH滴定至pH 7.3)。串联电阻补偿通常应用于至少75%。采集前,从Vm=-120 mV重复施加20ms至0 mV的脉冲(0.05 Hz),直到获得稳定的电流响应。所有实验均在室温(21-24°C)下进行。在HEK 293细胞系中通过在-120 mV的电压钳位产生IC50值,然后进入失活的V0.5 5秒以积累化合物结合。随后,在20ms测试步骤至0mV之前,100 ms返回至-120 mV。具有大TTX-S电流的细胞(>5 nA小鼠,>8 nA人类)和串联电阻值大于15 MΩ或可变串联电阻的细胞从分析中省略[2]。
Nav1.7表达细胞活力/增殖检测: - 将稳定转染人Nav1.7的人胚肾(HEK293)细胞以5,000个/孔接种于96孔板[1] - 24小时后,加入浓度范围为0.01-10 μM的PF-05089771,孵育24-72小时[1] - 使用MTT或ATP检测法评估细胞活力,在570 nm处测量吸光度[1] |
| 动物实验 |
豚鼠被随机分为若干组。第一组豚鼠在吸入辣椒素气雾剂(25 μM)5分钟前2.5小时,经口(po)注射NaV1.7抑制剂PF-05089771(15 mg/kg,溶于1 ml水中)或溶剂(DMSO)。药物溶液或溶剂以1 mL的剂量随机经口注射到体重约350 g的豚鼠体内。每次使用前,药物溶液均需涡旋混匀。缓慢给药以确保动物吞服全部剂量的药物溶液。由于本实验采用非配对设计,10天后比较各组在未进行任何干预的情况下,辣椒素诱发的咳嗽情况,结果未观察到显著差异(数据未显示)。在第二组实验中,动物先吸入PF-05089771(100 μM)或溶剂的气溶胶10分钟,再吸入含有PF-05089771(100 μM)或溶剂的辣椒素(25 μM)气溶胶5分钟。该实验采用配对设计,两次咳嗽刺激间隔10天。动物随机接受PF-05089771或溶剂的刺激。我们还设置了第三组较小的动物,采用类似的实验方案,但PF-05089771的浓度较低,为10 μM。为了探究NaV1.7抑制剂对呼吸频率的潜在影响,我们统计了1分钟内的呼吸周期数。呼吸频率的测定时间为PF-05089771吸入后的最后一分钟。在全身口服给药PF-05089771的实验中,由于在吸入辣椒素的第一分钟内,16只动物未检测到咳嗽,4只动物仅检测到一次咳嗽[3],因此测定了吸入辣椒素第一分钟内的呼吸频率。
1. 在啮齿动物疼痛模型中的镇痛效果: - 受试者:雄性Sprague-Dawley大鼠或C57BL/6小鼠(6-8周龄)[1][11] - 疼痛模型: - 炎症性疼痛:通过足底注射弗氏完全佐剂(CFA)或角叉菜胶诱导后爪疼痛[1] - 神经性疼痛:通过慢性压迫性损伤(CCI)或脊神经结扎诱导[11] - 给药途径: - 鞘内注射:PF-05089771溶于无菌生理盐水(1-10 mmol/L)。将 PF-05089771(μg/10 μL)用 30 号针头注射到腰椎蛛网膜下腔 [11] - 全身给药途径:将 PF-05089771 溶解于载体(10% DMSO + 40% PEG 400 + 50% 生理盐水)中,以 0.1-10 mg/kg 的剂量进行静脉或口服给药 [1] - 疗效评估: - 机械性痛觉过敏:将冯·弗雷丝丝应用于后爪足底;使用上下法确定 50% 缩爪阈值 [1] - 热痛觉过敏:将热板(52°C)或辐射热(哈格里夫斯装置)应用于后爪;记录撤药潜伏期[1] ### 2. 在豚鼠咳嗽模型中的镇咳疗效: - 受试者:雄性哈特利豚鼠(300-500 g)[5] - 诱导咳嗽: - 使用雾化器将清醒的豚鼠暴露于雾化辣椒素(10 μM 生理盐水)30 秒[5] - 记录辣椒素暴露后 5 分钟内的咳嗽情况[5] - 给药: - 将溶于载体(生理盐水 + 10% DMSO)的 PF-05089771 经耳缘静脉静脉注射,剂量为 0.3-3 mg/kg,或口服,剂量为 10-30 mg/kg[5] - 给药 30 分钟后,用辣椒素激发动物[5] - 疗效评估: - 比较治疗组和赋形剂对照组的咳嗽频率(每5分钟咳嗽次数)[5] - 咳嗽抑制率计算公式为:(1 - (治疗组咳嗽频率/对照组咳嗽频率)) × 100% [5] |
| 药代性质 (ADME/PK) |
吸收:在啮齿动物和非人灵长类动物中具有口服生物利用度[3][4]
- 分布: - 易于穿过血脑屏障 (BBB) [3][11] - 大鼠的分布容积 (Vd) 约为 10 L/kg,表明组织分布广泛[4] - 代谢: - 主要通过肝细胞色素 P450 酶代谢,其中 CYP3A4 是主要同工酶[4] - 在人肝微粒体中,固有清除率 (CLint) 约为 50 μL/min/mg 蛋白[4] - 消除: - 大鼠的末端半衰期 (t1/2) 约为 2-3 小时[4] - 在人体中,口服给药后 4-6 小时内达到最大浓度 (Tmax)[4] - 主要以代谢物的形式经尿液排泄,其中不到 5% 的剂量以原形排出[4] |
| 毒性/毒理 (Toxicokinetics/TK) |
急性毒性:在啮齿动物中,静脉注射后 LD50 > 100 mg/kg [3]
- 心血管安全性: - 在治疗浓度下,PF-05089771 对心脏钠通道 (Nav1.5) 的影响极小,IC50 > 10 μM,从而降低了 QT 间期延长和心律失常的风险 [3][6] - 在体外心脏动作电位测定中,浓度高达 1 μM 时,对动作电位时程或传导速度没有显著影响 [3] - 神经系统安全性: - 全身给药时,治疗剂量下药物对中枢神经系统的渗透有限,最大限度地降低了镇静、认知障碍或运动功能障碍的可能性 [3][11] - 在治疗浓度下,对骨骼肌功能没有显著影响,因为骨骼肌主要表达 Nav1.4,而 PF-05089771 对 Nav1.4 的抑制作用不显著 [3] |
| 参考文献 |
[1]. Alexandrou AJ, et al. Subtype-Selective Small Molecule Inhibitors Reveal a Fundamental Role for Nav1.7 in Nociceptor Electrogenesis, Axonal Conduction and Presynaptic Release. PLoS One. 2016 Apr 6;11(4):e0152405.
[2]. Theile JW, et al. The Selective Nav1.7 Inhibitor, PF-05089771, Interacts Equivalently with Fast and Slow Inactivated Nav1.7 Channels. Mol Pharmacol. 2016 Nov;90(5):540-548. [3]. The effect of the voltage-gated sodium channel NaV1.7 blocker PF-05089771 on cough in the guinea pig. Respir Physiol Neurobiol. 2022 May:299:103856. |
| 其他信息 |
治疗潜力:
- 疼痛性疾病:神经性疼痛、炎症性疼痛、术后疼痛、癌症疼痛和偏头痛[1][3][11] - 呼吸系统疾病:与哮喘、慢性阻塞性肺疾病 (COPD) 和特发性肺纤维化相关的慢性咳嗽[5][7][10] - 瘙痒性疾病:与特应性皮炎、银屑病和尿毒症相关的瘙痒[11] - 构效关系: - PF-05089771 是一种带有环烷基醚取代基的芳基磺酰胺衍生物,该取代基赋予其对 Nav1.7 的高选择性[3][6] - 磺酰胺基团对于与 Nav1.7 的细胞外电压门控结构域 (VSD) 结合至关重要[6] - 临床开发状态: - 已完成在健康志愿者中进行的 I 期临床试验,结果表明其安全性良好,且药代动力学[4][5] - 针对慢性疼痛和咳嗽患者的II期临床试验正在进行或已完成[4][5] - 与其他钠通道阻滞剂相比的优势: - 选择性作用于主要表达于外周感觉神经元的Nav1.7通道,从而最大限度地减少中枢和心脏副作用[1][3] - 状态依赖性抑制优先靶向反复放电的过度兴奋神经元,这正是疼痛和咳嗽的特征[2][6] - 由于与通道缓慢解离,作用持续时间长,因此可以减少给药频率[2] |
| 分子式 |
C25H20CL2FN5O6S3
|
|
|---|---|---|
| 分子量 |
672.54
|
|
| 精确质量 |
670.993
|
|
| CAS号 |
1430806-04-4
|
|
| 相关CAS号 |
PF 05089771;1235403-62-9
|
|
| PubChem CID |
71554187
|
|
| 外观&性状 |
Typically exists as solid at room temperature
|
|
| tPSA |
222
|
|
| 氢键供体(HBD)数目 |
4
|
|
| 氢键受体(HBA)数目 |
12
|
|
| 可旋转键数目(RBC) |
7
|
|
| 重原子数目 |
42
|
|
| 分子复杂度/Complexity |
927
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
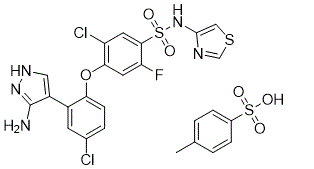
C1C(Cl)=C(OC2C(C3C(N)=NNC=3)=CC(Cl)=CC=2)C=C(F)C=1S(=O)(=O)NC1=CSC=N1.C1C=C(C)C=CC=1S(=O)(=O)O
|
|
| InChi Key |
NVKBPDYKPNYMDR-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C18H12Cl2FN5O3S2.C7H8O3S/c19-9-1-2-14(10(3-9)11-6-24-25-18(11)22)29-15-5-13(21)16(4-12(15)20)31(27,28)26-17-7-30-8-23-17;1-6-2-4-7(5-3-6)11(8,9)10/h1-8,26H,(H3,22,24,25);2-5H,1H3,(H,8,9,10)
|
|
| 化学名 |
4-[2-(5-amino-1H-pyrazol-4-yl)-4-chlorophenoxy]-5-chloro-2-fluoro-N-(1,3-thiazol-4-yl)benzenesulfonamide;4-methylbenzenesulfonic acid
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
注意: 如下所列的是一些常用的体内动物实验溶解配方,主要用于溶解难溶或不溶于水的产品(水溶度<1 mg/mL)。 建议您先取少量样品进行尝试,如该配方可行,再根据实验需求增加样品量。
注射用配方
注射用配方1: DMSO : Tween 80: Saline = 10 : 5 : 85 (如: 100 μL DMSO → 50 μL Tween 80 → 850 μL Saline)(IP/IV/IM/SC等) *生理盐水/Saline的制备:将0.9g氯化钠/NaCl溶解在100 mL ddH ₂ O中,得到澄清溶液。 注射用配方 2: DMSO : PEG300 :Tween 80 : Saline = 10 : 40 : 5 : 45 (如: 100 μL DMSO → 400 μL PEG300 → 50 μL Tween 80 → 450 μL Saline) 注射用配方 3: DMSO : Corn oil = 10 : 90 (如: 100 μL DMSO → 900 μL Corn oil) 示例: 以注射用配方 3 (DMSO : Corn oil = 10 : 90) 为例说明, 如果要配制 1 mL 2.5 mg/mL的工作液, 您可以取 100 μL 25 mg/mL 澄清的 DMSO 储备液,加到 900 μL Corn oil/玉米油中, 混合均匀。 View More
注射用配方 4: DMSO : 20% SBE-β-CD in Saline = 10 : 90 [如:100 μL DMSO → 900 μL (20% SBE-β-CD in Saline)] 口服配方
口服配方 1: 悬浮于0.5% CMC Na (羧甲基纤维素钠) 口服配方 2: 悬浮于0.5% Carboxymethyl cellulose (羧甲基纤维素) 示例: 以口服配方 1 (悬浮于 0.5% CMC Na)为例说明, 如果要配制 100 mL 2.5 mg/mL 的工作液, 您可以先取0.5g CMC Na并将其溶解于100mL ddH2O中,得到0.5%CMC-Na澄清溶液;然后将250 mg待测化合物加到100 mL前述 0.5%CMC Na溶液中,得到悬浮液。 View More
口服配方 3: 溶解于 PEG400 (聚乙二醇400) 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.4869 mL | 7.4345 mL | 14.8690 mL | |
| 5 mM | 0.2974 mL | 1.4869 mL | 2.9738 mL | |
| 10 mM | 0.1487 mL | 0.7435 mL | 1.4869 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 Inhibition of human Nav1.7 by PF-05089771 develops and recovers slowly.Mol Pharmacol.2016 Nov;90(5):540-548. Inhibition of human Nav1.7 by PF-05089771 develops and recovers slowly.Mol Pharmacol.2016 Nov;90(5):540-548. |
|---|
 Time course of block by PF-05089771 is independent of the availability of kinetically defined inactivated states.Mol Pharmacol.2016 Nov;90(5):540-548. |
 Onset of inhibition develops over similar time course using different conditioning trains with equal time at 0 mV.Mol Pharmacol.2016 Nov;90(5):540-548. |