| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
BRD2-BD1 (Kd = 1.6 nM); BRD3-BD1 (Kd = 2.1 nM); BRD4-BD1 (Kd = 1.7 nM); 5 nM (BRDT-BD1), 5.9 nM (BRD2-BD2), 6.2 nM (BRD3-BD2), 6.1 nM (BRD4-BD2), 120 nM (BRDT-BD2), ∼100 nM (CBP), ∼100 nM (EP300)
BRD4 [1] BET family proteins (structurally distinct BET inhibitor targeting the inducible ZA channel) [1] |
|---|---|
| 体外研究 (In Vitro) |
PLX51107 的 BD1 的 Kd 值分别为 1.6、2.1、1.7 和 5 nM,BRD2、BRD3 和 BRD4 的 Kd 值分别为 5.9、6.2、6.1 和 120 nM,BRDT 的 Kd 值分别为 5.9、6.2、6.1 和 120 nM。此外,PLX51107 与 EP300 和 CBP 的溴结构域相互作用(Kd,在 100 nM 范围内)。 PLX51107 (0.156-10 μM) 可防止原发性慢性淋巴细胞白血病 (CLL) 细胞在接触 CpG 时增殖。此外,PLX51107 还可降低 c-MYC 水平,增加 p21 和 IκBα 积累,并修饰促凋亡蛋白和抗凋亡蛋白。 CLL 驱动基因受 PLX51107 特异性调控 [1]。
PLX51107对CpG刺激的原代CLL细胞具有剂量依赖性增殖抑制作用,连续处理72小时或处理4小时后洗脱均有效;其 potency与其他BET抑制剂(OTX015、JQ1、iBET762)相当[1] 在CLL患者来源的CD19⁺细胞(n=13)与人类Hs27或小鼠9–15c骨髓来源基质细胞的共培养体系中,PLX51107(1、2、5μM)处理72小时后,通过膜联蛋白-V/碘化丙啶(Annexin-V/PI)染色检测,可降低CLL细胞存活率[1] PLX51107处理恶性B细胞系(MEC-1、OCI-LY1)72小时后,呈现剂量依赖性增殖抑制(各细胞系p<0.001),疗效与其他BET抑制剂相近[1] 1μM PLX51107处理CpG刺激的CLL细胞4小时后,通过GeneChip Human Transcriptome Array HTA 2.0芯片分析发现基因表达发生改变,CLL相关基因下调,且与B细胞受体信号通路及致癌通路相关的经典通路富集[1] 实时定量PCR和蛋白质印迹法证实,PLX51107(0.1、1、2μM)可下调CpG刺激的CLL细胞中BTK、IKZF1、cMYC、IKZF3、ZBTB17的表达,上调HEXIM1的表达(处理24小时和48小时,n=5)[1] 染色质免疫沉淀测序(ChIP-seq)分析显示,PLX51107可降低CLL患者来源细胞中BRD4在增强子区域的占位,改变RNA聚合酶II(RNA Pol II)在基因启动子和基因体上的占位,并调节BRD4调控的超级增强子相关基因的表达[1] |
| 体内研究 (In Vivo) |
在 Ba/F3(小鼠 IL3 依赖性前 B 细胞系)脾肿大小鼠模型中,PLX51107(2 mg/kg,口服)使脾肿大减少 75%,结果与 25 mg/kg OTX015 相似。每日口服一次时,PLX51107(20 mg/kg,每日一次,口服)在里氏转化 (RT) 和侵袭性慢性淋巴细胞白血病 (CLL) 模型中显示出强大的抗白血病作用 [1]。
在Ba/F3诱导的小鼠脾肿大模型中,PLX51107的 potency是OTX015的10倍[1] 在MV4-11肿瘤异种移植模型中,单次给予PLX51107后,其诱导的转录变化(以HEXIM1为标志)持续时间超过血浆药物浓度存在时间;药代动力学参数为AUC₀–₂₄h=90,100 ng•h/mL(205μM•hr),终末半衰期(T₁/₂)=2.8小时[1] 对患有晚期白血病的Eμ-TCL1小鼠,口服给予PLX51107(20 mg/kg,每日一次,连续8天),可减少全身循环和脾脏中的白血病细胞,并调节cMYC、P21、BTK、IKZF1、IKZF3和TCL1A的蛋白水平[1] 在Eμ-TCL1过继转移模型中,白血病发病时给予PLX51107(20 mg/kg,每日一次,口服灌胃),可显著延长总生存期(中位生存期:93天 vs 对照组34天,p<0.0001),减少循环白血病外周血淋巴细胞(PBLs),降低脾脏重量,并通过HE和Ki67染色证实脾脏、肺和血液中的淋巴细胞耗竭[1] 在移植了Eμ-TCL1白血病脾细胞的C57BL/6小鼠中,PLX51107(20 mg/kg,每日一次,口服灌胃)可将中位生存期延长至41天,显著长于对照组(21天,p=0.024)和伊布替尼组(32天,p=0.049)[1] 在Eμ-Myc/TCL1过继转移的高级别淋巴瘤模型(类似Richter转化)中,PLX51107(20 mg/kg,每日一次,口服灌胃)可延长生存期,降低外周血白细胞计数,减少CD19/CD5/CD45⁺ PBLs,减轻脾脏和淋巴结重量;HE和Ki67染色显示组织架构保留,非典型肿瘤淋巴细胞耗竭[1] |
| 酶活实验 |
通过共晶体结构分析确定PLX51107与BRD4-BD1的结合模式;该化合物源自4-氮杂吲哚骨架,可穿过ZA通道并与BRD4-BD1的Lys91形成盐桥,诱导的构象变化与乙酰化RelA acK310肽段引起的构象变化相似[1]
对比PLX51107与OTX015和BRD4-BD1的结合相互作用,阐明其BET抑制活性的结构基础[1] |
| 细胞实验 |
ChIP-Seq与数据处理[1]
原代CLL细胞(每组1E7个细胞)分别用载体(DMSO)、1μM PLX51107(含或不含CpG寡核苷酸(3.2 μM))处理4小时。细胞用1%甲醛固定15分钟,用0.125 M甘氨酸猝灭。通过添加裂解缓冲液分离染色质,然后用Dounce均质机破坏。对裂解物进行超声处理,将DNA剪切至300-500 bp的平均长度。有关详细的交叉链接过程,请参阅补充信息。利用抗BRD4、H3K27ac和RNA Pol II的4μg抗体分离基因组DNA目标区域。配合物被洗涤,用SDS缓冲液从珠子中洗脱,并进行RNase和蛋白酶K处理。65°C孵育过夜逆转交联,用苯酚-氯仿提取和乙醇沉淀纯化ChIP DNA。 用梯度浓度的PLX51107、OTX015、JQ1或iBET762连续处理CpG刺激的原代CLL细胞72小时,或处理4小时后洗脱;评估细胞增殖情况以明确剂量依赖性抑制效应[1] 将CLL患者来源的CD19⁺细胞与骨髓来源基质细胞(Hs27或9–15c)共培养,加入PLX51107(1、2、5μM)处理72小时,通过Annexin-V/PI染色检测细胞存活率[1] 用梯度浓度的PLX51107及其他BET抑制剂处理恶性B细胞系(MEC-1、OCI-LY1)72小时;检测细胞增殖情况以对比疗效[1] 用1μM PLX51107或DMSO处理CpG刺激的CLL细胞4小时;通过GeneChip Human Transcriptome Array HTA 2.0芯片分析和实时定量PCR检测基因表达变化[1] 对经PLX51107处理的CLL细胞进行ChIP-seq实验,检测BRD4和H3K27ac的结合情况及RNA Pol II的占位;分析增强子活性和转录调控的变化[1] 通过蛋白质印迹法检测PLX51107处理的CpG刺激CLL细胞中BTK、IKZF1、cMYC、IKZF3、ZBTB17、HEXIM1等蛋白的表达水平[1] |
| 动物实验 |
20 mg/kg;qd,po
Ba/F3 脾肿大小鼠模型。为进行移植研究,将 1E7 个细胞通过尾静脉注射移植到 C57BL/6 野生型小鼠体内,这些细胞来源于患有活动性疾病的 Eμ-TCL1 或 Eμ-Myc/TCL1 小鼠的脾细胞。在白血病发作时(Eμ-TCL1:≥10% CD19/CD5/CD45 阳性循环细胞;Eμ-Myc/TCL1:白细胞计数 ≥ 8 和/或 ≥ 5% CD19/CD5/CD45 阳性循环细胞),将小鼠随机分组,并按所示方式进行治疗。载体 = 10% N-甲基-2-吡咯烷酮 (NMP) 加稀释剂(40% PEG400、5% TPGS、5% 泊洛沙姆 407 和 50% 水)。当小鼠达到早期移除标准(ERC:体重减轻>20%、运动能力受损、脾肿大和明显的肿瘤肿块)时,对其进行处死,并收集组织进行进一步分析。[1] 建立Ba/F3诱导的小鼠脾肿大模型;给予PLX51107和OTX015,比较它们在减轻脾肿大方面的效力。[1] 建立MV4-11肿瘤异种移植小鼠模型;单次给予PLX51107,在不同时间点收集血浆样本,以确定药代动力学参数(AUC₀–₂₄h、T₁/₂),并检测肿瘤中HEXIM1的表达以评估转录效应。[1] 使用患有晚期白血病的Eμ-TCL1小鼠;根据白血病 PBL 和脾脏触诊评分对小鼠进行分层,然后给予 PLX51107(20 mg/kg,每日一次,灌胃)8 天;收集外周血、脾脏和组织样本,以评估白血病细胞负荷和蛋白质表达 [1] 通过将白血病细胞移植到野生型小鼠中建立 Eμ-TCL1 过继转移模型;在白血病发作时将小鼠随机分为载体组或 PLX51107(20 mg/kg,每日一次,灌胃)组,监测 150 天的存活率和白血病 PBL,并对脾脏、肺和血液样本进行 HE 和 Ki67 染色 [1] 将 Eμ-TCL1 白血病脾细胞移植到 C57BL/6 小鼠中;在白血病发作时,用PLX51107(20 mg/kg,每日一次,灌胃)、伊布替尼或载体治疗小鼠;监测总生存期以比较治疗效果[1] 建立Eμ-Myc/TCL1过继转移高级别淋巴瘤模型;在疾病发作时(≥5% CD19/CD5/CD45⁺ PBL 和/或白细胞计数升高)给予PLX51107(20 mg/kg,每日一次,灌胃);监测生存期、白细胞计数和 PBL,并对脾脏和淋巴结样本进行HE染色和Ki67染色[1] |
| 药代性质 (ADME/PK) |
在MV4-11肿瘤异种移植小鼠中单次给药后,PLX51107的AUC₀–₂₄h为90,100 ng•h/mL (205 μM•hr),末端半衰期(T₁/₂)为2.8 h [1]
|
| 参考文献 | |
| 其他信息 |
PLX51107 是一种强效且选择性的溴结构域和末端结构域 (BET) 蛋白家族抑制剂。PLX51107 目前正在临床试验 NCT04022785(PLX51107 联合阿扎胞苷治疗急性髓系白血病或骨髓增生异常综合征患者)中进行研究。
BRD4 抑制剂 PLX51107 是一种溴结构域蛋白 4 (BRD4) 抑制剂,具有潜在的抗肿瘤活性。给药后,BRD4 抑制剂 PLX51107 与 BRD4 蛋白溴结构域中的乙酰化赖氨酸识别基序结合,从而阻止 BRD4 与组蛋白上的乙酰化赖氨酸结合。这会破坏染色质重塑和基因表达。抑制某些促生长基因的表达可能导致BRD4过表达肿瘤细胞凋亡和增殖抑制。BRD4是人溴结构域和末端外结构域(BET)蛋白家族的成员,是一种转录调节因子,在某些肿瘤细胞中过表达,并在细胞增殖中发挥重要作用。 溴结构域和末端外结构域(BET)蛋白家族是癌症中基因表达的关键调节因子。本文中,我们利用BRD4谱分析来识别参与慢性淋巴细胞白血病(CLL)发病机制的关键通路。BRD4在CLL中过表达,并且富集于CLL中上调或新表达的基因附近,这些基因在疾病的发病机制和进展中具有已知功能。这些基因,包括B细胞受体(BCR)信号通路的关键成员,为这种治疗方法在其他类型癌症中识别新靶点提供了理论依据。此外,我们描述了PLX51107,一种结构独特的BET抑制剂,具有新颖的体外和体内药理学特性,在CLL的临床前模型中,其疗效可与BCR信号通路药物媲美甚至超越。本文中,BRD4参与CLL核心转录程序的发现,为PLX51107作为CLL表观遗传疗法的临床研究以及BRD4谱分析在其他癌症中的应用提供了强有力的理论依据。意义:迄今为止,尚缺乏关于BRD4在CLL中功能的研究。通过整合基因组学、功能学和药理学分析,我们揭示了BRD4调控的CLL核心转录程序的存在,并提出了临床前概念验证研究,证实BET抑制作为一种表观遗传学方法,可用于靶向CLL中的BCR信号通路。Cancer Discov; 8(4); 458-77. ©2018 AACR。本文在“本期亮点”栏目中重点介绍,第1-10页。 371.[1] PLX51107是一种新型的、结构独特的BET抑制剂,其非苯二氮卓类骨架源自PLX5981(修饰的4-氮杂吲哚骨架)[1] 它靶向BET家族蛋白的诱导型ZA通道,其结合模式与已知的BET抑制剂(如OTX015)不同[1] PLX51107调节CLL中BRD4调控的核心转录程序,靶向包括B细胞受体信号通路在内的关键通路,并在临床前CLL模型中模拟或超越BCR信号通路药物的疗效[1] 该药物在侵袭性CLL和里氏转化(Richter's Transformation)临床前模型中显示出强大的抗白血病作用,支持其作为CLL表观遗传疗法的潜力[1] PLX51107诱导的转录变化肿瘤的持续时间超过了其在血浆中的存在时间,表明其具有持续的药效学作用[1] |
| 分子式 |
C26H22N4O3
|
|
|---|---|---|
| 分子量 |
438.477885723114
|
|
| 精确质量 |
438.169
|
|
| 元素分析 |
C, 71.22; H, 5.06; N, 12.78; O, 10.95
|
|
| CAS号 |
1627929-55-8
|
|
| 相关CAS号 |
|
|
| PubChem CID |
90448953
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
4
|
|
| tPSA |
94
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
5
|
|
| 重原子数目 |
33
|
|
| 分子复杂度/Complexity |
684
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
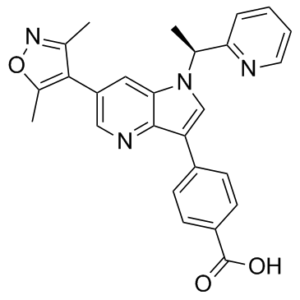
O1C(C)=C(C(C)=N1)C1=CN=C2C(C3C=CC(C(=O)O)=CC=3)=CN(C2=C1)[C@H](C1C=CC=CN=1)C
|
|
| InChi Key |
AMSUHYUVOVCWTP-INIZCTEOSA-N
|
|
| InChi Code |
InChI=1S/C26H22N4O3/c1-15-24(17(3)33-29-15)20-12-23-25(28-13-20)21(18-7-9-19(10-8-18)26(31)32)14-30(23)16(2)22-6-4-5-11-27-22/h4-14,16H,1-3H3,(H,31,32)/t16-/m0/s1
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.70 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.70 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.70 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2806 mL | 11.4030 mL | 22.8061 mL | |
| 5 mM | 0.4561 mL | 2.2806 mL | 4.5612 mL | |
| 10 mM | 0.2281 mL | 1.1403 mL | 2.2806 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Scaffold-based discovery and cellular profile of PLX51107 as a nonbenzodiazepine BET inhibitor targeting the inducible ZA channel.Cancer Discov.2018 Apr;8(4):458-477. |
|---|
Cytotoxic effect of BET inhibition in malignant B-cell lines and CLL patient-derived B cells is independent of survival signals.Cancer Discov.2018 Apr;8(4):458-477. |
Epigenetic characterization of BET inhibition in primary CLL.Cancer Discov.2018 Apr;8(4):458-477. |
Targeting BRD4 with PLX51107 proves potent antileukemic effects in disease models of aggressive CLL and RT.Cancer Discov.2018 Apr;8(4):458-477. |
|---|
PLX51107 demonstratesin vivoantitumor effects in a preclinical model of aggressive leukemia/lymphoma.Cancer Discov.2018 Apr;8(4):458-477. |
BRD4 inhibition modulates key CLL pathways.Cancer Discov.2018 Apr;8(4):458-477. |