| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| Other Sizes |
|
| 靶点 |
Proton pump[1]
Zastaprazan is a potassium-competitive acid blocker (P-CAB) that inhibits the gastric H+/K+-ATPase (proton pump). It binds reversibly and competitively to both active and inactive proton pumps. [1] |
|---|---|
| 体外研究 (In Vitro) |
作用机制描述如下:与质子泵抑制剂不同,Zastaprazan无需酸激活,可直接抑制质子泵,无论其活化状态如何。其代谢不依赖CYP2C19,且具有酸稳定性,无需肠溶包衣。[1]
Zastaprazan是一种小分子药物。其国际非专利名中包含的词干 "-prazan" 表明该药属于质子泵抑制剂,且其作用不依赖于酸激活。目前,Zastaprazan正在一项临床试验(NCT05814809)中接受评估,该研究旨在考察其在健康成年志愿者中的安全性和药代动力学特征。该药物的单同位素分子量为362.21 Da。 |
| 体内研究 (In Vivo) |
在一项健康志愿者的I期研究中(引用),Zastaprazan显示出强效的胃酸抑制作用,给药后2小时内胃内pH>4,并可维持24小时的酸抑制,呈剂量依赖性。[1]
在本项针对糜烂性食管炎患者的III期研究中,Zastaprazan 20 mg每日一次,持续最多8周,其8周累积愈合率(全分析集)为97.92%(141/144),4周愈合率为95.14%(137/144)。4周愈合率显著高于埃索美拉唑40 mg组(87.68%,P = 0.026)。[1] 在基线LA分级为B/C/D的患者中,Zastaprazan组的4周和8周愈合率数值上均高于埃索美拉唑组(4周:91.84% vs 78.72%;8周:95.92% vs 89.36%)。[1] 通过反流性疾病问卷和GERD相关生活质量评分评估的症状反应显示,Zastaprazan治疗较基线有显著改善,与埃索美拉唑相当。[1] Zastaprazan组血清胃泌素水平从基线(45.3 ± 87.0 pg/mL)至治疗结束时(114.9 ± 116.2 pg/mL)显著升高(P < 0.0001)。升高幅度略高于埃索美拉唑组(P = 0.047),但在治疗结束后2周均恢复至基线水平。[1] |
| 动物实验 |
研究设计与方法:[1]
这项III期、多中心、随机、双盲、非劣效性试验纳入了300名经内镜确诊的糜烂性食管炎患者。受试者被随机分配接受每日一次20 mg的扎他普拉赞或40 mg的埃索美拉唑治疗,疗程最长为8周。主要终点是第8周时经内镜确诊的糜烂性食管炎愈合患者的累积比例。次要终点包括第4周时的愈合率、症状缓解情况和生活质量指标。此外,还评估了安全性以及血清胃泌素水平的变化。 主要发现[1] 在完整分析集中,第 8 周扎他普拉赞组的累积愈合率为 97.92% (141/144),埃索美拉唑组为 94.93% (131/138) (P=0.178)。第 4 周时,扎他普拉赞组的愈合率显著高于埃索美拉唑组 (95.14% [137/144] vs. 87.68% [121/138];P=0.026)。在符合方案分析中,两组在第 4 周或第 8 周的愈合率、症状缓解、生活质量评估或总体安全性方面均未观察到统计学意义上的显著差异。两组患者在治疗期间血清胃泌素水平均有所升高,组间差异显著(P=0.047),但停止治疗后均恢复至基线水平。 |
| 参考文献 |
| 分子式 |
C22H26N4O
|
|---|---|
| 分子量 |
362.468044757843
|
| 精确质量 |
362.21
|
| 元素分析 |
C, 72.90; H, 7.23; N, 15.46; O, 4.41
|
| CAS号 |
2133852-18-1
|
| 相关CAS号 |
2936619-43-9 (citrate)
|
| PubChem CID |
138622158
|
| 外观&性状 |
White to off-white solid powder
|
| LogP |
4.4
|
| tPSA |
49.6
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
27
|
| 分子复杂度/Complexity |
526
|
| 定义原子立体中心数目 |
0
|
| SMILES |
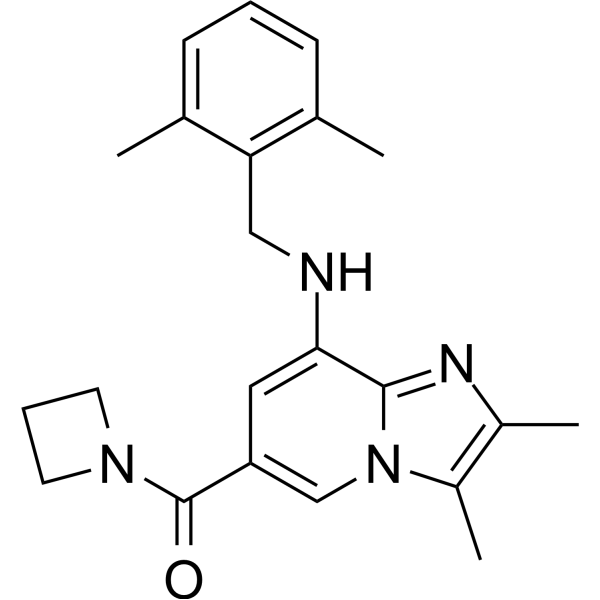
O=C(C1C=C(C2=NC(C)=C(C)N2C=1)NCC1C(C)=CC=CC=1C)N1CCC1
|
| InChi Key |
FEQFUBYYZYQTOJ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C22H26N4O/c1-14-7-5-8-15(2)19(14)12-23-20-11-18(22(27)25-9-6-10-25)13-26-17(4)16(3)24-21(20)26/h5,7-8,11,13,23H,6,9-10,12H2,1-4H3
|
| 化学名 |
azetidin-1-yl-[8-[(2,6-dimethylphenyl)methylamino]-2,3-dimethylimidazo[1,2-a]pyridin-6-yl]methanone
|
| 别名 |
Zastaprazan; 2133852-18-1; Zastaprazan [INN]; W9S9KZX5MD; Zastaprazan (INN);
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 33.33 mg/mL (91.95 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.90 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.90 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.7588 mL | 13.7942 mL | 27.5885 mL | |
| 5 mM | 0.5518 mL | 2.7588 mL | 5.5177 mL | |
| 10 mM | 0.2759 mL | 1.3794 mL | 2.7588 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。