| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 药代性质 (ADME/PK) |
吸收、分布和排泄
L-脯氨酸经胃肠道吸收。摄入的膳食蛋白质由于胃内低pH值而变性。蛋白质的变性和展开使其链易于被蛋白酶水解。高达15%的膳食蛋白质可被胃蛋白酶在胃中水解成肽和氨基酸。在十二指肠和小肠中,消化通过水解酶(例如胰蛋白酶、糜蛋白酶、弹性蛋白酶、羧肽酶)继续进行。由此产生的肽和氨基酸混合物随后通过氨基酸以及二肽和三肽的特异性载体系统转运至黏膜细胞。消化产物被迅速吸收。与其他氨基酸一样,L-脯氨酸在回肠和远端空肠被吸收。 吸收的肽进一步水解生成游离氨基酸,这些氨基酸通过黏膜细胞内的特定载体系统分泌到门静脉血中。或者,它们在细胞内代谢。吸收的氨基酸进入肝脏,一部分氨基酸在那里被利用。剩余的氨基酸进入体循环,被外周组织利用。L-脯氨酸通过主动转运从肠道黏膜表面到达浆膜表面。其吸收机制是离子梯度吸收。所有L-氨基酸的吸收都是通过钠离子依赖的载体介导过程进行的。这种转运依赖于ATP提供的能量。据报道,正常受试者血浆中L-脯氨酸的浓度约为168 μM/L ± 60 mM/L,该浓度是在健康志愿者空腹过夜后采集的血浆样本中测得的。与大多数营养物质一样,血浆中L-脯氨酸的浓度受体内平衡的调节。多种激素(例如甲状腺激素、儿茶酚胺和生长激素)在疾病状态下可能影响血浆氨基酸水平。然而,在生理状态下,它们的影响可能微乎其微。不过,皮质醇和胰高血糖素组成的拮抗激素系统会影响参与糖异生的氨基酸(例如L-脯氨酸)的血液水平。 由于肾脏滤过的氨基酸会被主动重吸收,因此体内氨基酸的丢失量极少。皮肤的丢失也微乎其微。由于哺乳动物体内没有氨基酸的长期储存机制,过量的氨基酸会被降解,主要在肝脏中降解。氨基酸的代谢包括去除氨基,氨基被转化为尿素并随尿液排出体外。去除氨基后,剩余的氨基酸可作为能量来源或用于合成其他内源性物质。 /氨基酸/ 代谢 / 代谢物 肝脏 L-脯氨酸与其他几种氨基酸一样,遵循相同的代谢途径。因此,L-脯氨酸的代谢由整个代谢途径描述。该途径(也称为“鸟氨酸和脯氨酸代谢”)描述了人体内精氨酸、鸟氨酸、脯氨酸、瓜氨酸和谷氨酸的共代谢。精氨酸由瓜氨酸在胞质酶精氨琥珀酸合成酶 (ASS) 和精氨琥珀酸裂解酶 (ASL) 的连续作用下合成。瓜氨酸可通过脯氨酸或谷氨酰胺/谷氨酸的分解代谢从鸟氨酸衍生而来。许多由鸟氨酸生成脯氨酸和谷氨酸所需的反应都位于线粒体中。脯氨酸由谷氨酸及其直接前体1-吡咯啉-5-羧酸生物合成而来。精氨酸、谷氨酰胺和脯氨酸之间的代谢途径是双向的。因此,这些氨基酸的净利用或生成高度依赖于细胞类型和发育阶段。从全身层面来看,精氨酸的合成主要通过肠-肾轴进行。小肠上皮细胞主要利用谷氨酰胺和谷氨酸合成瓜氨酸,并与肾脏近端小管细胞协同作用,后者从血液循环中吸收瓜氨酸并将其转化为精氨酸,精氨酸随后返回血液循环。因此,小肠或肾脏功能受损会降低内源性精氨酸的合成,从而增加膳食需求。脯氨酸和精氨酸都是蛋白质合成所需的氨基酸,它们分别通过脯氨酰tRNA和精氨酰tRNA掺入蛋白质中,而脯氨酰tRNA和精氨酰tRNA则分别由各自的tRNA合成酶合成。精氨酸还可以通过中间体胍基乙酸作为肌酸和磷酸肌酸合成的前体。精氨酸/脯氨酸代谢途径的关键成分是鸟氨酸。在小肠上皮细胞中,鸟氨酸主要用于合成瓜氨酸和精氨酸;在门静脉周围的肝细胞中,鸟氨酸主要作为尿素循环的中间体;在中央静脉周围的肝细胞中,鸟氨酸用于合成谷氨酸和谷氨酰胺;而在许多外周组织中,鸟氨酸用于合成谷氨酸和脯氨酸。 |
|---|---|
| 毒性/毒理 (Toxicokinetics/TK) |
毒性概述
识别和用途:L-脯氨酸为固体。它用于生物化学和营养研究、微生物学检测、培养基、实验室试剂和膳食补充剂。它也用于注射剂或输液制剂。人体暴露和毒性:目前尚无相关数据。动物研究:在一项为期30天的研究中,一组7只雌性大鼠每天饮用含50 mg/kg体重L-脯氨酸的水。另设10只大鼠作为对照组。30天后,所有动物均进行称重、解剖,并进行全面的肉眼检查。对肝脏和肾脏进行组织病理学和显微镜检查。采集血清样本用于测定酶活性以及肌酐和总蛋白浓度。与对照组相比,每日给予大鼠50 mg/kg体重L-脯氨酸未观察到任何治疗相关效应。在20种常见氨基酸中,仅脯氨酸能增强鼠伤寒沙门氏菌TA98在大鼠肝微粒体中测得的诱变活性。在鼠伤寒沙门氏菌回复突变试验中,浓度高达1000 mg/mL的L-脯氨酸,无论是否经过代谢活化,在多种鼠伤寒沙门氏菌菌株(TA92、TA97、TA98、TA100、TA102、TA1530、TA1531、TA1532、TA1535、TA1537、TA1538和TA1964)中均未观察到回复突变。生态毒性研究:与镉处理的植物相比,脯氨酸处理的植物根和叶中抗氧化酶(超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶)活性更高。脯氨酸在植物应对各种环境胁迫中发挥着重要作用。例如,补充脯氨酸可以减轻幼年橄榄树暴露于镉胁迫下的有害影响。 脯氨酸在肾脏中经L-脯氨酸氧化酶的作用,开环氧化生成L-谷氨酸,从而参与糖原合成。L-鸟氨酸和L-谷氨酸经由L-谷氨酸-γ-半醛转化为L-脯氨酸。L-脯氨酸大量存在于胶原蛋白中,并与关节和腱索的功能密切相关。 相互作用 脯氨酸在植物应对各种环境胁迫中发挥着重要作用。然而,其在缓解植物重金属胁迫中的作用机制尚不明确。本研究探讨了外源脯氨酸(10和20 mM)对镉诱导的幼龄橄榄树(Olea europaea L. cv. Chemlali)生长抑制作用的缓解效果。实验中,土壤镉浓度分别为10和30 mg CdCl₂/kg。镉处理导致根和叶组织中镉的大量积累,并降低了气体交换、光合色素含量、必需元素(Ca、Mg和K)的吸收以及植物生物量。此外,还观察到抗氧化酶活性(超氧化物歧化酶、过氧化氢酶、谷胱甘肽过氧化物酶)和脯氨酸含量升高,同时伴有较高的过氧化氢、硫代巴比妥酸反应物和电解质渗漏。值得注意的是,外源脯氨酸的施用减轻了镉积累引起的氧化损伤。事实上,用脯氨酸处理的镉胁迫橄榄植株表现出抗氧化酶活性、光合作用活性、营养状况、植株生长和橄榄果实含油量的增加。总体而言,脯氨酸的补充似乎减轻了镉胁迫对幼龄橄榄植株的有害影响。 本研究探讨了外源相容性溶质(如脯氨酸)对抗镉(Cd)对幼龄椰枣(Phoenix dactylifera L. cv Deglet Nour)植株抑制作用的能力。将两年生椰枣植株置于不同镉胁迫水平(0、10 和 30 mg CdCl2/kg 土壤)下处理五个月,并分别在灌溉水中添加或不添加外源脯氨酸(20 mM)。不同水平的镉胁迫改变了植株的生长、气体交换、叶绿素含量以及水分状况,但改变的程度各不相同。相反,镉处理植物的抗氧化酶活性增加,同时脯氨酸含量、过氧化氢(H₂O₂)、硫代巴比妥酸反应物(TBARS)和电解质渗漏(EL)也较高。有趣的是,外源脯氨酸减轻了镉对幼龄椰枣树的不利影响。事实上,它缓解了镉积累引起的氧化损伤,并改善了植物的生长、水分状况和光合作用活性。此外,与镉处理植物相比,脯氨酸处理植物的根和叶中抗氧化酶(超氧化物歧化酶、过氧化氢酶和谷胱甘肽过氧化物酶)活性更高。 本研究还进行了水培实验,以探讨外源施用脯氨酸(Pro;25 μM)对缓解茄子幼苗砷酸盐(As(V);5 和 25 μM)毒性的影响。五价砷(As(V))暴露会抑制茄子的生长,并伴随砷的积累增加。然而,外源施用脯氨酸(Pro)可通过降低砷的积累来缓解茄子幼苗中As(V)的毒性。荧光特性(JIP测试):phiP0、psi0、phiE0、PIABS、ABS/RC、TR0/RC、ET0/RC、DI0/RC、NPQ和qP也受到As(V)的影响。然而,As(V)对PIABS、DI0/RC和NPQ的影响更为显著。在Pro处理的幼苗中,phiP0、psi0、phiE0和PIABS等参数受到刺激,而能量通量参数(ABS/RC、TR0/RC、ET0/RC和DI0/RC)则受到抑制。外源施用Pro可减轻As(V)对光系统II(PS II)光化学的毒性作用。氧化应激标志物:超氧自由基、过氧化氢和丙二醛(脂质过氧化)在五价砷(As(V))暴露下升高,但外源施用脯氨酸(Pro)可显著降低其水平。As(V)处理刺激了超氧化物歧化酶、过氧化物酶和过氧化氢酶的活性,但谷胱甘肽-S-转移酶的活性未受影响。外源施用Pro提高了酶促抗氧化剂的活性。As(V)处理组和Pro处理组幼苗的内源Pro水平较高。Pro生物合成的关键酶——δ1-吡咯啉-5-羧酸合成酶的活性在Pro处理组幼苗中较高。As(V)胁迫抑制了Pro脱氢酶的活性,在Pro+As(V)组合处理下,其活性最低。这些结果表明,脯氨酸代谢可能在调节砷的积累和抗氧化剂水平方面发挥关键作用,与单独使用五价砷(As(V))处理相比,这两者共同促进了茄子幼苗的生长。 本研究旨在评估一种特定混合物(包含维生素C、赖氨酸、脯氨酸、表没食子儿茶素没食子酸酯和锌)以及α-1-抗胰蛋白酶对苯并[a]芘[B(a)P]诱导的小鼠肺肿瘤发生的保护和治疗作用。瑞士白化小鼠被分为两个主要实验组:实验组(1)小鼠注射100 mg/kg B(a)P,持续28周;实验组(2)小鼠注射8次,每次50 mg/kg B(a)P,持续16周。实验1和2均分为五组:I组接受赋形剂,II组接受保护剂混合物,III组接受致癌物苯并[a]芘(B(a)P),IV组同时接受保护剂和致癌物,V组先接受致癌物再接受保护剂。在两项实验中,与对照组相比,III组的总唾液酸、硫代巴比妥酸反应物、血管内皮生长因子、羟脯氨酸水平以及弹性蛋白酶和明胶酶活性均显著升高(P < 0.001)。这些生化指标的改变与组织病理学改变相关。在两项实验中,与III组相比,IV组和V组接受保护剂后,上述指标显著降低,组织病理学改变也得到改善(P < 0.001)。本保护性混合物能够抑制苯并[a]芘诱导的小鼠肺癌的肿瘤发生,并使生化和组织病理学参数恢复正常。此外,本混合物更侧重于保护作用而非治疗作用。 有关(L)-脯氨酸(共8种)的更多相互作用(完整)数据,请访问HSDB记录页面。 非人类毒性值 大鼠口服LD50 >5110 mg/kg体重 |
| 其他信息 |
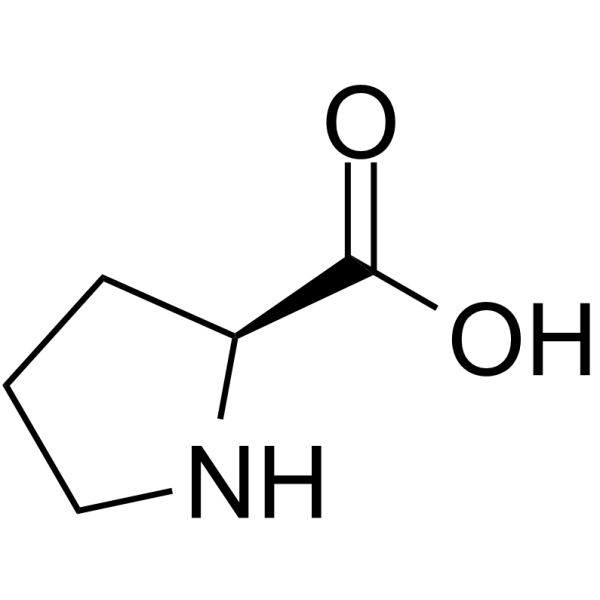
L-脯氨酸是一种吡咯烷,其2位上的脯氨酸-S氢被羧酸基团取代。在20种DNA编码的氨基酸中,L-脯氨酸是唯一一种羧基α位上带有仲氨基的氨基酸。它是胶原蛋白的重要组成部分,对关节和肌腱的正常功能至关重要。它还有助于维持和增强心肌。L-脯氨酸是一种微量营养素、营养保健品、藻类代谢产物、酿酒酵母代谢产物、大肠杆菌代谢产物、小鼠代谢产物以及相容性渗透调节剂。它属于谷氨酰胺家族氨基酸、蛋白质生成氨基酸、脯氨酸和L-α-氨基酸。它是L-脯氨酸盐的共轭碱。它是L-脯氨酸盐的共轭酸。它是D-脯氨酸的对映异构体。它是L-脯氨酸两性离子的互变异构体。
脯氨酸是构成生物体蛋白质的二十种氨基酸之一。脯氨酸有时被称为亚氨基酸,尽管IUPAC对亚胺的定义要求其含有碳氮双键。脯氨酸是一种非必需氨基酸,由谷氨酸合成。它是胶原蛋白的重要组成部分,对关节和肌腱的正常功能至关重要。 L-脯氨酸是大肠杆菌(K12菌株、MG1655菌株)中发现或产生的代谢产物。 据报道,在当归、微绿藻和其他有相关数据的生物体中也发现了脯氨酸。 脯氨酸是一种环状非必需氨基酸(实际上是亚氨基酸),在人体内由谷氨酸和其他氨基酸合成,是许多蛋白质的组成成分。脯氨酸在胶原蛋白中含量丰富,几乎占其氨基酸残基的三分之一。胶原蛋白是皮肤、肌腱、骨骼和结缔组织的主要支撑蛋白,促进它们的健康和愈合。(NCI04) L-脯氨酸是构成生物体蛋白质的二十种氨基酸之一。脯氨酸有时被称为亚氨基酸,但根据国际纯粹与应用化学联合会(IUPAC)的定义,亚胺需要碳氮双键。脯氨酸是一种非必需氨基酸,由谷氨酸合成。它是胶原蛋白的重要组成部分,对关节和肌腱的正常功能至关重要。 一种由谷氨酸合成的非必需氨基酸。它是胶原蛋白的重要组成部分,对关节和肌腱的正常功能至关重要。 药物适应症 L-脯氨酸对关节和肌腱的正常功能极其重要,还有助于维持和增强心肌。 作用机制 在肾脏中,L-脯氨酸氧化酶使其开环并氧化生成L-谷氨酸,从而发挥糖原生成作用。L-鸟氨酸和L-谷氨酸经由L-谷氨酸-γ-半醛转化为L-脯氨酸。它大量存在于胶原蛋白中,并与关节和腱索的功能密切相关。 治疗用途 /EXPL THER/ 本研究旨在评估一种特定混合物(包含维生素C、赖氨酸、脯氨酸、表没食子儿茶素没食子酸酯和锌)以及α-1-抗胰蛋白酶对苯并[a]芘[B(a)P]诱导的小鼠肺肿瘤发生的保护和治疗作用。瑞士白化小鼠被分为两个主要实验组:实验组(1)小鼠注射100 mg/kg B(a)P,持续28周;实验组(2)小鼠注射8次,每次50 mg/kg B(a)P,持续16周。实验1和2均分为五组:I组接受赋形剂,II组接受保护剂混合物,III组接受致癌物苯并[a]芘(B(a)P),IV组同时接受保护剂和致癌物,V组先接受致癌物再接受保护剂。在两项实验中,与对照组相比,III组的总唾液酸、硫代巴比妥酸反应物、血管内皮生长因子、羟脯氨酸水平以及弹性蛋白酶和明胶酶活性均显著升高(P < 0.001)。这些生化指标的改变与组织病理学改变相关。在两项实验中,与III组相比,IV组和V组接受保护剂后,上述指标显著降低,组织病理学改变也得到改善(P < 0.001)。本保护性混合物能够抑制苯并[a]芘诱导的小鼠肺癌的肿瘤发生,并使生化和组织病理学参数恢复正常。此外,本混合物更侧重于保护作用而非治疗作用。 药效学 L-脯氨酸是软骨中的主要氨基酸,对维持皮肤年轻状态以及修复肌肉、结缔组织和皮肤损伤至关重要。它对免疫系统以及本配方的必要平衡也至关重要。它是胶原蛋白的重要组成部分,对关节和肌腱的正常功能至关重要。L-脯氨酸对关节和肌腱的正常功能极其重要。有助于维持和增强心肌。 |
| 分子式 |
C5H9NO2
|
|---|---|
| 分子量 |
115.1305
|
| 精确质量 |
115.063
|
| CAS号 |
147-85-3
|
| 相关CAS号 |
25191-13-3
|
| PubChem CID |
145742
|
| 外观&性状 |
Flat needles from alcohol + ether; prisms from water
White crystals or crystalline powder |
| 密度 |
1.2±0.1 g/cm3
|
| 沸点 |
252.2±33.0 °C at 760 mmHg
|
| 熔点 |
228 °C (dec.)(lit.)
|
| 闪点 |
106.3±25.4 °C
|
| 蒸汽压 |
0.0±1.1 mmHg at 25°C
|
| 折射率 |
1.487
|
| LogP |
-0.57
|
| tPSA |
49.33
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
1
|
| 重原子数目 |
8
|
| 分子复杂度/Complexity |
103
|
| 定义原子立体中心数目 |
1
|
| SMILES |
O([H])C([C@]1([H])C([H])([H])C([H])([H])C([H])([H])N1[H])=O
|
| InChi Key |
ONIBWKKTOPOVIA-BYPYZUCNSA-N
|
| InChi Code |
InChI=1S/C5H9NO2/c7-5(8)4-2-1-3-6-4/h4,6H,1-3H2,(H,7,8)/t4-/m0/s1
|
| 化学名 |
(2S)-pyrrolidine-2-carboxylic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: (1). 本产品在运输和储存过程中需避光。 (2). 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~50 mg/mL (~434.29 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (868.58 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 8.6858 mL | 43.4292 mL | 86.8583 mL | |
| 5 mM | 1.7372 mL | 8.6858 mL | 17.3717 mL | |
| 10 mM | 0.8686 mL | 4.3429 mL | 8.6858 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT06083116 | Completed | Drug: Hydrochlorothiazide、Henagliflozin Proline | Diabetes in Adults | Jiangsu HengRui Medicine Co., Ltd. | 2019-08-28 | Phase 1 |
| NCT00216983 | Withdrawn | Burns | Massachusetts General Hospital | 1997-09 | ||
| NCT06363448 | Recruiting | Procedure: Yamani Technique versus Prolene Mesh for Intraocular Lens Scleral Fixation in Aphakia |
Aphakia, Postcataract | Sohag University | 2024-01-01 | Not Applicable |
| NCT05775276 | Not yet recruiting | Procedure: Proline mesh in hernioplasty | Incidence of Mesh Infection In Hernioplasty | Assiut University | 2023-03 | Not Applicable |
| NCT05196542 | Completed | Procedure: patients with apical prolapse who will do Sacro hysteropexy using mersilene tape |
Apical Prolapse | Mohamed Elsibai Anter | 2019-11-01 | Not Applicable |