| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 10g |
|
||
| Other Sizes |
|
| 靶点 |
Raspberry ketone inhibits adipogenesis in 3T3-L1 adipocytes by targeting adipogenic transcription factors (PPARγ, C/EBPα) and lipogenic enzymes (FAS, ACC)[1]
Raspberry ketone protects against nonalcoholic steatohepatitis (NASH) by regulating hepatic lipid metabolism and inflammatory signaling pathways (e.g., NF-κB)[2] Raspberry ketone alleviates isoproterenol-induced myocardial infarction by targeting oxidative stress (SOD, CAT) and apoptotic signaling (Bcl-2/Bax/caspase-3)[3] |
|---|---|
| 体外研究 (In Vitro) |
在 3T3-L1 前脂肪细胞中,覆盆子酮(1、10、20 和 50 μM)可抑制脂肪生成和脂质积累。覆盆子酮 (10 µM) 会增加 ATGL、HSL 和 CPT1B 的表达,同时显着阻断 C/EBPα、PPARγ 和 aP2 的表达 [1]。
在诱导分化的3T3-L1前脂肪细胞中,覆盆子酮(Raspberry ketone)(10-100 μM)剂量依赖性抑制脂肪细胞分化:100 μM时通过油红O染色检测显示脂质堆积减少约60%,RT-PCR检测显示脂肪生成基因PPARγ(约50%)、C/EBPα(约45%)及脂生成基因FAS(约55%)、ACC(约40%)的mRNA水平下调[1] Western blot分析显示,覆盆子酮(Raspberry ketone)(50-100 μM)使分化的3T3-L1脂肪细胞中PPARγ和C/EBPα蛋白表达降低约40-50%,且在浓度高达100 μM时无显著细胞毒性(MTT实验)[1] |
| 体内研究 (In Vivo) |
与高脂肪饮食诱导的 NASH 模型相比,覆盆子酮(0.5%、1% 或 2%)会升高总胆固醇 (TC)、甘油三酯 (TG)、低密度脂蛋白胆固醇 (LDL-C)、 ISI(胰岛素敏感性指数)、PPAR-水平α和LDLR,并降低AST(天冬氨酸转氨酶)、ALT(丙氨酸转氨酶)、ALP(碱性磷酸酶)、IRI(胰岛素抵抗指数)、葡萄糖(GLU)、INS(胰岛素)敏感性指数)、LEP(瘦素)和 TNF-α 的血清水平。增加 SOD 活性是覆盆子酮的另一个作用 [2]。覆盆子酮的 PPAR-α 激动活性可能是其对异丙肾上腺素诱导的大鼠心肌梗死具有心脏保护作用的原因 [3]。
在高脂饮食(HFD)喂养8周的Sprague-Dawley大鼠中,覆盆子酮(Raspberry ketone)(200 mg/kg/天,灌胃)较HFD对照组,体重增长减少约25%,肝脏甘油三酯(TG)含量减少约40%,血清ALT/AST水平降低约30-35%;RT-PCR检测显示其还可下调肝脏TNF-α(约50%)和IL-6(约45%)的mRNA水平,并改善肝脏脂肪变性(组织学评分从3.5降至1.5)[2] 在异丙肾上腺素(85 mg/kg,皮下注射2天)诱导心肌梗死的Wistar大鼠中,覆盆子酮(Raspberry ketone)(100 mg/kg/天,注射异丙肾上腺素前灌胃14天)较模型对照组,血清CK-MB(约40%)和LDH(约35%)水平降低,心肌SOD活性增加约30%,MDA含量减少约45%;western blot检测显示其还可上调Bcl-2(约50%)、下调Bax(约40%)和活化型caspase-3(约45%)的蛋白水平,TTC染色显示心肌梗死面积减少约35%[3] |
| 酶活实验 |
脂生成酶活性检测(FAS/ACC):裂解经覆盆子酮(Raspberry ketone)(10-100 μM)处理的分化3T3-L1脂肪细胞;FAS活性检测:将裂解液与乙酰辅酶A、丙二酰辅酶A和NADPH混合,37°C孵育30分钟,在340 nm处检测NADPH氧化量;ACC活性检测:使用[14C]-乙酰辅酶A定量乙酰辅酶A羧化反应,计数放射性[1]
肝脏炎症细胞因子检测(TNF-α/IL-6):匀浆经覆盆子酮(Raspberry ketone)处理的HFD大鼠肝脏;ELISA检测TNF-α和IL-6水平:将匀浆上清液与包被捕获抗体的酶标板混合,4°C孵育过夜,洗涤后加入检测抗体,在450 nm处测定吸光度[2] 心肌氧化应激酶检测(SOD/CAT):匀浆异丙肾上腺素处理大鼠的心肌组织;SOD活性通过抑制羟胺生成亚硝酸盐检测,CAT活性通过监测240 nm处H₂O₂分解速率检测[3] |
| 细胞实验 |
3T3-L1脂肪细胞分化实验:将3T3-L1前脂肪细胞接种于6孔板(2×10⁴个细胞/孔),用含10%胎牛血清(FBS)的DMEM培养。汇合度达80%时,用含10% FBS、0.5 mM IBMX、1 μM地塞米松和10 μg/mL胰岛素的DMEM诱导分化,同时加入覆盆子酮(Raspberry ketone)(10-100 μM)。8天后,用0.5%油红O异丙醇溶液染色30分钟,洗涤后用异丙醇提取染料,在510 nm处测定吸光度定量脂质堆积[1]
脂肪生成基因RT-PCR检测:提取经覆盆子酮(Raspberry ketone)处理的3T3-L1细胞总RNA,合成cDNA后,用PPARγ、C/EBPα、FAS、ACC及内参GAPDH的引物进行PCR扩增;PCR产物经琼脂糖凝胶电泳分离后,密度分析定量[1] 脂肪生成蛋白western blot检测:将经覆盆子酮(Raspberry ketone)处理的3T3-L1细胞裂解液进行SDS-PAGE分离,转印至PVDF膜,用抗PPARγ、抗C/EBPα和抗β-肌动蛋白抗体孵育,化学发光显影[1] |
| 动物实验 |
高脂饮食诱导的非酒精性脂肪性肝炎(NASH)模型:将6周龄雄性Sprague-Dawley大鼠随机分为3组:正常饮食组(ND)、高脂饮食组(HFD,45%脂肪)、高脂饮食+覆盆子酮组(HFD+覆盆子酮,200 mg/kg/天)。覆盆子酮溶于0.5%羧甲基纤维素(CMC)溶液中,每日灌胃一次,持续8周。每周测量体重;处死后,采集血清和肝脏样本进行生化和组织学分析[2]。异丙肾上腺素诱导的心肌梗死模型:将8周龄雄性Wistar大鼠分为3组:对照组、模型组(第14和15天皮下注射异丙肾上腺素85 mg/kg)、模型+覆盆子酮组(100 mg/kg/天)。将覆盆子酮溶于生理盐水中,每日一次通过灌胃法给予大鼠,持续14天(在注射异丙肾上腺素之前)。第16天,处死大鼠;收集血清和心肌组织,用于酶活性和组织学分析[3]
|
| 药代性质 (ADME/PK) |
代谢/代谢物
尿液分析显示,所有受试动物在第7周和第13周的尿液中均检测到酮体。作者报告称,大鼠连续7天饲喂含1% 4-(对羟基苯基)-2-丁酮的饲料后,12小时内出现酮体,恢复正常饮食后9小时内酮体消失。这种酮尿症可能由尿液中存在的代谢物引起,被认为不属于毒性作用。 1. 本研究在大鼠、豚鼠和兔中研究了4-(4-羟基苯基)丁-2-酮(覆盆子酮)的代谢。2. 灌胃给药(1 mmol/kg)后,所有物种的尿代谢物排泄在24小时内几乎完全,约占给药剂量的90%。 3. 尿液中最主要的代谢产物是覆盆子酮及其相应的甲醇,两者主要与葡萄糖醛酸和/或硫酸盐结合。酮的还原程度在兔中最为显著。4. 氧化代谢包括环羟基化和侧链氧化。侧链氧化途径生成1,2-和2,3-二醇衍生物。推测后者发生裂解,生成检测到的C6-C3和C6-C2衍生物。 在饲喂含1%对羟基苯基丁酮饲料的大鼠尿液中发现了一种酮(可能是丙酮)。单次给予200 mg剂量后,大鼠在24小时内排出约6%的原形药物。仅在给药后1至6小时内产生的尿液中检测到酮的阳性反应。 |
| 毒性/毒理 (Toxicokinetics/TK) |
非人类毒性值
大鼠腹腔注射LD50:雄性0.7 g/kg,雌性0.35 g/kg(对羟基苯基丁酮溶于丙二醇)/ 兔急性经口和急性经皮LD50:5 g/kg(对羟基苯基丁酮溶于丙二醇)/ 大鼠口服LD50:雄性1.32 g/kg,雌性1.40 g/kg(对羟基苯基丁酮溶于丙二醇)/ |
| 参考文献 |
|
| 其他信息 |
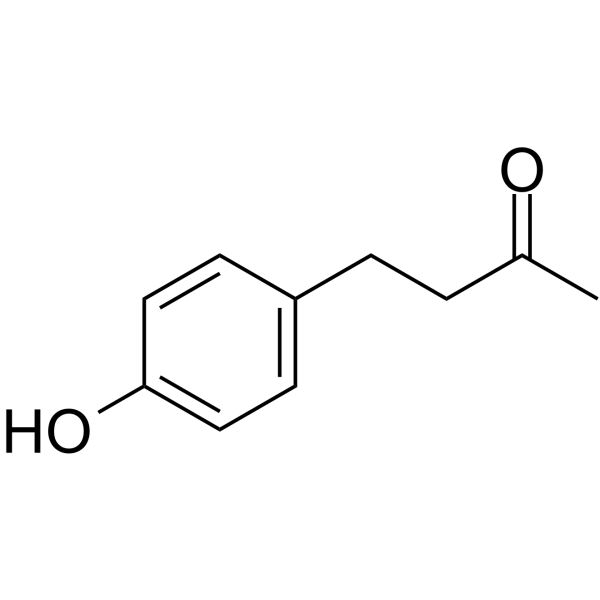
覆盆子酮是一种酮类化合物,其结构为4-苯基丁-2-酮,其中苯环的4位被羟基取代。它存在于多种水果中,包括覆盆子、黑莓和蔓越莓,并用于香水和化妆品行业。覆盆子酮具有多种用途,包括作为调味剂、香料、代谢产物、保肝剂、化妆品成分和雄激素拮抗剂。它属于酚类化合物,也是一种甲基酮。
据报道,4-(4-羟基苯基)-2-丁酮存在于白花豆树(Nidula niveotomentosa)、掌叶大黄(Rheum palmatum)和其他一些有相关数据的生物体中。 治疗用途 探索性研究:本研究在体外培养的小鼠B16黑色素瘤细胞和体内斑马鱼及小鼠中,探讨了覆盆子酮(RK)对黑色素生成的抑制作用。在B16细胞中,RK通过转录后调控酪氨酸酶基因表达抑制黑色素生成,导致细胞酪氨酸酶活性和酪氨酸酶蛋白含量均下调,而酪氨酸酶mRNA转录水平不受影响。在斑马鱼中,RK也通过降低酪氨酸酶活性抑制黑色素生成。在小鼠中,将0.2%或2%的RK凝胶制剂涂抹于小鼠皮肤,一周内即可显著提高皮肤美白程度。与RK在香水和化妆品中广泛使用的调味特性不同,本研究证实了RK的皮肤美白功效。基于我们在此报道的研究结果,RK在化妆品行业具有很高的应用潜力。 探索治疗 卵巢切除术、衰老和其他因素引起的骨质疏松症会导致骨量减少,同时骨髓脂肪组织增多。成骨细胞和脂肪细胞之间的平衡受相互影响。通过抑制骨髓脂肪组织来促进局部/全身骨形成的方法对于治疗骨折或代谢性骨病(如骨质疏松症)至关重要。本研究探讨了覆盆子酮[4-(4-羟苯基)丁-2-酮:RK](覆盆子的主要芳香化合物之一,具有抗肥胖作用)是否能够促进C3H10T1/2干细胞的成骨细胞分化。将汇合的C3H10T1/2干细胞在含有10-100 μg/mL RK的培养基中培养6天,培养基中同时加入10 nM全反式维甲酸(ATRA)或300 ng/mL重组人骨形态发生蛋白(rhBMP)-2蛋白(作为成骨细胞分化剂)。在 ATRA 存在的情况下,RK 以剂量依赖的方式增加碱性磷酸酶 (ALP) 活性。在 rhBMP-2 存在的情况下,RK 也增加 ALP 活性。与单独使用 ATRA 相比,在 ATRA 存在的情况下,RK 还增加了骨钙素、α1(I) 型胶原和 TGF-β(TGF-β1、TGF-β2 和 TGF-β3)的 mRNA 水平。RK 促进 C3H10T1/2 干细胞向成骨细胞分化。然而,RK 不影响早期脂肪细胞分化的抑制。我们的结果表明,RK 增强 C3H10T1/2 干细胞向成骨细胞的分化,并且可能通过与脂肪细胞分化无关的作用促进骨形成。 探索治疗:市面上销售的许多天然产品声称可以减轻体重和减少脂肪,但很少有产品经过成品特异性研究来证明其安全性和有效性。本研究旨在评估一种主要成分为覆盆子酮、咖啡因、辣椒素、大蒜、生姜和酸橙(Citrus aurantium,商品名:Prograde Metabolism [METABO])的多成分补充剂作为为期八周的减肥计划辅助手段的安全性和有效性。采用随机、安慰剂对照、双盲设计,将70名肥胖但其他方面健康的受试者随机分配至METABO组或安慰剂组,并进行为期八周的每日补充剂服用、低热量饮食和运动训练。研究检测了受试者的身体成分变化、血清脂肪细胞因子(脂联素、抵抗素、瘦素、TNF-α、IL-6)水平以及包括心率和血压在内的健康指标。在完成研究的 45 名受试者中,观察到以下方面存在显著差异:体重(METABO -2.0% vs. 安慰剂 -0.5%,P<0.01)、脂肪量(METABO -7.8% vs. 安慰剂 -2.8%,P<0.001)、瘦体重(METABO +3.4% vs. 安慰剂 +0.8%,P<0.03)、腰围(METABO -2.0% vs. 安慰剂 -0.2%,P<0.0007)、臀围(METABO -1.7% vs. 安慰剂 -0.4%,P<0.003)以及根据锚定视觉模拟量表 (VAS) 计算的能量水平(METABO +29.3% vs. 安慰剂 +5.1%,P<0.04)。在最初的4周内,METABO组与安慰剂组相比,血清瘦素水平维持升高(P<0.03),血清抵抗素水平降低(P<0.08),且观察到相关效应/趋势。两组间未观察到全身血液动力学、临床血液化学指标、不良事件或膳食摄入量的变化。METABO可作为为期8周的饮食和运动减肥计划的安全有效辅助手段,增强身体成分、腰围和臀围的改善。坚持完成为期8周的减肥计划也使安慰剂组的体脂含量发生了有益的变化。目前正在进行相关研究,以证实这些结果并阐明METABO发挥上述有益作用的机制(例如,生化和神经内分泌介质)。/含有覆盆子酮的多成分补充剂/ EXPL THER 覆盆子酮 (RK) 是红覆盆子中的一种天然酚类化合物。据报道,给雄性小鼠补充RK可预防高脂饮食引起的体重增加,并促进白色脂肪细胞的脂肪分解。为了阐明RK抗肥胖作用的可能机制,本研究探讨了RK对3T3-L1细胞中脂联素表达和分泌、脂肪分解以及脂肪酸氧化的影响。结果表明,10 μM RK处理显著促进了分化的3T3-L1细胞的脂肪分解。免疫分析显示,RK可增加脂联素(一种主要由脂肪组织表达和分泌的脂肪细胞因子)的表达和分泌。此外,10 μM RK处理还促进了3T3-L1脂肪细胞的脂肪酸氧化,并抑制了脂质的积累。这些研究结果表明,覆盆子酮(RK)作为一种草药具有巨大的应用前景,因为它的生物活性能够改变3T3-L1脂肪细胞的脂质代谢。覆盆子酮(4-(4-羟苯基)丁-2-酮;RK)是红覆盆子(Rubus idaeus)的主要芳香化合物。RK的结构与辣椒素和辛弗林相似,辣椒素和辛弗林已知具有抗肥胖作用并能改变脂质代谢。本研究旨在阐明RK是否有助于预防啮齿动物肥胖并激活其脂质代谢。为了测试其对肥胖的影响,我们设计了以下体内实验:1)小鼠喂食含0.5%、1%或2% RK的高脂饮食,持续10周;2)小鼠先喂食高脂饮食6周,随后喂食含1% RK的相同高脂饮食5周。 RK可预防高脂饮食引起的体重增加以及肝脏和内脏脂肪组织(附睾、腹膜后和肠系膜)重量的增加。RK还能降低高脂饮食引起的这些组织重量和肝脏甘油三酯含量的增加。RK显著增强了去甲肾上腺素诱导的脂肪分解,并促进了激素敏感性脂肪酶从胞质溶胶向脂滴的转位,从而改善大鼠附睾脂肪细胞的脂肪代谢。总之,RK可预防和改善肥胖和脂肪肝。这些效应似乎源于覆盆子酮 (RK) 对脂质代谢的改变,更具体地说,是其增强去甲肾上腺素诱导的白色脂肪细胞脂肪分解的作用。 覆盆子酮是一种天然存在的酚类化合物,主要从覆盆子(Rubus idaeus)的果实中分离得到[1]。 覆盆子酮在 3T3-L1 细胞中的抗脂肪生成机制涉及下调 PPARγ/C/EBPα,这些因子是脂肪细胞分化的关键转录因子,从而抑制脂肪生成基因的表达和脂质的积累[1]。 在高脂饮食诱导的非酒精性脂肪性肝炎 (NASH) 大鼠中,覆盆子酮通过减少肝脏脂质沉积和抑制炎症反应发挥保肝作用[2]。 覆盆子酮通过增强抗氧化能力(增加 SOD/CAT 活性)和抑制心肌细胞凋亡(上调)来缓解心肌梗死。 Bcl-2,下调 Bax/caspase-3)[3] |
| 分子式 |
C10H12O2
|
|---|---|
| 分子量 |
164.2011
|
| 精确质量 |
164.083
|
| CAS号 |
5471-51-2
|
| PubChem CID |
21648
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
292.2±15.0 °C at 760 mmHg
|
| 熔点 |
81-85 °C(lit.)
|
| 闪点 |
122.9±13.0 °C
|
| 蒸汽压 |
0.0±0.6 mmHg at 25°C
|
| 折射率 |
1.535
|
| LogP |
0.94
|
| tPSA |
37.3
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
12
|
| 分子复杂度/Complexity |
146
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
NJGBTKGETPDVIK-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C10H12O2/c1-8(11)2-3-9-4-6-10(12)7-5-9/h4-7,12H,2-3H2,1H3
|
| 化学名 |
4-(4-hydroxyphenyl)butan-2-one
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~609.01 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (15.23 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (15.23 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (15.23 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 6.0901 mL | 30.4507 mL | 60.9013 mL | |
| 5 mM | 1.2180 mL | 6.0901 mL | 12.1803 mL | |
| 10 mM | 0.6090 mL | 3.0451 mL | 6.0901 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。