| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
PARP-1 ( Ki = 1.4 nM ); PARP-2; PARP-3
Rucaparib (AG014699) is a potential AG14644 N-demethylation metabolite[1]. Rucaparib (0.1, 1, 10, 100 μM; 24 hours) is cytotoxic; in Capan-1 (BRCA2 mutant) cells, its LC50 is 5 μM, while in MX-1 (BRCA1 mutant) cells, it is only 100 nM[2]. Rucaparib causes radiosensitization independent of SSB repair inhibition, as it inhibits NF-κB activation downstream. Without impairing other essential inflammatory functions, rucaparib can target NF-κB that is activated by DNA damage and overcome the toxicity seen with classical NF-κB inhibitors[5]. Rucaparib inhibits PARP-1 activity in permeabilized D283Med cells by 97.1% at a concentration of 1 μM[6]. |
|---|---|
| 体外研究 (In Vitro) |
体外活性:Rucaparib 是纯化全长人 PARP-1 的有效抑制剂,对 LoVo 和 SW620 细胞中的细胞 PARP 显示出更高的抑制作用。此外,Rucaparib 可检测地与其他 8 个 PARP 结构域结合,包括 PARP2、3、4、10、15、16、TNKS1 和 TNKS2。 Rucaparib 的放射增敏作用是由于下游 NF-κB 激活的抑制,并且与 SSB 修复抑制无关。 Rucaparib 可以靶向由 DNA 损伤激活的 NF-κB,并克服经典 NF-κB 抑制剂观察到的毒性,而不损害其他重要的炎症功能。在透化的 D283Med 细胞中,浓度为 1 μM 的 Rucaparib 可抑制 PARP-1 活性 97.1%。激酶测定:测量[32P]NAD+掺入对人全长重组PARP-1的抑制。使用 PhosphorImager 对掺入酸不溶性材料中的 [32P]ADP-核糖进行定量。 Ki是通过非线性回归分析计算的。细胞测定:在过表达人(h) ABCB1的MDCKII亲本细胞系中,rucaparib的顶部和基底外侧定向易位是相同的。用 ABCB1 抑制剂 zosuquidar 处理细胞导致顶端定向转运略有减少,这可能是由于基底外侧未识别的 rucaparib 摄取转运蛋白的特异性抑制,或内源性犬 ABCB1 的抑制。结果表明rucaparib是ABCB1的转运底物。
Rucaparib 进入SW620人结直肠癌细胞的摄取是载体介导的,遵循米氏动力学 (Km = 8.4 ± 1.2 μM, Vmax = 469 ± 22 pmol/10^6 细胞/10分钟)。它在30分钟内细胞内积累浓度超过细胞外浓度的10倍以上。[2] 在400 nM rucaparib脉冲处理30分钟后,药物在细胞中滞留,呈双相外排。在SW620、Capan-1和MX-1细胞系中,PARP活性被抑制≥70%至少72小时,且在药物移除72小时后,活性仍比基线对照低约35%。[2] 在克隆形成实验中,rucaparib显示出细胞毒性活性。在BRCA2突变的Capan-1人胰腺癌细胞中,24小时药物暴露后的LC₅₀为5 μM;在BRCA1突变的MX-1人乳腺癌细胞中,LC₅₀为100 nM。[2] Rucaparib的一个羧酸代谢物在加入到透化细胞中时,能以约550 nM的IC₅₀抑制PARP活性,但在完整细胞中不抑制PARP,表明其膜渗透性差。[2] |
| 体内研究 (In Vivo) |
Rucaparib 无毒,但在具有 DNA 修复蛋白能力的 D384Med 异种移植物中显着增强替莫唑胺诱导的 TGD。药代动力学研究还表明,Rucaparib在脑组织中被检测到,这表明Rucaparib具有治疗颅内恶性肿瘤的潜力。 Rucaparib 显着增强拓扑替康和替莫唑胺在 NB-1691、SH-SY-5Y 和 SKNBE (2c) 细胞中的细胞毒性。 Rucaparib 增强替莫唑胺的抗肿瘤活性,并表明 NB1691 和 SHSY5Y 异种移植物中的肿瘤完全且持续消退。
在携带Capan-1 (BRCA2突变) 异种移植瘤的小鼠中,单次口服rucaparib (150 mg/kg) 在24小时抑制肿瘤PARP活性>70%,且抑制持续长达7天。[2] 每周口服rucaparib (150 mg/kg,每周一次,持续6周) 显著抑制Capan-1异种移植瘤的生长,其效果与每日腹腔给药 (10 mg/kg,每周5天,持续6周) 相当或更优。每周给药方案在10只小鼠中导致了3例完全缓解。[2] 在携带MX-1 (BRCA1突变) 异种移植瘤的小鼠中,给予rucaparib (10 mg/kg 腹腔注射,每周5天,持续6周;或50 mg/kg 腹腔注射/150 mg/kg 口服,每周一次,持续6周) 并未显著延缓肿瘤生长,尽管单次口服150 mg/kg后24小时肿瘤中PARP抑制>80%。[2] |
| 酶活实验 |
测量 [32P]NAD+ 掺入诱导的人全长重组 PARP-1 抑制的量。使用 PhosphorImager,测量添加到酸不溶性材料中的 [32P]ADP-核糖的量。非线性回归分析用于计算Ki。
在细胞和组织匀浆中测量PARP活性。简而言之,在过量NAD⁺ (350 μM) 存在下,用双链寡核苷酸最大程度刺激透化细胞或组织匀浆中的PARP活性。形成的聚腺苷二磷酸核糖 (PAR) 聚合物量通过免疫印迹,使用抗PAR抗体并参照PAR标准曲线进行定量。活性表示为每10^6细胞或每毫克蛋白质的pmol PAR。[2] |
| 细胞实验 |
MTT 测定用于测量细胞增殖。在 96 孔板中,细胞以 5×103 细胞/ml 的密度接种在 200 μl/孔的体积中。第二天,将不同浓度的 DMSO、BKM120 或 rucaparib 添加到细胞中。四天后,每个孔接受 20 μl MTT (5 mg/ml)。在 37 °C 下额外孵育 4 小时后,测定 490 nm 处的吸光度。 CalcuSyn 软件用于分析生长抑制实验的数据,以确定药物组合的效果。接下来,计算组合指数(CI)。
Rucaparib积累研究: 指数生长的SW620细胞与[¹⁴C]rucaparib和[³H]蔗糖/菊粉(用于校正细胞外液)一起孵育。在不同时间点,将细胞铺在覆盖有KOH的硅油上并离心。收集细胞沉淀(溶于KOH),中和后通过闪烁计数测量放射性以确定细胞内药物浓度。使用各种转运蛋白抑制剂(乌本苷、细胞松弛素B、双嘧达莫、BCH)或修改的缓冲液来研究摄取机制。[2] 细胞毒性实验(克隆形成存活): 将指数生长的Capan-1或MX-1细胞以低密度接种于多孔板中。贴壁后,细胞暴露于浓度递增的rucaparib (0–50 μM) 24小时,然后洗涤并在无药培养基中培养10-14天。用结晶紫染色菌落,计数,并计算相对于未处理对照的存活率。[2] |
| 动物实验 |
溶于生理盐水;1 mg/kg;每日一次或四次,用于已建立D283Med异种移植瘤的ipCD-1裸鼠。体内抗肿瘤活性测定[1]
用于抗肿瘤研究的雌性无胸腺裸鼠(CD1 nu/nu)在特定病原体清除(SPF)条件下于隔离器中饲养和处理。我们将SW620结直肠肿瘤细胞(每只动物1 × 10⁷个细胞)皮下植入每只小鼠的一侧腹部,在肿瘤可触及时(植入后10-12天)对小鼠(每组五只)进行治疗,并使用二维游标卡尺测量监测肿瘤生长。肿瘤体积使用公式a² × b / 2计算,其中a为最小测量值,b为最大测量值。数据以中位相对肿瘤体积(RTV)表示,定义为计算的肿瘤体积除以治疗初始日(第0天)计算的肿瘤体积。因此,在第 0 天,RTV 值为 1,RTV4 值表示肿瘤体积是其初始值的四倍。 单剂量研究。[1] 我们以 200 mg/kg 的剂量口服替莫唑胺(生理盐水混悬液),单独给药或与单次腹腔注射 PARP 抑制剂联合给药,剂量分别为 0.1 [AG14447 和 MS-AG14644(相当于 0.078 mg/kg 游离 AG14644)]、1.0 和 10 mg/kg(甲磺酸盐相当于 0.79 和 7.9 mg/kg 游离 AG14451 和 AG14452 以及 0.78 和 7.8 mg/kg 游离 AG14531 和 AG14644)。对照组动物分别接受生理盐水口服和腹腔注射,或生理盐水口服联合PARP抑制剂10 mg/kg腹腔注射。 五日给药研究。[1] 我们用替莫唑胺(以生理盐水混悬液形式)口服给药,每日五次,单独给药或与以下PARP抑制剂联合腹腔注射,每日五次:0.05、0.15和0.5 mg/kg AG14447;0.15和0.5 mg/kg MS-AG14644(相当于0.12和0.39 mg/kg游离AG14644);1.5、5和15 mg/kg AG14361;以及5 mg/kg AG14452。对照组动物分别接受生理盐水口服和腹腔注射,或生理盐水口服联合较高剂量(0.5、5 或 15 mg/kg,取决于所研究的化合物)的 PARP 抑制剂腹腔注射。 组织分布[1] 我们向携带 SW620 异种移植瘤(约 10 × 10 mm)的小鼠(每组三只)腹腔注射 AG14361、AG14452 或 AG14447(10 mg/kg)。120 分钟后,在全身麻醉下,通过心脏穿刺取血,切除肿瘤并立即置于液氮中速冻。分离血浆并储存于 -20°C。采用反相高效液相色谱法(等度流动相:40%乙腈/0.1%甲酸铵,Hypersil BDS 3 μm 4.6 × 250 mm色谱柱,Waters Alliance 2690高效液相色谱仪;Waters公司,英国赫特福德郡埃尔斯特里)通过加标法测定乙腈处理血浆和匀浆肿瘤中PARP抑制剂的浓度。 异种移植瘤建立:将10-12周龄的雌性CD-1裸鼠侧腹部皮下植入10^7个Capan-1细胞(溶于PBS)或2×10^6个MX-1细胞(溶于Matrigel和培养基1:1混合物)。[2] 药代动力学和组织分布研究:荷瘤小鼠单次注射rucaparib(10腹腔注射或口服 50、100、150 mg/kg 的剂量。在给药后特定时间点(0.5、4、24、48、72、168 小时),处死小鼠。采集血液用于血浆分析,并取出肿瘤和脑组织,速冻后保存。采用高效液相色谱-荧光检测法测定rucaparib及其代谢物的组织浓度。[2] 疗效研究:将携带可触及的 Capan-1 或 MX-1 肿瘤(≥5×5 mm)的小鼠随机分为治疗组。根据不同的给药方案(例如,10 mg/kg 腹腔注射,每日一次,每周 5 次,持续 6 周;150 mg/kg 口服,每周一次,持续 6 周),分别给予赋形剂或rucaparib。定期测量肿瘤大小并计算体积。当肿瘤达到预定的大小限制或出现应激迹象时,小鼠将被实施安乐死。[2] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
在每日两次,每次 240 mg 至 840 mg 的剂量范围内,鲁卡帕尼的药代动力学呈线性特征。在批准的推荐剂量下,鲁卡帕尼的平均稳态血药浓度峰值 (Cmax) 为 1940 ng/mL (54%),平均 AUC0-12h 为 16900 h× ng/mL (54%)。平均 AUC 累积倍数为 3.5 至 6.2 倍。在批准的推荐剂量下,稳态血药浓度峰值时间 (Tmax) 的中位数为 1.9 小时,范围为 0 至 5.98 小时。平均绝对生物利用度为 36%,范围为 30% 至 45%。高脂餐使 Cmax 和 AUC0-24h 分别增加 20% 和 38%。 Tmax 延迟了 2.5 小时。 单次口服放射性标记的 rucaparib 后,未代谢的 rucaparib 占放射性总量的 64%。尿液和粪便中的放射性分别占 45% 和 95%。 平均(变异系数)表观分布容积为 2300 L (21%)。 稳态下平均(变异系数)表观总清除率为 44.2 L/h (45%)。 代谢/代谢物 体外研究表明,rucaparib 主要由 CYP2D6 代谢,其次由 CYP1A2 和 CYP3A4 代谢。除 CYP 介导的氧化外,rucaparib 还会发生 N-去甲基化、N-甲基化和葡萄糖醛酸化。在一项研究中,研究人员在血浆、尿液和粪便中鉴定出了七种鲁卡帕尼代谢物。 生物半衰期 平均(变异系数)末端消除半衰期为 26 (39%) 小时。 在荷瘤小鼠中,单次腹腔注射(10 mg/kg)后,母体药物鲁卡帕尼仅在 30 分钟时才能在血浆中检测到。[2] 单次口服(50、100、150 mg/kg)后,母体药物鲁卡帕尼可在血浆中检测到长达 4 小时,在较高剂量下,部分小鼠甚至可在长达 48 小时内检测到。[2] 鲁卡帕尼在 Capan-1 肿瘤中蓄积,4 小时时其浓度可达血浆浓度的 10 倍,且在肿瘤中的滞留时间比在血浆中更长(口服后 3 天,大多数小鼠仍可检测到)。剂量)。[2] 脑组织摄取量低(≤血浆浓度的10%)。[2] 羧酸代谢物在血浆中的浓度高于母体药物,但在肿瘤中的浓度低于母体药物。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在鲁卡帕尼的大型临床试验中,常规肝功能检查异常较为常见;74%的患者出现血清ALT升高,其中13%的患者ALT值超过正常值上限(ULN)的5倍。尽管临床试验中治疗期间血清酶升高较为常见,但未见出现伴有黄疸的肝炎或肝功能衰竭的报告。在鲁卡帕尼获批并更广泛应用后,尚未有已发表的临床上明显的肝损伤归因于该药物的报告。因此,鲁卡帕尼是血清酶升高的常见原因,但尚未发现与显著肝毒性相关。 可能性评分:E(未经证实但怀疑是临床上明显的肝损伤的原因)。 妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于鲁卡帕尼在哺乳期临床应用的信息。制造商建议在接受 rucaparib 治疗期间以及末次给药后 2 周内停止母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 蛋白结合 Rucaparib 在体外与人血浆蛋白的结合率为 70%。 Rucaparib优先分布于红细胞,血血浆浓度比为1.8。 据报道,单药rucaparib在50 mg/kg剂量下,以5天为周期重复给药6个月,对小鼠无毒性。[2] 与替莫唑胺(1 mg/kg,每日一次,连续5天)联合用药时,rucaparib的有效剂量和最大耐受剂量均有所降低。[2] 在已报道的疗效研究中,rucaparib治疗在任何测试方案下均未导致小鼠体重显著下降。[2] |
| 参考文献 | |
| 其他信息 |
药效学
鲁卡帕尼是一种抗癌药物,对癌细胞具有细胞毒性作用。其作用机制是通过抑制聚(ADP-核糖)聚合酶(PARP),PARP是一种参与DNA修复的酶。鲁卡帕尼可抑制PARP-1、PARP-2和PARP-3。它也能与PARP-4、PARP-10、PARP-12、PARP-15和PARP-16相互作用,但程度较轻。在小鼠体内,鲁卡帕尼可在肿瘤中积累并滞留,持续抑制PARP酶活性长达7天。鲁卡帕尼可抑制BRCA1/2和其他DNA修复基因缺陷的肿瘤细胞系的生长。除PARP抑制外,鲁卡帕尼还表现出对癌细胞的非PARP依赖性细胞毒性机制。与其他化疗药物联合使用时,rucaparib 在体外和体内均表现出协同或叠加效应。有证据表明,rucaparib 可以增强癌细胞对化疗的敏感性。 Rucaparib 还能引起血管舒张,这可能增加肿瘤灌注,并增强细胞毒性药物在癌细胞中的积累。 Rucaparib 是一种 PARP 抑制剂,它利用同源重组修复缺陷肿瘤(例如携带 BRCA1/2 突变的肿瘤)的合成致死性。[2] 在体外和体内观察到的 PARP 抑制作用的延长,归因于载体介导的药物在细胞内的积累和滞留,而不仅仅是 PARP 在 DNA 上的捕获。[2] 该研究表明,由于靶点抑制作用持续存在,rucaparib 的间歇性(例如每周一次)给药方案在临床前模型中可以达到与每日给药方案相当的抗肿瘤疗效,这表明替代给药方案具有潜在的临床应用价值。[2] 尽管体外试验显示其对 MX-1 异种移植瘤敏感,但该模型中缺乏疗效,这可能与该模型中肿瘤生长缓慢以及较高的这些肿瘤中的基线PARP活性。[2] |
| 分子式 |
C19H18FN3O
|
|---|---|
| 分子量 |
323.37
|
| 精确质量 |
323.143
|
| 元素分析 |
C, 70.57; H, 5.61; F, 5.88; N, 12.99; O, 4.95
|
| CAS号 |
283173-50-2
|
| 相关CAS号 |
1859053-21-6 (camsylate); 459868-92-9 (phosphate); 283173-50-2
|
| PubChem CID |
9931954
|
| 外观&性状 |
Yellow solid powder
|
| 密度 |
1.3±0.1 g/cm3
|
| 沸点 |
625.2±55.0 °C at 760 mmHg
|
| 闪点 |
331.9±31.5 °C
|
| 蒸汽压 |
0.0±1.8 mmHg at 25°C
|
| 折射率 |
1.649
|
| LogP |
2.85
|
| tPSA |
56.92
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
24
|
| 分子复杂度/Complexity |
466
|
| 定义原子立体中心数目 |
0
|
| SMILES |
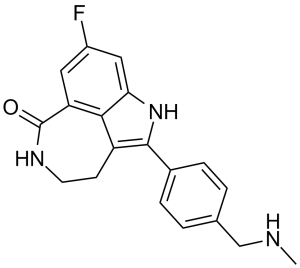
FC1=C([H])C2C(N([H])C([H])([H])C([H])([H])C3=C(C4C([H])=C([H])C(C([H])([H])N([H])C([H])([H])[H])=C([H])C=4[H])N([H])C(=C1[H])C3=2)=O
|
| InChi Key |
HMABYWSNWIZPAG-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C19H18FN3O/c1-21-10-11-2-4-12(5-3-11)18-14-6-7-22-19(24)15-8-13(20)9-16(23-18)17(14)15/h2-5,8-9,21,23H,6-7,10H2,1H3,(H,22,24)
|
| 化学名 |
6-fluoro-2-[4-(methylaminomethyl)phenyl]-3,10-diazatricyclo[6.4.1.04,13]trideca-1,4,6,8(13)-tetraen-9-one
|
| 别名 |
AG014699; PF-01367338; AG 14447; AG 014699; PF 01367338; AG-014699,PF01367338; AG-14447; AG14447; Trade name: Rubraca
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (7.73 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (7.73 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (7.73 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 30% propylene glycol, 5% Tween 80, 65% D5W: 30mg/mL 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.0924 mL | 15.4622 mL | 30.9243 mL | |
| 5 mM | 0.6185 mL | 3.0924 mL | 6.1849 mL | |
| 10 mM | 0.3092 mL | 1.5462 mL | 3.0924 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03413995 | Recruiting | Drug: Rucaparib | Prostate Cancer Metastatic | Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins |
September 10, 2018 | Phase 2 |
| NCT03462212 | Recruiting | Drug: Rucaparib Drug: Paclitaxel |
Advanced (Stage IIIB-C-IV) Ovarian, Primary Peritoneal and Fallopian Tube Cancer |
Fondazione Policlinico Universitario Agostino Gemelli IRCCS |
March 17, 2021 | Phase 1 Phase 2 |
| NCT04826198 | Recruiting | Drug: Rucaparib Drug: Olaparib |
Ovarian Cancer | Gustave Roussy, Cancer Campus, Grand Paris |
October 5, 2020 | Phase 1 Phase 2 |
AG-014699 inhibits Single strand break (SSB) repair to a similar extent regardless of cellular NF-κB status.Oncogene, 2012, 31(2), 251-264. |
|---|