| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Gastric H/K-ATPase (Ki = 120 nM)
|
|---|---|
| 体外研究 (In Vitro) |
SCH28080 [1] 的 Ki 为 0.12 μM,竞争性抑制 K+ 刺激的 ATP 水解。 SCH28080 的 IC50 为 0.029 μM,可阻断组胺引起的离体兔壁细胞对 [14C]氨基比林的吸收 [1]。 SCH28080 以剂量依赖性方式降低细胞活力。处理2小时和24小时后,IC50值分别为22.9 µM和15.3 µM。处理两小时后,100 µM 的细胞活力低于 10% [2]。较高剂量的 SCH28080 会导致细胞凋亡并使其具有细胞毒性 [2]。通过激活 IK ATP 并阻断 L 型电压门控 Ca2+ 通道,SCH28080 抑制胰岛素产生,降低细胞活力,并以剂量依赖性方式导致细胞凋亡/坏死 [2]。
|
| 体内研究 (In Vivo) |
SCH28080(20 mg/kg;腹腔注射)可抑制大鼠幽门结扎引起的胃溃疡[3]。
|
| 酶活实验 |
对新型抗分泌剂SCH 32651和SCH 28080的体外抗分泌活性以及在兔胃底黏膜微粒体膜制备中抑制(H++K+)-ATP酶活性的能力进行了评估。SCH 32651和SCH 28080抑制了组胺和二丁酰cAMP刺激的[14C]-氨基比林向分离的壁细胞的摄取,IC50值分别为约1.5和0.02微M。SCH 32651和SCH 28080竞争性地抑制了(H++K+)-ATP酶催化的K+刺激的ATP水解,Ki值分别为16.3和0.12微M。这两种化合物对酶的抑制作用不受巯基还原剂二硫苏糖醇或β-巯基乙醇添加的影响,通过稀释或洗涤很容易逆转,并且取决于用于刺激酶的KCl浓度。这些数据表明,SCH 32651和SCH 28080是K+刺激的ATP水解的可逆竞争性抑制剂[1]。
|
| 细胞实验 |
细胞活力测定 [2]
细胞类型: INS-1E 细胞 测试浓度: 3.1 μM、6.25 μM、12.5 μM、25 μM、50 μM , 100 μM 孵育时间: 2 小时 (hrs (小时))、24 小时 (hrs (小时)) 实验结果: 引起剂量依赖性细胞活力降低。 |
| 动物实验 |
Animal/Disease Models: Male Wistar rat (280-350g), Shay rat model [3]
Doses: 20mg/kg Route of Administration: intraperitoneal (ip) injection Experimental Results: 91% inhibitory effect on gastric ulcer in pyloric ligated rats. |
| 参考文献 |
|
| 其他信息 |
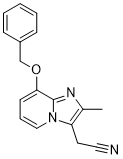
2-(2-甲基-8-苯基甲氧基-3-咪唑并[1,2-a]吡啶基)乙腈是一种咪唑并吡啶类化合物。
背景/目的:胰岛β细胞的葡萄糖刺激胰岛素分泌(GSIS)涉及葡萄糖的摄取和代谢、KATP通道的关闭和细胞膜电位(Vmem)的去极化、电压门控Ca2+电流(ICav)的激活和Ca2+内流,最终触发激素胞吐。除此经典途径外,KATP非依赖性机制,例如细胞内pH(pHi)或细胞体积的变化(这些变化也会影响β细胞的活力),也能诱导或调节胰岛素释放。在β细胞中,pHi的调节主要由Na+/H+交换器(NHE)完成。为了探究除非氢化氢通道(NHE)外,是否还有其他质子外排机制参与pH调节,我们检测了大鼠胰岛瘤细胞中非胃源性H+/K+ ATPase的存在,并评估了H+/K+ ATPase抑制剂SCH-28080对胰岛素分泌、细胞活力和凋亡的影响。[2] 方法:在INS-1E细胞培养中,采用逆转录PCR和Western blotting分析H+/K+ ATPase基因和蛋白的表达。使用BCECF,通过NH4Cl预脉冲法测定急性酸负荷后细胞内pH(pHi)的恢复情况。通过ELISA法测定细胞培养上清液中的胰岛素分泌量。使用膜片钳技术记录膜电位(Vmem)、K+和Ca2+电流。采用刃天青法(细胞活力)和细胞毒性试验测定细胞的总体反应。采用流式细胞术测定了平均细胞体积 (MCV)、细胞颗粒度(侧向散射;SSC)、磷脂酰丝氨酸 (PS) 暴露、细胞膜完整性、caspase 活性和线粒体膜电位 (ΔΨm)。[2] 结果:我们发现非胃 H+/K+ ATPase 的 α 亚基 (HKα2) 在 mRNA 和蛋白水平上均有表达。然而,与大鼠结肠组织相比,INS-1E 细胞中该亚基的 mRNA 丰度非常低。在 NH4Cl 预脉冲实验中,在无 Na+ 细胞外条件下未观察到 K+ 依赖性的细胞内 pH 值恢复。尽管如此,20 µM SCH-28080 在 1 小时内抑制了约 50% 的葡萄糖刺激胰岛素分泌 (GSIS),而基础胰岛素释放不受影响。L 型 ICav 阻滞剂硝苯地平在 10 和 20 µM 浓度下完全抑制了 GSIS。在 20 µM 浓度下,SCH-28080 对 ICav 的抑制作用与 20 µM 硝苯地平相当,此外,它还增强了在 -60 mV 处记录的 IKATP,并使 Vmem 超极化约 15 mV。SCH-28080 处理 2 小时和 24 小时后,细胞活力呈剂量依赖性抑制,IC50 值分别为 22.9 µM 和 15.3 µM。在 20 µM 浓度下,24 小时和 48 小时后,Annexin-V+、caspase+ 和碘化丙啶+ 细胞的百分比显著增加。同时,MCV 显著降低(凋亡体积减少,AVD),而 SSC 信号增强。当浓度高于 40-50 µM 时,SCH-28080 的细胞毒性逐渐增强,导致处理后 2 小时内坏死细胞数量急剧增加,并在 50 和 100 µM 浓度下 4 小时内导致线粒体膜电位 (ΔΨm) 破坏,而 10 和 20 µM 浓度在 24 小时内对 ΔΨm 没有影响。[2] 结论:我们证实了大鼠 INS-1E 细胞中 HKα2 的表达。然而,在给定条件下,该泵似乎没有功能。尽管如此,H+/K+ ATPase 阻断剂 SCH-28080 仍能抑制胰岛素分泌并诱导细胞死亡。重要的是,我们发现 SCH-28080 抑制 ICav 并激活 KATP 通道,这表明它们是该抑制剂的新型“脱靶点”,导致膜电位 (Vmem) 超极化并抑制胰岛素分泌。 |
| 分子式 |
C17H15N3O
|
|---|---|
| 分子量 |
277.3205
|
| 精确质量 |
277.122
|
| 元素分析 |
C, 73.63; H, 5.45; N, 15.15; O, 5.77
|
| CAS号 |
76081-98-6
|
| PubChem CID |
108137
|
| 外观&性状 |
Light yellow to brown solid powder
|
| 密度 |
1.16g/cm3
|
| 折射率 |
1.615
|
| LogP |
3.287
|
| tPSA |
50.32
|
| 氢键供体(HBD)数目 |
0
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
4
|
| 重原子数目 |
21
|
| 分子复杂度/Complexity |
385
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
PYKJFEPAUKAXNN-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C17H15N3O/c1-13-15(9-10-18)20-11-5-8-16(17(20)19-13)21-12-14-6-3-2-4-7-14/h2-8,11H,9,12H2,1H3
|
| 化学名 |
Imidazo(1,2-a)pyridine-3-acetonitrile, 2-methyl-8-(phenylmethoxy)-
|
| 别名 |
SCH28080; SCH-28080; 76081-98-6; Sch 28080; Sch-28080; 2-methyl-8-(phenylmethoxy)imidazo[1,2-a]pyridine-3-acetonitrile; SCH28080; Schering compound 28080; S28080; 2-(8-(benzyloxy)-2-methylimidazo[1,2-a]pyridin-3-yl)acetonitrile; SCH 28080.
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~360.59 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (9.01 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (9.01 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 3.6059 mL | 18.0297 mL | 36.0594 mL | |
| 5 mM | 0.7212 mL | 3.6059 mL | 7.2119 mL | |
| 10 mM | 0.3606 mL | 1.8030 mL | 3.6059 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。