| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
mAChR3/4/5
|
|---|---|
| 体外研究 (In Vitro) |
除了通过CYP2D6和CYP3A4进行氧化代谢外,索匹溴铵主要通过非酶水解进行代谢[1]。
|
| 体内研究 (In Vivo) |
通过以浓度依赖性方式降低豚鼠回肠组织的收缩活性,索氟溴铵表现出抗胆碱能作用。在大鼠模型中,溴化索吡啶可减少毒蕈碱受体激动剂毛果芸香碱引起的足垫出汗[1]。
|
| 毒性/毒理 (Toxicokinetics/TK) |
重要安全信息
Sofdra 仅供腋下皮肤外用。涂抹 Sofdra 后请立即洗手。涂抹 Sofdra 后请勿触摸腋下。Sofdra 易燃。涂抹 Sofdra 时请远离热源和明火。 哪些人不应使用 Sofdra? 如果您患有某些可能因服用抗胆碱能药物而加重的疾病,例如青光眼、重度溃疡性结肠炎 (UC) 或与重度 UC 相关的某些其他严重肠道问题、重症肌无力和干燥综合征,请勿使用 Sofdra。 使用 Sofdra 前我应该告知医护人员哪些信息? • 请告知您的医护人员您的所有健康状况,包括膀胱或肾脏问题、排尿困难、是否怀孕或哺乳,或计划怀孕或哺乳。目前尚不清楚 Sofdra 是否会对胎儿造成伤害或进入母乳。 • 请告知您的医疗保健提供者您正在服用的所有药物,包括处方药和非处方药,尤其是任何抗胆碱能药物。 Sofdra 可能有哪些副作用? 严重的副作用可能包括: • 视力模糊。如果出现视力模糊,请立即停止使用 Sofdra,并联系您的医疗保健提供者,在视力恢复清晰之前,请勿驾驶、操作机器或从事危险工作。• 出现新的或加重的尿潴留。如果您出现排尿困难、尿频、尿流细弱或滴尿、膀胱充盈或排尿困难,请立即停止使用 Sofdra 并联系您的医疗保健提供者。 Sofdra 最常见的副作用包括口干;视力模糊;腋下疼痛、发红、肿胀、瘙痒和刺激;瞳孔散大(散瞳);以及排尿困难。以上并非 Sofdra 的所有可能副作用。如需了解副作用方面的医疗建议,请咨询您的医生。 https://www.cliniexpert.com/article/983.html |
| 参考文献 | |
| 其他信息 |
溴化索非溴铵是一种小分子药物,目前处于IV期临床试验阶段,于2024年首次获批,用于治疗多汗症。
美国食品药品监督管理局(FDA)已批准12.45%溴化索非溴铵外用凝胶(Sofdra;Botanix)用于治疗9岁及以上成人和儿童的原发性腋窝多汗症。 据估计,美国约有1000万人患有多汗症,其特征是出汗异常增多,超过了调节体温所需的量。新闻稿指出,这种不成比例的出汗会对生活质量产生深远影响,包括工作效率、日常活动、情绪健康和人际关系。它是继痤疮和特应性皮炎之后第三大常见皮肤病。 “我们非常高兴能为美国1000万原发性腋窝多汗症患者提供一种新的治疗选择,”Botanix执行董事长Vince Ippolito在一份新闻稿中表示。“作为首个也是目前唯一的新化学实体,Sofdra代表了一种新的治疗方法,可供皮肤科医生用于治疗这种致残性疾病。” 此次获批是基于两项关键性3期CARDIGAN试验的结果,这两项试验评估了索非溴化铵与赋形剂相比的安全性和有效性。CARDIGAN I研究招募了350名受试者,他们被随机分配到每日一次使用15%索非溴化铵凝胶组或每日一次使用赋形剂凝胶组。主要疗效指标为:腋窝多汗症疾病严重程度量表(HDSM-Ax)7项总分较基线改善≥2分的受试者人数,以及受试者按重量法测定的汗液分泌量(GSP)较基线的变化。入选受试者需年满9岁,确诊为原发性腋窝多汗症,且症状持续至少6个月,HDSM-Ax评分为3或4分,双侧腋窝GSP至少为50 mg,双侧腋窝总GSP至少为150 mg。 CARDIGAN I 和 II 研究共纳入701例患者。在两项试验中,索匹溴铵治疗均达到了所有主要和次要终点,HDSM-Ax 7 和 GSP 评分较基线均有临床和统计学意义上的显著改善。 Botanix 计划于 2024 财年第三季度启动患者体验项目,以便符合条件的患者能够尽早获得治疗。这些患者将在远程医疗和医保报销流程的指导下,成为索匹溴铵的首批商业用户,预计将于第四季度初全面上市。 “索匹溴铵的获批对于多汗症患者群体来说是一个振奋人心的消息,他们一直苦于缺乏有效且便捷的治疗方案,”国际多汗症协会创始理事会成员、美国皮肤病学会前任主席 David Pariser 医学博士在新闻稿中表示。 “一种新的局部用药方案的出现令人振奋,它耐受性良好、疗效显著且使用方便,相信会受到患者和医生的欢迎。” 原发性多汗症是由神经信号异常触发外分泌汗腺过度活跃引起的,通常影响手掌、脚底、腋下,有时也会影响面部。它没有明确的病因,但可能具有家族遗传倾向。继发性多汗症是由潜在的疾病或某些药物引起的,可导致全身出汗。据梅奥诊所称,糖尿病、更年期、甲状腺疾病、某些类型的癌症、神经系统疾病和感染都可能导致继发性多汗症。 https://www.pharmacytimes.com/view/fda-approves-sofpironium-first-treatment-for-primary-axillary-hyperhidrosis |
| 分子式 |
C22H32BRNO5
|
|---|---|
| 分子量 |
470.397186279297
|
| 精确质量 |
469.146
|
| 元素分析 |
C, 56.17; H, 6.86; Br, 16.99; N, 2.98; O, 17.01
|
| CAS号 |
1628106-94-4
|
| 相关CAS号 |
1628251-49-9 (cation);1628106-94-4 (bromide); 2409055-48-5
|
| PubChem CID |
86301316
|
| 外观&性状 |
White to off-white solid powder
|
| tPSA |
72.8
|
| 氢键供体(HBD)数目 |
1
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
9
|
| 重原子数目 |
29
|
| 分子复杂度/Complexity |
555
|
| 定义原子立体中心数目 |
2
|
| SMILES |
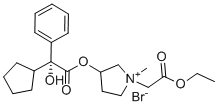
[Br-].O(C([C@](C1C=CC=CC=1)(C1CCCC1)O)=O)[C@@H]1CC[N+](C)(CC(=O)OCC)C1
|
| InChi Key |
FIAFMTCUJCWADZ-JOFREBOKSA-M
|
| InChi Code |
InChI=1S/C22H32NO5.BrH/c1-3-27-20(24)16-23(2)14-13-19(15-23)28-21(25)22(26,18-11-7-8-12-18)17-9-5-4-6-10-17;/h4-6,9-10,18-19,26H,3,7-8,11-16H2,1-2H3;1H/q+1;/p-1/t19-,22+,23?;/m1./s1
|
| 化学名 |
3-((R)-2-cyclopentyl-2-hydroxy-2-phenylacetoxy)-1-(2-ethoxy-2-oxoethyl)-1-methylpyrrolidin-1-ium bromide
|
| 别名 |
BBI4000; Ecclock; 1628106-94-4; Sofdra; BBI-4000; Sofpironium bromide [USAN];BBI-4000; Sofpironium bromide
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~212.59 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.31 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.31 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (5.31 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.1259 mL | 10.6293 mL | 21.2585 mL | |
| 5 mM | 0.4252 mL | 2.1259 mL | 4.2517 mL | |
| 10 mM | 0.2126 mL | 1.0629 mL | 2.1259 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。