| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 100mg |
|
||
| Other Sizes |
|
| 靶点 |
Na+/K+-ATPase
|
|---|---|
| 体外研究 (In Vitro) |
旋花蛋白对正常细胞无毒,对癌细胞(MCF-7、A549和HepG2细胞;0~10 μM;24小时)具有有效的生长抑制作用[1]。当 vololuvulin(0.5 至 500 µM)存在时,PBMC 中没有明显的细胞毒性。在 MCF-7 细胞上使用 volvulin (2 µM) 可将细胞周期终止于 G2/M 期 [1]。旋花蛋白对正常细胞无毒,可有效抑制MCF-7、A549和HepG2细胞中癌细胞的生长。在三种癌细胞(MCF-7、A549 和 HepG2)中,与未处理的对照相比,旋花青素抑制了检查点和细胞周期蛋白依赖性激酶的表达。通过使用旋转蛋白,可以将蛋白质从细胞核定位到细胞质和细胞膜。旋花蛋白具有糖苷配基部分且不含糖单元,是一种单糖强心苷。通过 p53 依赖性和 p53 独立机制抑制多种生化信号通路并在 G2/M 期停止细胞周期,volvulin 可引起细胞凋亡 [1]。
肺癌是癌症相关死亡中最常见的,而乳腺癌是女性中第二大主要癌症,占全球死亡人数最多。癌症是一种异质性疾病,根据激素受体和人类表皮生长因子受体2的存在与否,由几种亚型组成。已经开发了几种针对癌症生物标志物的药物;然而,由于癌症的高复发率和对这些药物的基本或获得性耐药性,它们的效率还不够,这导致了部分治疗可能性。最近对强心苷(CG)的研究将其定位为强效细胞毒性药物,靶向多种途径,在许多癌症中启动凋亡和自噬细胞死亡。在本研究中,我们的目的是鉴定天然CG(Strophanthidin)在人类乳腺癌(MCF-7)、肺癌(A549)和肝癌(HepG2)细胞中的抗癌活性。我们的研究结果表明,毒毛汉苷在MCF-7、A549和HepG2细胞中具有剂量依赖性的细胞毒性作用,这进一步得到了药物治疗中DNA损伤的支持。Strophanthidin将细胞周期阻滞在G2/M期;通过检测检查点和细胞周期蛋白依赖性激酶在毒毛蕨素诱导的细胞中的抑制表达,进一步验证了这一作用。此外,毒毛汉苷抑制了MAPK、PI3K/AKT/mTOR和Wnt/β-catenin信号传导中几种关键蛋白的表达,如MEK1、PI3K、AKT、mTOR、Gsk3α和β-catening。目前的研究充分显示了毒毛汉苷在调节细胞周期阻滞、凋亡和自噬性细胞死亡中各种关键蛋白的表达中的作用。我们的计算机研究表明,毒毛汉苷可以与来自不同途径的几种关键蛋白质相互作用。综上所述,这项研究证明了毒毛汉苷作为一种有前景的抗癌药物的可行性,这可能是一种新的抗癌药物。[1] Str/Strophanthidin0.1 nmol/L刺激Na+、K+-ATP酶活性(P<0.05),但对HR、LVP和+/-dp/dt(max)没有影响。Str 1 nmol/L增加了+dp/dt(max)(P<0.05)和Na+、K+-ATP酶活性(P<0.01)。Str 10和100 nmol/L显著增加了LVP(P<0.05)和+dp/dt(max)(P<0.05或P<0.01),对Na+、K+-ATP酶活性没有显著影响。然而,Str 1-100微摩尔/升首先增强了LVP和+dp/dtmax(P<0.01),然后由于不规则收缩而降低了它们,Strophanthidin/Str对Na+,K+-ATP酶活性的影响显示出浓度依赖性的抑制作用(P<0.01)。 结论:较高浓度的Strophanthidin/Str产生的正性肌力作用和不规则收缩是由于抑制了Na+,K+-ATP酶活性,而较低浓度的Str的正性变力作用与抑制Na+,K+-ATP酶活动无关。[2] 我们研究了用Strophanthidin抑制Na-K泵对细胞内Ca2+浓度([Ca2+]i)、肌浆网(s.r.)Ca2+含量和膜电流的影响。通过积分施加10mM咖啡因产生的Na-Ca交换电流来测量s.r.Ca2+含量。施用毒毛汉苷增加了舒张和收缩[Ca2+]i。5分钟后,伴随着s.r.Ca2+含量从17.9+/-1.5微摩尔/升的静息值增加到36.9+/-3.3微摩尔/l(n=16)。还测量了施用毒毛汉苷前后细胞内外Ca2+的收缩通量。在毒毛蕨苷存在的情况下,Ca2+流出(作为Na-Ca交换尾流的积分测量)稳步上升,而Ca2+流入(L型Ca2+电流的积分)减少。尽管如此,s.r.Ca2+含量仍大幅上升。在Cd2+(100微M)存在的情况下,抑制L型Ca2+电流,毒毛汉苷对电流的影响可以忽略不计,这表明去极化过程中通过Na-Ca交换的Ca2+内流并不能解释s.r.Ca2+含量的增加。这表明收缩期Ca2+通量的变化不是毒毛蕨素诱导的s.r.Ca2+增加的原因。我们得出结论,当Na-K泵受到抑制时,心脏细胞获得Ca2+的主要机制是舒张期的净内流[3]。 |
| 细胞实验 |
细胞活力测定 [1]
细胞类型: MCF-7、A549 和 HepG2 细胞 测试浓度: 0~10 μM 孵化持续时间:24小时 实验结果:抑制三种不同癌细胞的增殖。 细胞活力测定[1] 通过MTT法测定Strophantidin对MCF-7、A549、HepG2和正常细胞如L132、WRL68和PBMCs的抗增殖作用。将每孔约4000个细胞铺在96孔细胞培养微孔板中,并在完全培养基(含有10%FBS和抗生素的DMEM)中孵育过夜,使细胞粘附在板上。然后在无血清培养基中用15至0.1μM的不同浓度的毒毛汉苷处理细胞24小时。进行MTT测定以鉴定细胞存活率。使用多模平板读数器在570nm和650nm的参考波长(非特异性读数)下读取溶解的甲赞的吸光度。 细胞周期分析[1] 接种约1×105-106个细胞并孵育过夜,然后用Strophanthidin处理24小时。将适量细胞加入锥形管中,以1000 rpm离心3分钟。然后用冷磷酸缓冲盐水(PBS)洗涤细胞并涡旋10秒,以获得单细胞悬浮液。然后,在4°C下用4.5 ml冷冻乙醇(100%)固定细胞30分钟。然后用冷PBS冲洗细胞以去除乙醇,然后在37°C的黑暗中用10μg/ml的RNase孵育1-2小时。孵育后,用0.25μg/ml碘化丙啶对固定细胞染色30分钟,并用流式细胞仪测量细胞周期分布。 实时荧光定量PCR基因表达研究[1] 按照手册说明使用TRIzol®试剂分离总细胞RNA。用Strophanthidin处理细胞24小时,在TRIzol试剂中分离总RNA。使用NanoDrop估算纯度和浓度。Verso互补DNA(cDNA)合成试剂盒用于按照制造商的说明合成cDNA。总共2μg的预处理RNA用于cDNA的合成。在罗氏LightCycler 480系统中使用Origin SYBR Green Master Mix进行实时定量PCR。将RNA表达水平标准化为GAPDH的水平,并使用ΔΔCt法计算,log2值绘制在图中。本研究中使用的所有引物均列于补充表1中。 酶联免疫吸附试验[1] 简而言之,用致死剂量的Strophanthidin处理细胞24小时,用RIPA裂解缓冲液提取总细胞裂解液。使用胱天蛋白酶3、7、8和9的酶联免疫吸附试验(ELISA)抗体。实验是按照制造商的指导方针进行的。同样,我们进行了ELISA,以了解Strophanthidin在通路激活、细胞生长和凋亡中的作用。我们使用PathScan®MAP激酶多靶点夹心ELISA试剂盒来了解磷酸化MEK1/2(Ser217/Ser221)、磷酸化p38 MAPK(Thr180/Tyr182)、磷酸性p44/42 MAPK(Thr202/Tyr204)和磷酸化SAPK/JNK(Thr183/Tyr185)的磷酸化。在450nm处测量吸光度。将实验重复三次,并将获得的结果绘制在条形图中。 蛋白质印迹分析[1] 细胞最初用Strophantidin处理24小时。然后收集处理过的细胞,并在含有150 mM NaCl、100 mM Tris(pH 8.0)、1%Triton X-100、1%脱氧胆酸、0.1%十二烷基硫酸钠(SDS)、5 mM EDTA、10 mM甲酸钠、1 mM原钒酸钠、2 mM亮肽、2 mM抑肽酶、1 mM苯甲基磺酰氟、1 mM二硫苏糖醇和2 mM pepstatin A的裂解缓冲液中,以及蛋白酶抑制剂混合物中,在冰上裂解30分钟。在4°C下以14000 g离心15分钟后,收集上清液作为细胞总蛋白含量。通过Bradford蛋白质估算分析估算总蛋白质的浓度。对于不同大小的蛋白质,在12-15%的SDS聚丙烯酰胺凝胶电泳(PAGE)上分离出等浓度(30μg)的总蛋白质,并使用Trans-Blot Turbo Transfer System(Bio-Rad)将其转移到聚偏二氟乙烯(PVDF)膜上。然后用5%牛血清白蛋白(BSA)封闭膜,并在4°C下与一抗孵育过夜。用含有150 mM NaCl、10 mM Tris和0.1%吐温20的TBST在pH 7.4下洗涤三次后,将膜与辣根过氧化物酶(HRP)偶联的二抗一起孵育1小时,并以5分钟的间隔用TBST洗涤五到六次。用化学发光ECL底物检测免疫反应蛋白,并使用C-DiGit化学发光蛋白质印迹成像系统(LI-COR)进行定量。将独立实验的平均密度数据归一化为对照实验的数据。抗体的获取方式如下:胱天蛋白酶3、7和9以及PARP-1购自Cell Signaling Technology,使用Chk1、Chk2、细胞周期蛋白D1、p53、AKT、p38、MEK1、mTOR、CDK6、SAPK/JNK、C-Myc、BAX、JAK、STAT3、GSK3α、β-catenin、Beclin 1、p62、LC3、PI3K和GAPDH。 免疫荧光[1] 进行免疫荧光以了解用Strophanthidin处理后的蛋白质迁移。将约0.3×106个细胞接种在6孔板的盖玻片顶部。16小时后,用Strophantidin处理细胞并孵育24小时。孵育后,用4%多聚甲醛固定细胞20分钟,再次用0.1%Triton X孵育20分钟。盖玻片用1X TBS洗涤四至五次后,用5%BSA封闭1小时。然后将盖玻片与一抗在4°C下孵育过夜。然后用1X TBS洗涤盖玻片,并在二抗(Alexa Fluor 488)中孵育2小时。然后在黑暗中用0.1μg/ml浓度的DAPI洗涤盖玻片并孵育20分钟,并用1X TBS洗涤5至6次。然后将盖玻片转移到涂有ProLong Gold Antifade Mountant的干净载玻片上。去除过量的Antifade,用蜡密封载玻片,在放大40倍的荧光显微镜下观察。 s.r.Ca2+含量和肌膜Ca2+通量的定量[3] 如前所述,通过向电压钳位细胞施加10mM咖啡因产生的内向Na-Ca交换电流被积分并转化为总Ca2+通量。通过积分膜电流计算电压钳脉冲期间和之后Ca2+的净运动。去极化过程中Ca2+电流的积分是相对于去极化前的电流水平进行的。当膜电流超过零水平时,积分开始跟随电容电流,并持续到脉冲结束。尾电流的积分始于容量电流结束和(较慢)尾电流开始之间的拐点。本实验在豚鼠细胞中发现的一个并发症是,在咖啡因产生的初始瞬时内向电流之后,电流放松到一个通常比初始水平更内向的值(见图2)。这种电流的起源尚不清楚。我们使用最终的稳态水平作为积分的基线。由此引入的任何误差都可能影响s.r.Ca2+含量的基础测量。然而,它不会影响对s.r.Ca2+变化的估计,因为这种稳态电流的水平不受Strophanthidin的影响。Na-Ca交换电流首先针对非电致Ca2+排出途径的活性进行了校正。简而言之,需要纠正这样一个事实,即在咖啡因反应期间,一些Ca2+通过Na-Ca交换以外的机制从细胞质中去除,因此不会产生电流。该电流的大小估计如下。(1)在对照条件下(kcont)和(2)在10mM Ni2+(kNi)抑制Na-Ca交换的情况下测量咖啡因反应的衰减速率常数。将测量的Na-Ca交换通量乘以kcont/(kcont–kNi),得到校正的总Ca2+通量。这种校正用于咖啡因或复极(尾流)激活的Na-Ca交换通量。使用的倍增因子(从豚鼠心肌细胞获得)为1.19(Choi和D.Eisner,未发表的观察结果)。细胞体积是根据豚鼠的膜电容:体积比5pF/pl获得的膜表面积计算的。Ca2+含量和肌膜通量的所有变化都与计算出的细胞体积有关 |
| 动物实验 |
离体心脏的制备:本研究使用体重250±20 g的雌雄豚鼠。迅速取出心脏,经主动脉固定,并在改良的Langendorff灌注装置上以恒定灌注压(10 kPa)进行灌注。将装有生理盐水的聚乙烯套管插入左心室腔,并连接压力传感器,通过该传感器在多导生理记录仪上记录心率(HR)、左心室压力(LVP)及其一阶导数(±dp/dtmax)。心脏灌注液为KH缓冲溶液(37℃,pH 7.4,95% O₂和5% CO₂饱和)。KH缓冲溶液的成分如下(mmol/L):NaCl 118、NaHCO₃ 25.0、KCl 4.7、KH₂PO₄ 1.2、MgSO₄ 1.2、CaCl₂ 2.5和葡萄糖11.0。所有心脏首先在Langendorff灌注装置中用KH溶液灌注20-30分钟以稳定状态,然后随机分为8组(每组6-8颗心脏)。对照组用KH缓冲液灌注心脏,其余7组(毒毛旋花子苷/Str)分别用含有不同浓度毒毛旋花子苷/Str(0.1、1、10、100 nmol/L或1、10、100 µmol/L)的KH溶液灌注心脏。连续记录20分钟的心率(HR)、左心室压力(LVP)和±dp/dt(max)值。[2]
离体豚鼠心脏通过主动脉以Langendorff灌注模式进行灌注。使用八通道生理仪器记录心率(HR)、左心室压力(LVP)和LVP的一阶导数(±dp/dt(max))。采用比色法测定心肌肌膜Na+,K+-ATP酶活性。[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
6185 小鼠静脉注射 LD50 330 ug/kg CRC 抗生素化合物手册,第 1 卷 - ,Berdy, J.,Boca Raton, FL,CRC Press,1980,8(2)(224),1982
6185 小鼠脑内注射 LD50 63 ug/kg 行为:惊厥或对癫痫阈值的影响 Arzneimittel-Forschung。 Drug Research., 11(908), 1961 6185 cat LD50 静脉注射 224 ug/kg Journal of Pharmacology and Experimental Therapeutics., 103(420), 1951 [PMID:14908859] 6185 cat LDLo 未报告 260 ug/kg Archives Internationales de Pharmacodynamie et de Therapie., 148(471), 1964 [PMID:14181242] 6185 兔 LDLo 静脉注射 110 ug/kg Naunyn-Schmiedeberg's Archive fuer Experimentelle Pathologie und Pharmakologie., 185(329), 1937 |
| 参考文献 |
|
| 其他信息 |
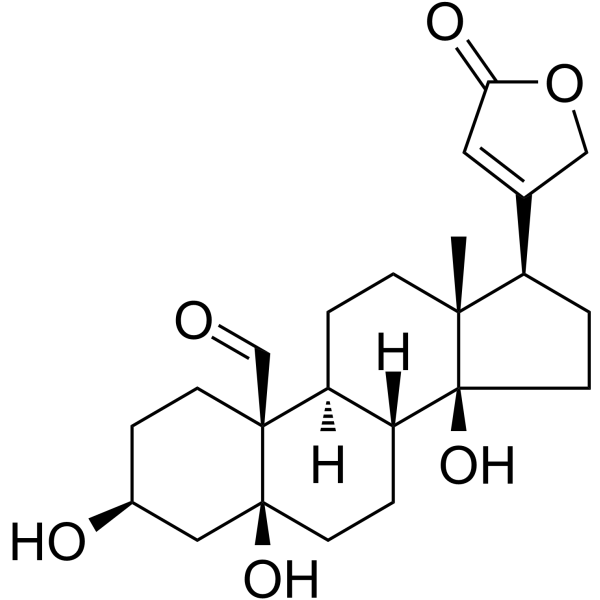
毒毛旋花子苷是一种3β-羟基甾体、14β-羟基甾体、5β-羟基甾体、19-氧代甾体,属于强心苷类化合物,也是一种甾体醛。它在功能上与5β-强心苷相关。
据报道,毒毛旋花子苷存在于夏花龙胆(Adonis aestivalis)、美丽紫菀(Erysimum pulchellum)和其他有相关数据的生物体中。 3β,5,14-三羟基-19-氧代-5β-强心苷-20(22)-烯内酯。它是从毒毛旋花子属植物(Strophanthus Kombe)、无刺毒毛旋花子(S. gratus)和其他物种中分离得到的强心苷元;它是一种剧毒物质,曾被用作洋地黄。同义词:阿普西马林;科尔乔林;毒毛旋花子毒素;综上所述,我们的体外和计算机模拟实验表明,天然化合物毒毛旋花子苷对乳腺癌、肺癌和肝癌细胞具有显著的抗癌作用。我们已阐明了这三种癌细胞凋亡的可能机制(图10)。毒毛旋花子苷抑制MCF-7细胞中PI3K的表达,而PI3K是PI3K/AKT/mTOR信号通路的关键蛋白。这种抑制作用导致AKT的进一步激活,并抑制mTOR,同时还表现出对p53的多步骤抑制,进而导致抗凋亡蛋白(Bcl-2)的失调和细胞凋亡。mTOR的抑制导致Beclin 1的下调,并刺激LC3和p62复合物的抑制,从而抑制自噬。在A549细胞中,由于PI3K的下调,MEK1受到抑制,并通过抑制Gsk3α和β-catenin发挥关键作用,而Gsk3α和β-catenin可直接靶向c-Myc和cyclin D1,从而影响细胞凋亡。MEK1失调可靶向p38MAPK,并抑制STAT3和c-Myc的表达,进而启动细胞凋亡。A549细胞表现出与其增殖速率相符的自噬通量,而毒毛旋花子苷通过抑制MEK1来抑制LC3和p62复合物的表达;因此,该化合物似乎可以抑制自噬。自噬的抑制会加剧细胞凋亡,而细胞凋亡是癌细胞维持细胞能量和营养稳态的关键机制。 MEK1通过多步骤刺激激活BAX的表达,这可能是启动caspase 7激活的重要因素,进而导致caspase 3的表达,并通过死亡受体信号通路和caspase介导的细胞凋亡途径诱导HepG2细胞凋亡。此外,毒毛旋花子苷在癌细胞中表现出差异表达,表明其可诱导p53依赖性和p53非依赖性细胞凋亡。据我们所知,这是首个研究毒毛旋花子苷如何通过改变多种生化凋亡信号转导通路(如MAPK信号通路、PI3K/AKT/mTOR通路和Wnt/β-catenin通路)来启动细胞凋亡的研究。总之,本研究首次揭示了毒毛旋花子苷通过抑制多种生化信号通路,并利用p53依赖性和p53非依赖性机制将细胞周期阻滞在G2/M期来诱导细胞凋亡。 [1] 总之,我们的结果表明,低浓度的毒毛旋花子苷仍具有正性肌力作用,其机制并非通过抑制Na+,K+-ATP酶实现。[2] 总之,我们发现,肌浆网钙离子含量的增加伴随着收缩期钙离子含量的减少,这表明舒张期每次脉搏间钙离子流入增加,超过了收缩期净流出的增加,从而导致肌浆网钙离子含量的增加。[3] |
| 分子式 |
C23H32O6
|
|---|---|
| 分子量 |
404.49658
|
| 精确质量 |
404.22
|
| 元素分析 |
C, 68.29; H, 7.97; O, 23.73
|
| CAS号 |
66-28-4
|
| PubChem CID |
6185
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.432 g/cm3
|
| 沸点 |
620.7ºC at 760 mmHg
|
| 熔点 |
169ºC
|
| 闪点 |
214.9ºC
|
| 折射率 |
1.674
|
| LogP |
1.898
|
| tPSA |
104.06
|
| 氢键供体(HBD)数目 |
3
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
29
|
| 分子复杂度/Complexity |
777
|
| 定义原子立体中心数目 |
8
|
| SMILES |
O=C1OCC([C@H]2CC[C@@]3([C@@H]4CC[C@]5(O)C[C@H](CC[C@]5(C=O)[C@H]4CC[C@]23C)O)O)=C1
|
| InChi Key |
ODJLBQGVINUMMR-HZXDTFASSA-N
|
| InChi Code |
InChI=1S/C23H32O6/c1-20-6-3-17-18(4-8-22(27)11-15(25)2-7-21(17,22)13-24)23(20,28)9-5-16(20)14-10-19(26)29-12-14/h10,13,15-18,25,27-28H,2-9,11-12H2,1H3/t15-,16+,17-,18+,20+,21-,22-,23-/m0/s1
|
| 化学名 |
(3S,5S,8R,9S,10S,13R,14S,17R)-3,5,14-trihydroxy-13-methyl-17-(5-oxo-2H-furan-3-yl)-2,3,4,6,7,8,9,11,12,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthrene-10-carbaldehyde
|
| 别名 |
k-Strophanthidin; Strophanthidin; strophanthidin; Convallatoxigenin; Strophanthidine; Corchsularin; k-Strophanthidin; Corchorgenin; Erysimupicrone; ...; 66-28-4; k Strophanthidin; NSC 86078; NSC86078; NSC-86078; Apocymarin
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
Ethanol : ~25 mg/mL (~61.80 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (6.18 mM) (饱和度未知) in 10% EtOH + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL 澄清 EtOH 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL 生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.18 mM) (饱和度未知) in 10% EtOH + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清乙醇储备液加入 900 μL 20% SBE-β-CD 生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.18 mM) (饱和度未知) in 10% EtOH + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.4722 mL | 12.3609 mL | 24.7219 mL | |
| 5 mM | 0.4944 mL | 2.4722 mL | 4.9444 mL | |
| 10 mM | 0.2472 mL | 1.2361 mL | 2.4722 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。