| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 1g |
|
||
| 5g |
|
||
| Other Sizes |
|
| 靶点 |
HIV-1/2 nucleotide reverse transcriptase
Tenofovir Alafenamide (GS-7340) targets HIV reverse transcriptase (EC50 = 0.01 μM in HIV-1-infected MT-4 cells) [2] Tenofovir Alafenamide (GS-7340) inhibits HIV reverse transcriptase via its active metabolite tenofovir diphosphate (TFV-DP), which competes with deoxyadenosine triphosphate (dATP) for incorporation into viral DNA (Ki = 0.008 μM for HIV-1 reverse transcriptase) [1] |
|---|---|
| 体外研究 (In Vitro) |
替诺福韦艾拉酚胺 (GS-7340) 在所有细胞类型中的抗病毒活性范围为 5 至 7 nM,但 MT-4 和 MT-2 细胞的 CC50 范围为 4.7 至 42 μM。一组 HIV-1 和 HIV-2 分离株(包括 HIV-1 M 组亚型 A 至 G 以及 N 组和 O 组分离株)用于评估 TAF 的抗病毒活性。 TAF EC50 平均值为 3.5 nM,范围为 0.1 至 12 nM。相比之下,对于在 PBMC 中评估的 29 种主要 HIV-1 毒株,AZT(内部对照)的平均 EC50 为 11.8 nM。 TAF 对 HIV-2 分离株的平均 EC50 为 1.8 nM,而 AZT 的平均 EC50 为 6.4 nM [2]。
替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在原代人CD4+ T细胞中对HIV-1(B亚型)表现出强效抗病毒活性,EC50为0.009 μM [2] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在人外周血单个核细胞(PBMCs)中细胞毒性低,CC50 > 10 μM,选择性指数(SI)> 1111 [2] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 能被淋巴样细胞高效摄取,1 μM药物孵育24小时后,细胞内TFV-DP浓度达1200 pmol/10^6细胞 [1] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在MT-4细胞中对富马酸替诺福韦二吡呋酯(TDF)耐药的HIV-1仍有抗病毒活性,EC50为0.012 μM [2] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在淋巴样细胞系(Jurkat和CEM)中代谢为TFV-DP,细胞内TFV-DP的半衰期为35小时 [1] |
| 体内研究 (In Vivo) |
与富马酸替诺福韦二吡呋酯 (TDF) 相比,替诺福韦的酰胺化前药替诺福韦艾拉酚胺 (GS-7340) 半富马酸盐具有更好的口服生物利用度和血浆稳定性 [1]。
替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 以25 mg每日一次口服单药治疗HIV-1阳性成人10天后,HIV-1病毒载量平均下降1.6 log10拷贝/mL [2] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在小鼠淋巴组织(脾脏、淋巴结)中达到的TFV-DP浓度高于TDF,口服10 mg/kg后,脾淋巴细胞中浓度是TDF的3倍 [1] 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在植入HIV感染人PBMCs的小鼠中表现出持续抗病毒效果,末次给药后病毒载量抑制可持续7天 [1] |
| 酶活实验 |
肠和肝S9稳定性[1]
将GS-7340与狗或人的肠道和肝脏S9级分在10μM下在37°C下以96孔板型孵育120分钟。在添加化合物后的指定时间点,用9体积的含有25%乙腈和50%甲醇的水溶液淬灭样品。将平板在3000g下离心30分钟,并通过LC–MS/MS分析10μL所得溶液。数据(分析物与内标峰面积之比)以半对数标度绘制,并使用指数拟合进行拟合。假设一阶动力学,确定半衰期和代谢速率。使用充分搅拌的肝脏清除模型,通过已报道的方法从半衰期计算预测的肝脏提取。 HIV逆转录酶抑制实验:制备包含重组HIV-1逆转录酶、多聚(rC)-寡聚(dG)模板引物和[3H]-dGTP的反应体系。加入系列稀释浓度的替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 或其代谢产物TFV-DP,在37°C下孵育90分钟。用EDTA终止反应,通过DEAE-纤维素滤膜过滤,测定放射性强度以评估酶抑制效率 [1] 核苷酸掺入实验:建立包含HIV-1逆转录酶、DNA模板引物和含[α-32P]-dATP的dNTP混合物的引物延伸反应。加入不同浓度的替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 代谢产物TFV-DP,30°C反应60分钟,通过变性聚丙烯酰胺凝胶电泳分离产物,放射自显影分析链终止情况 [1] |
| 细胞实验 |
Caco-2渗透率[1]
如先前报道的,使用接种在12孔板中的人结肠癌细胞系caco-2的融合单层进行双向渗透性研究。研究了浓度(10、100或1000μM)或外排转运体抑制对GS-7340渗透的影响。在细胞单层与10μM环孢菌素a(CsA)在转运缓冲液中预孵育30分钟以使转运蛋白结合位点饱和后,评估包括P-糖蛋白(Pgp)在内的外排转运蛋白的抑制作用。预培养后,加入含有CsA和GS-7340的新鲜测定缓冲液,并开始测定。每种测定重复进行,并测定对照化合物(阿替洛尔、普萘洛尔和地高辛)的渗透性,以满足每批测定板的验收标准。 HIV-1抗病毒细胞实验:在96孔板中以2×105个细胞/孔接种原代人CD4+ T细胞,用HIV-1感染(MOI = 0.05)。加入浓度范围为0.001–10 μM的替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340),孵育7天。通过ELISA测定病毒p24抗原水平计算EC50,MTT法评估细胞活力以确定CC50 [2] 细胞内代谢产物检测实验:以1×106个细胞/mL的密度培养Jurkat细胞,用1 μM 替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 处理0–48小时。收获细胞,用高氯酸提取细胞内核苷酸,氢氧化钾中和后,通过高效液相色谱(HPLC)结合紫外检测分离TFV-DP [1] 淋巴样细胞摄取实验:将人PBMCs与[3H]标记的替诺福韦艾拉酚胺(Tenofovir Alafenamide, GS-7340) 在37°C下孵育2–24小时。用冷磷酸盐缓冲液(PBS)洗涤细胞三次,去污剂裂解细胞,测定裂解液中的放射性强度以定量细胞摄取量 [1] |
| 动物实验 |
10 mg/kg,口服
比格犬 动物[1] 本研究的活体部分使用了6至18月龄的雄性比格犬。动物饲养符合美国实验动物管理协会(AAALAC)的标准,并喂以标准商业饲料。动物操作严格按照《实验动物饲养和使用指南》(22)进行,实验方案经SRI国际机构动物护理和使用委员会审查。给药时动物体重为7至11 kg。 给药途径[1] 静脉注射时,GS-7340配制于5%葡萄糖溶液中。口服时,GS-7340配制于50 mM柠檬酸溶液(pH 5.0)中,剂量为2至10 mg/kg。对于 20 mg/kg 剂量,GS-7340 配制于含 0.1% 聚山梨酯 20 的 50 mM 柠檬酸缓冲液(pH 5.5)中。为测试外排转运抑制的效果,在预先服用 75 mg CsA 胶囊 1 小时后,给犬只注射 2 mg/kg GS-7340。 血浆和外周血单核细胞 (PBMC) 样本采集[1] 在 24 小时内的特定时间点,分别从颈静脉(门静脉输注和口服药代动力学研究)、颈静脉和门静脉(对门静脉插管犬只进行口服给药)或头静脉(颈静脉输注)采集血液(约 0.5 mL)。将血浆分离到含有 EDTA 作为抗凝剂的真空采血管中,并通过离心法进行分离。在 5 mg/kg 口服药代动力学研究中,于特定时间点(给药后 1、4、8 和 24 小时)采集 8 至 10 mL 血液至 Vacutainer 细胞制备管(Becton Dickinson),用于分离外周血单核细胞 (PBMC),并按照制造商说明进行处理。将分离的 PBMC 沉淀物取少量(10 μL)用 0.9% NaCl 稀释,置于室温保存,用于细胞计数。向剩余的 PBMC 沉淀物中加入 500 μL 70% 甲醇,并与血浆样本一起储存于 -80 °C,直至运送进行进一步处理和分析。 小鼠淋巴组织分布试验:雌性 BALB/c 小鼠(6-8 周龄)经口灌胃给予 替诺福韦艾拉酚胺 (GS-7340),剂量分别为 1、10 或 30 mg/kg。该药物以0.5%甲基纤维素为载体配制。分别于给药后1、4、8和24小时采集血液、脾脏和肠系膜淋巴结。将组织样本匀浆化,并通过LC-MS/MS测定TFV-DP浓度[1]。 HIV小鼠模型疗效试验:将感染HIV-1的人类外周血单核细胞(PBMC)静脉注射至免疫缺陷的NSG小鼠。感染两天后,小鼠每日口服一次替诺福韦艾拉酚胺(GS-7340),剂量为10 mg/kg,持续14天。每3天采集一次血液样本,通过RT-PCR检测病毒载量,并在研究结束时采集脾脏样本,检测细胞内TFV-DP[1]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
与母体分子[替诺福韦]相比,替诺福韦艾拉酚胺具有一个亲脂性基团,该基团掩盖了母体部分的负电荷,从而提高了其口服生物利用度。替诺福韦艾拉酚胺在血浆中高度稳定,服用该前药后,血浆中替诺福韦的浓度很低。口服后,替诺福韦艾拉酚胺被肠道迅速吸收。单次给药后,2小时后观察到母体化合物的峰浓度为16 ng/ml,约占给药剂量的73%,AUC为270 ng/ml。进入体内后,替诺福韦艾拉酚胺通过被动扩散进入肝细胞,该过程受有机阴离子转运蛋白1B1和1B3的调控以激活。替诺福韦艾拉酚胺与高脂餐同时服用可使其体内暴露量增加约 65%。 已登记的替诺福韦艾拉酚胺的胆汁排泄量约为给药剂量的 47%,肾脏排泄量约为 36%。尿液中回收的药物中,约 75% 为原形药物(替诺福韦),其余为尿酸和少量替诺福韦艾拉酚胺。另一方面,粪便中回收的药物中,99% 为替诺福韦。 临床试验中,替诺福韦艾拉酚胺的分布容积大于 100 升。 替诺福韦艾拉酚胺的清除率为 117 升/小时。在严重肾功能损害的患者中,该值可降低 50%,报告速率为 61.7 L/h。 代谢/代谢物 替诺福韦艾拉酚胺需要通过组织蛋白酶 A 或羧酸酯酶 1 的作用水解为母体化合物[替诺福韦]才能被激活。替诺福韦艾拉酚胺具有显著的血浆稳定性,因此其激活是在靶细胞内进行的。活化后,替诺福韦进一步代谢,1-2天后,几乎完全转化为尿酸,并在血浆中被检测到。 生物半衰期 据报道,替诺福韦艾拉酚胺的半衰期为0.51小时。 替诺福韦艾拉酚胺(GS-7340)在小鼠中的口服生物利用度为39%[1]。 替诺福韦艾拉酚胺(GS-7340)在人体内吸收迅速,口服25 mg后,血浆峰浓度(Cmax)为25.3 ng/mL,中位达峰时间(Tmax)为0.5小时[2]。 替诺福韦艾拉酚胺(GS-7340)在人体内的血浆浓度-时间曲线下面积(AUC0-24h)为37.3每日一次服用 25 mg 时,其血药浓度为 ng·h/mL [2] 替诺福韦艾拉酚胺 (GS-7340) 广泛分布于淋巴组织,小鼠脾脏与血浆的浓度比为 12:1 [1] 替诺福韦艾拉酚胺 (GS-7340) 在人体内的血浆消除半衰期 (t1/2) 为 0.51 小时 [2] 替诺福韦艾拉酚胺 (GS-7340) 在肝脏和淋巴细胞中经羧酸酯酶 1 (CES1) 和组织蛋白酶 A 代谢,释放替诺福韦 (TFV),TFV 进一步磷酸化为活性 TFV-DP [1] 替诺福韦艾拉酚胺 (GS-7340) 的肾脏排泄量占给药剂量的 28%。在人体内,有1.3%以原药形式排出体外[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
蛋白质结合
据报道,替诺福韦艾拉酚胺可与血浆蛋白结合,体外研究表明,该药物给药剂量的约 80% 以结合状态存在。 替诺福韦艾拉酚胺 (GS-7340)在浓度高达 100 μM 时,对人肝癌细胞 (HepG2) 未显示出明显的细胞毒性[1]。 在 HIV-1 阳性成人中,每日一次口服 25 mg 替诺福韦艾拉酚胺 (GS-7340),持续 10 天,耐受性良好,未报告 3-4 级不良事件;最常见的轻度不良事件是头痛(8% 的受试者)[2] 替诺福韦艾拉酚胺 (GS-7340) 未引起人体受试者血清肌酐、丙氨酸氨基转移酶 (ALT) 或天冬氨酸氨基转移酶 (AST) 水平的显著变化[2] 替诺福韦艾拉酚胺 (GS-7340) 在人体中的血浆蛋白结合率为 82%–86%[2] 替诺福韦艾拉酚胺 (GS-7340) 在体外未显示对细胞色素 P450 酶(CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4)的抑制作用[2] |
| 参考文献 |
|
| 其他信息 |
药效学
替诺福韦艾拉酚胺已被证实是乙型肝炎病毒复制的强效抑制剂。与同类药物[替诺福韦酯]相比,替诺福韦艾拉酚胺具有更好的肾脏耐受性。这种更佳的安全性似乎与替诺福韦的血浆浓度较低有关。在临床试验中,与替诺福韦酯相比,替诺福韦艾拉酚胺对 HIV-1 的抗病毒活性提高了 5 倍。 替诺福韦艾拉酚胺 (GS-7340) 是替诺福韦的核苷酸前药,旨在增强其向淋巴细胞(HIV 感染的主要靶点)的递送[1]。 替诺福韦艾拉酚胺 (GS-7340) 通过转化为 TFV-DP 发挥其抗病毒作用,TFV-DP 通过终止病毒 DNA 合成链来抑制 HIV 逆转录酶[1]。 在一项 1b 期临床试验中,每日一次 25 mg 的替诺福韦艾拉酚胺 (GS-7340) 单药治疗 10 天,使 92% 的 HIV-1 阳性受试者的病毒载量降低[2]。 替诺福韦艾拉酚胺与富马酸替诺福韦二吡呋酯 (TDF) 相比,GS-7340 显示出更好的淋巴组织穿透性,从而降低了全身暴露量,并可能减少肾毒性 [1] |
| 分子式 |
C21H29N6O5P
|
|
|---|---|---|
| 分子量 |
476.47
|
|
| 精确质量 |
476.193
|
|
| 元素分析 |
C, 52.94; H, 6.13; N, 17.64; O, 16.79; P, 6.50
|
|
| CAS号 |
379270-37-8
|
|
| 相关CAS号 |
Tenofovir alafenamide fumarate;379270-38-9;Tenofovir alafenamide hemifumarate;1392275-56-7
|
|
| PubChem CID |
9574768
|
|
| 外观&性状 |
White to off-white solid
|
|
| 密度 |
1.39±0.1 g/cm3
|
|
| 沸点 |
640.4±65.0 °C at 760 mmHg
|
|
| 熔点 |
104-107 ºC
|
|
| 闪点 |
341.1±34.3 °C
|
|
| 蒸汽压 |
0.0±1.9 mmHg at 25°C
|
|
| 折射率 |
1.630
|
|
| LogP |
2.2
|
|
| tPSA |
153.29
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
12
|
|
| 重原子数目 |
33
|
|
| 分子复杂度/Complexity |
680
|
|
| 定义原子立体中心数目 |
3
|
|
| SMILES |
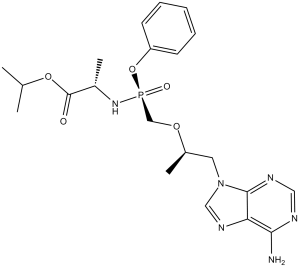
[P@](C([H])([H])OC([H])(C([H])([H])[H])C([H])([H])N1C([H])=NC2=C(N([H])[H])N=C([H])N=C12)(N([H])C([H])(C(=O)OC([H])(C([H])([H])[H])C([H])([H])[H])C([H])([H])[H])(=O)OC1C([H])=C([H])C([H])=C([H])C=1[H]
|
|
| InChi Key |
LDEKQSIMHVQZJK-AZFZMOAFSA-N
|
|
| InChi Code |
InChI=1S/C21H29N6O5P/c1-14(2)31-21(28)16(4)26-33(29,32-17-8-6-5-7-9-17)13-30-15(3)10-27-12-25-18-19(22)23-11-24-20(18)27/h5-9,11-12,14-16H,10,13H2,1-4H3,(H,26,29)(H2,22,23,24)/t15-,16+,33?/m1/s1
|
|
| 化学名 |
(S)-isopropyl 2-(((S)-((((R)-1-(6-amino-9H-purin-9-yl)propan-2-yl)oxy)methyl)(phenoxy)phosphoryl)amino)propanoate
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.08 mg/mL (4.37 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (4.37 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (4.37 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 配方 4 中的溶解度: 40 mg/mL (83.95 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶. 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.0988 mL | 10.4938 mL | 20.9877 mL | |
| 5 mM | 0.4198 mL | 2.0988 mL | 4.1975 mL | |
| 10 mM | 0.2099 mL | 1.0494 mL | 2.0988 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
|
|---|
|