RP 5264; RP-5264; TGR 1202; Umbralisib; TGR1202; TGR-1202; RP5264;
厄布利塞 TGR-1202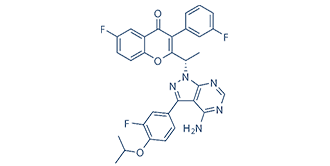
| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
PI3Kδ (IC50 = 22.2 nM); PI3Kδ (Kd = 6.2 nM); PI3Kγ (Kd = 1400 nM); PI3Kβ (Kd > 10000 nM); PI3Kα (Kd > 10000 nM)
Umbralisib (TGR1202; RP-5264) potently inhibits phosphatidylinositol 3-kinase delta (PI3Kδ) with an IC₅₀ of 22 nM and casein kinase 1 epsilon (CK1ε) with an IC₅₀ of 36 nM [3] It shows high selectivity for PI3Kδ over other PI3K isoforms (PI3Kα IC₅₀ = 1600 nM, PI3Kβ IC₅₀ = 2100 nM, PI3Kγ IC₅₀ = 1300 nM) [3] |
|---|---|
| 体外研究 (In Vitro) |
Umbralisib 在 100-300 nM 之间对人全血 CD19 细胞增殖产生半最大抑制[3]。Umbralisib (10 nM-100 μM) 在人淋巴瘤和白血病细胞系中以浓度依赖性方式抑制 Ser473 磷酸化 AKT[ 4].Umbralisib (15-50 μM) 的独特结构特征适合靶向淋巴瘤细胞中的 CK1,并且它能有效抑制 DLBCL 细胞系 LY7 中 c-Myc 的表达[4]。
厄布利塞(TGR1202;RP-5264)剂量依赖性抑制慢性淋巴细胞白血病(CLL)患者原代B细胞增殖,IC₅₀=0.5μM。阻断PI3Kδ介导的AKT磷酸化及下游信号通路,降低抗凋亡蛋白Bcl-2和Mcl-1的表达[3] 在CLL T细胞中,该药物在1μM浓度下可增加Th1细胞因子(IFN-γ、IL-2)的产生,减少Th2细胞因子(IL-4、IL-10),同时增强T细胞增殖及对CLL细胞的细胞毒性[1] 厄布利塞(TGR1202;RP-5264)抑制血液系统恶性肿瘤细胞系生长,包括Raji(伯基特淋巴瘤,IC₅₀=0.3μM)和MEC-1(CLL,IC₅₀=0.4μM),其机制为通过双重抑制PI3Kδ和CK1ε沉默c-Myc翻译[4] 诱导MEC-1细胞凋亡,EC₅₀=0.6μM,上调切割型caspase-3和PARP的表达,下调c-Myc和周期蛋白D1[4] |
| 体内研究 (In Vivo) |
在使用 MOLT-4 细胞系的 NOD/SCID 小鼠 T 细胞急性淋巴细胞白血病 (T-ALL) 皮下异种移植模型中,Umbralisib(150 mg/kg,每日口服)在第 25 天显着缩小肿瘤[4]。
厄布利塞(TGR1202;RP-5264)以50mg/kg/天的剂量口服给药28天,显著抑制裸鼠Raji异种移植瘤生长。与对照组相比,肿瘤体积减少约75%,瘤内p-AKT和c-Myc表达下调[4] 在CLL小鼠模型中,该药物(30mg/kg/天,口服35天)使外周血和脾脏中的CLL细胞数量分别减少约68%和72%,存活期延长45%[3] 与化疗药物(氟达拉滨)联合使用时,在MEC-1异种移植瘤模型中表现出协同抗肿瘤效应,联合指数为0.8[4] |
| 酶活实验 |
Umbralisib (TGR-1202) 是一种新型 PI3Kδ 抑制剂,IC50 和 EC50 分别为 22.2 nM 和 24.3 nM; Umbralisib (TGR-1202) 还具有针对 CK1ε 的活性,EC50 值为 6.0 μM。
将重组PI3Kδ和CK1ε激酶结构域分别与ATP及特异性底物在系列稀释的厄布利塞(TGR1202;RP-5264)(0.01-1000nM)存在下孵育,反应在37°C下进行60分钟,采用均相时间分辨荧光(HTRF)法检测磷酸化底物。通过与溶媒对照组的荧光强度对比计算抑制率,从量效曲线中得出IC₅₀值[3] 采用相同方案检测该药物对重组PI3Kα、PI3Kβ和PI3Kγ激酶的抑制活性以评估选择性,反应条件保持一致,通过确定IC₅₀值证实其对PI3Kδ的优先靶向性[3] |
| 细胞实验 |
将多发性骨髓瘤抗性 (MM-1R) 或敏感 (MM-1S) 细胞与所需浓度的 RP5264 一起孵育。 96小时后,使用MTT测定来测量生长。
从CLL患者样本中分离原代B细胞和T细胞,接种到96孔板中,用厄布利塞(TGR1202;RP-5264)(0.1-5μM)处理72小时,采用四唑盐法检测细胞活性并计算IC₅₀值[1,3] 用该药物(0.2-1μM)处理Raji和MEC-1细胞24小时,裂解后通过蛋白质印迹法检测p-AKT、AKT、c-Myc、Bcl-2、切割型caspase-3、PARP和GAPDH的表达[4] CLL T细胞经厄布利塞(TGR1202;RP-5264)(0.5-2μM)处理48小时后,通过酶联免疫吸附试验(ELISA)定量细胞上清液中的细胞因子水平;采用BrdU掺入法评估T细胞增殖,乳酸脱氢酶(LDH)释放试验检测对CLL细胞的细胞毒性[1] |
| 动物实验 |
雌性Balb/c小鼠
12.5、25、50 mg/kg 口服给药 携带Raji异种移植瘤(100-150 mm³)的裸鼠被随机分为对照组和治疗组。Umbralisib (TGR1202; RP-5264)悬浮于0.5%羧甲基纤维素溶液中,以50 mg/kg/天的剂量口服给药,持续28天。每3天测量一次肿瘤体积,并处死小鼠收集肿瘤组织,用于p-AKT和c-Myc的Western blot分析[4]。 通过过继转移Eμ-TCL1转基因B细胞建立小鼠CLL模型。小鼠以30 mg/kg/天的剂量口服Umbralisib (TGR1202; RP-5264)治疗,持续35天。采集外周血和脾脏样本,通过流式细胞术计数 CLL 细胞,并记录生存时间 [3]。在联合治疗研究中,将携带 MEC-1 异种移植瘤的裸鼠接受 Umbralisib (TGR1202; RP-5264)(30 mg/kg/天,口服)联合氟达拉滨(20 mg/kg/周,腹腔注射)治疗 21 天。在治疗结束时测量肿瘤重量,以计算联合治疗指数 [4]。 |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
乌姆拉利西布在胃肠道内迅速吸收。乌姆拉利西布的达峰时间(Tmax)约为4小时。与乌姆拉利西布同时摄入高脂肪、高热量食物后,其AUC增加61%,Cmax增加115%。 在药代动力学研究中,约81%的乌姆拉利西布剂量从粪便中排出(17%为原形)。在健康志愿者服用 800 mg 放射性标记剂量后,尿液中检测到约 3% 的药物(其中 0.02% 为原形)。 umbralisib 的平均表观中心分布容积为 312 L。 umbralisib 的平均表观清除率为 15.5 L/h。 代谢/代谢物 体外研究表明,umbralisib 由 CYP2C9、CYP3A4 和 CYP1A2 酶代谢。 生物半衰期 Umbralisib 的有效半衰期约为 91 小时。 小鼠单次口服 50 mg/kg 剂量后,umbralisib (TGR1202; RP-5264) 的口服生物利用度约为 73%。血浆半衰期约为10.5小时,给药后2小时达到最大血浆浓度(Cmax)为5.8 μg/mL [2] 在大鼠中,口服30 mg/kg后,24小时AUC₀-24h为62.3 μg·h/mL。该药物广泛分布于淋巴组织(脾脏、淋巴结),组织/血浆浓度比约为3.1 [2] 在健康志愿者中,每日一次口服800 mg,Cmax为4.2 μg/mL,24小时AUC₀-24h为58.6 μg·h/mL,血浆半衰期为18小时。该药物主要通过细胞色素P450 3A4代谢,7天内72%的剂量经粪便排出,18%经尿液排出 [2] |
| 毒性/毒理 (Toxicokinetics/TK) |
肝毒性
在成人淋巴瘤患者的umbralisib临床试验中,治疗期间血清酶升高的发生率在15%至35%之间,其中5%至8%的患者血清酶水平超过正常值上限(ULN)的5倍,偶尔超过ULN的20倍。 由于umbralisib会影响B细胞功能,它也可能诱发乙型肝炎病毒(HBV)的再激活,尽管在已发表的该药物试验中,未报告HBV再激活的病例。 可能性评分:E(未经证实,但怀疑是临床上明显的肝损伤的罕见原因)。 蛋白结合 Umbralisib的蛋白结合率超过99.7%。 小鼠以50 mg/kg/天的剂量接受Umbralisib(TGR1202;RP-5264)治疗28天后,体重略有下降(约5%),但未出现显著的肝损伤。未观察到肝肾毒性。血清ALT、AST和肌酐水平均在正常范围内[3] 在I期临床试验中,最常见的不良事件为腹泻(43%)、疲乏(35%)和恶心(28%)。3/4级毒性包括中性粒细胞减少症(12%)和肝酶升高(8%)。剂量高达1200 mg/天时未观察到剂量限制性毒性[2] 通过平衡透析法测定,Umbralisib(TGR1202;RP-5264)在人血浆中的血浆蛋白结合率约为92%[2] |
| 参考文献 |
|
| 其他信息 |
边缘区淋巴瘤是一种罕见的、进展缓慢的非霍奇金淋巴瘤,最初采用利妥昔单抗(一种抗CD20药物)进行治疗,可单独使用或与化疗联合使用。然而,许多患者会出现复发或对这些药物产生耐药性。此时治疗选择有限,需要寻找其他淋巴瘤治疗方法来控制疾病进展。滤泡性淋巴瘤也采用利妥昔单抗和其他化疗药物进行治疗,但其进展情况可能与边缘区淋巴瘤类似。2021年2月5日,美国食品药品监督管理局(FDA)基于临床试验的良好结果,加速批准了PI3K-δ和酪蛋白激酶CK1-ε的激酶抑制剂umbralisib上市。该药由TG Therapeutics公司以Ukoniq为商品名销售,并已获批用于治疗成人复发/难治性边缘区淋巴瘤和滤泡性淋巴瘤。 Umbralisib 是一种酪蛋白激酶抑制剂,酪蛋白激酶是蛋白质翻译的主要调节因子,其活性成分为激酶-1ε,这使其与其他淋巴瘤治疗药物有所区别。尽管最初它为复发或难治性疾病患者提供了一种很有前景的疗法,但由于安全性问题,Umbralisib 被撤出市场,因为该药物可能增加死亡风险,其获益可能大于风险。
Umbralisib 是一种激酶抑制剂。Umbralisib 的作用机制是作为激酶抑制剂。 Umbralisib 是一种口服激酶抑制剂,于 2021 年获得加速批准,用于治疗成人复发或难治性边缘区淋巴瘤和滤泡性淋巴瘤,但一年后,由于一项试验数据显示其使用会导致死亡率升高,该批准被撤销。 Umbralisib治疗期间血清酶升高发生率较低,但未见报道引起临床上明显的急性肝损伤症状或黄疸。 Umbralisib是一种口服生物利用度高的选择性抑制剂,可抑制I类磷脂酰肌醇-3激酶(PI3K)110 kDa催化亚基的δ亚型,具有潜在的抗肿瘤活性。PI3Kδ抑制剂TGR-1202可抑制PI3K并阻止PI3K/AKT激酶信号通路的激活。这可降低易感肿瘤细胞的增殖并诱导其死亡。与其他PI3K亚型不同,PI3Kδ主要在肿瘤细胞和造血细胞中表达。靶向抑制PI3Kδ可使PI3K信号在正常非肿瘤细胞中发挥作用。 PI3K 是一种在癌细胞中经常过表达的酶,在肿瘤细胞的调控和存活中起着至关重要的作用。 另见:乌姆布拉利西布甲苯磺酸盐(活性成分)。 药物适应症 乌姆布拉利西布目前尚无任何获批的治疗适应症。 作用机制 PI3K 通路在恶性肿瘤中失调,导致 p110 亚型(p110α、p110β、p110δ、p110γ)的过表达,从而诱导细胞发生恶性转化。乌姆布拉利西布抑制多种蛋白激酶,包括 PI3Kδ 和酪蛋白激酶 CK1ε。PI3Kδ 在健康细胞和恶性 B 细胞中均有表达。CK1ε 被认为参与了包括淋巴瘤在内的恶性细胞的发病机制。这可减缓复发或难治性淋巴瘤的进展。生化分析表明,umbralisib 可抑制 ABL1 的突变形式。体外实验表明,umbralisib 可抑制恶性细胞增殖、CXCL12 介导的细胞黏附以及 CCL19 介导的细胞迁移。 药效学 Umbralisib 通过阻断 PI3K 通路发挥抗边缘区淋巴瘤的作用;PI3K 通路是 B 细胞受体信号传导的关键通路,而 B 细胞受体信号传导是淋巴瘤进展的重要因素。此外,Umbralisib 还可抑制其他参与特定类型淋巴瘤的通路,包括酪蛋白激酶通路。临床试验中记录到的总缓解率为 55%,边缘区淋巴瘤 1 年无进展生存率为 71%。临床研究观察到,umbralisib 稳态暴露量越高,不良反应(包括腹泻和 AST/ALT 升高)的发生率也越高。该药物对QT间期的影响尚未完全明确。 Umbralisib(TGR1202;RP-5264)是一种新型口服PI3Kδ和CK1ε双重抑制剂,旨在靶向血液系统恶性肿瘤的关键信号通路。其双重机制可抑制肿瘤细胞增殖并调节免疫微环境[4]。 该药已获得FDA批准,用于治疗成人复发或难治性慢性淋巴细胞白血病(CLL)/小淋巴细胞淋巴瘤(SLL)和滤泡性淋巴瘤(FL)[2]。 该药对CLL中的T细胞具有独特的免疫调节作用,可增强抗肿瘤免疫,并可能克服肿瘤微环境中的免疫抑制[1]。 |
| 分子式 |
C31H24F3N5O3
|
|
|---|---|---|
| 分子量 |
571.5492
|
|
| 精确质量 |
571.183
|
|
| 元素分析 |
C, 65.14; H, 4.23; F, 9.97; N, 12.25; O, 8.40
|
|
| CAS号 |
1532533-67-7
|
|
| 相关CAS号 |
Umbralisib hydrochloride;1532533-78-0;Umbralisib R-enantiomer;1532533-69-9;Umbralisib tosylate;1532533-72-4;Umbralisib sulfate;1532533-75-7
|
|
| PubChem CID |
72950888
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| 熔点 |
139 - 142 °C
|
|
| LogP |
7.243
|
|
| tPSA |
109.06
|
|
| 氢键供体(HBD)数目 |
1
|
|
| 氢键受体(HBA)数目 |
10
|
|
| 可旋转键数目(RBC) |
6
|
|
| 重原子数目 |
42
|
|
| 分子复杂度/Complexity |
1020
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
FC1C([H])=C([H])C2=C(C=1[H])C(C(C1C([H])=C([H])C([H])=C(C=1[H])F)=C([C@]([H])(C([H])([H])[H])N1C3C(=C(N([H])[H])N=C([H])N=3)C(C3C([H])=C([H])C(=C(C=3[H])F)OC([H])(C([H])([H])[H])C([H])([H])[H])=N1)O2)=O
|
|
| InChi Key |
IUVCFHHAEHNCFT-INIZCTEOSA-N
|
|
| InChi Code |
InChI=1S/C31H24F3N5O3/c1-15(2)41-24-9-7-18(12-22(24)34)27-26-30(35)36-14-37-31(26)39(38-27)16(3)29-25(17-5-4-6-19(32)11-17)28(40)21-13-20(33)8-10-23(21)42-29/h4-16H,1-3H3,(H2,35,36,37)/t16-/m0/s1
|
|
| 化学名 |
2-[(1S)-1-[4-amino-3-(3-fluoro-4-propan-2-yloxyphenyl)pyrazolo[3,4-d]pyrimidin-1-yl]ethyl]-6-fluoro-3-(3-fluorophenyl)chromen-4-one
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: ~100 mg/mL (~175 mM)
Water: <1 mg/mL (slightly soluble or insoluble) Ethanol: ~7 mg/mL (~12.2 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (3.50 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL 澄清 DMSO 储备液加入900 μL 玉米油中,混合均匀。 配方 2 中的溶解度: 2% DMSO+30% PEG 300+2% Tween 80+H2O: 3mg/mL 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7496 mL | 8.7481 mL | 17.4963 mL | |
| 5 mM | 0.3499 mL | 1.7496 mL | 3.4993 mL | |
| 10 mM | 0.1750 mL | 0.8748 mL | 1.7496 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Status | Interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03269669 | Recruiting | Drug: Prednisone Drug: Umbralisib |
Grade 1 Follicular Lymphoma Grade 2 Follicular Lymphoma |
National Cancer Institute (NCI) |
August 10, 2017 | Phase 2 |
| NCT03919175 | Active Recruiting |
Drug: Umbralisib Drug: Rituximab |
Lymphoma Follicular Lymphoma |
Massachusetts General Hospital |
September 1, 2019 | Phase 2 |
| NCT04783415 | Active Recruiting |
Drug: Acalabrutinib Drug: Umbralisib |
Mantle Cell Lymphoma | City of Hope Medical Center | March 26, 2021 | Phase 2 |
| NCT04624633 | Active Recruiting |
Drug: Acalabrutinib Drug: Umbralisib |
Chronic Lymphocytic Leukemia Small Lymphocytic Lymphoma |
Jennifer R. Brown, MD, PhD | March 26, 2021 | Phase 2 |
| NCT03671590 | Active Recruiting |
Drug: TG-1701 Drug: Umbralisib |
Non Hodgkin Lymphoma | TG Therapeutics, Inc. | September 10, 2018 | Phase 1 |
TGR-1202 and carfilzomib synergistically inhibit survival of lymphoma and leukemia cell lines and primary cells.Blood.2017 Jan 5;129(1):88-99. |
TGR-1202 and carfilzomib synergistically inhibits translation of c-Myc in lymphoma and myeloma cell lines.Blood.2017 Jan 5;129(1):88-99. |
TGR-1202 and carfilzomib inhibits c-Myc–dependent gene transcription.Blood.2017 Jan 5;129(1):88-99. |