| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 2mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
homologous nucleoside antibiotic; N-linked glycosylation; GlcNAc phosphotransferase (GPT)
|
|---|---|
| 体外研究 (In Vitro) |
在 CD44+/CD24- 和原代 MCF7 细胞中,tunitamycin(2 μg/mL;24 小时)处理增强了片段相关的 XBP-1、ATF6 核易位水平和 CHOP 蛋白表达 [1]。研究结果表明,富含 CD44+/CD24- 和 CD44+/CD24 的 MCF7 细胞培养物表现出衣霉素的以下作用:它们减少迁移、增加细胞死亡并阻止迁移 [1]。
|
| 体内研究 (In Vivo) |
在 CD133+/- MHCC97L 细胞异种移植模型(BALB/c (nu/nu) 小鼠)中,tunitoxin(0.1 mg/kg 或 0.5 mg/kg)治疗可大大减少肿瘤生长 [2]。
|
| 细胞实验 |
蛋白质印迹分析
细胞类型: CD44+/CD24- 和原始 MCF7 细胞[1] 测试浓度: 2 µg/mL 孵育时间:24小时 实验结果:在CD44+/CD24-和原始MCF7细胞中检测到剪接的XBP-1、ATF6核转移以及CHOP蛋白表达水平增加。 肝细胞癌对许多抗癌药物具有化学耐药性。衣霉素是一种N-糖基化抑制剂,可引起未折叠蛋白反应,被广泛用作内质网应激的药理学诱导剂。本研究采用多种设计来研究肝细胞癌Hep3B细胞对喜树碱和依托泊苷的耐药机制。衣霉素显著抑制喜树碱或依托泊苷诱导的细胞凋亡。衣霉素既不改变拓扑异构酶水平,也不抑制喜树碱和依托泊苷引起的ATM激活。数据表明,衣霉素诱导的耐药性可能是由药物捕获的拓扑异构酶DNA复合物和DNA双链断裂的下游事件引起的。喜树碱和依托泊苷可增加几种细胞周期调节因子的蛋白表达,并诱导Bcl-2家族蛋白的切割。这些细胞内分子事件被衣霉素消除。添加衣霉素后的设计表明,G1检查点阻滞是耐药机制的一部分。姜黄素是本研究中的另一种G1期阻滞诱导剂,能够诱导类似的抗性效应。此外,转染GRP78 siRNA的细胞对衣霉素诱导的凋亡具有部分抗性,但对细胞周期调节因子没有抑制作用,这表明GRP78和G1期阻滞是衣霉素介导的抗性机制的两个独立因素。总之,数据表明,衣霉素通过GRP78上调和细胞周期G1期阻滞诱导对拓扑异构酶抑制剂的耐药性。这些发现也促使人们思考,化疗药物和中草药联合用药可能会导致耐药性,这会诱导癌症细胞的内质网应激和/或细胞周期阻滞。[1] |
| 动物实验 |
6~8周龄的BALB/c (nu/nu)小鼠按照上海市实验动物伦理委员会制定的实验方案,在标准条件下饲养。实验结束后,处死小鼠,切除肿瘤并称重,然后用福尔马林固定。冷冻肿瘤样本采用Western blotting和实时PCR进行分析。详细信息见补充数据。[2]
|
| 参考文献 | |
| 其他信息 |
肝细胞癌具有高度化疗耐药性,ATP结合盒转运蛋白G亚家族成员2 (ABCG2) 被认为在这种耐药性中起着关键作用。本研究旨在开发有效的治疗策略,以降低ABCG2的表达水平并克服肝细胞癌化疗的耐药性。首先,我们证实了ABCG2蛋白水平与肝细胞癌细胞系的耐药性之间存在正相关性。ABCG2在富含CD133的高耐药性肝细胞癌癌干细胞(CSC)中优先表达。此外,ABCG2在肝细胞癌细胞中发生N-糖基化修饰,这种修饰参与维持其蛋白稳定性。N-糖基化(NLG)抑制剂衣霉素显著降低了ABCG2的表达,改变了其亚细胞定位,并逆转了其在多种肝细胞癌细胞系中的药物外排作用。此外,衣霉素降低了多种癌症干细胞(CSC)标志物的表达水平,并抑制了CD133(+) CSC的致瘤性。衣霉素联合顺铂(CDDP)可抑制增殖细胞核抗原(PCNA)的表达并增加PARP的裂解;ABCG2或Akt-myr的过表达可部分逆转这种效应。与单药治疗相比,联合治疗能更有效地抑制异种移植小鼠的肿瘤生长。最后,CDDP治疗联合UDP-GlcNAc-多萜醇-磷酸N-乙酰氨基葡萄糖-1-磷酸转移酶(DPAGT1)敲低,可重现CDDP与衣霉素联合使用时观察到的效果。总之,我们的研究结果表明,衣霉素可能通过靶向DPAGT1/Akt/ABCG2通路逆转肝细胞癌的耐药性,并提高联合治疗的疗效[2]。
内质网(ER)中未折叠蛋白的积累会触发未折叠蛋白反应(UPR),这是一种应激信号通路。UPR协调ER分子伴侣的诱导、蛋白质合成的减少以及细胞周期G1期的生长停滞。然而,UPR诱导G1期细胞周期停滞的分子机制仍不甚明了。本文报道,衣霉素(TM,一种ER应激诱导剂)激活UPR反应会导致黑色素瘤细胞中p27的积累和G1期细胞周期停滞。p27的积累是由于TM处理抑制了其多聚泛素化及其随后的降解。与 p27 稳定化相关的是,p27 的 E3 连接酶 Skp2 的水平在 TM 处理后降低。更重要的是,敲低 p27 可显著降低 TM 诱导的 G1 期细胞周期阻滞。综上所述,这些数据表明 p27 是内质网应激诱导生长停滞的关键介质。[3] |
| 分子式 |
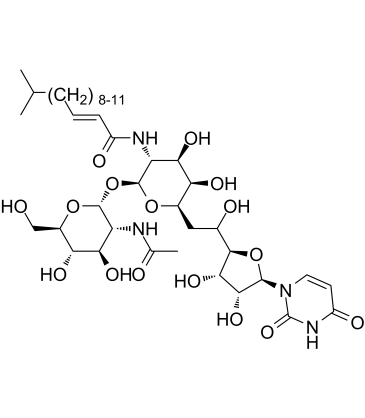
C₃₉H₆₄N₄O₁₆(N=₁₀)
|
|---|---|
| 分子量 |
844.94 (n=10)
|
| 精确质量 |
844.94 (n=10)
|
| CAS号 |
11089-65-9
|
| 外观&性状 |
Off-white to light yellow solid powder
|
| 密度 |
1.4±0.1 g/cm3
|
| 熔点 |
234 - 235ºC
|
| 折射率 |
1.617
|
| LogP |
2.58
|
| tPSA |
311.82
|
| InChi Key |
ZHSGGJXRNHWHRS-VIDYELAYSA-N
|
| InChi Code |
InChI=1S/C30H46N4O16/c1-11(2)5-4-6-16(38)32-19-23(43)20(40)14(47-29(19)50-28-18(31-12(3)36)22(42)21(41)15(10-35)48-28)9-13(37)26-24(44)25(45)27(49-26)34-8-7-17(39)33-30(34)46/h4,6-8,11,13-15,18-29,35,37,40-45H,5,9-10H2,1-3H3,(H,31,36)(H,32,38)(H,33,39,46)/b6-4+/t13?,14-,15-,18-,19-,20+,21-,22-,23-,24+,25-,26-,27-,28-,29+/m1/s1
|
| 化学名 |
(E)-N-((2S,3R,4R,5R,6R)-2-(((2R,3R,4R,5S,6R)-3-acetamido-4,5-dihydroxy-6-(hydroxymethyl)tetrahydro-2H-pyran-2-yl)oxy)-6-(2-((2R,3S,4R,5R)-5-(2,4-dioxo-3,4-dihydropyrimidin-1(2H)-yl)-3,4-dihydroxytetrahydrofuran-2-yl)-2-hydroxyethyl)-4,5-dihydroxytetrahydro-2H-pyran-3-yl)-5-methylhex-2-enamide
|
| 别名 |
NSC 177382; NSC177382; NSC-177382
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~33.33 mg/mL
H2O : < 0.1 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2 mg/mL (Infinity mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 20.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2 mg/mL (Infinity mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.0mg/mL澄清的DMSO储备液加入到900μL 20%SBE-β-CD生理盐水中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2 mg/mL (Infinity mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。