| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| Other Sizes |
|
| 靶点 |
Her3 (ErbB3) (IC50 = 23 nM)
|
|---|---|
| 体外研究 (In Vitro) |
TX1-85-1 对 Ovcar8、HCC827 GR6 和 PC9 GR4 细胞的抗增殖 EC50 分别为 9.9、11.5 和 16.9 μM[1]。
在迭代合成和测定约100种吡唑并嘧啶丙烯酰胺后,我们开发了“先导”化合物TX1-85-1(4),其在结合试验中的IC50为23 nM(图1a,b)。TX1-85-1可以被视为KIN001-051铰链结合部分和KIN001-111溶解度增强尾部的分子汞合金,与丙烯酰胺臂结合到达Cys721(图1c)。正如共价抑制剂所预期的那样,与蛋白质孵育更长时间后,表观IC50会降低,并在约3小时时达到平稳状态(补充图2)。质谱用于确认TX1-85-1共价添加到重组Her3激酶结构域蛋白中,随后用胰蛋白酶对Her3进行蛋白水解,MS2分析揭示了Cys721的独特修饰(补充图3)。接下来,我们使用细胞竞争结合试验研究了TX1-85-1是否可以在细胞中与Her3形成共价键。为了实现这些实验,我们合成了一种生物素化衍生物(TX1-85-1-biotin)(5),该衍生物仍然保留了与Her3共价结合的能力(图1a,补充图4,IC50=50.7 nM)。将细胞与TX1-85-1一起孵育,然后用TX1-85-1-生物素标记裂解物,以量化在最初与TX1-855-1孵育时未标记的Her3的量。我们确定,将PC9 GR4细胞(EGFR E746_A750/T790M)与5μM TX1-85-1孵育8小时,可以完全保护Her3免受随后TX1-85-1-生物素的标记(图1d)。这一结果表明,TX1-85-1(分子量=580Da)可以穿过细胞膜,并能够在细胞内与Her3完全“靶向结合”。为了检查TX1-85-1修饰Her3的特异性,我们使用KiNativ®方法进行了活细胞化学蛋白质组学实验,该实验证明了与Her3以及Lyn、Her2和其他几种Src家族激酶的有效结合(补充表1)。预计会与Lyn、Her2和其他几种Src家族激酶结合,因为这些激酶被非丙烯酰胺筛选靶化合物KIN001-111等效结合,这表明与这些靶标的相互作用是非共价的。总的来说,这些结果表明TX1-85-1能够在体外和细胞内共价修饰Her3的Cys721。[1] TX1-85-1不会阻止Her3依赖性信号传导或生长[1] 接下来,我们评估了TX1-85-1抑制Her3依赖性信号传导和生长的能力。我们使用了两种已建立的肺癌细胞系,PC9 GR4(EGFR E746_A750/T790M)、HCC827 GR6(EGFR E646_A750/MET扩增)18,37和卵巢癌症细胞系Ovcar8,我们使用siRNA介导的Her3缺失再次确认其对Her3“上瘾”(补充图5)。TX1-85-1对所有三种细胞系都具有大于或等于约10μM的抗增殖EC50(图2a)。当TX1-85-1的浓度足以完全标记细胞中的Her3时(5μM),PC9 GR4细胞没有生长抑制,Her3的重要下游效应器Akt的磷酸化也没有受到抑制(图2b)。这些结果表明,尽管TX1-85-1成功地将Her3靶向结合到细胞中,但在所研究的条件下,该化合物不能抑制Her3依赖性功能。 TX1-85-1-金刚烷偶联物诱导Her3降解[1] 最近的报道表明,用疏水性小分子共价修饰蛋白质会导致其蛋白酶体介导的降解25,26,38,39。虽然对这一现象的详细机制尚不清楚,但有相当多的证据表明,细胞已经进化出复杂的蛋白质稳态机制,可以消除未折叠和受损的蛋白质,这些蛋白质可能是由这种疏水标记策略参与的。在报道的疏水标签中,我们选择了金刚烷基团,因为它能够以最小的分子量增加密集地引入疏水性。合成了一系列具有将TX1-85-1与金刚烷部分连接的各种连接体的化合物,并证实其与Her3有效结合,鉴定出一种代表性分子(TX2-121-1)(6),在基于蛋白质的结合分析中显示IC50为49.2 nM。为了确认TX2-121-1的选择性与TX1-85-1的选择性保持相似,我们进行了KiNativ®分析。TX2-121-1的选择性与TX1-85-1非常相似,与Her3的结合最强(90.3%)。TX2-121-1脱靶标记列表包括Her2、EGFR、几种Src家族激酶,如Src、Yes和Lyn,正如预期的那样,与TX1-85-1的脱靶列表相同。(附表1)。为了研究TX1-85-1和TX2-121-1是否可以直接抑制EGFR或Her2,我们使用Ba/F3 EGFR VIII细胞系进行了酶法测定(Z′-LYTE)和细胞增殖测定(补充图6)。TX2-121-1在低于10μM的浓度下不直接抑制EGFR或Her2的酶活性,也不抑制EGFR依赖性增殖。 为了证实观察到的药理学是Her3依赖性的,我们改造了PC9 GR4细胞,使其具有含有反应性Cys721的天然Her3或含有非反应性丝氨酸突变C721S的Her3。ErbB3的Sanger DNA测序证实了突变(补充图7)。我们使用TX1-85-1-生物素偶联化合物进行下拉分析,验证了靶点参与。事实上,TX1-85-1-biotin有效地降低了Her3-WT,但没有降低Her3-C721S,这表明TX1-85-1-biotin的丙烯酰胺基序与C721形成了特定的共价相互作用,但没有与C721S-Her3形成共价键(补充图8)。 我们对表达野生型或C721S突变体Her3的PC9 GR4细胞进行了细胞增殖试验,其中TX1-85-1和TX2-121-1及其相应的丙酰胺对照(TX1-85-3(9)和TX2-135-2),以研究亲电丙烯酰胺和金刚烷部分的重要性。这些实验表明,C721S Her3的EC50向右偏移了6倍(PC9 GR4 Her3 C721S的EC50=5.5μM),而野生型Her 3表达细胞(PC9 GRU4 WT Her3的EC 50=0.9μM)仅对TX2-121-1具有亲电弹头和金刚烷部分(图4a,补充图9),下游信号蛋白质印迹与抗增殖结果一致(图4b)。所有其他化合物:TX1-85-1、TX1-85-3和TX2-135-2在PC9 GR4 Her3 WT和PC9 GR4-Her3 C721S上的EC50相似。这些结果表明,在这种细胞系统中,有效抑制Her3依赖性生长需要共价修饰和金刚烷部分的存在。顺便说一句,我们还观察到两个可逆的对照,即带有金刚烷基团的TX2-135-2比TX1-85-3更具抗增殖性[1]。 抑制ErbB2或ErbB3抑制了miPSCs向CSCs的转化[2] 为了评估ErbB2/ErbB3信号在转化过程中的作用,前一节提出的假设是,拉帕替尼作为ErbB2的酪氨酸激酶抑制剂,TX1-85-1作为ErbB3抑制剂,用于中断酪氨酸激酶。MTT法显示,拉帕替尼对miPSCs的IC50约为12µM,而TX1-85-1的IC50约等于25µM(图3A)。miPSCs通常与白血病抑制因子(LIF)一起培养以保持其干燥性,miPSCs将开始分化并停止生长,即在没有LIF的情况下无法存活。在没有LIF的情况下培养的miPSCs失去了GFP表达,无法通过传代存活。相比之下,在PK8细胞的CM存在下,miPSCs在没有LIF的情况下保持GFP表达并保持增殖。含有1µM或5µM拉帕替尼的CM似乎维持了GFP,而观察到5µM的粘附细胞分化增强(图3B)。用CM和10µM TX1-85-1培养的一部分细胞保持GFP,分化的细胞在粘附细胞培养条件下显示为GFP阴性细胞。细胞完全失去GFP表达,并用20µM TX1-85-1分化,在治疗一周后无法存活(图3C)。 我们的研究小组已经证明,当在癌症细胞的CM中培养时,转化为CSC的iPSC保持自我更新和结肠形成能力。在转化过程中评估了拉帕替尼和TX1-85-1对集落和球体形成的影响。在1和5µM拉帕替尼存在下培养的miPSCs显示菌落数量减少(图4A)。虽然1µM的减少微不足道,但5µM的菌落数量从250个显著减少到17个(图4B)。用TX1-85-1培养的细胞以剂量依赖的方式显示集落数减少。1、5和10µM TX1-85-1的平均菌落数分别为217、163和20(图4A、C)。1µM和5µM拉帕替尼、5µM和10µM TX1-85-1也抑制了在无血清培养基中低附着培养条件下培养的miPSCs的球体形成能力,而用CM培养的miPSC保持了球体形成能力(图4C)。 抑制ErbB2或ErbB3可增强Erk的激活,并在转化过程中减弱茎性[2] 为了研究ErbB2和ErbB3信号传导在转化过程中的作用,评估了拉帕替尼和TX1-85-1对miPSC在转化期间获得CSC特征的影响。western blot显示,与用LIF培养的miPSCs相比,在CM中培养的miPSC保持Oct3/4水平,而作为CSC标志物的CD24略有增加。另一方面,在1µM拉帕替尼存在下培养的miPSCs中,Oct3/4和CD24的水平得以维持。与没有拉帕替尼培养的细胞中的水平相比,在5µM拉帕替尼存在的情况下,Oct3/4和CD24水平显著降低(图6Aa,B)。数据还显示,与不含拉帕替尼的miPSCs相比,在5µM拉帕替尼存在下培养的miPSCs中Erk过度激活,干性减弱。与没有拉帕替尼的情况相比,1µM拉帕替尼可降低CM中培养的miPSCs中的Erk激活(图6Aa,B)。用小干扰RNA(siRNA)或10µMTX1-85-1抑制ErbB3会降低Oct3/4和Nanog水平,并过度激活Erk。与阴性siRNA对照相比,用siRNA靶向ErbB3也显示出CD24水平的降低。(图6Ab、c、c、D)。 |
| 酶活实验 |
Her3标记为TX1-85-1[1]
通过在室温下将浓度为15μM(0.5mg/ml)的纯化Her3蛋白与150μM TX1-85-1在含有50mM MOPS pH 7、50mM硫酸铵、1mM TCEP和5%甘油的缓冲液中孵育2小时,实现了用TX1-85-1标记。 LanthaScreen®技术激酶结合分析[1] 结合效力(IC50)通过LanthaScreen®Eu激酶结合试验进行测量,该试验基于Alexa Fluor 647标记的ATP竞争性激酶抑制剂支架的结合和置换。使用铕标记的抗标记抗体(抗GST)检测示踪剂与激酶的结合。纯化的ErbB3(665-1001)蛋白从Life Technologies获得,浓度为1.19 mg/ml,溶于50 mM Tris(pH 7.5)、150 mM NaCl、0.5 mM EDTA、0.02%Triton®X-100、2 mM DTT、50%甘油中。典型的实验程序是用激酶缓冲液A(50 mM HEPES,pH 7.5,10 mM MgCl2,1 mM EGTA,0.01%Brij-35)将ErbB3蛋白稀释至30 nM,然后将ErbB蛋白1:1与12 nM LanthaScreen®Eu抗GST抗体溶液混合,该溶液也在激酶缓冲液A.中稀释。使用前,将抗体管解冻并在约10000 g下离心5分钟,从溶液顶部吸取用于测定的量。此离心步骤将消除因产品中的任何颗粒而偶尔出现的虚假数据点。接下来,将5μl ErbB3蛋白和Eu抗GST的混合物加入康宁384板中每孔5μl的测试化合物溶液中。然后,以每孔39 nM的浓度加入5μl激酶示踪剂178。然后将平板在4°C下孵育3小时,并用Perkin-Elmer EnVision®读取。 完整Her3[1]的质谱分析 将经TX1-85-1处理的Her3(约1μg)装载到自填充反相柱上(外径1/32英寸x内径500μm,含5cm POROS 10R2树脂)。脱盐后,用HPLC梯度(4分钟内0%–100%B,A=0.2 M乙酸水溶液,B=0.2 M醋酸乙腈溶液,流速=10μl/min)将蛋白质洗脱到QSTAR Elite质谱仪中,扫描M/z 330–1500。使用MagTran1.03b2软件对质谱进行解卷积。 蛋白酶消化和肽片段的纳米LC/MS分析[1] TX1-85-1处理的Her3(约1μg)用碳酸氢铵缓冲液(pH 8.0)稀释,在56°C下用10 mM DTT还原30分钟,用22.5 mM碘乙酰胺烷基化30分钟(室温黑暗),并在37°C下与胰蛋白酶消化过夜。将消化的肽(约2 pmol)注射到自填充的预柱(4 cm POROS10R2)上,并使用HPLC梯度(20分钟内0%~35%的B,a=0.2 M乙酸水溶液,B=0.2 M醋酸乙腈溶液,流速~30 nl/min)52洗脱到质谱仪中。对每次MS扫描(图像电流检测;分辨率=30K)中的前10个离子进行CAD(电子倍增检测,相对碰撞能量35%,q=0.25)。启用了动态排除,重复计数为1,排除持续时间为15秒。 |
| 细胞实验 |
MTT法[2]
将miPSCs以5000个细胞/孔的密度接种在96孔板中,用补充了50%CM的miPS培养基接种,并在37°C和5%CO2下孵育。接种24小时后,用不同浓度的拉帕替尼或TX1-85-1孵育细胞,孵育24小时后用噻唑蓝-四唑蓝评估细胞存活率。将浓度为0.5mg/mL的MTT溶液加入孔中,并在37°C的5%CO2中孵育平板4小时。孵育后,丢弃培养基,用100µL DMSO溶解甲赞晶体,用MTP-800 Lab酶标仪在570 nm处测量吸光度。根据存活曲线估算IC50值。 菌落和球体形成试验[2] 为了进行菌落分析,将1000个miPSCs培养在60mm培养皿中,培养基中含有1000U/ml LIF的miPS培养基。接种24小时后,培养基改为不含LIF的miPS培养基,补充50%CM、50%CM和1µM拉帕替尼、50%CM与5µM拉帕替尼,或补充50%CM和1.5或10µM TX1-85-1。细胞在37°C和5%CO2中孵育7天。孵育后,用75%甲醇固定细胞,并用Giemsa染色。对培养皿进行拍照,并使用ImageJ软件对直径为 ≥ 50 µm.为了评估细胞形成球体的能力,将在补充了上述条件的miPS培养基中培养一周的miPSCs以1000个细胞/孔的密度接种到24孔超低附着板中,该板含有由DMEM、2 mM L-谷氨酰胺、0.1 mMβ-ME、0.1 mM NEAA和ITS-X组成的无血清培养基,并补充了青霉素/链霉素和0.1或5µM拉帕替尼或1、5、10µM TX1-85-1。然后将细胞在37°C的5%CO2中孵育7天,并使用配备有光荧光装置的Olympus IX81显微镜拍摄形成的球体。 蛋白质印迹[2] 在含有50%CM、50%CM和1µM拉帕替尼或50%CM和5µM拉帕替尼或含有50%CM和10µMTX1-85-1的miPS培养基中培养一周的miPSCs,用由50 mM Tris pH 8.0、150 mM氯化钠、0.05%Triton X-100和0.5 mM乙二胺四乙酸(EDTA)组成的裂解缓冲液裂解转染有阴性对照siRNA或ErbB3 siRNA的细胞。蛋白酶和磷酸酶抑制剂也加入到裂解缓冲液中。裂解的细胞进一步超声处理,在4°C下以15000xg离心30分钟,收集上清液并保持在-80°C。通过Pierce™BCA蛋白检测试剂盒评估总蛋白浓度,将30µg总蛋白装载在SDS-PAGE上,转移到Immobilon FL转移膜上。 |
| 参考文献 | |
| 其他信息 |
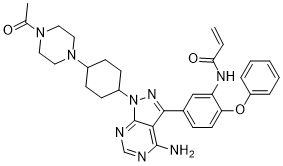
TX1-85-1 是一种芳香醚。
本文报道了首个小分子 Her3 ATP 竞争性结合剂 TX1-85-1 的开发,该化合物可通过共轭加成与 Cys721 共价修饰 Her3。用微摩尔浓度的 TX1-85-1 处理细胞,可使 Her3 发生共价修饰,且其激酶组选择性与该化合物的化学类型一致。尽管 TX1-85-1 成功结合靶点,但 PC9 肺癌细胞系的增殖和 Her3 依赖性功能(包括下游效应分子 Akt 的磷酸化)并未受到影响。然而,尽管 TX1-85-1 对 Her3 依赖性细胞系(如 Ovcar8 和 HCC2935)的生长抑制作用很弱(EC50>10 μM),但它能够诱导 Her3 蛋白的部分降解并减弱 Her3 依赖性信号传导。这些结果与一些研究结果一致,这些研究表明,某些非共价激酶抑制剂,如 Her2(拉帕替尼)和 b-Raf(维莫非尼),也会导致其激酶靶标的部分降解。[1] |
| 分子式 |
C32H36N8O3
|
|---|---|
| 分子量 |
580.680046081543
|
| 精确质量 |
580.291
|
| 元素分析 |
C, 66.19; H, 6.25; N, 19.30; O, 8.27
|
| CAS号 |
1603845-32-4
|
| PubChem CID |
78243752
|
| 外观&性状 |
White to light yellow solid powder
|
| LogP |
3.3
|
| tPSA |
132
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
8
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
43
|
| 分子复杂度/Complexity |
962
|
| 定义原子立体中心数目 |
0
|
| SMILES |
C(NC1=CC(C2C3=C(N)N=CN=C3N(C3CCC(N4CCN(C(C)=O)CC4)CC3)N=2)=CC=C1OC1=CC=CC=C1)(=O)C=C
|
| InChi Key |
FYICDSWKKFSYOM-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C32H36N8O3/c1-3-28(42)36-26-19-22(9-14-27(26)43-25-7-5-4-6-8-25)30-29-31(33)34-20-35-32(29)40(37-30)24-12-10-23(11-13-24)39-17-15-38(16-18-39)21(2)41/h3-9,14,19-20,23-24H,1,10-13,15-18H2,2H3,(H,36,42)(H2,33,34,35)
|
| 化学名 |
N-[5-[1-[4-(4-acetylpiperazin-1-yl)cyclohexyl]-4-aminopyrazolo[3,4-d]pyrimidin-3-yl]-2-phenoxyphenyl]prop-2-enamide
|
| 别名 |
TX185-1 TX1 85-1 TX1-85-1
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~3.85 mg/mL (~6.63 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 0.38 mg/mL (0.65 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 3.8 mg/mL 澄清的 DMSO 储备液加入到400 μL PEG300中,混匀;再向上述溶液中加入50 μL Tween-80,混匀;然后加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 0.38 mg/mL (0.65 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 3.8 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.7221 mL | 8.6106 mL | 17.2212 mL | |
| 5 mM | 0.3444 mL | 1.7221 mL | 3.4442 mL | |
| 10 mM | 0.1722 mL | 0.8611 mL | 1.7221 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。