| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
Activin receptor-like kinase 5 (ALK5) (IC50 = 12.9 nM)
Vactosertib (EW7197; TEW7197) targets ALK-5 (TGF-β type I receptor) (IC₅₀ = 14.3 nM for ALK-5 kinase activity inhibition) [1] Vactosertib (EW7197; TEW7197) also inhibits ALK-4 (IC₅₀ = 56.4 nM) and ALK-7 (IC₅₀ = 134 nM) at higher concentrations [1] |
|---|---|
| 体外研究 (In Vitro) |
Vactosertib(10-1000 nM;30 分钟;4T1 细胞)治疗以剂量依赖性方式抑制 4T1 细胞中 TGFβ 诱导的 Smad2 或 Smad3 磷酸化 [1]。在 4T1 和 MCF10A 细胞中,vactosertib 可防止 TGFβ 诱导的 Smad2/3 核转位。在 4T1 细胞中,Vactosertib 针对 pSmad3 的 IC50 值为 10–30 nM[1]。 vactosertib 可以阻止 TGFb1 诱导的肿瘤细胞迁移和侵袭 [1]。 TGFβ1 上调 FN1、HMGA2(高迁移率组 AT-hook 2)、SNAI1 和 SNAI2(分别为 Snail 家族锌指 1 和 2)并下调 CDH1 mRNA 水平。此外,vactosertib 消除了 TGFβ1 诱导的对上皮间质转化 (EMT) 相关基因的影响 [1]。
新型ALK5激酶抑制剂EW-7197在体外抑制CML-LIC的生长。EW-7197抑制人慢性粒细胞白血病LICs的体外集落形成能力[2]。 Vactosertib (EW7197; TEW7197)在MDA-MB-231乳腺癌细胞中抑制TGF-β1诱导的Smad2/3磷酸化的IC₅₀为30 nM;同时该药物可阻断TGF-β1诱导的p3TP-luc报告基因在这些细胞中的转录激活[1] - 通过划痕愈合实验和transwell侵袭实验检测发现,该化合物(1 μM)可显著降低MDA-MB-231细胞的体外迁移和侵袭能力;还能下调这些细胞中间充质标志物(N-钙粘蛋白、波形蛋白)的表达,上调上皮标志物E-钙粘蛋白的表达[1] - 在K562和KU812慢性髓系白血病(CML)细胞中,Vactosertib (EW7197; TEW7197)(0.1-10 μM)呈剂量依赖性抑制细胞增殖,处理72小时后对K562细胞的IC₅₀为2.3 μM,对KU812细胞的IC₅₀为1.8 μM[2] - Vactosertib (EW7197; TEW7197)(1 μM)可诱导K562和KU812细胞凋亡,表现为Annexin V/PI染色阳性细胞比例增加、caspase-3/7活化;同时下调抗凋亡蛋白(Bcl-2、Mcl-1)的表达,上调促凋亡蛋白Bax的表达[2] - 该化合物(1 μM)可抑制慢性期CML患者来源的CML CD34⁺细胞的集落形成能力,而对正常骨髓CD34⁺细胞的集落形成无显著影响[2] - Vactosertib (EW7197; TEW7197)(1 μM)可抑制CML细胞中TGF-β诱导的Smad2/3磷酸化,并降低CML CD34⁺细胞中干细胞相关基因(Oct4、Sox2、Nanog)的表达[2] |
| 体内研究 (In Vivo) |
用 vabotosertib(40 mg/kg;腹腔注射;每隔一天;持续 10 周)治疗的 MMTV/c-Neu 雌性小鼠不太可能出现肺转移、细胞迁移、侵袭和 Smad/TGFβ 信号传导 [1]。此外,在 4T1 原位移植小鼠和用 TGFβ 处理的乳腺癌细胞中,vactosertib 抑制上皮间质转化 (EMT)。此外,在4T1原位移植小鼠中,vactosertib可以增加细胞毒性T细胞的活性,延长4T1-Luc和4T1乳腺癌荷瘤动物的生存期[1]。
TKI联合EW-7197治疗慢性粒细胞白血病小鼠的延长生存期。 TKI联合EW-7197在体内根除小鼠CML‐MPPs。 EW-7197联合波那替尼治疗抑制TKI耐药CML小鼠的疾病复发。[2] 在携带MDA-MB-231原位乳腺肿瘤的裸鼠中,口服Vactosertib(EW7197;TEW7197)(50毫克/公斤/天)显著减少了与对照组相比80%的肺转移;它还减少了血液中循环肿瘤细胞(CTCs)的数量,并下调了原发肿瘤的间充质标志物。[1] -该化合物(50毫克/千克/天)对裸鼠原发性MDA-MB-231乳腺肿瘤的生长没有显著影响,表明其主要作用是转移而不是原发性肿瘤的增长[1] -在小鼠CML模型(移植BCR-ABL+Ba/F3细胞)中,口服Vactosertib(EW7197;TEW7197)(50 mg/kg/day)显著延长小鼠的存活时间;与伊马替尼(50 mg/kg/day)联合治疗相比,对存活的协同效应显著。[2] Vactosertib(EW7197;TEW7197)(50 mg/kg/天)通过限制稀释法评估,减少了CML小鼠骨髓和脾脏中CML起始细胞的数量,还减少了这些组织中干细胞标记物(CD34,c-Kit)的表达。[2] 在患者来源的异种移植(PDX)慢性粒细胞白血病模型中,口服该化合物(50 mg/kg/天)显著抑制肿瘤生长,并减少骨髓中慢性粒细胞白血病干细胞的出现频率。[2] |
| 酶活实验 |
蛋白激酶测定[1]
使用ProQinase提供的放射性蛋白激酶测定法,在1×10−8、1×10-7、1×10-6和1×10-5mol/L的剂量下,对Vactosertib(EW7197)对320种蛋白激酶进行了选择性分析。详细信息见补充材料和方法。 ALK-5激酶活性测定[1] : 使用重组的ALK-5激酶域来测量Vactosertib (EW7197; TEW7197) 对激酶活性的抑制效果。该酶与不同浓度的该化合物、肽底物和反应缓冲液中的ATP共同孵育。孵育后,使用发光或比色法检测磷酸化底物的量,然后根据剂量-反应曲线计算ALK-5抑制的IC₅₀值。使用相同的测定方法评估了ALK-4和ALK-7激酶活性的抑制情况,并确定了相应的IC₅₀数值 - 斯马德依赖型转录报告实验[1] : MDA-MB-231细胞被转染了p3TP-luc报告质粒,该质粒包含与荧光素酶基因相连的TGF-β响应元件。转染后的细胞被处理TGF-β1(5 ng/ml)和不同浓度的Vactosertib(EW7197; TEW7197)达24小时。使用发光计测量荧光素酶活性,并根据相对荧光素酶单位(RLU)量化该化合物阻断TGF-β诱导的转录激活的能力。 |
| 细胞实验 |
蛋白质印迹分析[1]
细胞类型: 4T1 细胞 测试浓度: 10 nM、30 µM、50 nM、100 µM、300 nM、500 nM,1000 nM 孵育时间: 30 分钟 实验结果: 以剂量依赖性方式阻断 TGFb 诱导的 Smad2 或 Smad3 磷酸化。 蛋白质印迹分析[1] 将小鼠组织或细胞在RIPA缓冲液中均质化。通过聚丙烯酰胺凝胶电泳分离含有4至50μg总蛋白的裂解物,然后将其电泳转移到聚偏二氟乙烯转移膜上。用5%牛血清白蛋白封闭膜,并在4°C下与指定的一抗一起孵育过夜(补充表S1)。然后将膜与辣根过氧化物酶偶联的二抗一起孵育。用Western Blotting Luminol试剂检测结合抗体。 伤口愈合试验[1] 将4T1细胞和MDA-MB-231细胞接种在6孔板中。当每个孔的面积超过80%被细胞占据时,将10%的HI-FBS培养基改为0.2%的HI-FBS-培养基。24小时后,用塑料移液管尖端刮擦形成“伤口”(时间=0),用TGFβ1(2 ng/mL)在有或没有ALK5抑制剂的情况下处理细胞24小时(4T1)或53小时(MDA-MB-231)。根据显微镜上连接的相机捕获的细胞相位对比图像,使用ImageJ程序测量零时间或终点的伤口面积。伤口面积的闭合以初始伤口面积的百分比计算。 基质胶侵袭试验[1] Transwell(直径6.5-mm,孔径8-μm;康宁)的上表面涂有20μL稀释的33.3%Matrigel。在有或没有ALK5抑制剂的情况下,将4T1细胞以每孔4×104个细胞的速度接种在Transwell的上腔中,在无血清培养基中加入或不加入TGFβ1(2ng/mL)。下腔室内填充了与上腔相同的培养基,但含有10%的HI-FBS。孵育20小时后,用棉签去除膜上表面残留的细胞,并使用荧光显微镜观察底面残留的DAPI染色细胞。从五个随机场中获得每个视场的平均细胞数。 菌落形成能力[2] 为了确定Vactosertib(EW7197)加IM或EW-7197加ponatinib联合治疗后的集落形成能力,我们在DMSO或EW-7217的存在下,将新鲜分离的CML-LIC在OP-9基质细胞上共培养24小时。18然后用额外的DMSO、1μM IM或1μM ponatinip(AP24534)处理细胞,并再培养2天(共3天)。如前所述,7天后对菌落进行了计数。 原发性人类慢性粒细胞白血病-LIC的集落形成能力[2] 来自三名慢性粒细胞白血病患者的活骨髓单核细胞购自Allcells。细胞用抗CD34(8G12)、抗CD38(HIT2)、抗-CD3(SK7)、抗CD16(3G8)、抗/CD19(SJ25C1)、抗CD20(L27)、反CD14(MϕP9)和抗CD56(NCAM16.2)抗体染色。使用识别CD3、CD16、CD19、CD20、CD14和CD56的单克隆抗体混合物来鉴定Lin−细胞,并纯化CD34+CD38-Lin-细胞。18为了确定单独使用或Vactosertib (EW7197)加达沙替尼组合使用Vactosertib(EW7197)的效果,在缺氧条件下(3%O2)在OP−9基质细胞上培养CD34+CD38-2in−细胞。在PBS中收获和洗涤后,通过在半固体培养基中培养来评估原始人类CML-LIC的集落形成能力。 乳腺癌细胞迁移和侵袭试验[1] : 针对伤口愈合试验,MDA-MB-231细胞被接种在培养皿中,并在已汇合的单层细胞表面划出伤口;随后细胞被处理以接受 Vactosertib(EW7197;TEW7197) (1 μM)或溶剂的处理,并在 0、24 和 48 小时内拍摄并定量伤口的闭合情况。对于透壁侵袭试验,细胞被接种在 Matrigel 涂层插片的上层腔室中,下层腔室则含有作为化学吸引剂的血清;在化合物(1 μM)处理后,通过显微镜计数穿过 Matrigel 的细胞数量,以评估侵袭能力。 - 上皮-间质转化(EMT)标志物的Western blot分析[1] : MDA-MB-231细胞被处理于Vactosertib (EW7197; TEW7197) (1 μM)或TGF-β1联合该化合物48小时。制备细胞裂解液,等量蛋白质经SDS-PAGE分离,转移至膜上,并使用针对E-钙粘蛋白、N-钙粘蛋白、波形蛋白和GAPDH(内参)的抗体进行探针检测。使用成像软件量化条带强度,以确定蛋白质表达的变化 CML细胞增殖和凋亡测定[2] :K562和KU812细胞在96孔板中播种,并用Vactosertib(EW7197;TE W7197)在浓度范围为0.1至10μM的条件下持续72小时。用比色法测定细胞增殖,计算IC 50值。细胞凋亡分析用Annexin V和碘化丙啶(PI)染色处理的细胞,用流式细胞术测定凋亡细胞百分比。Caspase-3/7活性是通过荧光测定试剂盒测定的,以确认凋亡诱导。 - CML和正常CD34+细胞的集落形成测定[2] :将CML CD34细胞(来自慢性期CML患者)和正常骨髓CD34细胞分离并接种于含有细胞因子的甲基纤维素培养基中。用Vac to sert ib(EW7197;TEW 7197)(1μM)或赋形剂处理细胞,培养14天后计数菌落。该化合物对克隆生长的影响表现为与对照组相比形成的菌落百分比。 - 干细胞相关基因的qPCR分析[2] :用Vac to sert ib(EW7197;TEW 7197)(1μM)处理CML CD 34+细胞48小时后,提取总RNA并反向转录成cDN A。使用Oct4、Sox2、Nanog和GAPDH(家政基因)特异性引物进行定量PCR。使用2ΔΔCt方法计算每个基因的相对表达,以评估该化合物对干细胞基因表达的影响。 |
| 动物实验 |
动物/疾病模型:乳腺肿瘤病毒 (MMTV)/c-Neu 雌性小鼠(32 周龄)[1]
\n剂量: 40 mg/kg \n给药途径:腹腔注射 (ip);隔日一次;持续 10 周 \n实验结果:抑制 MMTV/c-Neu 小鼠的 Smad/TGFβ 信号通路、细胞迁移、侵袭和肺转移。 \n\n使用 MMTV/c-Neu 小鼠的乳腺癌模型 #1 [1] \n\n当乳腺肿瘤总体积达到 100 mm3 时,将 32 周龄的 MMTV/c-Neu 小鼠随机分组,并分别腹腔注射生理盐水(Veh;n = 7)或溶于生理盐水的 Vactosertib (EW7197)·HCl(43.7 mg/kg;相当于 40 mg/kg EW-7197,n = 10),每周三次,持续 10 周。\n \n使用 4T1 细胞的乳腺癌模型 #2、#3 和 #4原位移植小鼠[1] \n\n在疗效实验(模型#2和#3)中,将1.2 × 10⁴个4T1细胞悬浮于生理盐水中,并植入雌性BALB/c小鼠的左侧乳腺脂肪垫(#4)(50 μL/只;第0天)。每周测量肿瘤大小和体重。从第4天开始,每周五次,连续28天,分别给小鼠口服人工胃液(Veh)、溶于Veh的Vactosertib(EW7197)(5或20 mg/kg)或LY2157299(40或80 mg/kg)(模型#2;n = 10/组)。从第4天开始,每周三次给小鼠注射载体或Vactosertib (EW7197)(5、10、20或40 mg/kg),共持续28天(模型#3;每组n=6~8只)。在模型#3的TGFβ1刺激实验中,从每组中随机选取2只小鼠,于第28天用指定浓度的EW-7197处理。30分钟后,每组1只小鼠静脉注射TGFβ1(50 ng/只),另一只小鼠不进行任何处理。TGFβ1注射90分钟后,处死小鼠。在生存实验(模型#4)中,按照模型#2的方法注射1.6 × 10⁴个4T1细胞,并将溶于Veh的Veh或EW-7197(2.5或5 mg/kg)从第7天开始,每周五次口服给小鼠,直至死亡(n = 11/组)。\n \n乳腺癌模型#5采用4T1-luc尾静脉小鼠模型[1] \n\n将4T1-luc细胞[2 × 10⁵;转染质粒构建体pGL4(CMV-Luc)]悬浮于生理盐水中,并注射到雌性BALB/c小鼠的尾静脉中(50 μL/只;第0天)。将溶于 Veh 的人工胃液 (Veh) 或 Vactosertib (EW7197) (0.625、1.25、2.5 或 5 mg/kg) 每周五次经口给予小鼠,从第 0 天开始直至死亡(每组 n = 13)。在第 15 天,使用体内成像系统分析存活小鼠,以比较肺部转移情况。使用 IVIS-200 系统对荧光素酶阳性的 4T1 细胞进行成像。使用 Living Image 软件对采集的图像进行定量分析。\n \n乳腺癌模型 #6,使用 4T1-luc 原位移植小鼠 [1] \n\n4T1-luc 细胞 [3 × 10⁴;将转染了质粒构建体pGL4(CMV-Luc)的肿瘤细胞植入雌性BALB/c小鼠左侧第4乳腺脂肪垫,方法与模型2相同(第0天)。每周测量肿瘤大小和体重。将溶于人工胃液 (Veh) 的 Vactosertib (EW7197) (2.5、5、10 或 20 mg/kg) 以口服方式给予小鼠,每周 5 次(2.5、5 或 10 mg/kg)或每周 3 次(20 mg/kg),从第 4 天开始,共 28 天(每组 n = 15)。小鼠存活率 [2] 对于使用 CML 小鼠进行的“TKI 不敏感”存活实验,在移植 BCR-ABL1 + CML-MPP 后第 8-90 天,通过灌胃给予小鼠 IM(诺华公司,巴塞尔,瑞士)(200 mg/kg/天)。18 对于使用 T315I CML 小鼠进行的“TKI 耐药”复发实验,使用 ponatinib在移植 BCR‐ABL1‐T315I+ CML‐MPP 后的第 8 至 60 天,通过灌胃法(15 mg/kg/天)给予小鼠 (AP24534)。在这两种情况下,我们都使用了 Vactosertib (EW7197) 的储备液,该储备液在人工胃液溶液(900 mL 双蒸水,含 2.0 g NaCl、7 mL 浓 HCl 和 3.2 g 胃蛋白酶)中配制成 2 μg/mL 的浓度。在移植 BCR-ABL1 + CML-MPP 后第 15 至 90 天,或在移植 BCR-ABL1-T315I + CML-MPP 后第 15 至 60 天,每隔 3 天,将该混合物稀释于人工胃液中,通过灌胃法给予患有 CML 的小鼠,以达到 2.5 mg EW-7197/kg 体重的最终浓度。在“TKI不敏感”实验中监测小鼠存活125天,在“TKI耐药”复发实验中监测小鼠存活100天。\n \n药代动力学[2] \n\n为了评估Vactosertib (EW7197)的药代动力学,将四环素诱导型tg-CML小鼠禁食过夜,然后按照上述方法通过灌胃给予Vactosertib (EW7197) (10 mg/kg)。在治疗前以及治疗后30分钟、2小时、4小时和8小时采集血样。采用液相色谱/串联质谱法,使用配备电喷雾电离源的安捷伦 1200 系列高效液相色谱仪和安捷伦 6410 三重四极杆质谱仪测定 EW-7197 的血浆浓度。\n \n采用 Duolink® 原位 PLA 技术进行药效学研究[2] \n\n基于 Smad3 的磷酸化测定 Vactosertib (EW7197) 的药效学。通过灌胃法给予四环素诱导的 tg-CML 小鼠 Vactosertib (EW7197) (2.5 mg/kg)。然后,我们使用 FACSAria III 流式细胞仪(BD Biosciences)从 tg-CML 小鼠中分离出含有原始 LT-CML 干细胞(CD150+CD135−CD48−KLS 细胞)的细胞组分。27 使用抗 Smad3 和兔抗磷酸化 Ser423/425 Smad3 (ab51451) 抗体,通过高灵敏度的 Duolink® 原位 PLA 技术检测细胞中的磷酸化 Smad3。\n \n外周血白细胞计数测定[2] \n\nCML 小鼠接受达沙替尼(5 mg/kg/天)加载体或 Vactosertib (EW7197)(每三天 2.5 mg/kg)灌胃,持续 30 天。血细胞计数方面,从眼眶后静脉采集外周血,置于肝素化微量离心管中,并在 CellTac 血细胞分析仪上进行分析。 \n裸鼠原位乳腺癌转移模型[1] \n:将 MDA-MB-231 细胞 (1 × 10⁶) 注射到雌性裸鼠的乳腺脂肪垫中,建立原位肿瘤模型。当肿瘤体积达到约 100 mm³ 时,将小鼠随机分为对照组和治疗组。Vactosertib (EW7197; TEW7197) 溶解于溶剂(由 0.5% CMC-Na 和 0.1% Tween 80 组成)中,以 50 mg/kg 的剂量每日一次灌胃给药,持续 4 周。对照组小鼠仅接受溶剂。治疗结束后,采集肺组织,并在显微镜下计数转移结节;采集血样,通过流式细胞术定量循环肿瘤细胞(CTC)。 \n- BCR-ABL⁺ Ba/F3 细胞 CML 小鼠模型 [2] \n:将 BCR-ABL⁺ Ba/F3 细胞(5 × 10⁵ 个细胞/只)静脉注射到 BALB/c 小鼠体内,以诱导 CML。细胞注射后 7 天开始,小鼠接受 Vactosertib(EW7197;TEW7197)(50 mg/kg/天,灌胃)、伊马替尼(50 mg/kg/天,灌胃)或两者联合治疗,持续 21 天。对照组小鼠接受溶剂(0.5% CMC-Na + 0.1% Tween 80)。每天监测小鼠的存活情况,持续60天,并收集骨髓/脾脏样本,通过有限稀释法评估CML起始细胞的频率。 \n- CML患者来源的异种移植(PDX)模型[2] \n:将患者的原代CML细胞通过尾静脉注射移植到免疫缺陷的NOD/SCID小鼠体内。移植成功后(通过检测外周血中的人CD45⁺细胞确认),小鼠接受Vactosertib(EW7197;TEW7197)(50 mg/kg/天,灌胃)治疗4周。使用流式细胞术检测骨髓和脾脏中的人CD45⁺细胞水平来评估肿瘤负荷;通过集落形成试验和有限稀释分析确定CML干细胞的频率。 |
| 药代性质 (ADME/PK) |
EW-7197 在 tg-CML 小鼠体内的药代动力学和药效学 [2]
接下来,我们通过评估治疗后血浆浓度-时间曲线,确定了 EW-7197 在四环素诱导的 tg-CML 小鼠血液中的药代动力学。我们观察到,EW-7197 能迅速从 tg-CML 小鼠的胃肠道吸收进入血液,然后以 3.26 ± 2.47 小时的终末半衰期 (T1/2) 消除(图 2a)。给药后 30 分钟测得药物在血浆中的最大浓度 (Cmax) 为 625.0 ± 529.7 ng/mL (n = 7)。 Vactosertib (EW7197; TEW7197) 是一种口服生物利用度高的小分子药物;小鼠口服给药 (50 mg/kg) 后,该化合物被迅速吸收并分布到包括肺、骨髓和脾脏在内的组织中 [1][2] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外实验表明,浓度高达 10 μM 的 Vactosertib (EW7197; TEW7197) 对正常骨髓 CD34⁺ 细胞无显著细胞毒性 [2]。体内实验表明,对裸鼠和 BALB/c 小鼠口服 Vactosertib (EW7197; TEW7197)(50 mg/kg/天,持续 4 周)未引起明显的体重减轻或器官毒性(通过对肝脏、肾脏和肺组织进行 H&E 染色评估)[1][2]。
|
| 参考文献 | |
| 其他信息 |
Vactosertib 正在临床试验 NCT03724851(Vactosertib 联合帕博利珠单抗治疗转移性结直肠癌或胃癌)中进行研究。
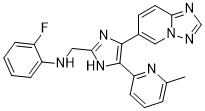
Vactosertib 是一种口服生物利用度高的丝氨酸/苏氨酸激酶抑制剂,可抑制转化生长因子 (TGF)-β 受体 1 型 (TGFBR1),也称为激活素受体样激酶 5 (ALK5),具有潜在的抗肿瘤活性。口服后,Vactosertib 可抑制 TGFBR1 的活性,并阻断 TGF-β/TGFBR1 介导的信号传导。这可抑制 TGFBR1 过表达肿瘤细胞的生长。TGFBR1 在多种肿瘤细胞类型中过表达,并在肿瘤细胞增殖中发挥关键作用。 TGF-β的表达促进肿瘤细胞增殖,增强肿瘤细胞迁移,并抑制宿主免疫系统对肿瘤细胞的反应。晚期肿瘤会产生过量的转化生长因子β(TGFβ),从而促进恶性肿瘤晚期的进展。本研究旨在开发抗TGFβ疗法用于癌症治疗。我们合成了一种新型小分子TGFβ受体I激酶(激活素受体样激酶5)抑制剂,命名为N-[[4-([1,2,4]三唑并[1,5-a]吡啶-6-基)-5-(6-甲基吡啶-2-基)-1H-咪唑-2-基]甲基]-2-氟苯胺(EW-7197),并研究了其在小鼠乳腺肿瘤病毒(MMTV)/c-Neu小鼠和4T1原位移植小鼠中的潜在抗转移疗效。 EW-7197抑制了MMTV/c-Neu小鼠和4T1原位移植小鼠的Smad/TGFβ信号通路、细胞迁移、侵袭和肺转移。EW-7197还抑制了TGFβ处理的乳腺癌细胞和4T1原位移植小鼠的上皮间质转化(EMT)。此外,EW-7197增强了4T1原位移植小鼠的细胞毒性T淋巴细胞活性,并延长了4T1-Luc和4T1乳腺肿瘤荷瘤小鼠的生存期。总之,EW-7197 显示出强大的体内抗转移活性,表明其具有作为抗癌疗法的潜力。[1] 近年来,慢性粒细胞白血病 (CML) 患者的治疗策略主要集中于探索酪氨酸激酶抑制剂 (TKI) 的新组合,以及寻找能够根除 CML 白血病起始细胞 (CML-LIC) 的新型转化研究药物。然而,人们对这类靶向 CML-LIC 的疗法可能给 CML 患者带来的治疗益处知之甚少。在本研究中,我们探讨了 EW-7197(一种口服生物利用度高的转化生长因子-β 信号通路抑制剂,近期已获美国国立卫生研究院 (NIH) 批准作为研究性新药)在体内抑制 CML-LIC 的治疗潜力。与单独使用 TKI 治疗相比,对 CML 小鼠联合使用 TKI 和 EW-7197 可显著延缓疾病复发并延长生存期。值得注意的是,即使 CML-LIC 表达了对 TKI 耐药的 T315I 突变 BCR-ABL1 癌基因,EW-7197 与 TKI 联合治疗也能有效清除 CML-LIC。总的来说,这些结果表明 EW-7197 可能是一种有前景的新型治疗候选药物,它与酪氨酸激酶抑制剂 (TKI) 联合使用可根除慢性粒细胞白血病起始细胞 (CML-LIC),从而显著改善 CML 患者的预后。[2] Vactosertib (EW7197; TEW7197) 是一种新型的选择性 TGF-β I 型受体 (ALK-5) 小分子抑制剂。[1] - 该化合物通过抑制 TGF-β/Smad 信号通路并逆转肿瘤细胞的上皮-间质转化 (EMT),在乳腺癌中发挥抗转移作用。[1] - 在 CML 中,Vactosertib (EW7197; TEW7197) 通过抑制 TGF-β 介导的干细胞维持通路靶向 CML 起始细胞(癌症干细胞),并与伊马替尼协同作用,增强抗白血病疗效。 [2] - Vactosertib (EW7197; TEW7197) 正在被研究用于治疗转移性乳腺癌和慢性粒细胞白血病,重点在于克服与癌症干细胞相关的转移和耐药性[1][2] |
| 分子式 |
C22H18FN7
|
|
|---|---|---|
| 分子量 |
399.42
|
|
| 精确质量 |
399.16
|
|
| 元素分析 |
C, 66.15; H, 4.54; F, 4.76; N, 24.55
|
|
| CAS号 |
1352608-82-2
|
|
| 相关CAS号 |
Vactosertib Hydrochloride;1352610-25-3; 1352608-82-2
|
|
| PubChem CID |
54766013
|
|
| 外观&性状 |
Light yellow to yellow solid powder
|
|
| 密度 |
1.4±0.1 g/cm3
|
|
| 折射率 |
1.725
|
|
| LogP |
3.19
|
|
| tPSA |
83.79
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
6
|
|
| 可旋转键数目(RBC) |
5
|
|
| 重原子数目 |
30
|
|
| 分子复杂度/Complexity |
566
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
CC1=NC(=CC=C1)C2=C(N=C(N2)CNC3=CC=CC=C3F)C4=CN5C(=NC=N5)C=C4
|
|
| InChi Key |
FJCDSQATIJKQKA-UHFFFAOYSA-N
|
|
| InChi Code |
InChI=1S/C22H18FN7/c1-14-5-4-8-18(27-14)22-21(15-9-10-20-25-13-26-30(20)12-15)28-19(29-22)11-24-17-7-3-2-6-16(17)23/h2-10,12-13,24H,11H2,1H3,(H,28,29)
|
|
| 化学名 |
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.5 mg/mL (6.26 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (6.26 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (6.26 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.5036 mL | 12.5182 mL | 25.0363 mL | |
| 5 mM | 0.5007 mL | 2.5036 mL | 5.0073 mL | |
| 10 mM | 0.2504 mL | 1.2518 mL | 2.5036 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
EW-7197 inhibits TGFβ1/Smad signaling.Mol Cancer Ther.2014 Jul;13(7):1704-16. |
|---|
Effect of EW-7197 on cell migration and invasion.Mol Cancer Ther.2014 Jul;13(7):1704-16. |
Effect of EW-7197 on EMT.Mol Cancer Ther.2014 Jul;13(7):1704-16. |
EW-7197 inhibits breast cancer metastasis to the lung.Mol Cancer Ther.2014 Jul;13(7):1704-16. |
|---|
EW-7197 prolongs the life span of BALB/c 4T1 mice via inhibition of EMT.Mol Cancer Ther.2014 Jul;13(7):1704-16. |
EW-7197 inhibits metastasis and enhances the activity of CTLs in 4T1 orthotopic–grafted mice.Mol Cancer Ther.2014 Jul;13(7):1704-16. |