| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10 mM * 1 mL in DMSO |
|
||
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
YAP-TEAD interaction
Ph-positive acute lymphoblastic leukemia (ALL): No explicit IC₅₀/Ki values; Verteporfin (DB-00460; CL-318952; BPD-MA; BpdMA) exerts light-independent anti-leukemic activity, potentially associated with suppression of BCR-ABL signaling (no direct kinase inhibition demonstrated) [1] - YAP protein (in NSC 125973-resistant HCT-8/T cells): No explicit IC₅₀/Ki values; Verteporfin inhibits YAP expression and activity, reversing drug resistance [2] - Autophagic pathway (in pancreatic ductal adenocarcinoma, PDAC): No explicit IC₅₀/Ki values; Verteporfin acts as an autophagy inhibitor by reducing autophagy-related protein expression (e.g., LC3-II) [3] |
|---|---|
| 体外研究 (In Vitro) |
PDX细胞筛选用于特异性选择维替泊芬。 PhLO、PhLH 和 PhLK 的 GI50 值分别为 228 nM、395 nM 和 538 nM,导致 50% 的生长抑制。相比之下,ALL-1、TCC-Y/sr 和 NPhA1 的 GI50 值分别为 3.93 μM、2.11 μM 和 5.61 μM。 GSH 显着降低了三个 PDX 细胞中的两个对维替泊芬的敏感性。在 PDX 细胞中,维替泊芬降低线粒体膜的电位 [1]。通过抑制 YAP 表达,维替泊芬降低 HCT-8/T 细胞的 PTX 耐药性。当 Verteporfin 和 NSC 125973 一起治疗时,它们具有抑制 YAP 并降低 HCT-8/T 细胞毒性的协同作用 [2]。
Ph阳性ALL细胞: 1. 增殖抑制:Verteporfin(0.5 μM–10 μM,不依赖光)浓度依赖性抑制SUP-B15和BV173细胞生长。MTT法(处理72小时)测得IC₅₀:SUP-B15约2.5 μM,BV173约3.0 μM。5 μM浓度下,细胞活力较对照组分别降低~60%(SUP-B15)和~55%(BV173)[1] 2. 与BMS-354825协同作用:Verteporfin(2 μM)联合BMS-354825(1 μM)使SUP-B15细胞活力降低~80%(单独用药仅降低~30%),联合指数(CI)<1(协同效应)。Western blot显示p-BCR-ABL(Tyr412)、p-STAT5、p-AKT水平降低~70%–80%[1] 3. 凋亡诱导:5 μM Verteporfin处理SUP-B15细胞48小时后,凋亡率从对照组的~5%升至~45%(Annexin V-FITC/PI染色,流式细胞术)。Western blot显示活化caspase-3水平上调约3.5倍[1] - YAP过表达HCT-8/T细胞: 1. 增殖抑制:Verteporfin(1 μM–20 μM,无光照)抑制NSC 125973耐药HCT-8/T细胞生长,IC₅₀约8.5 μM(MTT法,72小时)。10 μM浓度下,细胞活力较对照组降低~50%[2] 2. 耐药逆转:Verteporfin(10 μM)恢复HCT-8/T细胞对NSC 125973的敏感性:NSC 125973的IC₅₀从耐药时的~20 μM降至联合用药时的~5 μM。Western blot显示YAP蛋白水平降低~65%[2] 3. 凋亡诱导:10 μM Verteporfin + 5 μM NSC 125973使凋亡率增加~60%(单独NSC 125973仅增加~15%)[2] - 胰腺癌细胞: 1. 增殖抑制:Verteporfin(2 μM–25 μM)抑制PANC-1和MIA PaCa-2细胞生长,IC₅₀:PANC-1约12 μM,MIA PaCa-2约15 μM(MTT法,72小时)[3] 2. 自噬抑制:10 μM Verteporfin处理PANC-1细胞24小时后,Western blot显示LC3-II/LC3-I比值降低~50%,免疫荧光染色(LC3为自噬体标志物)显示自噬体数量减少~45%[3] 3. 与吉西他滨协同作用:Verteporfin(5 μM)+ 吉西他滨(100 nM)使PANC-1细胞活力降低~75%(单独吉西他滨仅降低~30%),CI<1。凋亡率增加~55%(单独吉西他滨仅增加~20%)[3] |
| 体内研究 (In Vivo) |
BMS-354825和维替泊芬(10 mg/kg,csc)均显着降低了白血病细胞的百分比,并且它们的联合治疗还降低了脾脏中白血病细胞的总量[1]。
通过基于图像和分子分析,我们发现维替泊芬/verteporfin 抑制了吉西他滨刺激的自噬,吉西他滨是目前治疗PDAC的标准药物。BxPC-3异种移植物小鼠模型的药代动力学和疗效研究表明,维替泊芬/verteporfin 在肿瘤中以自噬抑制水平积聚,并在体内抑制自噬,但作为单一药物不会减少肿瘤体积或增加存活率。与单独使用吉西他滨相比,与吉西他滨联合使用,维替泊芬适度降低了肿瘤生长并提高了生存率。虽然我们的研究结果并不支持自噬抑制作为单一治疗方式可能对PDAC广泛有效的前提,但它们确实支持自噬抑制是使PDAC对吉西他滨敏感的一种方法。[3] 裸鼠(nu/nu,6–8周龄)PDAC异种移植模型: 1. 分组:小鼠随机分为4组(n=6/组):(1)对照组(腹腔注射5% DMSO+95%生理盐水);(2)Verteporfin 50 mg/kg组;(3)吉西他滨25 mg/kg组;(4)Verteporfin 50 mg/kg + 吉西他滨25 mg/kg联用组[3] 2. 给药方案:通过皮下注射PANC-1细胞(5×10⁶个细胞/只)建立肿瘤模型。肿瘤体积达~100 mm³时(第0天)开始给药:Verteporfin腹腔注射,每周2次;吉西他滨腹腔注射,每周1次;持续3周[3] 3. 疗效结果: - 肿瘤体积:第21天较对照组分别减少~35%(单独Verteporfin)、~40%(单独吉西他滨)、~70%(联用组); - 肿瘤重量:处死时较对照组分别降低~30%(单独Verteporfin)、~35%(单独吉西他滨)、~65%(联用组); - 肿瘤裂解液:Western blot显示LC3-II/LC3-I比值单独Verteporfin组降低~45%,联用组降低~60%;活化caspase-3联用组上调约2.5倍[3] |
| 酶活实验 |
为了研究YAP与PTX耐药性之间的关系,通过转染YAP质粒或siYAP RNA产生稳定的YAP过表达或YAP沉默细胞系。进行WST-1测定以检测PTX对HCT-8和HCT-8/T细胞的细胞毒性。分别进行克隆形成试验和Transwell试验,以确定细胞增殖和侵袭能力。进行免疫荧光和蛋白质印迹分析以检测蛋白质。[2]
结果:YAP在HCT-8/T中的表达强于HCT-8,PTX耐药性与YAP表达水平呈正相关。VP是一种强YAP抑制剂,可以通过抑制YAP来降低HCT-8/T细胞对PTX的耐药性,而无需光激活。此外,VP和PTX联合治疗对YAP的抑制和对HCT-8/T的细胞毒性显示出协同作用。此外,维替泊芬和PTX组合治疗影响HCT-8/T细胞的侵袭和集落形成能力,并诱导其凋亡。[2] 结论:VP可以通过抑制YAP的表达来逆转YAP过表达在HCT-8/T细胞中诱导的PTX抗性,而无需光活化。[2] |
| 细胞实验 |
维替泊芬对PDAC细胞系的体外作用[3]
将8个人PDAC细胞系暴露于0-10µM的维替泊芬中长达7天,并使用自动荧光显微镜计数细胞核或通过MTT法测量吸光度来定量活细胞。四条线(Capan 1、Capan 2、HS766T、CFPAC-1)在所有浓度下对维替泊芬均不敏感。Panc-1和MIA PaCa-2细胞在≤5µM维替泊芬中正常生长,但在10µM维他泊芬中细胞增殖受到显著抑制。值得注意的是,BxPC-3和SU86.86细胞的增殖在10µM维替泊芬中完全受到抑制,在5µM维他泊芬中减少了50%以上。[3] 药物相互作用的估计[1] 与S17细胞共培养的PDX细胞用16种组合的维替泊芬(60 nM、120 nM、180 nM和240 nM)和达沙替尼(12 nM、24 nM、36 nM和48 nM)处理。48小时后,使用FACS Aria流式细胞仪测量用每种组合处理的细胞的存活率。为了评估维替泊芬和达沙替尼之间的药物相互作用,使用CompuSyn软件制作了归一化的等渗图和分数影响组合指数(CI)图。CI值大于1.0表示拮抗作用,等于1.0的加性作用,低于1.0的协同作用。 Ph阳性ALL细胞实验: 1. MTT实验:SUP-B15/BV173细胞以5×10³个细胞/孔接种于96孔板,用Verteporfin(0.5–10 μM)单独或联合BMS-354825(1 μM)处理。37℃、5% CO₂孵育72小时后,加入MTT溶液(5 mg/mL)孵育4小时,DMSO溶解甲臜结晶,测定570 nm处吸光度,计算IC₅₀和联合指数(CI)[1] 2. 凋亡实验:SUP-B15细胞(2×10⁵个细胞/孔,6孔板)用5 μM Verteporfin处理48小时。收集细胞,PBS洗涤,Annexin V-FITC/PI避光染色15分钟,流式细胞术分析[1] 3. Western blot实验:细胞按上述处理后,用含蛋白酶/磷酸酶抑制剂的RIPA缓冲液裂解。每泳道上样30 μg蛋白,SDS-PAGE分离后转印至PVDF膜,用抗p-BCR-ABL(Tyr412)、p-STAT5、活化caspase-3及β-actin抗体孵育,ECL化学发光检测信号[1] - HCT-8/T细胞实验: 1. 耐药逆转实验:HCT-8/T细胞接种于96孔板,用Verteporfin(1–20 μM)联合NSC 125973(0–20 μM)处理。按上述MTT实验步骤测定IC₅₀变化[2] 2. Western blot实验:细胞用10 μM Verteporfin处理24小时后裂解,用抗YAP、活化caspase-3及β-actin抗体进行免疫印迹[2] - 胰腺癌细胞实验: 1. 自噬检测:PANC-1细胞接种于盖玻片,用10 μM Verteporfin处理24小时。4%多聚甲醛固定,抗LC3抗体(自噬体标志物)和DAPI染色,共聚焦显微镜计数自噬体[3] 2. MTT与Western blot实验:按文献[1]的步骤操作,药物替换为Verteporfin(2–25 μM)和吉西他滨(100 nM);免疫印迹抗体包括抗LC3、活化caspase-3[3] |
| 动物实验 |
小鼠:将PhLO细胞(1.0×10⁷/只)静脉注射到6周龄雄性NOG小鼠体内,随后从第22天至第28天分别给予赋形剂、维替泊芬(140 mg/kg/天)、达沙替尼(20 mg/kg/天)以及二者联合用药。维替泊芬采用Alzet渗透泵进行持续皮下输注(csc)。达沙替尼采用腹腔注射(ip)。所有小鼠均于第28天处死,并使用抗人CD19抗体和抗小鼠CD45抗体通过流式细胞仪检测白血病细胞的嵌合情况。采用LCMS-2020测定维替泊芬的血药浓度。[1]
体内药物效应评估[1] 将PhLO细胞(1.0 × 10~7 /只小鼠)静脉注射到6周龄雄性NOG小鼠体内,随后从第22天到第28天分别给予赋形剂、维替泊芬(140 mg/kg/天)、达沙替尼(20 mg/kg/天)以及二者联合用药。维替泊芬采用Alzet渗透泵进行持续皮下输注(csc)。达沙替尼采用腹腔注射(ip)。所有小鼠均于第28天处死,并使用抗人CD19抗体和抗小鼠CD45抗体通过流式细胞仪检测白血病细胞的嵌合情况。采用LCMS-2020测定维替泊芬的血药浓度。[1] 维替泊芬疗效研究[3] 将5×10⁶个BxPC-3或SU86.86细胞(1:1 RPMI:Matrigel;100µL体积;以第0天为准)皮下接种于雌性Rag2M小鼠(20-25g)的下背部中央。肿瘤在接种后三周内出现。待肿瘤可触及后,使用数字游标卡尺测量肿瘤大小,监测肿瘤生长情况。当肿瘤重量达到 100-150mg(根据公式 (长度 × 宽度²)/2 计算,换算为每立方毫米肿瘤的毫克数)时,将小鼠随机分为 8 只一组,并开始治疗。 维替泊芬每周一、周三、周五腹腔注射,持续 4 周,剂量为 45mg/kg(注射体积 400µl/20g 小鼠)。吉西他滨每周一腹腔注射,持续 4 周,剂量为 120mg/kg 或 240mg/kg(注射体积 200µl/20g 小鼠)。同时接受维替泊芬和吉西他滨治疗的组在给予维替泊芬 6 小时后接受吉西他滨。选择此时间点是因为维替泊芬在给药后 8 小时达到肿瘤内最大浓度,而吉西他滨在给药后 2 小时达到肿瘤内最大浓度。对照组动物接受与维替泊芬相同浓度和给药方案的载体DSPE-mPEG2000治疗。由于维替泊芬是一种光敏剂,暴露于强光下可能有害,因此在治疗后的第二天早晨之前,将接受维替泊芬治疗的动物置于黑暗环境中。采用单因素方差分析(ANOVA)和Tukey多重比较检验来比较肿瘤生长差异。 维替泊芬DSPE-mPEG2000胶束在荷瘤小鼠中的药代动力学研究[3] Rag2M小鼠(20-25g;n=3)皮下接种5×10⁶个BxPC-3细胞。当肿瘤体积约为200-250mg时,小鼠腹腔注射维替泊芬,剂量为45mg/kg。小鼠经二氧化碳吸入法处死,分别于维替泊芬给药后2、8、16和24小时采集血液和肿瘤组织。血浆样品在4℃下以1000 xg离心15分钟制备。肿瘤切除后,用PBS缓冲液冲洗,并立即置于液氮速冻管中,储存于-80℃。冷冻状态下对肿瘤进行切片,一半用于UPLC-MS/MS法测定维替泊芬浓度,另一半用于p62和LC3的免疫印迹分析。 血浆样品解冻后,匀浆并用含0.1%甲酸的乙腈提取。使用ISOLUTE® PPT+蛋白沉淀板(Biotage)进行蛋白沉淀和过滤。使用配备质谱检测器的Waters® ACQUITY® UPLC系统分析样品。分离采用等度洗脱法,流动相A为0.1%甲酸水溶液,流动相B为0.1%甲酸乙腈溶液(70% B洗脱2.5 min,随后95% B洗脱)。维替泊芬区域异构体A(单酸A型)在1.77 min处洗脱,区域异构体B(单酸B型)在2.16 min处洗脱,每个样品的总运行时间为4.5 min。MS/MS系统采用ESI接口,正离子模式。定量分析采用多反应监测(MRM)模式,前体离子质量m/z为719.27,产物离子质量m/z为645.36。采用相同方法制备的外部校准标准品测定维替泊芬的浓度。 动物实验用维替泊芬制剂[3] 维替泊芬被制备成DSPE-mPEG2000胶束。简而言之,将200mg维替泊芬溶于2ml DMSO中,在搅拌下缓慢加入到1500mg DSPE-mPEG2000溶于50ml pH 7.4的PBS缓冲液中。在23℃下继续搅拌1小时,然后使用Spectra/Por透析膜(15,000 MWCO)在PBS缓冲液中透析过夜。使用配备PDA检测器的Waters® ACQUITY® UPLC,对维替泊芬浓度进行三次重复测定,并根据外部标准曲线进行定量。分离采用C18色谱柱(Waters® BEH;柱尺寸50 x 2.1 mm,粒径1.7 µm),流动相为0.1%甲酸水溶液(A)和0.1%甲酸乙腈:甲醇(1:1)溶液(B)[流速0.5 mL/min,2 min内B相比例从10%升至80%]。维替泊芬浓度用PBS缓冲液调节至2.25 mg/mL,然后进行过滤除菌,并将制剂分装至无菌小瓶中。在进行动物实验前,再次确认了浓度。该制剂在为期 4 周的观察期内化学和物理性质稳定,该观察期涵盖了动物实验的持续时间,并通过超高效液相色谱 (UPLC) 和偏光显微镜验证。 裸鼠胰腺导管腺癌 (PDAC) 异种移植方案: 1. 动物饲养:雌性裸鼠(6-8 周龄,18-22 克)饲养于 SPF 级动物房(22-25°C,12 小时光照/黑暗循环),自由摄食饮水 [3] 2. 肿瘤植入:将 PANC-1 细胞(5×10⁶ 个细胞/只小鼠)重悬于 100 μL PBS/Matrigel (1:1) 混合液中,皮下注射至小鼠右侧腹部 [3] 3. 分组和治疗:当肿瘤体积达到约 100 mm³(第 0 天)时,将小鼠随机分为 4 组:(1)对照组:腹腔注射溶剂(10 μL/g 体重)。 (1)体重);(2)维替泊芬:50 mg/kg(溶于溶剂),腹腔注射,每周两次;(3)吉西他滨:25 mg/kg,腹腔注射,每周一次;(4)联合用药:维替泊芬 + 吉西他滨(剂量/频率相同)。治疗持续 3 周 [3] 4. 监测和分析:每 3 天测量一次肿瘤体积(体积 = 长 × 宽² / 2)。小鼠经 CO₂ 吸入安乐死,切除肿瘤并称重。制备肿瘤裂解液用于蛋白质印迹分析(抗 LC3,裂解型 caspase-3)[3] |
| 毒性/毒理 (Toxicokinetics/TK) |
体外毒性:用 5 μM 维替泊芬处理人外周血单核细胞 (PBMC) 72 小时:细胞活力降低 <15%,表明其对正常细胞的毒性较低 [1]
- 体内毒性:用维替泊芬(50 mg/kg,腹腔注射,每周两次,持续 3 周)处理裸鼠: 1. 无明显体重减轻(<5% vs. 基线)或死亡; 2. 血清 ALT、AST、肌酐和 BUN 水平在正常范围内; 3. 肝脏、肾脏或脾脏未见病理损伤(组织学检查)[3] |
| 参考文献 |
|
| 其他信息 |
一种用于光化学疗法治疗湿性黄斑变性的苯并卟啉衍生物。一种具有光动力活性的合成光活化剂。全身给药后,维替泊芬会在眼部新生血管中积聚,并在氧气存在下受到非热红光刺激后,产生高活性短寿命单线态氧和其他活性氧自由基,导致新生血管内皮局部损伤和血管阻塞。
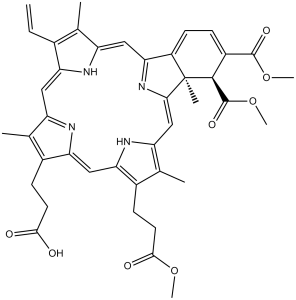
反式-(+-)-18-乙烯基-4,4a-二氢-3,4-双(甲氧羰基)-4a,8,14,19-四甲基-23H,25H-苯并[b]卟啉-9,13-二丙酸的9-甲基酯和13-甲基酯的等摩尔混合物。它被用作光动力疗法中的光敏剂,以消除与新生血管性(湿性)年龄相关性黄斑变性相关的眼部异常血管。维替泊芬在这些异常血管中积聚,并在氧气存在下被红光(693 nm)激光激活时,产生高活性短寿命的单线态氧和其他活性氧自由基,导致内皮局部损伤和血管阻塞。 细胞系已被用作药物发现的癌症模型;然而,它们并不能忠实地重现癌症,尤其是在微环境独立性方面。患者来源的异种移植(PDX)是通过将原发肿瘤细胞直接从患者移植到免疫缺陷小鼠体内而建立的,可以在所需时间提供所需数量的类似原发肿瘤细胞。我们开发了一种使用PDX细胞的高通量药物筛选系统,并使用费城染色体阳性急性淋巴细胞白血病(Ph+ ALL)的PDX细胞进行了药物筛选。我们构建了四只Ph+ ALL PDX小鼠模型,并利用这些PDX小鼠的白血病细胞对3440种化合物进行了高通量筛选(PDX细胞筛选)。PDX细胞筛选得到的药物谱与Ph+ ALL细胞系筛选得到的药物谱显著不同。我们发现,FDA批准的药物维替泊芬表现出强烈的PDX细胞特异性细胞毒性。在验证实验中,维替泊芬在三种PDX细胞中的GI50值分别为228 nM、395 nM和538 nM,在三种细胞系中的GI50值分别为3.93 µM、2.11 µM和5.61 µM。尽管维替泊芬是一种光敏剂,需光照激活,但其细胞毒性作用是通过光非依赖性活性氧的产生介导的;因此,即使没有光照,其抗白血病作用也能在体内发挥。此外,它与ABL激酶抑制剂达沙替尼表现出协同作用。这些结果表明维替泊芬具有作为新型抗白血病药物的潜力。[1] 紫杉醇(PTX)是最有效的抗癌药物之一。然而,多药耐药性仍然是阻碍PTX有效治疗癌症的主要因素。包括YAP过表达在内的多种因素可导致PTX耐药。本研究旨在验证YAP在PTX耐药中的作用,探索维替泊芬(VP)逆转PTX耐药性的方法,并研究PTX和VP联合治疗对PTX耐药结肠癌细胞(HCT-8/T)的影响。[2] 胰腺导管腺癌(PDAC)对化疗具有高度耐药性。有研究表明,PDAC的生长需要自噬水平的升高,因此抑制自噬被认为是一种治疗策略。迄今为止,所有研究自噬药理学抑制的临床前报告和临床试验均使用了氯喹或羟氯喹,这些药物会干扰溶酶体功能并在自噬后期阻断自噬。维替泊芬是一种新发现的自噬抑制剂,它通过抑制自噬体的形成在自噬早期阻断自噬。本文报道,体外实验表明,胰腺导管腺癌(PDAC)细胞系对维替泊芬的敏感性存在差异,提示细胞系对自噬的依赖性存在差异。通过图像分析和分子分析,我们发现维替泊芬能够抑制吉西他滨(目前PDAC的标准治疗药物)诱导的自噬。在BxPC-3异种移植小鼠模型中进行的药代动力学和疗效研究表明,维替泊芬在肿瘤中积累至足以抑制自噬的水平,并在体内抑制自噬,但作为单药治疗并未缩小肿瘤体积或延长生存期。与吉西他滨联合用药时,维替泊芬能够适度抑制肿瘤生长并延长生存期,优于吉西他滨单药治疗。虽然我们的结果并不支持自噬抑制作为单一疗法可广泛有效治疗胰腺导管腺癌(PDAC)的前提,但它们确实支持自噬抑制作为一种增强PDAC对吉西他滨敏感性的方法。[3] 维替泊芬传统上是光动力疗法(PDT)的光敏剂,但文献主要关注其光非依赖性生物活性:抗白血病、逆转耐药性和自噬抑制[1][2][3] - 作用机制:(1) 在Ph阳性急性淋巴细胞白血病(ALL)中:抑制BCR-ABL下游信号通路(p-STAT5、p-AKT)以诱导细胞凋亡,并与BMS-354825(Src抑制剂)协同作用[1];(2) 在YAP过表达细胞中:降低YAP蛋白表达以逆转NSC 125973耐药性[2]; (3)在胰腺导管腺癌中:抑制自噬(减少LC3-II)以增强吉西他滨的抗肿瘤作用[3] |
| 分子式 |
C41H42N4O8
|
|
|---|---|---|
| 分子量 |
718.79
|
|
| 精确质量 |
718.30
|
|
| 元素分析 |
C, 68.51; H, 5.89; N, 7.79; O, 17.81
|
|
| CAS号 |
129497-78-5
|
|
| 相关CAS号 |
|
|
| 外观&性状 |
Typically exists as Brown to black solid at room temperature
|
|
| LogP |
10.246
|
|
| tPSA |
337.48
|
|
| SMILES |
[C@]12(C)[C@@H](C(=O)OC)C(C(=O)OC)=CC=C1C1=CC3=NC(C(C=C)=C3C)=CC3NC(=C(C=3C)CCC(=O)O)C=C3C(CCC(=O)OC)=C(C)C(=N3)C=C2N1.[C@]12(C)[C@@H](C(=O)OC)C(=CC=C1C1NC2=CC2C(C)=C(CCC(=O)O)C(=CC3NC(=C(C)C=3CCC(=O)OC)C=C3C(C=C)=C(C)C(=N3)C=1)N=2)C(=O)OC |c:26,t:16,40,54,73,84,99,109,&1:0,2,53,55|
|
|
| InChi Key |
YTZALCGQUPRCGW-MXVXOLGGSA-N
|
|
| InChi Code |
InChI=1S/C41H42N4O8/c1-9-23-20(2)29-17-34-27-13-10-26(39(49)52-7)38(40(50)53-8)41(27,5)35(45-34)19-30-22(4)25(12-15-37(48)51-6)33(44-30)18-32-24(11-14-36(46)47)21(3)28(43-32)16-31(23)42-29/h9-10,13,16-19,38,42,44H,1,11-12,14-15H2,2-8H3,(H,46,47)/b28-16-,29-17-,30-19-,31-16-,32-18-,33-18-,34-17-,35-19-/t38-,41+/m0/s1
|
|
| 化学名 |
(1): 3-[(23S,24R)-14-ethenyl-5-(3-methoxy-3-oxopropyl)-22,23-bis(methoxycarbonyl)-4,10,15,24-tetramethyl-25,26,27,28-tetraazahexacyclo[16.6.1.13,6.18,11.113,16.019,24]octacosa-1,3,5,7,9,11(27),12,14,16,18(25),19,21-dodecaen-9-yl]propanoic acid.
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 5 mg/mL (6.96 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 50.0 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 5 mg/mL (6.96 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 50.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.3912 mL | 6.9561 mL | 13.9123 mL | |
| 5 mM | 0.2782 mL | 1.3912 mL | 2.7825 mL | |
| 10 mM | 0.1391 mL | 0.6956 mL | 1.3912 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT04590664 | Recruiting | Drug: Verteporfin | Glioblastoma Recurrent Glioblastoma |
Emory University | January 15, 2021 | Phase 1 Phase 2 |
| NCT03067051 | Recruiting | Drug: Verteporfin Device: SpectraCure P18 System |
Recurrent Prostate Cancer | SpectraCure AB | March 21, 2017 | Phase 1 Phase 2 |
| NCT00674323 | Completed Has Results | Drug: Verteporfin Photodynamic Therapy |
Polypoidal Choroidal Vasculopathy | Novartis | April 2008 | Phase 4 |
| NCT00433017 | Terminated Has Results | Drug: Verteporfin Photodynamic Therapy |
Macular Degeneration | Novartis | May 2007 | Phase 2 Phase 3 |
|
 |