| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
5-HT1A Receptor
Vilazodone has an IC50 of 0.5 nM for the SERT and 0.2 nM at the human 5-HT1A receptor. Vilazodone exhibits high affinity (pKi≥9.3) for human recombinant and native tissue 5-HT1A receptors from rats, mice, marmosets, and guinea pigs, and it preferentially binds to the high agonist affinity state of human 5-HT1A receptors. Vilazodone functions at 5-HT1A receptors as a partial agonist with high efficacy. A single concentration of Vilazodone (100nM) increases basal binding by approximately 70% of that produced by the full 5-HT1A receptor agonist, 8‐OH‐PIPAT, in [35S]GTPγS binding studies in Sf9 cells expressing h5-HT1A receptors. Vilazodone exhibits potent partial agonistic effects on the 5‐HT1A receptor, as demonstrated by [35S]GTPγS binding studies conducted in rat hippocampal membranes. Its intrinsic activity is 0.61 and its pEC50 is 8.1. Vilazodone has a potent inhibitory effect on 5‐HT reuptake in the cortex of rats and guinea pigs. Vilazodone has an 8.8 pIC50 to inhibit [3H]5-HT uptake in LLCPK cells that express human SERT[1]. |
|---|---|
| 体外研究 (In Vitro) |
Vilazodone 对人 5-HT1A 受体的 IC50 为 0.2 nM,对 SERT 的 IC50 为 0.5 nM。 Vilazodone 优先与人 5-HT1A 受体的高激动剂亲和力状态结合,并且对人重组体以及大鼠、豚鼠、小鼠和狨猴天然组织 5-HT1A 受体表现出高亲和力 (pKi≥9.3)。 Vilazodone 是 5-HT1A 受体的高效部分激动剂。在表达 h5-HT1A 受体的 Sf9 细胞中的 [35S]GTPγS 结合研究中,单一浓度的维拉佐酮 (100nM) 可使基础结合增加约 70%,而基础结合是完全 5-HT1A 受体激动剂 8-OH-PIPAT 产生的。在大鼠海马膜的 [35S]GTPγS 结合研究中,Vilazodone 是一种有效的 5-HT1A 受体部分激动剂,pEC50 为 8.1,内在活性为 0.61。 Vilazodone 在大鼠和豚鼠皮层中充当有效的 5-HT 再摄取抑制剂。在表达人 SERT 的 LLCPK 细胞中,维拉佐酮抑制 [3H]5-HT 摄取,pIC50 为 8.8[1]。
维拉佐酮在人和啮齿动物5-HT₁ₐ受体上表现为高效部分激动剂,对[³H]8-OH-DPAT的pKᵢ值 ≥ 9.3。 其对拮抗剂放射性配体[³H]WAY100635的亲和力低约2个对数单位,表明其优先结合于5-HT₁ₐ受体的高激动剂亲和状态。 在表达人5-HT₁ₐ受体的HEK细胞中进行[³⁵S]GTPγS结合实验,维拉佐酮表现为完全激动剂,pEC₅₀为9.0。 在大鼠海马膜中,维拉佐酮为强效部分激动剂,pEC₅₀为8.1,内在活性为0.61。 维拉佐酮抑制表达人SERT的LLCPK细胞对[³H]5-HT的摄取,pIC₅₀为8.8 ± 0.05。 [1] |
| 体内研究 (In Vivo) |
在体内微透析研究中,维拉佐酮(腹膜内注射;3 mg/kg;单剂量)可增加大鼠额叶皮层 (FC) 和腹侧海马 (vHipp) 的细胞外 5-HT 水平。在 3 mg/kg 时观察到最大增加,FC 和 vHipp 分别达到注射前基线值的 527% 和 558%[2]。维拉佐酮(口服强饲;55 mg/kg;单剂量)在给药后 120 和 210 分钟的大鼠超声发声测试中抑制应激诱导的发声[2]。
在大鼠前额叶皮层和腹侧海马中,维拉佐酮(3 mg/kg 腹腔注射)使细胞外5-HT水平分别升至基线的527%和558%。 与氟西汀不同,维拉佐酮引起的5-HT升高仅被8-OH-DPAT部分逆转。 维拉佐酮未引起大鼠5-HT综合征行为或降低体温,而8-OH-DPAT则引起这些效应。 在大鼠焦虑模型中,维拉佐酮在超声发声和电击探针掩埋测试中显示抗焦虑效果,但在高架十字迷宫中无效。 在强迫游泳试验中,维拉佐酮以1 mg/kg腹腔注射剂量减少大鼠和小鼠的不动时间。 [1] |
| 酶活实验 |
维拉唑酮的受体结合谱由Heinrich等人报道。维拉唑酮对人5‐HT1A受体的IC50为0.2 nM,对SERT的IC50为0.5 nM。在这些研究中,其最接近的交叉亲和性是多巴胺D3受体(IC50为71 nM),其次是5‐HT4受体(IC50为252 nM)。我们使用5‐HT1A受体激动剂[3H]8‐OH‐DPAT进行的内部放射性配体结合研究表明,维拉唑酮对人重组体和大鼠、豚鼠、小鼠和狨猴的天然组织5‐HT1A受体具有高亲和力(pKi≥9.3)(未发表的数据见表1)。相比之下,维拉唑酮取代了拮抗剂放射性配体[3H]WAY100635。(在Gpp(NH)p存在的情况下)与pKi值比使用[3H]8‐OH‐DPAT获得的值低2个log单位(表2)。这些数据表明,维拉唑酮优先结合人类5‐HT1A受体的高激动剂亲和力状态,表明该分子具有部分激动剂活性。据报道,用[3H]8‐OH‐DPAT和[3H]WAY100635测定的化合物对5‐HT1A受体的亲和力差异与其内在激动剂活性成正比。因此,考虑到对[3H]8‐OH‐DPAT cf. [3H]WAY100635测定的亲和力差异与内源性激动剂5‐HT观察到的相似,这些数据表明维拉唑酮将作为5‐HT1A受体的高效部分激动剂。这一假设在表达h5‐HT1A受体的Sf9细胞中得到了[35S] gtp - γ - s结合研究的支持,其中单一浓度的维拉唑酮(100nM)使基础结合增加了约70%的5‐HT1A受体激动剂8‐OH‐PIPAT产生的基础结合。然而,由于本研究仅使用单一浓度,因此无法准确测定h5‐HT1A受体的内在活性或功能效力。此后,对表达h5‐HT1A受体的HEK细胞进行了更广泛的研究(未发表的数据)。在这些研究中,维拉唑酮作为完全激动剂,与5‐HT相比,pEC50为9.0 [1]。
相比之下,5-HT1A/B/D受体部分激动剂SB-272183((5-氯- 2,3 -二氢-6-[4-甲基哌嗪-1-酰基]-1[4-吡啶-4-酰基]napth-1-ylaminocarbonyl]- 1h -吲哚),已被报道作为啮齿动物和人类天然组织5-HT1A受体的5-HT1A受体拮抗剂,在同一研究中显示出约0.3的内在活性(图2)。在[35S]大鼠海马膜GTPγS结合研究(5-HT1A受体占主导地位的功能性制剂)中,维拉唑酮作为一种有效的5-HT1A受体部分激动剂,其pEC50为8.1,内在活性为0.61。相比而言,(±)8-OH-DPAT (pEC50 7.2)产生的部分激动剂反应的内在活性为0.45,部分激动剂丁螺环酮的pEC50= 6.5±0.35,内在活性为0.19。综上所述,这些数据表明维拉唑酮在体内可能是一种高效的5-HT1A受体部分激动剂。重组和天然组织系统内在活性的明显差异可能是受体储备程度不同的结果。事实上,据报道,体内的天然组织体树突5-HT1A自受体存在受体储备[49],但体外的天然突触后5-HT1A受体不存在受体储备,这可以解释为什么维拉唑酮在海马中表现出部分激动剂特性。因此,一个可能的结论是,维拉唑酮是一种5-HT1A受体部分激动剂,在具有高受体储备和/或提高受体- g蛋白偶联效率的系统中具有作为完全激动剂的潜力。在一些体内模型中,维拉唑酮似乎对突触前5-HT1A受体比突触后5-HT1A受体具有更高的疗效,这一观察结果支持了这一概念,但可能与一些神经化学观察结果相矛盾。[1] 生化和电生理研究表明,维拉唑酮在大鼠和豚鼠皮层中是一种有效的5-羟色胺再摄取抑制剂。我们已经在表达人SERT的LLCPK细胞中证实了这种高效能,维拉唑酮抑制[3H]5-羟色胺摄取的pIC50值为8.8±0.05(图3)。该效价值比氟西汀高约1个对数单位,但与帕罗西汀相似(未发表的观察结果)。这些数据,加上维拉唑酮是一种有效的5-HT1A受体部分激动剂的观察结果,将这种分子置于一类新的化合物中,这种化合物有可能通过5-HT1A受体激动作用直接或间接通过SERT抑制内源性5-HT的升高而迅速脱敏5-HT1A自受体。[1] 使用激动剂放射性配体[³H]8-OH-DPAT和拮抗剂放射性配体[³H]WAY100635(在Gpp(NH)p存在下)进行受体结合实验,评估维拉佐酮对人重组及天然组织5-HT₁ₐ受体的亲和力。 在表达人5-HT₁ₐ受体的HEK细胞和大鼠海马膜中进行[³⁵S]GTPγS结合实验,以测定维拉佐酮的功能性激动剂活性和内在活性。 [1] |
| 细胞实验 |
在表达人重组SERT的LLCPK细胞中进行[³H]5-HT摄取抑制实验,评估维拉佐酮作为血清素再摄取抑制剂的效力。 [1]
|
| 动物实验 |
焦虑模型中的疗效[1]
三项独立研究评估了维拉唑酮在多种被认为可预测抗焦虑活性的啮齿动物模型中的疗效。在大鼠超声波发声测试中,维拉唑酮(55 mg/kg,口服)在给药后 120 分钟和 210 分钟抑制了应激诱导的发声。相比之下,8-OH-DPAT(0.55 mg/kg,皮下注射)产生了类似的活性,但持续时间较短,且该活性可被 WAY 100635 逆转。相反,选择性血清素再摄取抑制剂(SSRI)氟西汀(100 mg/kg,口服)除非与 8-OH-DPAT 联合使用,否则无效。这些数据共同表明,维拉唑酮在该模型中的疗效是通过其 5-HT1A 受体激动剂活性介导的。在另外两种大鼠焦虑模型中,即高架十字迷宫和电击探针埋藏实验中,维拉唑酮(10-40 mg/kg,腹腔注射)在电击探针实验中表现出剂量依赖性疗效,但有趣的是,在高架十字迷宫中却无效。阳性对照药物地西泮在两种实验范式中均有效。最后,研究人员在由家猫无保护暴露引起的捕食者诱导应激模型中检验了维拉唑酮的作用。捕食者应激增加了大鼠在高架十字迷宫中的焦虑样行为,并增强了其对声惊吓的反应。急性给药或预防性给药(行为测试前1周)的维拉唑酮(20-40 mg/kg,腹腔注射)可减轻应激诱导的惊吓反应增强,但对高架十字迷宫中应激诱导的焦虑反应没有影响。有趣的是,较低剂量(10 mg/kg)的维拉唑酮对惊吓反应产生了相反的效果,这表明存在某种尚未解释的双向效应。所有剂量均能增强惊吓诱发的应激反应,这可能提示存在类似焦虑的反应。最后,这些研究的数据还表明,维拉唑酮既无镇静作用也无兴奋作用,但确实产生了情境依赖性疗效。 抗抑郁活性模型中的疗效[1] 强迫游泳试验(FST)被广泛用于评估分子的抗抑郁活性,因为所有主要类别的抗抑郁药物,包括三环类抗抑郁药(TCA)、选择性5-羟色胺和去甲肾上腺素再摄取抑制剂(SNRI)、选择性5-羟色胺再摄取抑制剂(SSRI)、单胺氧化酶抑制剂和非典型抗抑郁药[70-74],在该应激模型中均有效。 Page等人证实,单次注射维拉唑酮(1 mg/kg,腹腔注射)即可在该模型的鼠类和大鼠模型中产生疗效(即减少不动时间),而更高剂量(3和10 mg/kg)则无效。该疗效的程度与氟西汀大致相当。该模型中的疗效通常被认为是由5-HT介导的,并可被受体拮抗剂和5-HT1A受体基因敲除阻断。因此,维拉唑酮的疗效可能是通过直接激动5-HT1A受体,也可能是通过提高内源性5-HT水平间接发挥作用。或许,这两种作用机制相结合的主要驱动力是加速5-HT1A受体的脱敏,从而加快治疗活性的起效。因此,对一些被认为能模拟此过程的模型(例如啮齿动物社交互动或定时诱导的多饮症)进行临床前疗效评估将很有帮助,但遗憾的是,迄今为止尚未有相关报道。 大鼠微透析研究:腹腔注射(3 mg/kg)或口服(1–10 mg/kg)维拉唑酮,以测量额叶皮层和腹侧海马的细胞外5-羟色胺水平。 行为学测试:腹腔注射(1–10 mg/kg)或口服(最高55 mg/kg)维拉唑酮,进行超声波发声、高架十字迷宫、电击探针埋藏、捕食者应激和强迫游泳测试。 体温测量:口服维拉唑酮(55 mg/kg)给大鼠,并记录体温。[1] |
| 药代性质 (ADME/PK) |
吸收、分布和排泄
维拉唑酮与食物同服时的生物利用度为72%。 1%的剂量以原形经尿液排出,2%的剂量以原形经粪便排出。 维拉唑酮的分布容积未知,但较大。 轻度至中度肾功能损害患者的维拉唑酮清除率为19.9-25.1升/小时,而健康对照组的清除率为26.4-26.9升/小时。 维拉唑酮的血药浓度在给药后4-5小时(Tmax)达到峰值,并以约25小时的末端半衰期下降。维拉唑酮与食物同服时的绝对生物利用度为72%。与食物(高脂或低脂餐)同服 VIIBRYD 可提高口服生物利用度(Cmax 增加约 147-160%,AUC 增加约 64-85%)。 维拉唑酮分布广泛,蛋白结合率约为 96-99%。 维拉唑酮可分泌至哺乳期大鼠的乳汁中。 代谢/代谢物 维拉唑酮主要通过细胞色素 P450 (CYP) 3A4 代谢,少量通过 CYP2C19 和 CYP2D6 代谢。尽管维拉唑酮的代谢途径尚未完全研究,但2017年发表了一项关于其在大鼠体内代谢机制的推测。 维拉唑酮主要通过CYP和非CYP途径(可能通过羧酸酯酶)代谢,仅有1%的剂量以原形维拉唑酮的形式从尿液中排出,2%的剂量从粪便中排出。在CYP途径中,CYP3A4是其代谢的主要途径,CYP2C19和CYP2D6的贡献较小。体外人微粒体和人肝细胞研究表明,维拉唑酮不太可能抑制或诱导其他CYP底物(CYP2C8除外)的代谢;体内使用CYP2C19、2D6和3A4探针底物进行的研究表明,维拉唑酮不改变这些探针底物的药代动力学。然而,一项使用 CYP2C19 探针底物的体内研究表明,CYP2C19 的诱导作用较弱。强效 CYP3A4 抑制剂(例如酮康唑)可降低维拉唑酮在体内的代谢,从而增加其暴露量。相反,强效 CYP3A4 诱导剂(例如卡马西平)可降低维拉唑酮的暴露量。 生物半衰期 25 小时。其他研究表明,单次服用 40mg 剂量后,维拉唑酮的半衰期为 24±5.2 小时;重复给药后,半衰期为 28.9±3.2 小时。维拉唑酮的终末半衰期约为 25 小时。维拉唑酮代谢为 6-羟基-5-氰基吲哚化合物,并以葡萄糖醛酸盐的形式排出体外。在一项使用 [¹¹C]WAY100635 的 PET 研究中,当血浆浓度 >50 ng/mL 时,维拉唑酮(40 mg)优先占据健康受试者的突触前 5-HT₁ₐ 受体。[1] |
| 毒性/毒理 (Toxicokinetics/TK) |
毒性总结
识别和用途:维拉唑酮是一种白色至类白色固体,制成薄膜包衣片剂。维拉唑酮是一种选择性5-羟色胺再摄取抑制剂和5-羟色胺1A型(5-HT1A)受体部分激动剂的复方制剂。它用于治疗成人重度抑郁症。人体暴露和毒性:临床试验中,200-280毫克维拉唑酮的毒性作用包括5-羟色胺综合征、嗜睡、躁动、幻觉和定向障碍。即使在治疗剂量下,也有报道称会出现5-羟色胺综合征这种可能危及生命的毒性反应。5-羟色胺综合征的症状可能包括精神状态改变(躁动、幻觉、谵妄和昏迷)、自主神经功能紊乱(心动过速、血压波动、头晕、多汗、潮红、体温过高)、神经肌肉症状(震颤、强直、肌阵挛、反射亢进、运动不协调)和癫痫发作。和/或胃肠道症状(恶心、呕吐、腹泻)。虽然在维拉唑酮单药治疗期间已有血清素综合征的报道,但当与其他血清素能药物以及影响血清素代谢的药物(特别是单胺氧化酶抑制剂 (MAOI))合用时,尤其需要关注。维拉唑酮与用于治疗精神疾病的 MAOI 合用是禁忌的。维拉唑酮也未获准用于儿童患者。对短期安慰剂对照抗抑郁药(选择性血清素再摄取抑制剂和其他药物)研究的汇总分析表明,这些药物会增加患有重度抑郁症和其他精神疾病的儿童、青少年和年轻成人的自杀意念和行为风险。此外,一些在出生后第三阶段接触过血清素能抗抑郁药(包括维拉唑酮)的新生儿也出现了类似的情况。妊娠中期出现并发症,需要长期住院、呼吸支持和管饲。此类并发症可能在分娩后立即出现。已报道的临床表现包括呼吸窘迫、紫绀、呼吸暂停、癫痫发作、体温不稳定、喂养困难、呕吐、低血糖、肌张力低下、肌张力亢进、反射亢进、震颤、烦躁不安、易怒和持续哭闹。在某些病例中,临床表现与血清素综合征一致。妊娠期暴露于维拉唑酮的婴儿也可能增加新生儿持续性肺动脉高压的风险,这是一种罕见的心肺疾病,与新生儿较高的发病率和死亡率相关。动物研究:维拉唑酮对大鼠有发育毒性,但对大鼠或兔无致畸性。在器官形成期以及整个妊娠和哺乳期,以相当于人类最大推荐剂量30倍的口服剂量给予妊娠大鼠维拉唑酮,可减少活产幼崽的数量。剂量有所降低。幼崽早期出生后死亡率增加,存活的幼崽体重下降,成熟延迟,成年后生育力下降。该剂量下存在一定的母体毒性。 药物相互作用 维拉唑酮与中效CYP3A4抑制剂(例如红霉素)合用可导致血浆维拉唑酮浓度升高。与中效CYP3A4抑制剂(例如红霉素)合用时,若患者出现无法耐受的不良反应,维拉唑酮的剂量应减至每日一次,每次20毫克。 维拉唑酮与强效CYP3A4抑制剂(例如克拉霉素、酮康唑)合用可使血浆维拉唑酮浓度升高约50%。生产商指出,若同时服用强效CYP3A4抑制剂,维拉唑酮的剂量应减至每日一次,每次20毫克。与强效CYP3A4抑制剂合用时,可能会出现潜在的严重不良反应,有时甚至致命。 正在接受或近期接受过单胺氧化酶(MAO)抑制剂治疗的患者,如果随后开始使用与维拉唑酮药理作用相似的抗抑郁药(例如,选择性5-羟色胺再摄取抑制剂,SSRIs),或在开始使用MAO抑制剂前不久接受过SSRI治疗的患者,可能会出现此类不良反应。MAO抑制剂与维拉唑酮合用是禁忌的。此外,停用MAO抑制剂后至少应间隔2周再开始使用维拉唑酮,反之亦然。 利奈唑胺是一种抗感染药物,也是一种可逆性MAO抑制剂,它与多种药物相互作用有关,可能导致5-羟色胺综合征,包括一些与SSRIs相关的相互作用。鉴于这种潜在风险,通常不应在接受维拉唑酮治疗的患者中使用利奈唑胺。美国食品药品监督管理局(FDA)迄今为止,美国食品药品监督管理局 (FDA) 尚未收到利奈唑胺和维拉唑酮合用引起血清素综合征的报告,其风险被认为与选择性血清素再摄取抑制剂 (SSRI) 相当。然而,FDA 指出,在某些危及生命或紧急情况下,正在服用血清素能药物的患者可能需要立即使用利奈唑胺治疗。在此类紧急情况下,应考虑是否有其他抗感染药物可用,并权衡利奈唑胺的获益与血清素综合征的风险。如果此类紧急情况下需要使用利奈唑胺,则必须立即停用维拉唑酮,并对患者进行为期 2 周或直至末次服用利奈唑胺后 24 小时(以先到者为准)的中枢神经系统毒性症状监测。末次服用利奈唑胺 24 小时后可恢复使用维拉唑酮。如果计划对正在服用维拉唑酮的患者在非紧急情况下使用利奈唑胺,则应在开始使用利奈唑胺前至少 2 周停用维拉唑酮。开始使用利奈唑胺。正在接受利奈唑胺治疗的患者不应开始使用维拉唑酮;如有必要,可在最后一次服用利奈唑胺 24 小时后开始使用维拉唑酮。 有关维拉唑酮的更多药物相互作用(完整)数据(共 13 项),请访问 HSDB 记录页面。 在临床试验中,维拉唑酮的耐受性总体良好。常见不良反应包括腹泻、恶心、嗜睡和头晕。[1] |
| 参考文献 |
|
| 其他信息 |
治疗用途
抗抑郁药 Viibryd适用于治疗重度抑郁症(MDD)。Viibryd的疗效已在两项为期8周的随机、双盲、安慰剂对照试验中得到证实,受试者为确诊为MDD的成年患者。重度抑郁症由一次或多次重度抑郁发作组成。重度抑郁发作(DSM-IV-TR)是指显著且相对持续(至少2周,几乎每天都出现)的抑郁或烦躁情绪,通常会干扰日常生活功能,并包含以下9种症状中的至少5种:情绪低落、对日常活动失去兴趣、体重和/或食欲显著变化、失眠或嗜睡、精神运动性激越或迟滞、疲劳感加剧、内疚感或无价值感、思维迟缓或注意力不集中,或自杀未遂或自杀意念。 /美国产品标签包含/ 探索治疗 性功能障碍在重度抑郁症 (MDD) 中很常见,许多血清素能抗抑郁药会对性功能产生不良影响。维拉唑酮是一种新型血清素 (5-HT) 再摄取抑制剂和 5-HT1A 部分激动剂,已获准用于治疗 MDD,其作用于 5-HT 转运体以及突触前和突触后 5-HT1A 受体。这种机制可能有助于减轻性功能障碍。目的:总结维拉唑酮(40 mg/天,随餐服用)对 MDD 成人患者性功能的影响。/数据来自/三项 III 期研究:两项为期 8 周的安慰剂对照研究和一项为期 52 周的开放标签研究。采用经验证的测量方法,分析从基线到治疗结束 (EOT) 的变化来评估性功能。纳入研究人群包括来自安慰剂对照研究的 869 例患者(维拉唑酮组 436 例,安慰剂组 433 例)和来自开放标签研究的 599 例患者。治疗前性功能障碍的发生率较高(男性 50%,女性 68%),维拉唑酮组和安慰剂组的性功能障碍发生率在治疗期间均有所下降,表明平均而言有所改善。在治疗结束时,安慰剂对照研究中 ≥ 91% 的患者性功能稳定或有所改善;治疗结束时,两组患者的性功能障碍差异在统计学上无显著性差异。与安慰剂组相比,性功能评分较基线的变化差异较小,且通常无统计学意义;效应量(Cohen's d)通常较低。在安慰剂对照研究中,8.0% 的维拉唑酮治疗患者和 0.9% 的安慰剂治疗患者报告了 ≥ 1 次与性功能相关的治疗期间出现的不良事件(P<0.001)。基线时,一半男性和三分之二女性重度抑郁症患者存在性功能障碍;维拉唑酮组和安慰剂组的性功能平均均有所改善。结果表明,相对于基线时重度抑郁症成人患者性功能障碍的高患病率,维拉唑酮可能对性功能产生较小的不良影响。 药物警告 /黑框警告/ 警告:自杀意念和行为。短期研究表明,抗抑郁药会增加儿童、青少年和年轻成人的自杀意念和行为风险。这些研究并未显示24岁以上患者使用抗抑郁药会增加自杀意念和行为的风险;65岁及以上患者使用抗抑郁药则可降低风险。对于所有年龄段开始接受抗抑郁药治疗的患者,应密切监测临床症状是否恶化以及是否出现自杀意念和行为。告知家属和照护者密切观察并与处方医生保持沟通的必要性。Viibryd 未获准用于儿童患者。 无论是否服用抗抑郁药,患有重度抑郁症或其他精神疾病的成人和儿童患者均可能出现抑郁症状加重和/或出现自杀意念和行为(自杀倾向)或行为异常改变。这种风险可能持续到临床症状显著缓解为止。自杀是抑郁症和其他某些精神疾病的已知风险,而这些疾病本身也是自杀的最强预测因素。然而,长期以来人们一直担心,抗抑郁药可能在某些患者的治疗早期阶段诱发抑郁症状加重和自杀倾向的出现。对短期安慰剂对照抗抑郁药研究的汇总分析(例如,选择性血清素再摄取抑制剂 (SSRI) 和其他抗抑郁药)显示,患有重度抑郁症和其他精神疾病的儿童、青少年和青年(18-24 岁)的自杀风险增加。在 24 岁以上的成年人中,与安慰剂相比,抗抑郁药并未显示出自杀风险增加,而在 65 岁及以上的成年人中,观察到自杀风险降低。美国食品药品监督管理局 (FDA) 建议,所有接受抗抑郁药治疗的患者,无论其适应症如何,都应接受适当的监测,并密切观察其临床症状是否恶化、是否存在自杀倾向以及行为异常变化,尤其是在治疗初期(即最初几个月)和剂量调整期间。对于接受抗抑郁药物治疗的重度抑郁症或其他精神或非精神疾病患者,其家属和照护者应被告知每日监测患者是否出现躁动、易怒或异常行为改变,以及自杀倾向,并应立即向医护人员报告此类症状。尽管尚未证实焦虑、躁动、惊恐发作、失眠、易怒、敌意、攻击性、冲动、静坐不能、轻躁狂和/或躁狂等症状与抑郁症加重和/或自杀冲动的出现之间存在因果关系,但人们担心这些症状可能是自杀倾向出现的先兆。因此,对于抑郁症状持续加重的患者,或出现突发性自杀倾向或可能预示抑郁症状或自杀倾向加重的症状的患者,应考虑改变治疗方案或停止治疗,尤其是在这些症状严重、突然发作或并非患者就诊时的主要症状时。如果决定停止治疗,应尽可能快速地减少维拉唑酮的剂量,但同时也应考虑突然停药的风险。 FDA 还建议,应在保证良好患者管理的前提下,尽可能使用最小剂量开具这些药物,以降低过量用药的风险。 据报道,单独使用抗抑郁药可能会引起危及生命的血清素综合征或神经阻滞剂恶性综合征 (NMS) 样反应,尤其是在同时使用其他血清素能药物(包括血清素(5-羟色胺;5-HT)1 型受体激动剂(曲坦类药物))、损害血清素代谢的药物(例如,单胺氧化酶抑制剂)或抗精神病药物或其他多巴胺拮抗剂时。血清素综合征的临床表现可能包括精神状态改变(例如,躁动、幻觉、昏迷)、自主神经功能紊乱(例如,心动过速、血压波动、高热)、神经肌肉异常(例如,反射亢进、运动不协调)和/或胃肠道症状(例如,恶心、呕吐、腹泻)。在最严重的情况下,血清素综合征可能类似于神经阻滞剂恶性综合征(NMS),其特征是高热、肌肉强直、自主神经功能紊乱(可能伴有生命体征的快速波动)以及精神状态改变。服用维拉唑酮的患者应监测血清素综合征或NMS样体征和症状的发生。禁止同时或近期(即2周内)使用单胺氧化酶抑制剂(MAO抑制剂)治疗抑郁症。如果临床上确有必要同时使用维拉唑酮和5-HT1受体激动剂(曲坦类药物),则应密切观察患者,尤其是在治疗初期、剂量增加时或开始使用其他血清素能药物时。不建议同时使用维拉唑酮和血清素前体(例如色氨酸)。如果出现血清素综合征或神经阻滞剂恶性综合征(NMS)的体征和症状,应立即停止使用维拉唑酮以及任何同时使用的血清素能或抗多巴胺能药物(包括抗精神病药物),并开始支持和对症治疗。 孕期暴露于选择性血清素再摄取抑制剂(SSRIs)的婴儿可能增加新生儿持续性肺动脉高压(PPHN)的风险。持续性肺动脉高压 (PPHN) 在普通人群中的发生率为每 1000 例活产婴儿中有 1-2 例,并与新生儿发病率和死亡率显著相关。近期几项流行病学研究表明,孕期使用选择性血清素再摄取抑制剂 (SSRI)(包括维布利德)与 PPHN 之间存在统计学上的正相关性。其他研究则未发现显著的统计学相关性。 有关维拉唑酮(共 16 条)的更多药物警告(完整)数据,请访问 HSDB 记录页面。 药效学 维拉唑酮通过抑制血清素的再摄取,同时作为血清素-1A 受体的部分激动剂,提高大脑中的血清素水平。由于这种活性,维拉唑酮有时被称为选择性部分激动剂和再摄取抑制剂 (SPARI)。 维拉唑酮是一种结合了5-羟色胺再摄取抑制剂和5-HT₁ₐ受体部分激动剂的药物,旨在通过使胞体树突5-HT₁ₐ自身受体脱敏来加速抗抑郁药的起效。 它已进入治疗重度抑郁症的III期临床试验,并在蒙哥马利-奥斯伯格抑郁评定量表(MADRS)上显示出显著优于安慰剂的疗效。 该药物最初由默克集团(Merck KGaA)研发,后授权给葛兰素史克(GSK)和Clinical Data公司。[1] |
| 分子式 |
C₂₆H₂₇N₅O₂
|
|---|---|
| 分子量 |
441.52
|
| 精确质量 |
441.22
|
| CAS号 |
163521-12-8
|
| 相关CAS号 |
Vilazodone Hydrochloride; 163521-08-2; Vilazodone-d8; 1794789-93-7; Vilazodone carboxylic acid; 163521-19-5
|
| PubChem CID |
6918314
|
| 外观&性状 |
White to light yellow solid powder
|
| 密度 |
1.34 g/cm3
|
| 沸点 |
745.1ºC at 760 mmHg
|
| 熔点 |
203-205ºC
|
| LogP |
5.534
|
| tPSA |
102.29
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
5
|
| 可旋转键数目(RBC) |
7
|
| 重原子数目 |
33
|
| 分子复杂度/Complexity |
729
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
SGEGOXDYSFKCPT-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C26H27N5O2/c27-16-18-4-6-23-22(13-18)19(17-29-23)3-1-2-8-30-9-11-31(12-10-30)21-5-7-24-20(14-21)15-25(33-24)26(28)32/h4-7,13-15,17,29H,1-3,8-12H2,(H2,28,32)
|
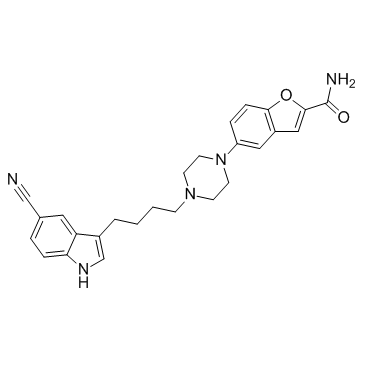
| 化学名 |
5-[4-[4-(5-cyano-1H-indol-3-yl)butyl]piperazin-1-yl]-1-benzofuran-2-carboxamide
|
| 别名 |
EMD 68843; SB659746A; 5-(4-(4-(5-Cyano-1H-indol-3-yl)butyl)piperazin-1-yl)benzofuran-2-carboxamide; Viibryd; EMD 515259; vilazodona; vilazodonum; UNII-S239O2OOV3; Vilazodone; EMD68843; EMD-68843
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO: 75~88 mg/mL (199.3~169.9 mM)
Ethanol: ~14 mg/mL |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (5.66 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (5.66 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL 澄清 DMSO 储备液加入到 900 μL 玉米油中并混合均匀。 请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.2649 mL | 11.3245 mL | 22.6490 mL | |
| 5 mM | 0.4530 mL | 2.2649 mL | 4.5298 mL | |
| 10 mM | 0.2265 mL | 1.1325 mL | 2.2649 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT05948579 | Not yet recruiting | Drug: Intervention B Vilazodone Hydrochloride (HCl) Drug: Intervention B Placebo |
Post Traumatic Stress Disorder | U.S. Army Medical Research and Development Command |
August 2023 | Phase 2 |
| NCT05422612 | Recruiting | Drug: Intervention A Placebo Drug: Intervention B Placebo |
Post Traumatic Stress Disorder | U.S. Army Medical Research and Development Command |
November 2, 2023 | Phase 2 |
| NCT02015546 | Completed | Drug: Vilazodone | Major Depressive Disorder (MDD) |
Duke University | December 2012 | Phase 3 |
| NCT02436239 | Completed | Drug: Vilazodone | Major Depressive Disorder | Forest Laboratories | May 2, 2015 | Phase 3 |
| NCT01828515 | Completed | Drug: Vilazodone Drug: Placebo |
Memory Impairment | University of Texas Southwestern Medical Center |
December 2012 | Phase 2 |