| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 1mg |
|
||
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| Other Sizes |
|
| 靶点 |
Sphingosine 1-phosphate (S1P) receptors; S1P1 (pKi = 7.86); S1P3 (pKi = 5.93); S1P1 (pEC50 = 6.58); S1P3 (pEC50 = 7.07)
VPC23019 is a dual antagonist of sphingosine-1-phosphate receptor 1 (S1PR1) and sphingosine-1-phosphate receptor 3 (S1PR3) . The reported pKi values are 7.86 for S1P1 (approximately 13.8 nM) and 5.93 for S1P3 (approximately 1.17 μM), indicating approximately 100-fold selectivity for S1P1 over S1P3 . It acts as a competitive antagonist in both broken cell and whole cell assays . The compound does not significantly affect S1P2 or S1P5 at similar concentrations; one study reported an EC50 of 7.28 for S1P5, but VPC23019 is not primarily characterized as an S1P5 antagonist . |
|---|---|
| 体外研究 (In Vitro) |
VPC23019对S1P1和S1P3受体缺乏激动作用。
VPC23019阻断S1P1和S1P3受体的激动剂活性
该系列的先导化合物VPC23019在破细胞和全细胞实验中被发现对S1P(1)和S1P(3)受体具有竞争性拮抗剂的作用。该系列的构效关系较陡;例如,先导化合物的轻微修饰导致VPC25239,其在S1P(3)受体上的效力提高了一个对数数量级。这些新的化学实体将有助于进一步了解S1P信号,并为进一步开发S1P受体拮抗剂提供线索。[1]
VPC23019在多种细胞类型和实验模型中展现出多样化的体外活性。在人微血管内皮细胞中,使用VPC23019处理可阻断砷刺激的血管生成基因表达和管形成,表明其在抑制S1P1介导的血管生成中发挥作用。在神经干细胞中,VPC23019抑制了S1P诱导的迁移。在甲状腺癌细胞和卵巢癌细胞中,VPC23019同样阻断了S1P诱导的细胞迁移。在人肺动脉平滑肌细胞中,VPC23019(连同其他S1PR3抑制剂如TY52156)减少了TGF-β1诱导的α-平滑肌肌动蛋白上调,提示其在调节收缩基因表达中的作用。在浆细胞分化研究中,鞘氨醇磷酸胆碱对浆细胞分化的抑制作用可被VPC23019特异性阻断,该效应归因于对S1PR3而非S1PR1或S1PR2的拮抗。在小鼠胚胎成纤维细胞和其他细胞系统中,VPC23019抑制了S1P诱导的钙流和下游信号通路,包括RhoA/ROCK的激活。 |
| 体内研究 (In Vivo) |
VPC23019已在多个体内模型中得到评估。在阿尔茨海默病小鼠模型(双转基因APP/PS1小鼠)中,注射VPC23019(联合骨髓间充质干细胞来源的外泌体)用于阻断S1P1信号,该化合物减少了Aβ沉积并改善了认知功能恢复。在一项肥胖研究中,对ob/ob小鼠口服给予VPC23019并未引起体重增长、脂肪细胞大小或葡萄糖耐受性的显著变化;然而,VPC23019与S1P1激动剂SEW-2871联合给药消除了SEW-2871的有益效应,证实VPC23019在体内有效拮抗S1P1。在佩吉特病小鼠模型中,加入VPC23019阻断了破骨细胞条件培养基诱导的成骨细胞分化增强,表明S1PR3在骨形成中发挥作用。在一项使用器官型内嗅-海马切片培养研究去神经诱导的树突萎缩的实验(离体模型)中,使用VPC23019(1 μM)处理可防止去神经诱导的树突丢失并维持树突稳定性。在大鼠缺血性卒中模型中,VPC23019被用作S1P1拮抗剂,以证实非促有丝分裂FGF1部分通过S1P1通路促进血管生成。在一项糖尿病肾病研究中,载脂蛋白M的保护作用可被VPC23019处理部分抑制,但不受S1P2拮抗剂的影响,证实了S1P1/S1P3参与该保护效应。
|
| 酶活实验 |
VPC23019在S1P1和S1P3受体上的结合常数的测定[1]
VPC23019在S1P1和S1P3受体上的结合常数(Kb)由Schild分析确定,该曲线采用Lew和Angus讨论的非线性回归方法拟合。简单地说,在没有和存在不同浓度拮抗剂的情况下,通过绘制从激动剂剂量-反应曲线获得的EC50值的负对数所产生的最佳拟合线的非线性分析,与拮抗剂的浓度作对比,得出Kb值。还进行了f检验分析,以确定拮抗剂是否符合简单竞争性相互作用的标准。[1] S1P放射性标记[1]< br > [32P]S1P是用瞬时转染人鞘氨醇激酶2型DNA的HEK293T细胞裂解液培养鞘氨醇和[γ-32P]ATP制备的。0.2 ml的反应中含有0.025 mm鞘氨醇、1 mCi的[γ-32P]ATP (7000 Ci/mmol)和激酶缓冲液(10 mm Mg(C2H3O2)2 in 50 mm Tris、pH 7.5、10 mm NaF和2 mm半脲)。反应开始时,加入0.02 mg细胞裂解液蛋白,在37℃下孵育至少30分钟。[32P]S1P通过在反应混合物中分别加入1 n HCl和2.0 m KCl、甲醇和氯仿提取。然后将混合物在1000 × g下旋转离心5-10 min。分离有机层,并对剩余的水馏分重复提取2次。结合的有机馏分在氮气流下干燥,并在0.1%无脂肪酸的牛血清白蛋白水溶液中重悬浮。产物[32P]S1P的比活度估计为放射性标记的底物[γ-32P]ATP的比活度,即7000 Ci/mmol。[1] [32P]S1P结合试验[1] 从瞬时转染受体和g蛋白dna的HEK293T细胞中提取含有0.005 mg蛋白质的膜,在0.5 ml结合缓冲液(50 mm HEPES, 100 mm NaCl, 10 mm MgCl2, pH 7.5), 50 pm [32P]S1P和指示脂质(s)中室温孵育1小时。结合配体通过快速过滤从游离配体中分离出来,并在液体闪烁计数器中进行分析。非特异性结合是指在过量S1P存在的情况下,辐射配体与瞬时转染受体和g蛋白dna的HEK293T细胞的膜(热变性和非热变性)的残余结合;它通常占总结合量的60%。利用Chang-Prusoff方程(Ki = IC50/(1 + [L]/Kd)确定与配体-受体相互作用相关的结合常数(Ki)。在应用该方程时,放射性配体(L)的浓度为0.05 nm,使用的Kd值为报道的S1P-S1P1受体相互作用的Kd值,即8.1 nm。[1] |
| 细胞实验 |
细胞迁移试验[1]
细胞迁移实验使用改良的Boyden室(组织培养,直径24 mm,厚度0.010 mm,孔隙0.008 mm, Transwell®)进行,其中含有聚碳酸酯膜,底部涂有0.1%明胶。用迁移液(Dulbecco's modified Eagle's medium/F-12不含酚红和0.1%无脂肪酸BSA)冲洗聚碳酸酯膜的底部一次,然后浸入含有2ml迁移液的下腔中。稳定转染人S1P1受体DNA的T24细胞在Dulbecco改良Eagle培养基/F-12培养基中生长,其中含有炭/葡聚糖-剥离FBS和0.010 mg/ml嘌霉素,在150 × 25 mm组织培养板中100%融合,血清饥饿至少12小时。血清饥饿细胞从10×胰蛋白酶- edta培养皿中取出,用迁移液洗涤一次,重悬于迁移液中(106个细胞/ml)。在上移室中加入1毫升细胞悬液,在下移室中加入S1P激动剂VPC22277 (10 nm)。在37℃下,细胞在有或没有拮抗剂(VPC23019 (0-1000 nm), VPC23019, VPC23031, VPC23089和VPC25239(各50 nm))的情况下向膜下迁移4小时,并将其添加到下腔中。将附着在膜底表面的迁移细胞用10倍胰酶- edta除去,通过将0.1 ml细胞悬液与等体积的CyQuant染料溶液(3.0 ml 2倍裂解缓冲液和0.015 ml CyQuant染料)结合来测定其质量,并使用FlexStation™荧光仪(Molecular Devices, Menlo Park, CA)对所得荧光进行定量。每个测定值代表两个单独迁移室的平均值。为了确定与VPC23019相关的拮抗作用的可逆转性,将细胞与0.01 mm VPC23019在37°C下孵育30分钟。单层用磷酸盐缓冲盐水洗涤三次,并立即处理进行细胞迁移实验,如上所述。 细胞内钙动员[1] 测定 使用FlexStation™荧光仪测量天然T24细胞和稳定转染人S1P2或人S1P3受体DNA的T24细胞的细胞内钙。细胞在96孔透明底黑色微孔板中接种(~ 50,000个细胞/孔),在37°C下放置过夜。细胞用0.004 mm Fluo-4AM酯在上样缓冲液(Hanks平衡盐溶液,pH 6.4,含20 mm HEPES, 0.1%无脂肪酸BSA, 2.5 mm丙烯酸)中染色,37°C下30分钟。用磷酸盐缓冲盐水洗涤细胞单层三次后,加入上样缓冲液,细胞在FlexStation™中于25°C下暴露于化合物组中3分钟。在所有情况下,每种化合物的每种浓度都至少进行了三次测试。为了测定VPC23019 (0.010 mm)相关拮抗作用的可逆性,将该化合物与负载染料一起添加到细胞中,并在37℃下孵育30分钟。如上所述,用磷酸盐缓冲盐水洗涤细胞并立即暴露于化合物中。 |
| 动物实验 |
VPC23019在动物研究中通过多种途径给药。在ob/ob小鼠研究(肥胖模型)中,VPC23019通过口服给药以评估其对体重、脂肪细胞大小和葡萄糖耐受性的影响。摘要中未详细说明给药方案和具体浓度,但该化合物单独或与S1P1激动剂SEW-2871联合给药。在双转基因APP/PS1阿尔茨海默病小鼠模型中,VPC23019与骨髓间充质干细胞来源的外泌体联合注射(途径未具体说明)。在器官型切片培养研究(离体)中,VPC23019以1 μM的浓度加入到孵育培养基中。含药物的培养基每周更换三次,培养维持长达6周。在经VPC23019处理的未去神经培养物中未观察到毒性证据(起泡、树突萎缩/回缩)。
|
| 毒性/毒理 (Toxicokinetics/TK) |
在器官型内嗅-海马切片培养物中,VPC23019(1 μM)处理在未去神经的培养物中未显示出任何毒性证据,包括起泡、树突萎缩或回缩。对照细胞保持稳定,在此条件下没有成像细胞丢失。在所提供搜索结果中未报道VPC23019的其他系统毒性数据(如LD50、肝肾毒性或蛋白结合)。该化合物仅用于研究目的,未被批准用于人体或兽医用途。
|
| 参考文献 | |
| 其他信息 |
VPC23019是一种开创性的药理工具化合物,为S1P受体拮抗剂的构效关系研究奠定了基础。它的开发使研究人员能够剖析S1P1、S1P3和S1P2在各种生物学过程中的不同作用。该化合物已被广泛引用于血管生成、神经保护、炎症、纤维化、癌细胞迁移和代谢紊乱等研究。它通常与选择性激动剂(如针对S1P1的SEW-2871)或选择性拮抗剂(如针对S1P2的JTE-013、仅针对S1P1的W146)联合使用,以解析受体特异性效应。虽然VPC23019是S1P1/S1P3双重拮抗剂,但其对S1P1的选择性约为S1P3的100倍,因此可以在较低浓度下优先阻断S1P1。在较高浓度下,它也阻断S1P3,这对于研究两种受体都参与的情况非常有用。该化合物可从多个商业供应商处获得,通常以粉末形式在-20°C避光保存。
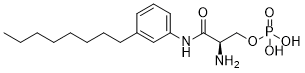
VPC 23019 是一种仲酰胺,由 O-磷酸-D-丝氨酸的羧基与间辛苯胺的氨基缩合而成。它是鞘氨醇-1-磷酸 (S1P) 的类似物,是 S1P1 和 S1P3 受体的强效拮抗剂。它能抑制 S1P 诱导的甲状腺癌细胞、卵巢癌细胞和神经干细胞的迁移。它既是鞘氨醇-1-磷酸受体 3 的拮抗剂,也是鞘氨醇-1-磷酸受体 1 的拮抗剂。它是一种 D-丝氨酸衍生物、仲酰胺、有机磷酸酯、磷酸酯和芳香酰胺。它在功能上与O-磷酸-D-丝氨酸相关。 鞘氨醇-1-磷酸(S1P)是一种溶血磷脂介质,可通过一系列细胞表面受体诱导多种细胞和组织反应。以免疫调节前药FTY720为代表的S1P受体激动剂的最新研究进展表明,S1P信号通路是淋巴细胞迁移的重要调节因子。为了理解S1P配体的构效关系并开发用于探索S1P生物学的工具化合物,我们合成并测试了多种S1P类似物。本文报道,我们合成的部分含芳基酰胺的化合物是S1P(1)和S1P(3)受体的拮抗剂。该系列先导化合物VPC23019在破碎细胞和全细胞实验中均表现出对S1P(1)和S1P(3)受体的竞争性拮抗作用。该系列化合物的构效关系非常显著;例如,对先导化合物进行微小修饰后得到的 VPC25239,其对 S1P(3) 受体的效力提高了一个数量级。这些新的化学实体将有助于进一步了解 S1P 信号传导,并为进一步开发 S1P 受体拮抗剂提供线索。[1] |
| 分子式 |
C17H29N2O5P
|
|---|---|
| 分子量 |
372.396325826645
|
| 精确质量 |
372.181
|
| 元素分析 |
C, 54.83; H, 7.85; N, 7.52; O, 21.48; P, 8.32
|
| CAS号 |
449173-19-7
|
| PubChem CID |
11588811
|
| 外观&性状 |
Light yellow to yellow solid powder
|
| LogP |
4.314
|
| tPSA |
135.18
|
| 氢键供体(HBD)数目 |
4
|
| 氢键受体(HBA)数目 |
6
|
| 可旋转键数目(RBC) |
12
|
| 重原子数目 |
25
|
| 分子复杂度/Complexity |
429
|
| 定义原子立体中心数目 |
1
|
| SMILES |
CCCCCCCCC1=CC(=CC=C1)NC(=O)[C@@H](COP(=O)(O)O)N
|
| InChi Key |
MRUSUGVVWGNKFE-MRXNPFEDSA-N
|
| InChi Code |
InChI=1S/C17H29N2O5P/c1-2-3-4-5-6-7-9-14-10-8-11-15(12-14)19-17(20)16(18)13-24-25(21,22)23/h8,10-12,16H,2-7,9,13,18H2,1H3,(H,19,20)(H2,21,22,23)/t16-/m1/s1
|
| 化学名 |
[(2R)-2-amino-3-(3-octylanilino)-3-oxopropyl] dihydrogen phosphate
|
| 别名 |
449173-19-7; VPC 23019; VPC23019; VPC-23019; (R)-2-Amino-3-((3-octylphenyl)amino)-3-oxopropyl dihydrogen phosphate; CHEMBL228102; N-(3-octylphenyl)-O-phosphono-D-serinamide; CHEBI:144948;
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~125 mg/mL (~335.66 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 2.08 mg/mL (5.59 mM) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 悬浮液;超声助溶。
例如,若需制备1 mL的工作液,可将100 μL 20.8 mg/mL澄清DMSO储备液加入400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.08 mg/mL (5.59 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 20.8 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.08 mg/mL (5.59 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.6853 mL | 13.4264 mL | 26.8528 mL | |
| 5 mM | 0.5371 mL | 2.6853 mL | 5.3706 mL | |
| 10 mM | 0.2685 mL | 1.3426 mL | 2.6853 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。