| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| Other Sizes |
|
| 靶点 |
D4 Receptor; sPLA2 ( pIC50 = 8.87 ); sPLA2 ( pA2 = 9.71 )
WAY-100635 Maleate is a highly selective antagonist of the 5-hydroxytryptamine 1A (5-HT₁A) receptor. In human recombinant 5-HT₁A receptors (expressed in CHO cells), it exhibits a Ki value of 0.9 nM; in rat hippocampal membrane preparations, the Ki for 5-HT₁A receptors is 1.2 nM [1] - WAY-100635 Maleate has negligible affinity for other 5-HT receptor subtypes, including 5-HT₁B (Ki > 1000 nM), 5-HT₂A (Ki > 5000 nM), and 5-HT₇ (Ki > 10,000 nM) receptors in human brain membranes [4] - WAY-100635 Maleate shows no significant binding to dopamine D₂ (Ki > 5000 nM) or α₁-adrenergic receptors (Ki > 10,000 nM) in rat striatal membranes [5] |
|---|---|
| 体外研究 (In Vitro) |
在注入 WAY 100635 (10 nM) 的中缝背核 (DRN) 切片中,大多数推定的 5-HT 神经元的放电率增加(基线率的 13%)。此外,WAY 100635 完全防止 5-HT (3-15 μM)、8-OH-DPAT (10 nM)、5-羧酰胺色胺 (20 nM) 和来苏必通 (100 nM) 产生的放电速率降低。通过将 5-HT 浓度增加至 300 μM,可以完全克服 WAY 100635 所产生的拮抗作用,IC50 为 0.95 nM。在海马切片中,WAY 100635 (0.5 nM -10 nM) 不会改变细胞内记录的 CA1 锥体细胞的静息膜电位或膜输入电阻。然而,WAY 100635 不仅可以完全防止超极化(IC50 为 1.3 nM),而且可以降低 5-HT 和 5-羧酰胺色胺产生的膜输入电阻,IC50 分别为 22.5 μM 和 50 nM。 WAY 100635 的 IC50 为 1.35 nM,相对于一系列其他 CNS 受体,对 5-HT1A 位点的选择性高 > 100 倍。 [3H]WAY 100635 特异性结合的 Bmax 始终比激动剂放射性配体 [3H]8-OH-DPAT 高 50-60%。 Mn2+(而非鸟嘌呤核苷酸)抑制 [3H]WAY 100635 特异性结合。 WAY 100635没有5-HT1A受体激动剂作用,但剂量依赖性地阻断激动剂对海马CA1区突触后5-HT1A受体和位于中缝背侧5-HT的体树突5-HT1A受体的激动剂作用神经元。 [3H]WAY 100635 的 Kd 约为 2.5 nM。在离体豚鼠回肠中,WAY 100635 是一种有效且高浓度的 5-羧酰胺色胺 5-HT1A 受体激动剂拮抗剂,其表观 pA2 值(0.3 nM)为 9.71。细胞测定:使用填充有 2 M NaC1 (12 MΩ-15 MΩ) 的玻璃微电极进行细胞外记录。根据以下标准将细胞鉴定为 5-HT 神经元:持续时间为 2 毫秒至 3 毫秒的双相动作电位、缓慢(0.5 Hz - 2.0 Hz)和规则的放电模式。通过将 α-1 肾上腺素能激动剂去氧肾上腺素 (3 μM) 添加到超融合 ACSF 中,在原本沉默的神经元中引发放电。在使用不同药物之前至少记录 10 分钟的基线活动。电信号被馈送到高输入阻抗放大器、示波器和电子速率计,这些电子速率计由连接到 A/D 转换器和个人计算机的各个动作电位触发。使用专用软件,可以记录、计算积分发射率并将其作为连续 10 秒样本显示在图表记录仪上。通过比较 WAY 100635 应用前 2 分钟内记录的平均放电频率与 WAY 100635 作用峰值时(通常是开始应用后 2-5 分钟)记录的平均放电频率来评估激动剂的效果。当在拮抗剂存在的情况下应用激动剂时,将激动剂的效果与基线放电速率以及单独灌注拮抗剂期间记录的频率进行比较。在重新测试激动剂的作用之前,让拮抗剂平衡 10 分钟至 25 分钟。
5-HT₁A受体拮抗作用(cAMP实验):在稳定表达人5-HT₁A受体的CHO细胞中,WAY-100635 Maleate(10⁻¹⁰-10⁻⁶ M)可浓度依赖性拮抗5-HT(10⁻⁷ M)对毛喉素刺激的cAMP生成的抑制作用:10⁻⁸ M可逆转50%的5-HT效应(IC₅₀=1.1 nM),10⁻⁶ M时实现完全逆转[1] - 大鼠海马膜结合实验:在大鼠海马膜制备物中,WAY-100635 Maleate(10⁻¹¹-10⁻⁶ M)可剂量依赖性取代[³H]-8-OH-DPAT(选择性5-HT₁A激动剂)的结合:10⁻⁹ M使特异性结合减少40%,10⁻⁶ M时取代率达98%(IC₅₀=1.3 nM)[4] - 海马神经元电生理实验:在原代培养的大鼠海马锥体细胞中,WAY-100635 Maleate(10 nM、100 nM)可阻断5-HT(1 μM)诱导的超极化(膜片钳技术检测):100 nM完全逆转5-HT介导的放电频率降低,证实其功能性5-HT₁A拮抗作用[3] - 细胞活力实验:在人神经母细胞瘤SH-SY5Y细胞中,WAY-100635 Maleate(1-100 μM)暴露24 h后对细胞活力无显著影响(MTT法);所有测试浓度下,活力均保持在溶媒对照组的95%以上[6] |
| 体内研究 (In Vivo) |
小鼠静脉注射后,[3H]WAY 100635 可选择性结合大脑 5-HT1A 受体。 WAY 100635 还以剂量依赖性方式阻断 8-OH-DPAT 抑制中缝背侧 5-HT 神经元放电的能力,并诱导 5-HT 综合征、体温过低、食欲过盛以及升高血浆 ACTH 水平。在小鼠明/暗盒焦虑模型中,WAY 100635 诱导类似抗焦虑的作用。 WAY 100635 对大鼠短期记忆延迟匹配位置模型中的认知没有内在影响,但逆转了 8-OH-DPAT 对运动动机表现的破坏性影响。 WAY 100635 以本身无抑制作用的剂量阻断 8-OH-DPAT 对麻醉大鼠中缝背神经元放电的抑制作用。在行为模型中,WAY 100635 本身不会引起明显的行为变化,但可有效拮抗 8-OH-DPAT 在大鼠和豚鼠中引起的行为综合征(最小有效剂量 = 0.003 mg/kg sc,ID50 = 0.01 mg/kg sc) , 分别)。 WAY 100635 还可阻断 8-OH-DPAT 在小鼠和大鼠中引起的体温过低,皮下注射的 ID50 值为 0.01 mg/kg
大鼠强迫游泳实验(FST):在雄性Sprague-Dawley大鼠中,腹腔注射WAY-100635 Maleate(0.1、0.3、1 mg/kg)30 min后进行FST,可剂量依赖性逆转8-OH-DPAT(5-HT₁A激动剂)的抗抑郁样作用:1 mg/kg使不动时间从8-OH-DPAT单独组的45 s增至120 s,恢复至溶媒组水平[2] - 小鼠高架十字迷宫(EPM)实验:在雄性ICR小鼠中,口服WAY-100635 Maleate(0.3、1、3 mg/kg)60 min后进行EPM测试,可拮抗5-HT(1 mg/kg,腹腔注射)诱导的抗焦虑样行为:3 mg/kg使开放臂停留时间从5-HT单独组的45%降至22%(溶媒组水平),开放臂进入次数减少50%[6] - 大鼠中缝背核(DRN)活性实验:在麻醉的雄性Wistar大鼠中,静脉注射WAY-100635 Maleate(0.01、0.03 mg/kg)可增加DRN 5-HT神经元的放电频率:0.03 mg/kg使放电频率较基线增加80%,逆转8-OH-DPAT的抑制效应[5] |
| 酶活实验 |
Sceening assay[6]
对于NIMH-PDSP在大量克隆受体和转运蛋白上的初步筛选(详见Roth等人(2002)和Shapiro等人(2003)),使用了10μM WAY-100635。在测量到显著抑制的情况下(四次测定的抑制率>50%),用6-10个浓度的未标记配体进行K i测定,并用GraphPad Prism分析数据。 饱和结合实验[6] 通过刮取培养基中的细胞,然后在1000×g下离心10分钟并吸出培养基来收集全细胞颗粒。然后将颗粒重新悬浮在冰冷的标准结合缓冲液(SBB:50 mM Tris-HCl,pH 7.4,10 mM MgCl2和0.1 mM EDTA)中,等分,在4°C下以14000×g离心20分钟,以沉淀膜部分,吸出并储存在-80°C下供将来使用。[6] 通过在冰冷的SBB中重新悬浮来洗涤5-HT1A颗粒,并在4°C下以14000×g离心15分钟,然后吸出缓冲液。类似地洗涤hD4.2颗粒,但在冰冷的多巴胺激动剂结合缓冲液(DABB:50 mM Tris-HCl pH 7.4,5 mM KCl,2 mM MgCl2,2 mM CaCl2)中洗涤。洗涤后的5-HT1A膜在室温SSB中均化,并在10μM 5-HT存在和不存在的情况下与0.004至2.3 nM的12种浓度的[3H]WAY-100635一起孵育,以分别测定总结合和非特异性结合。同样,将洗涤过的hD4.2膜在室温DABB中进行Dounce均质化,并在10μM氯丙嗪存在和不存在的情况下,用0.004至13.4 nM的12种浓度的[3H]WAY-100635孵育,以分别测定总结合和非特异性结合。在室温下2小时后,通过在冷的0.3%PEI预浸过滤器上快速过滤来终止反应。然后在4°C 50 mM Tris-HCl(pH 6.9)中洗涤过滤器三次。然后将过滤后的材料转移到与4ml Ecoscint-A闪烁液(National Diagnostic;美国佐治亚州亚特兰大)混合的闪烁瓶中,并在Beckman LS6500闪烁计数器上计数。[6] 放射性配体结合分析。[6] 细胞在20cm平板上生长至融合。倾析生长培养基,用10ml冰冷的裂解缓冲液(1mM HEPES,pH 7.4和2mM EDTA)代替。10分钟后,从平板上刮下细胞,在30000×g和4°C下离心20分钟。使用Kinematica均质器在6的设置下将所得沉淀重新悬浮在4 ml受体结合缓冲液(50 mM Tris-HCl,pH 7.4和4 mM MgCl)中5秒,然后将1.0 ml等分试样再次在13000×g下离心10分钟。将沉淀储存在-80°C下直至使用。[6] 然后将颗粒重新悬浮,在受体结合缓冲液(50μg蛋白质/100μl)中研磨使用,并一式两份添加到含有0.1-0.2 nM[3H]斯皮龙和适当药物的测定管中。使用(+)-丁卡醇(5μM)测定非特异性结合。如cAMP结合测定所述,在过滤前,将测定管在37°C下孵育30分钟。将滤板干燥,并向每个孔中加入30μl Packard Microscint-O闪烁液。使用Packard TopCount闪烁计数器测定每孔的放射性。[6] 还进行了放射性配体结合试验,以研究100μM鸟苷基-5′-亚氨基二磷酸(Gpp-[NH]p)对激动剂结合的影响。这些实验是在改良的受体结合缓冲液(50 mM Tris-HCl,pH 7.4,4 mM MgCl和120 mM NaCl)中使用HEK-hD4.4膜进行的。 人重组5-HT₁A结合实验(CHO细胞):收集表达人5-HT₁A受体的CHO细胞,在冰浴的Tris-HCl缓冲液(50 mM,pH7.4,含10 mM MgCl₂)中匀浆,48,000 × g离心15 min。取50 μg膜蛋白与[³H]-8-OH-DPAT(0.5 nM)及不同浓度的WAY-100635 Maleate(10⁻¹²-10⁻⁶ M)在25°C孵育60 min。非特异性结合定义为在10 μM未标记5-HT存在下的结合。反应通过预浸泡于0.1%聚乙烯亚胺的GF/B滤膜过滤终止,用冰浴缓冲液洗涤3次后,液体闪烁光谱法计数放射性,利用Cheng-Prusoff方程计算Ki值[1] - 大鼠海马结合实验:分离大鼠海马,在冰浴的HEPES缓冲液(25 mM,pH7.4,含4 mM CaCl₂)中匀浆,50,000 × g离心20 min。取75 μg膜蛋白与[³H]-8-OH-DPAT(0.3 nM)及WAY-100635 Maleate(10⁻¹¹-10⁻⁶ M)在37°C孵育45 min。非特异性结合用10 μM Metergoline确定,过滤和放射性计数步骤同上[4] |
| 细胞实验 |
使用已加载 2 M NaC1 (12 MΩ–15 MΩ) 的玻璃微电极进行细胞外记录。两或三毫秒双相动作电位、缓慢(0.5 Hz - 2.0 Hz)放电模式和规则放电模式是将细胞区分为 5-HT 神经元的特征。将 α-1 肾上腺素能激动剂去氧肾上腺素 (3 μM) 添加到超融合 ACSF 中,以引起原本沉默的神经元放电。在使用各种药物之前,跟踪基线活动至少十分钟。精确的动作电位耦合到 A/D 转换器和 PC 驱动单独的动作电位,从而驱动示波器、电子速率计和高输入阻抗放大器。使用专用软件测量、计算积分发射率,并将其作为连续 10 秒样本显示在图表记录器上。通过比较 WAY 100635 应用前两分钟内记录的平均放电频率与药物作用峰值时记录的频率(通常是应用开始后两到五分钟)来评估激动剂的效果。当在拮抗剂存在的情况下应用激动剂时,将激动剂的效果与在拮抗剂单次灌注期间观察到的基线放电速率和频率进行对比。在重新测试激动剂的作用之前,拮抗剂需要十到二十五分钟的时间来适应。
CHO细胞cAMP实验:将表达人5-HT₁A受体的CHO细胞以1×10⁴个细胞/孔接种于96孔板,用含10%胎牛血清(FBS)的DMEM培养基培养24 h。更换为含WAY-100635 Maleate(10⁻¹⁰-10⁻⁶ M)±5-HT(10⁻⁷ M)的无血清DMEM孵育10 min,随后加入毛喉素(10 μM)刺激cAMP生成。30 min后,用竞争性ELISA试剂盒检测cAMP水平,在450 nm处读取吸光度[1] - SH-SY5Y细胞活力实验:将SH-SY5Y细胞以5×10⁴个细胞/孔接种于24孔板,用含10% FBS的RPMI 1640培养基培养。贴壁24 h后,更换为含WAY-100635 Maleate(1-100 μM)的无血清RPMI孵育24 h。加入MTT试剂(5 mg/mL)孵育4 h,用DMSO溶解甲臜结晶后,在570 nm处测定吸光度以计算细胞活力[6] |
| 动物实验 |
溶于 0.9% NaCl;250 μL (30.4 μCi/mL);静脉注射
体重 25-30 g 的雄性 CD1 小鼠动物/疾病模型:雄性 SD (Sprague-Dawley) 大鼠 (220-240 g)[hytomedicine. 2012年9月15日;19(12):1117-24] 剂量: 1 mg/kg 给药途径: 皮下注射(药代动力学/PK研究) 实验结果: 总戒断评分降低,不动时间增加,埋藏行为增加。 [123I]6b 和 [123I]7b 在大鼠体内的生物分布研究:一般程序 动物实验采用体重约230 g的雄性Wistar大鼠。所采用的动物实验方案已获得荷兰国家动物护理委员会和内部伦理委员会的批准,符合荷兰动物实验法的相关规定。放射性标记化合物的溶液在实验前一天配制。大鼠用2%异氟烷麻醉,经尾静脉注射200 μL放射性标记化合物。在不同时间间隔后,在麻醉状态下,通过颈椎脱臼处死大鼠,并从断头处采集血液。取出目标组织,称重,并使用LKB Wallac 1282 CompuGamma CS测定其放射性。为了计算注射剂量,取五份注射液称重并计数放射性。结果经衰变校正后,以每克组织注射剂量的百分比±标准差(% ID/g ± SD)表示。[]J Med Chem. 2011年5月26日;54(10):3480-91. [123I]6b 使用了两组各四只大鼠。第一组大鼠静脉注射200 μL(7 MBq,<20 ng)放射性标记化合物,并在注射后45分钟处死。第二组大鼠在静脉注射[123I]6b(7 MBq)前5分钟,静脉注射非标记化合物1(2 mg/kg)。大鼠也在注射后45分钟处死并解剖。[J Med Chem. 2011 May 26;54(10):3480-91.] [123I]7b 本研究使用了三组大鼠,每组四只。每只大鼠静脉注射200 μL(7 MBq,<20 ng)放射性标记化合物。分别在注射后15、45和120分钟处死,并按上述方法处理。J Med Chem. 2011年5月26日;54(10):3480-91。 大鼠强迫游泳试验方案:雄性Sprague-Dawley大鼠(220-250克)禁食12小时(自由饮水),随机分为4组(每组n=8):赋形剂组(生理盐水+0.1% DMSO,腹腔注射)、WAY-100635马来酸盐组(0.1毫克/千克,腹腔注射)、WAY-100635马来酸盐组(0.3毫克/千克,腹腔注射)和WAY-100635马来酸盐组(1毫克/千克,腹腔注射)。给药30分钟后,所有大鼠均接受8-OH-DPAT(1毫克/千克,腹腔注射)。 8-OH-DPAT给药后60分钟,将大鼠置于水缸(25±1°C,15 cm深)中6分钟,并记录其不动时间(最后4分钟)[2] - 小鼠高架十字迷宫实验:雄性ICR小鼠(20-22 g)分为4组(每组n=10):载体组(0.5%甲基纤维素,灌胃)、WAY-100635马来酸盐0.3 mg/kg(灌胃)、1 mg/kg(灌胃)、3 mg/kg(灌胃)。灌胃后60分钟,小鼠腹腔注射5-HT(1 mg/kg)。30分钟后,将小鼠置于高架十字迷宫(开放臂:30×5 cm,封闭臂:30×5×15 cm)上5分钟。通过视频追踪记录动物在开放臂停留的时间和进入开放臂的次数[6] - 大鼠背侧缝核(DRN)电生理:雄性Wistar大鼠(280-320 g)用氨基甲酸乙酯(1.5 g/kg,腹腔注射)麻醉,并固定于立体定位仪上。将玻璃微电极插入DRN(坐标:AP -7.8 mm,ML 0 mm,DV -8.5 mm,以bregma为参考点)。记录10分钟的基线放电率,然后静脉注射WAY-100635马来酸盐(0.01、0.03 mg/kg)。继续记录30分钟的放电率以评估变化[5] |
| 毒性/毒理 (Toxicokinetics/TK) |
急性毒性:在雄性 Sprague-Dawley 大鼠中,WAY-100635 马来酸盐的腹腔注射 LD₅₀ >100 mg/kg;在小鼠中,口服 LD₅₀ >200 mg/kg。在剂量高达 50 mg/kg 的大鼠中,未观察到死亡或严重不良反应(例如,惊厥、呼吸抑制)[5]
- 血浆蛋白结合率:在大鼠血浆中(通过超滤法测定),WAY-100635 马来酸盐在 10–1000 ng/mL 的浓度范围内具有 85% 的蛋白结合率,且与浓度无关[6] - 神经系统安全性:在连续 7 天每日腹腔注射 WAY-100635 马来酸盐(1 mg/kg)的大鼠中,未观察到运动协调性(转棒试验)或运动活性(旷场试验)的显著变化,表明其神经毒性较低[2] |
| 参考文献 | |
| 其他信息 |
本研究旨在探讨N-(2-(4-2-甲氧基苯基)-1-哌嗪基)乙基)-N-(2-吡啶基)环己烷甲酰胺(WAY 100635)对背侧缝核(DRN)和海马CA1区5-HT1A受体介导反应的影响。在灌注WAY 100635(10 nM)的DRN脑片中,大多数假定的5-HT神经元的放电频率增加(基线频率的13 ± 2%)。此外,WAY 100635完全抑制了5-HT(3-15 μM)、8-OH-DPAT(10 nM)、5-羧酰胺色胺(20 nM)和雷索匹隆(100 nM)引起的放电频率降低。 WAY 100635 对 15 μM 5-HT 的拮抗作用(IC50 = 0.95 ± 0.12 nM)可通过将 5-HT 浓度提高至 300 μM 而完全逆转。在海马切片中,WAY 100635(0.5-10 nM)不改变胞内记录的 CA1 锥体细胞的静息膜电位或膜输入电阻。然而,WAY 100635 完全抑制了 5-HT(15-30 μM)和 5-羧酰胺色胺(50-300 nM)引起的超极化和膜输入电阻降低(IC50 = 0.9-1.7 nM)。相反,WAY 100635既不影响5-HT(15 μM)引起的动作电位频率适应阻滞和慢后超极化,也不影响GABA(B)受体激动剂巴氯芬(10 μM)灌注引起的超极化和膜输入电阻降低。WAY 100635使5-羧酰胺色胺(3 nM-10 μM)的累积浓度-超极化曲线右移(表观Kb = 0.23 ± 0.07 nM),并且该药物还降低了激动剂的最大反应。这些数据表明,WAY 100635是5-HT1A受体的强效拮抗剂,无论是在背侧缝核(DRN)还是在海马CA1区。在DRN中,这种拮抗作用明显是竞争性的,而在海马中则部分是非竞争性的。拮抗剂与受体相互作用的动力学特征可能解释这些区域差异。[1]
研究背景和目的:WAY-100635 是一种典型的 5-HT1A 受体拮抗剂,已被广泛用作药理学探针,用于研究 5-HT1A 受体的分布和功能。我们的研究结果表明,WAY-100635 能有效诱导与其 5-HT1A 受体亲和力无关的效应。在本研究中,我们评估了该化合物在两种 D2 样受体亚型上的体外药理学特性。方法:在稳定表达多巴胺 D2L 或 D4.4 受体的 HEK 293 细胞中评估了 WAY-100635 的功能特性和结合亲和力。结果:美国国立精神卫生研究院(NIMH)精神活性药物筛选项目进行的初步筛选表明,WAY-100635 对 D2L、D3 和 D4.2 受体的结合亲和力分别为 940 nM、370 nM 和 16 nM。随后的饱和分析表明,[3H]WAY-100635 在 D4.2 受体上的解离常数(Kd)为 2.4 nM,仅比 5-HT1A 受体高十倍。WAY-100635 及其主要代谢物 WAY-100634 在 HEK-D4.4 细胞中均为强效激动剂(EC50 分别为 9.7±2.2 nM 和 0.65±0.2 nM)。WAY-100635 表现为完全激动剂,而 WAY-100634 表现为近乎完全激动剂。在HEK-D2L细胞中,WAY-100635对300 nM喹吡罗的作用具有微弱的拮抗作用。后续的放射性配体结合实验证实,WAY-100635对D4.4受体具有高亲和力,但与D2L受体的结合较弱(分别为3.3±0.6 nM和420±11 nM)。结论:本研究表明,WAY-100635并非如先前报道的“选择性”5-HT1A受体拮抗剂,因此,以往将WAY-100635作为选择性5-HT1A受体拮抗剂的研究结论可能需要重新评估。 [6] 本研究采用全半球放射自显影技术和选择性5-HT1A受体拮抗剂[3H]WAY-100635([O-甲基-3H]-N-(2-(4-(2-甲氧基苯基)-1-哌嗪基)乙基)-N-(2-吡啶基)环己烷甲酰胺三盐酸盐)检测了死后人脑中5-HT1A受体的分布。放射自显影图显示,该拮抗剂与海马、中缝核和新皮层高度结合。新皮层的标记强度略低于海马,主要位于浅层,但在较深的新皮层中也可见一条微弱的标记带。其他区域,例如杏仁核、隔区和屏状核,以及尾状核和壳核、小脑或脑干结构(中缝核除外),均显示出较低的密度。用[3H]WAY-100635标记人5-HT1A受体可被5-HT1A受体配体(5-HT、丁螺环酮、吲哚洛尔或8-OH-DPAT (10 μM))拮抗,从而仅留下极低的非特异性结合背景。对来自多个人类脑区的半定量数据进行饱和分析表明,[3H]WAY-100635的Kd值约为2.5 nM。 [3H]WAY-100635 对 5-HT1A 受体的选择性标记清楚地表明,该化合物可用于进一步的体外人 5-HT1a 受体亚型研究。[11C]WAY-100635 用于正电子发射断层扫描 (PET) 对 5-HT1A 受体的表征。WAY-100635 还用短半衰期正电子发射放射性核素碳-11 (t1/2 = 20 分钟) 进行放射性标记,并用于对人脑半球冷冻切片进行体外放射自显影。[11C]WAY-100635 的图像与 [3H]WAY-100635 的图像在定性上相似,但分辨率较低。因此,海马结构被密集标记,而新皮层中的标记密度较低。丁螺环酮、吲哚洛尔或 8-OH-DPAT (10 μM) 可完全阻断 [11C]WAY-100635 的结合。利用放射性标记的 WAY-100635 进行体外放射自显影,可获得人脑中 5-HT1A 受体分布的详细定性和定量信息。此外,这些研究为解释先前使用 PET 和 [11C]WAY-100635 在人体中以较低分辨率获得的初步结果提供了参考信息。这些数据为预期 [11C]WAY-100635 在体内作为高选择性放射性配体提供了强有力的基础。[3] WAY-100635 马来酸盐是一种广泛用于研究 5-HT₁A 受体生理和病理作用的研究工具化合物;它尚未获准用于临床[1,3] - 作用机制:其选择性5-HT₁A受体拮抗作用使其能够阻断突触前(自身受体)和突触后5-HT₁A受体介导的效应,因此可用于区分5-HT₁A依赖性和非依赖性5-HT信号传导[4] - 研究应用:WAY-100635马来酸盐常用于在临床前模型中研究5-HT₁A受体在情绪障碍(例如抑郁症、焦虑症)、疼痛感知和认知功能中的作用[2,6] - 药理特异性:与非选择性5-HT拮抗剂不同,WAY-100635马来酸盐不干扰其他神经递质系统,从而最大限度地减少实验研究中的脱靶效应[5] |
| 分子式 |
C29H38N4O6
|
|
|---|---|---|
| 分子量 |
538.64
|
|
| 精确质量 |
538.279
|
|
| 元素分析 |
C, 64.67; H, 7.11; N, 10.40; O, 17.82
|
|
| CAS号 |
1092679-51-0
|
|
| 相关CAS号 |
WAY-100635; 162760-96-5
|
|
| PubChem CID |
11957721
|
|
| 外观&性状 |
White to off-white solid powder
|
|
| LogP |
3.54
|
|
| tPSA |
123.51
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
9
|
|
| 可旋转键数目(RBC) |
9
|
|
| 重原子数目 |
39
|
|
| 分子复杂度/Complexity |
665
|
|
| 定义原子立体中心数目 |
0
|
|
| SMILES |
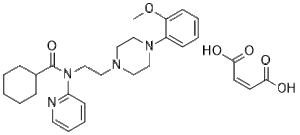
O=C(O)/C=C\C(O)=O.O=C(N(C1=NC=CC=C1)CCN2CCN(CC2)C3=CC=CC=C3OC)C4CCCCC4.[1:1]
|
|
| InChi Key |
XIGAHNVCEFUYOV-BTJKTKAUSA-N
|
|
| InChi Code |
InChI=1S/C25H34N4O2.C4H4O4/c1-31-23-12-6-5-11-22(23)28-18-15-27(16-19-28)17-20-29(24-13-7-8-14-26-24)25(30)21-9-3-2-4-10-21;5-3(6)1-2-4(7)8/h5-8,11-14,21H,2-4,9-10,15-20H2,1H3;1-2H,(H,5,6)(H,7,8)/b;2-1-
|
|
| 化学名 |
(Z)-but-2-enedioic acid;N-[2-[4-(2-methoxyphenyl)piperazin-1-yl]ethyl]-N-pyridin-2-ylcyclohexanecarboxamide
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中,避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|||
|---|---|---|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 25 mg/mL (46.41 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。 (<60°C).
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 1.8565 mL | 9.2826 mL | 18.5653 mL | |
| 5 mM | 0.3713 mL | 1.8565 mL | 3.7131 mL | |
| 10 mM | 0.1857 mL | 0.9283 mL | 1.8565 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
 |
|---|
 |
 |