| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 5g |
|
||
| Other Sizes |
|
| 体外研究 (In Vitro) |
对强制表达PGC-1α的原代小鼠肌细胞培养基进行液相色谱-质谱(LC-MS)代谢谱分析显示,与表达GFP的对照细胞相比,β-氨基异丁酸(BAIBA)的分泌增加了2.7倍。[1]
用5 µM的BAIBA处理从腹股沟白色脂肪组织(WAT)基质血管组分分化而来的原代小鼠脂肪细胞6天,能剂量依赖性地显著增加棕色脂肪细胞特异性基因UCP-1(5.3倍)和CIDEA(2.25倍)的mRNA表达,但不改变白色脂肪细胞基因ADIPOQ的表达。[1] 在分化过程中,用1 µM或10 µM的BAIBA处理人诱导多能干细胞(iPSC)来源的白色脂肪细胞,能诱导棕色脂肪细胞特异性基因(UCP-1, CIDEA, PRDM16, ELOVL3)的表达呈剂量依赖性增加。[1] 在相同的人iPSC来源的白色脂肪细胞中,用BAIBA处理(该实验未指定浓度)能显著增加基础和胰岛素刺激的葡萄糖摄取。同时,它还提高了基础耗氧率(OCR)、寡霉素不敏感的OCR(表明解偶联)以及由羰基氰化物间氯苯腙(CCCP)诱导的最大呼吸能力。[1] 用5 µM的BAIBA处理小鼠原代脂肪细胞,能使PPARα的mRNA表达增加2.4倍。该效应,以及BAIBA诱导的UCP-1和CIDEA的上调,可被选择性PPARα拮抗剂GW6471共处理或使用来自PPARα敲除小鼠的脂肪细胞所消除。[1] 用5 µM的BAIBA处理H4IIE肝细胞6天,能显著增加PPARα(5.4倍)和关键脂肪酸β-氧化基因(CPT1, ACADvl, ACADm, ACOX1)的mRNA表达。这种诱导作用可被PPARα拮抗剂GW6471共处理所消除。[1] 用浓度范围为0.1至10 µM的BAIBA处理H4IIE肝细胞6天,能剂量依赖性地增加由解偶联剂FCCP诱导的最大耗氧率(OCR)。[1] |
|---|---|
| 体内研究 (In Vivo) |
用3-氨基-2-甲基丙酸(BAIBA)治疗后,小鼠的体重有所下降。基于 MRI 的身体成分研究表明,BAIBA 疗法显着降低了小鼠的体脂。代谢笼研究显示,经 BAIBA 处理的小鼠的耗氧量 (VO2) 和全身能量消耗有所增加,但活动或食物摄入量没有任何显着变化,这与对生热和 β-氧化基因表达和体重的影响一致。此外,对小鼠进行腹膜内葡萄糖耐量试验(IPGTT)挑战。 IPGTT 曲线下面积表明 BAIBA 可以显着提高小鼠的糖耐量 [1]。
对C57BL6/J小鼠通过饮用水口服给予BAIBA(100 mg/kg/天或170 mg/kg/天)14天,能剂量依赖性地增加血浆BAIBA浓度(分别达到2 µM和8.9 µM),并显著上调腹股沟白色脂肪组织(WAT)中棕色脂肪细胞特异性基因(UCP-1, CIDEA, PGC-1α, 细胞色素C)的表达。[1] 肌肉特异性PGC-1α转基因(MCK-PGC1α)小鼠的血浆BAIBA浓度比对照组增加了11倍(6.5 µM)。相反,PGC-1α敲除小鼠的血浆BAIBA水平降低。[1] 进行3周自愿跑轮运动(锻炼)的野生型小鼠,与久坐对照组相比,血浆BAIBA浓度显著增加(增加19%,至2.6 µM)。[1] 对C57BL6/J小鼠通过饮用水口服给予BAIBA(100 mg/kg/天)14周(同时喂食高脂饮食),导致体重增加轻微减少,体脂百分比显著降低,全身耗氧量(VO2)和能量消耗增加(活动和食物摄入无变化),并且通过腹腔葡萄糖耐量试验(IPGTT)测量显示葡萄糖耐量改善。[1] BAIBA处理(100 mg/kg/天,14天)诱导的腹股沟WAT中棕色脂肪细胞特异性基因(UCP-1, CIDEA, PGC-1α, 细胞色素C)表达的增加,在PPARα敲除小鼠中被完全消除。[1] 对C57BL6/J小鼠通过饮用水口服给予BAIBA(100 mg/kg/天)14天,能显著增加肝脏中PPARα和关键β-氧化基因(CPT1, ACADvl, ACADm, ACOX1)的mRNA表达。这种诱导作用在PPARα敲除小鼠中不存在。[1] |
| 细胞实验 |
肌细胞培养与代谢物分析: 将原代小鼠成肌细胞分化为肌管。在分化第2天,用表达PGC-1α或GFP的腺病毒转导细胞。24小时后,更换为无血清培养基。再孵育24小时后,收集条件培养基,离心,上清液使用基于LC-MS的代谢谱分析平台进行小分子代谢物(包括BAIBA)的定量。[1]
原代小鼠脂肪细胞分化与处理: 从小鼠腹股沟白色脂肪组织中分离基质血管组分。细胞经培养后,使用含有胰岛素、地塞米松、IBMX、吲哚美辛、T3和罗格列酮的分化诱导混合物诱导分化为脂肪细胞。在为期6天的分化过程中,用载体或不同浓度的BAIBA(例如0.3, 1, 3, 5 µM)处理细胞。在抑制研究中,加入PPARα拮抗剂GW6471。分化结束后提取RNA,通过定量PCR(qPCR)进行基因表达分析。[1] 人iPSC向脂肪细胞分化: 将人诱导多能干细胞(iPSC)分化为间充质祖细胞,然后通过慢病毒表达PPARG2将其编程为白色脂肪细胞。在为期21天的脂肪形成分化过程中,培养基中添加或不添加BAIBA(1 µM或10 µM)。通过qPCR分析基因表达。[1] 人iPSC来源脂肪细胞的葡萄糖摄取实验: 将分化好的脂肪细胞进行血清饥饿处理,然后在Krebs-Ringer HEPES缓冲液中孵育。通过用放射性标记的2-脱氧-D-葡萄糖孵育细胞5分钟来测量葡萄糖摄取。在细胞松弛素B存在下测定非特异性摄取并扣除。[1] 细胞耗氧率(OCR)测量: 将分化好的脂肪细胞或肝细胞接种在专用的微孔板中。使用细胞外通量分析仪测量OCR。通过顺序注射寡霉素(ATP合酶抑制剂)、CCCP或FCCP(线粒体解偶联剂)和抗霉素A(复合体III抑制剂)来评估线粒体功能。[1] 肝细胞培养与处理: 将H4IIE肝细胞接种在胶原包被的板中,并在添加或不添加5 µM BAIBA和/或1 µM GW6471(PPARα拮抗剂)的标准培养基中培养6天,每两天更换一次培养基。然后提取RNA用于β-氧化基因的qPCR分析。[1] 肝细胞呼吸测定(OxoPlate法): 将H4IIE肝细胞接种在底部含有氧敏感荧光传感器的96孔板中。用一系列浓度的BAIBA(0-10 µM)处理细胞,处理时可添加或不添加GW6471,持续6天,并定期更换培养基。6天后,更换为含有相同化合物的无血清培养基,并覆盖矿物油。添加解偶联剂FCCP以诱导最大呼吸。在多个时间点测量荧光以计算耗氧率。[1] |
| 动物实验 |
在野生型和PPARα基因敲除小鼠中进行BAIBA治疗:将6周龄的C57BL6/J(野生型)或PPARα基因敲除小鼠按体重匹配后,随机分为对照组和治疗组。BAIBA以100 mg/kg/天或170 mg/kg/天的剂量溶于饮用水中。小鼠可自由饮用含药水(并根据实验需要喂食标准饲料或高脂饲料),持续14天或14周。对照组小鼠饮用普通饮用水。[1]
组织采集:治疗结束后,小鼠禁食、安乐死,并通过心脏穿刺采集血浆。快速解剖目标组织(例如,腹股沟白色脂肪组织、肝脏),液氮速冻,并保存用于后续的RNA提取和基因表达分析。 [1] 间接测热法:将小鼠用BAIBA(100 mg/kg/天)或水对照处理14周后,置于代谢笼(PhenoMaster系统)中。经过7天的适应期后,在可控光暗循环条件下,每两小时监测一次包括耗氧量(VO2)、二氧化碳生成量(VCO2)、食物摄入量、体重和运动活性在内的各项参数,持续数天,小鼠可自由摄取食物和(含药)水。[1] 腹腔葡萄糖耐量试验(IPGTT):小鼠禁食6小时后,腹腔注射葡萄糖溶液(1.5 mg葡萄糖/g体重)。使用血糖仪测量注射前(0分钟)以及注射后30、60和120分钟的尾静脉血血糖水平。计算曲线下面积(AUC)以评估葡萄糖耐量。 [1] 小鼠运动训练:12周龄野生型小鼠被允许使用自由跑轮进行为期3周的自愿耐力训练。对照组小鼠则被饲养在没有跑轮的环境中。训练结束后,收集血浆和肌肉组织进行代谢物分析。[1] |
| 参考文献 |
|
| 其他信息 |
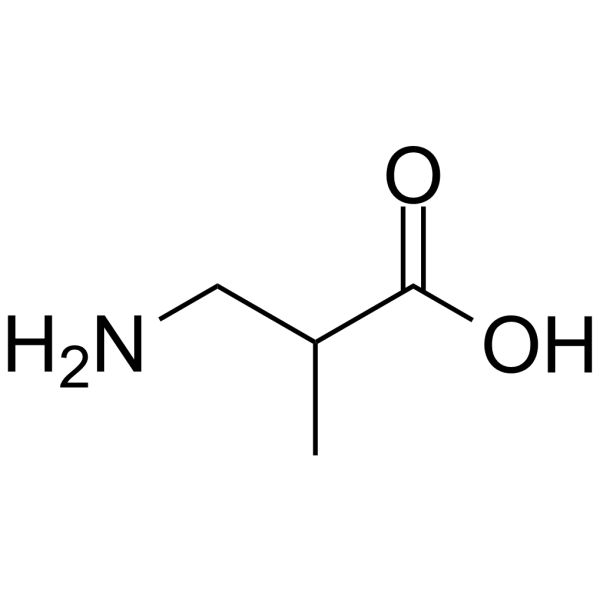
3-氨基异丁酸是一种β-氨基酸,是异丁酸的一个甲基氢被氨基取代后的产物。它是一种代谢产物,在功能上与异丁酸相关。它是3-氨基异丁酸酯的共轭酸,也是3-氨基异丁酸两性离子的互变异构体。
据报道,在果蝇、肠炎沙门氏菌和秀丽隐杆线虫中均发现了3-氮基-2-甲基丙酸酯,并有相关数据。 3-氨基异丁酸是氨基酸丙氨酸的衍生物,而丙氨酸是胸腺嘧啶代谢的产物,具有诱导下游代谢活性的潜力。运动期间,3-氨基异丁酸由肌肉细胞分泌到血液中。一旦该分子与脂肪细胞相互作用,它可能会诱导调节脂肪、胰岛素和胆固醇代谢的信号通路。 β-氨基异丁酸 (BAIBA) 被鉴定为一种新型小分子肌细胞因子,由骨骼肌细胞分泌,以响应运动诱导的转录共激活因子 PGC-1α 表达增加。[1] 在一项大型社区队列研究(弗雷明汉心脏研究,n=2067)中,血浆中 BAIBA 的水平与心血管代谢危险因素(空腹血糖、胰岛素、HOMA-IR、甘油三酯、总胆固醇)呈显著负相关。[1] 在一项对照运动干预研究(HERITAGE,n=80)中,20 周的耐力训练使血浆中 BAIBA 的浓度显著增加了 17%。 [1] 人类遗传关联研究发现,参与缬氨酸分解代谢和BAIBA生物合成途径的基因(例如AGXT2、ACADS、HADHA)中的单核苷酸多态性(SNP)与血浆BAIBA水平密切相关。研究还发现,这些途径中的几个基因在肌细胞中受PGC-1α转录上调。[1] 该研究提出,BAIBA是一种PGC-1α依赖的运动诱导信号,它促进肌肉和脂肪组织/肝脏之间的相互作用,从而促进代谢有益表型(白色脂肪组织褐变、肝脏β-氧化增强)并改善葡萄糖稳态,可能介导运动对代谢性疾病的某些保护作用。[1] |
| 分子式 |
C4H9NO2
|
|---|---|
| 分子量 |
103.1198
|
| 精确质量 |
103.063
|
| CAS号 |
144-90-1
|
| 相关CAS号 |
(S)-b-aminoisobutyric acid;4249-19-8;3-Amino-2-methylpropanoic acid-d3;1219803-65-2
|
| PubChem CID |
64956
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
223.6±23.0 °C at 760 mmHg
|
| 熔点 |
246.72°C (estimate)
|
| 闪点 |
89.0±22.6 °C
|
| 蒸汽压 |
0.0±0.9 mmHg at 25°C
|
| 折射率 |
1.462
|
| LogP |
-0.51
|
| tPSA |
63.32
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
3
|
| 可旋转键数目(RBC) |
2
|
| 重原子数目 |
7
|
| 分子复杂度/Complexity |
72.1
|
| 定义原子立体中心数目 |
0
|
| SMILES |
CC(CN)C(=O)O
|
| InChi Key |
QCHPKSFMDHPSNR-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C4H9NO2/c1-3(2-5)4(6)7/h3H,2,5H2,1H3,(H,6,7)
|
| 化学名 |
3-amino-2-methylpropanoic acid
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 本产品在运输和储存过程中需避光。 |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
H2O : ~100 mg/mL (~969.74 mM)
DMSO : ~1 mg/mL (~9.70 mM) |
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: 100 mg/mL (969.74 mM) in PBS (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液; 超声助溶。
请根据您的实验动物和给药方式选择适当的溶解配方/方案: 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 9.6974 mL | 48.4872 mL | 96.9744 mL | |
| 5 mM | 1.9395 mL | 9.6974 mL | 19.3949 mL | |
| 10 mM | 0.9697 mL | 4.8487 mL | 9.6974 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
Link: https://clinicaltrials.gov/ct2/show/NCT05328271
Conditions:Absorption; Chemicals