| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 10mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| 500mg |
|
||
| 5g |
|
||
| Other Sizes |
|
| 靶点 |
1. Tyrosinase (mushroom tyrosinase, IC50 = 1.8 μM for monophenolase activity, IC50 = 3.2 μM for diphenolase activity; murine tyrosinase, IC50 = 2.5 μM for diphenolase activity; Ki = 2.1 μM (competitive inhibition) for mushroom tyrosinase diphenolase activity) [2]
|
|---|---|
| 体外研究 (In Vitro) |
研究结果表明,4-丁基间苯二酚(4-n-丁基间苯二酚)对黑色素形成具有浓度依赖性的显着抑制作用。它还被发现可以抑制酪氨酸酶的作用,这种酶限制黑色素的产生速度。 4-丁基间苯二酚对 cAMP 反应元件结合蛋白 (CREB) 磷酸化没有影响,从而增加 MITF 的产生,也不会导致 ERK、Akt 激活或 MITF 降解。 4-在没有细胞的环境中,4-丁基间苯二酚显着降低酪氨酸酶活性。此外,扁柏酚和 4-丁基间苯二酚一起显示出降低 MITF 表达的相加效应 [2]。
1. 酪氨酸酶酶活性抑制:4-Butylresorcinol在体外呈剂量依赖性抑制酪氨酸酶的单酚酶和二酚酶活性。对蘑菇酪氨酸酶,其抑制单酚酶(以L-酪氨酸为底物)的IC50为1.8 μM,抑制二酚酶(以L-多巴为底物)的IC50为3.2 μM;Lineweaver-Burk图证实其对二酚酶的抑制为竞争性抑制(Ki=2.1 μM),表现为最大反应速率(Vmax)无变化,米氏常数(Km)从0.28 mM升至0.85 mM(5 μM药物处理组)。对小鼠B16黑色素瘤细胞来源的酪氨酸酶,其二酚酶抑制IC50为2.5 μM;浓度高达20 μM时,对过氧化物酶等其他氧化还原酶无显著抑制(残余活性>90%)[2] 2. B16黑色素瘤细胞黑色素合成抑制:在小鼠B16黑色素瘤细胞中,4-Butylresorcinol(0.5–10 μM)可剂量依赖性降低细胞内黑色素含量。5 μM浓度下,黑色素水平较未处理组降低68%,黑色素合成抑制的EC50为3.5 μM,且该浓度范围内对细胞活力无显著影响(10 μM时细胞活力>92%)。同时,该化合物可下调酪氨酸酶蛋白表达(5 μM时降低52%,蛋白印迹法检测)和mRNA水平(5 μM时降低45%,RT-PCR检测),但对酪氨酸酶相关蛋白1(TRP-1)和TRP-2的表达无显著影响(变化幅度<10%)[2] |
| 酶活实验 |
1. 蘑菇酪氨酸酶单酚酶活性抑制实验:在含L-酪氨酸(单酚底物)、系列浓度4-Butylresorcinol(0.1–20 μM)及纯化蘑菇酪氨酸酶的pH 6.8缓冲体系中构建反应。加入酪氨酸酶启动反应,37℃孵育30 min,每5 min检测475 nm处吸光度以监测单酚酶反应产物多巴色素的生成。根据吸光度-时间曲线的线性阶段计算初始反应速率,将残余酶活性以载体对照组为参照归一化,确定单酚酶抑制的IC50[2]
2. 蘑菇酪氨酸酶二酚酶活性抑制及动力学分析实验:在pH 6.8缓冲体系中,将L-多巴(二酚底物)、4-Butylresorcinol(0.5–10 μM)与蘑菇酪氨酸酶混合,37℃孵育20 min后检测475 nm吸光度,定量多巴色素生成量以计算二酚酶抑制IC50。动力学分析时,采用不同浓度L-多巴(0.1–1.0 mM)与固定浓度4-Butylresorcinol(0、2、5 μM)孵育,绘制Lineweaver-Burk图以确定抑制类型(竞争性)和Ki值[2] 3. 小鼠酪氨酸酶二酚酶活性抑制实验:通过硫酸铵沉淀和柱层析从B16黑色素瘤细胞裂解液中纯化小鼠酪氨酸酶,在pH 6.8缓冲体系中混合L-多巴、系列浓度4-Butylresorcinol(0.5–15 μM)与纯化小鼠酪氨酸酶,37℃孵育25 min后检测475 nm吸光度,拟合残余活性的量效曲线获得小鼠酪氨酸酶抑制的IC50[2] |
| 细胞实验 |
1. B16黑色素瘤细胞黑色素含量测定实验:将B16黑色素瘤细胞以2×10⁵个/孔接种于6孔板,培养至70%汇合度后,用系列浓度4-Butylresorcinol(0.5–10 μM)37℃、5% CO₂条件下处理72 h。收集细胞并冷PBS洗涤,加入碱性裂解液(1 M NaOH、10% DMSO)80℃加热1 h溶解黑色素,检测裂解液405 nm吸光度,以细胞总蛋白浓度(蛋白定量法测定)归一化黑色素含量,消除细胞数量差异的影响[2]
2. B16黑色素瘤细胞酪氨酸酶表达检测实验(蛋白印迹和RT-PCR):蛋白印迹分析时,将经4-Butylresorcinol(0–10 μM)处理48 h的B16细胞裂解,取等量蛋白进行SDS-PAGE电泳并转膜,封闭后4℃过夜孵育酪氨酸酶、TRP-1、TRP-2及内参蛋白一抗,室温孵育二抗1 h后显影,通过条带灰度定量蛋白表达。RT-PCR分析时,提取处理后细胞总RNA并逆转录为cDNA,用酪氨酸酶、TRP-1、TRP-2及管家基因的特异性引物进行扩增,采用相对Ct法计算mRNA相对表达量[2] 3. B16黑色素瘤细胞活力检测实验:将B16细胞以5×10⁴个/孔接种于96孔板,用4-Butylresorcinol(0–20 μM)处理72 h,加入细胞活力检测试剂37℃孵育2 h后检测对应波长吸光度。结果显示,该化合物在≤10 μM浓度下无显著细胞毒性(活力>92%),细胞活力IC50>20 μM[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
1. 体外细胞毒性:4-丁基间苯二酚对小鼠B16黑色素瘤细胞的细胞毒性较低,细胞活力IC50 > 20 μM(孵育72小时)。在浓度≤10 μM(有效抑制黑色素合成的浓度范围)时,细胞活力保持在92%以上,表明该浓度具有良好的黑色素抑制治疗窗口[2]
|
| 参考文献 | |
| 其他信息 |
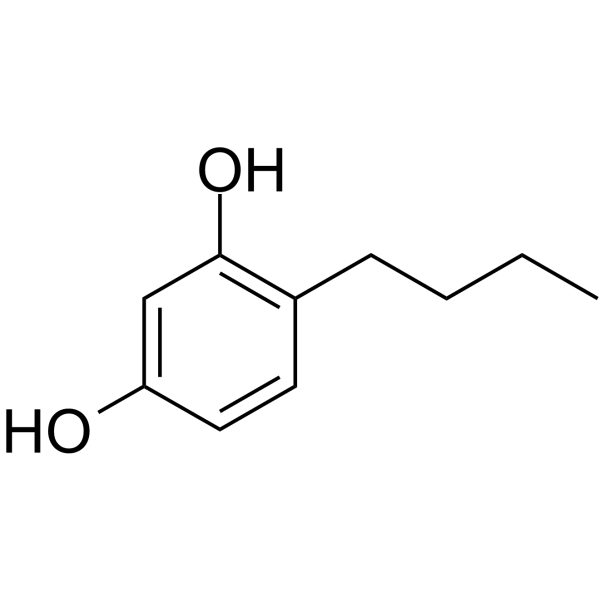
4-正丁基间苯二酚是间苯二酚类化合物的一种。
1. 4-丁基间苯二酚是一种合成酚类化合物,广泛用作化妆品美白剂,其核心结构为间苯二酚,4位被丁基链取代[2] 2. 美白作用机制:该化合物对黑色素生物合成具有双重作用:(1) 通过与酪氨酸酶二酚酶的活性位点结合(与L-DOPA竞争底物结合口袋),竞争性抑制酪氨酸酶二酚酶的活性;(2) 下调黑素细胞中酪氨酸酶mRNA和蛋白质的表达,减少可用于黑色素生成的活性酪氨酸酶的总量。值得注意的是,它不影响 TRP-1 或 TRP-2 的表达,表明其选择性靶向酪氨酸酶介导的黑色素合成途径 [2] 3. 活性比较:4-丁基间苯二酚 的酪氨酸酶抑制活性强于间苯二酚(间苯二酚对蘑菇酪氨酸酶二酚酶的 IC50 为 12.5 μM),与氢醌(一种经典的增白剂)的活性相当,但在有效浓度下细胞毒性更低 [2] |
| 分子式 |
C10H14O2
|
|---|---|
| 分子量 |
166.2170
|
| 精确质量 |
166.099
|
| CAS号 |
18979-61-8
|
| PubChem CID |
205912
|
| 外观&性状 |
White to off-white solid powder
|
| 密度 |
1.1±0.1 g/cm3
|
| 沸点 |
300.7±12.0 °C at 760 mmHg
|
| 闪点 |
144.5±14.2 °C
|
| 蒸汽压 |
0.0±0.7 mmHg at 25°C
|
| 折射率 |
1.555
|
| LogP |
2.82
|
| tPSA |
40.46
|
| 氢键供体(HBD)数目 |
2
|
| 氢键受体(HBA)数目 |
2
|
| 可旋转键数目(RBC) |
3
|
| 重原子数目 |
12
|
| 分子复杂度/Complexity |
125
|
| 定义原子立体中心数目 |
0
|
| InChi Key |
CSHZYWUPJWVTMQ-UHFFFAOYSA-N
|
| InChi Code |
InChI=1S/C10H14O2/c1-2-3-4-8-5-6-9(11)7-10(8)12/h5-7,11-12H,2-4H2,1H3
|
| 化学名 |
4-butylbenzene-1,3-diol
|
| HS Tariff Code |
2934.99.9001
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month |
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
DMSO : ~100 mg/mL (~601.61 mM)
|
|---|---|
| 溶解度 (体内实验) |
配方 1 中的溶解度: ≥ 2.5 mg/mL (15.04 mM) (饱和度未知) in 10% DMSO + 40% PEG300 + 5% Tween80 + 45% Saline (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。
例如,若需制备1 mL的工作液,可将100 μL 25.0 mg/mL澄清DMSO储备液加入到400 μL PEG300中,混匀;然后向上述溶液中加入50 μL Tween-80,混匀;加入450 μL生理盐水定容至1 mL。 *生理盐水的制备:将 0.9 g 氯化钠溶解在 100 mL ddH₂O中,得到澄清溶液。 配方 2 中的溶解度: ≥ 2.5 mg/mL (15.04 mM) (饱和度未知) in 10% DMSO + 90% (20% SBE-β-CD in Saline) (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 例如,若需制备1 mL的工作液,可将 100 μL 25.0 mg/mL澄清DMSO储备液加入900 μL 20% SBE-β-CD生理盐水溶液中,混匀。 *20% SBE-β-CD 生理盐水溶液的制备(4°C,1 周):将 2 g SBE-β-CD 溶解于 10 mL 生理盐水中,得到澄清溶液。 View More
配方 3 中的溶解度: ≥ 2.5 mg/mL (15.04 mM) (饱和度未知) in 10% DMSO + 90% Corn Oil (这些助溶剂从左到右依次添加,逐一添加), 澄清溶液。 1、请先配制澄清的储备液(如:用DMSO配置50 或 100 mg/mL母液(储备液)); 2、取适量母液,按从左到右的顺序依次添加助溶剂,澄清后再加入下一助溶剂。以 下列配方为例说明 (注意此配方只用于说明,并不一定代表此产品 的实际溶解配方): 10% DMSO → 40% PEG300 → 5% Tween-80 → 45% ddH2O (或 saline); 假设最终工作液的体积为 1 mL, 浓度为5 mg/mL: 取 100 μL 50 mg/mL 的澄清 DMSO 储备液加到 400 μL PEG300 中,混合均匀/澄清;向上述体系中加入50 μL Tween-80,混合均匀/澄清;然后继续加入450 μL ddH2O (或 saline)定容至 1 mL; 3、溶剂前显示的百分比是指该溶剂在最终溶液/工作液中的体积所占比例; 4、 如产品在配制过程中出现沉淀/析出,可通过加热(≤50℃)或超声的方式助溶; 5、为保证最佳实验结果,工作液请现配现用! 6、如不确定怎么将母液配置成体内动物实验的工作液,请查看说明书或联系我们; 7、 以上所有助溶剂都可在 Invivochem.cn网站购买。 |
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 6.0161 mL | 30.0806 mL | 60.1612 mL | |
| 5 mM | 1.2032 mL | 6.0161 mL | 12.0322 mL | |
| 10 mM | 0.6016 mL | 3.0081 mL | 6.0161 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。