| 规格 | 价格 | 库存 | 数量 |
|---|---|---|---|
| 5mg |
|
||
| 10mg |
|
||
| 25mg |
|
||
| 50mg |
|
||
| 100mg |
|
||
| 250mg |
|
||
| Other Sizes |
|
| 靶点 |
125I-SDF-CXCR4 ( IC50 = 13 nM ); HIV-1 (NL4.3 strain) ( IC50 = 1 nM ); HIV-1 (NL4.3 strain) ( IC50 = 9 nM ); HIV-1 (NL4.3 strain) ( IC50 = 3 nM ); HIV-1 (NL4.3 strain) ( IC50 = 26 nM )
Mavorixafor (AMD070) targets CXCR4 (IC₅₀ = 13 nM in CXCR4 ¹²⁵I-SDF inhibition binding assay) [1] Mavorixafor (AMD070) acts as an antagonist of the CXCL12/CXCR4 signaling axis [2] |
|---|---|
| 体外研究 (In Vitro) |
体外活性:AMD-070 对 MT-4 细胞中的 HIV-1、HIV-1 IIIb X4 株有活性,AMD-070 的 IC50 值高出 9 倍(0.009 μM vs 0.001 μM)和 8.7-与 MT-4 细胞相比,PBMC 中的浓度高出一倍(0.003 μM vs 0.026 μM)。 AMD-070具有抗病毒能力,IC50值为15.5 nM。激酶测定:首先将 SUP-T1 T 细胞与化合物(以 1 作为对照)在冰上预孵育 30 分钟,用含 2% FCS 的 PBS 洗涤,并与 PE 缀合的抗 CXCR4 mAb 在冰上孵育 30 分钟。用 PBS 洗涤后,用 1% 多聚甲醛的 PBS 溶液固定细胞样品,并在 FACS Calibur 流式细胞仪上进行分析。使用平均荧光强度值确定化合物对 mAb 结合的剂量依赖性抑制作用。细胞测定:激活的细胞(PHA刺激的母细胞)用PBS洗涤3次,完成病毒感染。 HIV 感染或模拟感染的 PHA 刺激的母细胞在 25 U/mL IL-2 和不同浓度的化合物存在下培养。第10天收集上清液,并通过p24病毒Ag ELISA试剂盒分析培养物上清液中的HIV-1核心抗原。如前所述进行MT-4细胞中HIV-1复制的抑制。抗 HIV-1 活性和细胞毒性测量同时进行。它们基于感染 HIV-1 的 MT-4 细胞在不同浓度的测试化合物存在下的活力。 ICsub>50定义为抑制50%的病毒感染细胞抵抗病毒细胞病变所需的浓度。
Mavorixafor (AMD070)在MT-4细胞中抑制T嗜性HIV-1(NL4.3株)复制的IC₅₀为2 nM,在PBMCs中为26 nM;该化合物在浓度超过23 μM时,对细胞无细胞毒性[1] - Mavorixafor (AMD070)对B88-SDF-1口腔癌细胞的贴壁依赖性生长无影响,但能显著抑制其非贴壁依赖性生长[3] - Mavorixafor (AMD070)可显著抑制B88-SDF-1口腔癌细胞由SDF-1/CXCR4介导的迁移和侵袭能力[3] |
| 体内研究 (In Vivo) |
AMD-070 在大鼠和狗中显示出良好的口服生物利用度。清除率取决于物种,与大鼠相比,AMD-070 在狗体内的清除率较低。
在CD-1小鼠中,经口给予200 μg/只或400 μg/只剂量的Mavorixafor (AMD070),可显著增加血液中白细胞的动员,且主要表现为淋巴细胞数量增多;药物同时升高白细胞计数,对红细胞和血小板无显著影响[2] - 在博来霉素(BLM)诱导的小鼠肺纤维化模型中,Mavorixafor (AMD070)处理未能缓解肺组织的炎症(H&E染色)和细胞外基质沉积(Masson三色染色),但可显著降低BLM诱导的肺损伤相关死亡率[2] - 在四氯化碳(CCl₄)诱导的C57BL/6小鼠肝纤维化模型中,Mavorixafor (AMD070)对肝纤维化(天狼星红染色)无改善作用,也未改变肝脏中Acta2和Col1a1的转录水平及血清AST水平[2] - 裸鼠中每日经口给予Mavorixafor (AMD070),可显著抑制B88-SDF-1口腔癌细胞的肺转移[3] |
| 酶活实验 |
这些化合物首先在冰上的 SUP-T1 T 细胞中预孵育 30 分钟,其中 1 个作为对照。随后,用含有 2% FCS 的 PBS 洗涤细胞,然后与 PE 缀合的抗 CXCR4 mAb 在冰上再孵育 30 分钟。细胞样品首先用 PBS 中的 1% 多聚甲醛固定,然后在 PBS 中清洗后使用 FACS Calibur 流式细胞仪进行检查。平均荧光强度值用于计算化合物对 mAb 结合的剂量依赖性抑制作用。
CXCR4受体结合实验 [1] : 采用放射性配体结合实验,以¹²⁵I-SDF作为标记配体,评估Mavorixafor (AMD070)与CXCR4的结合亲和力。将表达CXCR4的细胞与不同浓度的该化合物及定量的¹²⁵I-SDF共同孵育,分离游离和结合的配体后检测结合的放射性配体量,根据剂量-反应曲线计算出Mavorixafor (AMD070)抑制¹²⁵I-SDF与CXCR4结合的IC₅₀值。 |
| 细胞实验 |
在 96 孔板上,以 5 × 103 细胞/孔接种含有 10% FCS 的 DMEM。 24 小时后,用或不用 2 µM AMD3100 或 6.6 µM AMD-070 处理细胞。采用 MTT 的测定用于量化 24 或 48 小时后的细胞数量[2]。
MT-4细胞和PBMCs中HIV-1复制抑制实验 [1] : 将MT-4细胞和PBMCs感染T嗜性HIV-1(NL4.3株)后,用不同浓度的Mavorixafor (AMD070)处理。孵育特定时间后,通过检测病毒p24抗原产生量或病毒RNA水平确定病毒复制水平,依据剂量-反应关系计算药物在MT-4细胞和PBMCs中抑制HIV-1复制的IC₅₀值。同时采用细胞毒性实验评估细胞活力,确定化合物的无毒浓度范围。 - 口腔癌细胞贴壁依赖性和非贴壁依赖性生长实验 [3] : 贴壁依赖性生长实验中,将B88-SDF-1口腔癌细胞接种于培养板,加入不同浓度的Mavorixafor (AMD070),孵育一定时间后通过细胞计数或比色法检测细胞增殖情况。非贴壁依赖性生长实验中,将细胞悬浮于含药软琼脂中并接种于培养皿,培养数周后计数形成的集落数,评估化合物对集落形成的抑制作用。 - 细胞迁移和侵袭实验 [3] : 迁移实验中,将B88-SDF-1细胞接种于transwell小室上室,下室加入含或不含Mavorixafor (AMD070)的SDF-1,孵育后计数穿过膜的细胞数。侵袭实验中,先对transwell小室进行细胞外基质包被,再按迁移实验流程操作并计数侵袭细胞数,以此评估药物对SDF-1/CXCR4介导的侵袭的抑制作用。 |
| 动物实验 |
小鼠:在无病原体环境中饲养BALB/c裸鼠。小鼠达到8周龄后,实验开始。简而言之,将细胞接种到1×10⁶只裸鼠的血管中。第49天处死小鼠。采用H&E染色确定是否存在远处转移。小鼠每天口服0.2 mL生理盐水作为载体,或等体积的Mavorixafor(AMD-070)(2 mg/kg),作为实验化疗的一部分[2]。
CD-1和C57BL/6小鼠的药代动力学研究[2] :CD-1小鼠单次口服400 μg/只的Mavorixafor(AMD070),并在不同时间点采集肺组织样本,使用定量分析方法测定药物浓度。 C57BL/6 小鼠接受腹腔注射(IP)药物,并在不同时间点采集血浆、肝脏和肺脏样本,以确定这些组织中的药物浓度,并计算每个时间点的平均浓度和平均值的标准误差(SEM)。 - 小鼠白细胞动员研究[2] :CD-1 小鼠口服给予Mavorixafor (AMD070),剂量分别为 200 μg/只或 400 μg/只,并在不同时间点采集血样,使用标准血液学方法计数白细胞、红细胞、血小板,并进行细胞分类计数(淋巴细胞、中性粒细胞、单核细胞、嗜酸性粒细胞)。 C57BL/6小鼠腹腔注射400 μg/只的药物,并按照相同方案进行血细胞计数以评估白细胞动员。 - 博来霉素诱导的小鼠肺纤维化模型[2] :CD-1小鼠接受博来霉素(BLM)治疗以诱导肺纤维化,并在BLM治疗后特定时间开始口服给予Mavorixafor (AMD070)指定剂量。对照组接受PBS加醋酸盐缓冲液或BLM加醋酸盐缓冲液。在实验终点,收集肺组织进行苏木精-伊红染色(评估炎症)和马松三色染色(评估纤维化),并监测小鼠的存活情况,以分析药物对死亡率的影响。 - 四氯化碳诱导的小鼠肝纤维化模型[2] :用四氯化碳(CCl₄)处理C57BL/6小鼠以诱导肝纤维化,并腹腔注射一定剂量的Mavorixafor (AMD070)。对照组分别接受油加PBS或CCl₄加PBS。治疗结束后,收集肝组织进行Picosirius红染色以量化纤维化程度,并通过qPCR检测Acta2和Col1a1的转录水平;还测定了血清AST水平以评估肝损伤。 - 裸鼠口腔癌转移模型[3] :将B88-SDF-1口腔癌细胞注射到裸鼠体内,建立转移模型。从肿瘤细胞注射当天或预定时间点开始,每日口服特定剂量的Mavorixafor (AMD070)。对照组小鼠接受溶剂对照。一段时间后,处死小鼠,检查肺组织并计数转移结节的数量,以评估药物对肺转移的抑制作用。 |
| 药代性质 (ADME/PK) |
吸收
在患有WHIM综合征的成人中,每日一次服用400 mg后,稳态时平均(CV%)Cmax为3304 (58.6%) ng/mL,0至24小时AUC (AUC0-24h)为13970 (58.4%) ng·h/mL。Mavorixafor的药代动力学呈非线性,在50 mg(推荐剂量的0.125倍)至400 mg的剂量范围内,Cmax和AUC0-24h的增加幅度大于剂量比例。在健康受试者中,服用最高批准推荐剂量后,Mavorixafor的稳态血药浓度大约在9至12天后达到。在最高批准推荐剂量下,Mavorixafor的中位(范围)Tmax为2.8小时(1.9至4小时)。食物会降低Cmax和AUC。 排泄途径 在健康受试者中,单次口服放射性标记的马沃利沙福后,240 小时收集期内,74.2% 的给药剂量被回收,其中 61.0% 的放射性物质从粪便中回收,13.2%(3% 为原形)从尿液中回收。 分布容积 在患有 WHIM 综合征的成人中,马沃利沙福的分布容积为 768 L。 清除率 在健康受试者中,单次服用 400 mg 马沃利沙福后,平均(变异系数%)表观清除率为 62 L/h (40%)。马沃利沙福表现出至少部分非线性表观清除率;然而,在批准的推荐剂量下,这种非线性清除率不具有临床意义。 蛋白结合率 体外实验表明,马沃利沙福与人血浆蛋白的结合率 >93%。 代谢/代谢物 马沃利沙福主要通过CYP3A4代谢,其次通过CYP2D6代谢。 生物半衰期 健康受试者单次服用400 mg马沃利沙福后,平均(CV%)末端半衰期为82小时(34%)。 马沃利沙福(AMD070)是一种口服生物利用度高的小分子药物;在大鼠和犬中均观察到良好的口服生物利用度[1] - 在CD-1小鼠中,口服400 μg/只的Mavorixafor (AMD070)后,在肺组织中检测到了该药物,且其浓度随时间变化,EC₉₀ (44 ng/mL) 被用作药效学活性的参考阈值[2] - 在C57BL/6小鼠中,腹腔注射Mavorixafor (AMD070)后,该药物分布于血浆、肝脏和肺组织中,在不同时间点均可检测到其浓度[2] |
| 毒性/毒理 (Toxicokinetics/TK) |
Mavorixafor (AMD070)在体外浓度超过23 μM时对MT-4细胞和PBMC无细胞毒性[1]
妊娠和哺乳期影响 ◉ 哺乳期用药概述 目前尚无关于哺乳期使用mavorixafor的信息。生产商建议在治疗期间以及末次给药后三周内不要进行母乳喂养。 ◉ 对母乳喂养婴儿的影响 截至修订日期,未找到相关的已发表信息。 ◉ 对泌乳和母乳的影响 截至修订日期,未找到相关的已发表信息。 |
| 参考文献 |
|
| 其他信息 |
AMD 070 是一种氨基喹啉类药物。
Mavorixafor 是一种小分子候选药物,属于一类新型的抗 HIV 药物,称为病毒进入(融合)抑制剂。目前,仅有一种获得 FDA 批准的病毒进入抑制剂——恩夫韦地(Fuzeon)可用于治疗 HIV 感染。包括 mavorixafor 在内的几种实验性病毒进入抑制剂正处于早期临床试验阶段。Mavorixafor 是一种选择性 CXCR4 受体变构拮抗剂,可抑制 HIV 病毒进入并感染健康细胞。 Mavorixafor 是一种口服生物利用度高的 CXC 趋化因子受体 4 (CXCR4) 抑制剂,具有潜在的抗肿瘤和免疫检查点抑制活性。给药后,mavorixafor 选择性地与 CXCR4 结合,阻止 CXCR4 与其配体基质细胞衍生因子 1 (SDF-1 或 CXCL12) 结合。这抑制了受体活化,导致CXCR4过表达肿瘤细胞的增殖和迁移减少。此外,抑制CXCR4可阻止调节性T细胞和髓源性抑制细胞(MDSC)募集到肿瘤微环境,从而消除CXCR4介导的免疫抑制,并激活细胞毒性T淋巴细胞介导的针对癌细胞的免疫反应。G蛋白偶联受体CXCR4在多种肿瘤细胞类型中高表达,可诱导免疫抑制细胞募集到肿瘤微环境,抑制免疫监视,并促进肿瘤血管生成和肿瘤细胞增殖。它也是HIV进入T细胞的辅助受体。 药物适应症 已研究用于治疗HIV感染。 作用机制 已知表达于免疫细胞表面的趋化因子受体在病毒感染和传播中起着关键作用。CXCR4和另一种趋化因子受体CCR5参与HIV感染。HIV进入细胞的过程始于病毒包膜糖蛋白与CD4受体和仅有的两种趋化因子受体之一的结合,最终导致病毒膜与细胞膜融合。病毒进入为抗HIV治疗提供了新的靶点。迄今为止,至少已出现3个亚类的HIV病毒进入/融合抑制剂:1. CD4结合或附着——靶向病毒糖蛋白gp120与细胞表面CD4抗原的初始识别和结合。 2. 趋化因子共受体结合 - 靶向病毒与 CCR5 或 CXCR4 共受体的结合。3. 融合抑制 - 靶向病毒糖蛋白 gp41,抑制病毒与细胞的融合。不同的 HIV 毒株偏好不同的受体,或可能使用任一受体感染细胞。 35% 的毒株同时使用 CXCR4 和 CCR5 5% 的毒株仅使用 CXCR4 60% 的毒株仅使用 CCR5 感染者体内可能存在不同水平的 CXCR4 和 CCR5 结合病毒 使用 CXCR4 的病毒可独立预测 CD4 下降和 HIV 临床进展,并与早期死亡相关。 药效学 AMD-070 是一种小分子候选药物,属于一类新型的抗 HIV 研究药物,称为进入(融合)抑制剂。约76%病毒载量可测的HIV感染者感染了对一种或多种抗逆转录病毒药物耐药的病毒株,这限制了他们的治疗选择。与许多现有的HIV药物在病毒感染健康细胞后发挥作用不同,AMD-070通过阻断病毒进入健康细胞来阻止其复制。AMD-070靶向HIV病毒表面的CXCR4受体,阻止病毒进入并感染健康细胞。 AMD-070 特异性靶向 CXCR4 受体,体外实验表明其不与其他趋化因子受体相互作用。 AMD-070 体外实验表明其能强效抑制所有利用 CXCR4 受体的病毒(包括仅利用 CXCR4 受体的病毒和/或同时利用 CXCR4 和 CCR5 受体的病毒)的感染。 AMD-070 在动物体内具有口服生物利用度。 其药代动力学和毒性特征适合口服给药。 AMD-070 与其他已知的抗 HIV 药物联合使用时,体外实验表明其具有叠加或协同作用。 AMD-070 对体外实验中对现有抗逆转录病毒疗法耐药的利用 CXCR4 受体的 HIV 毒株具有活性。 对利用 CXCR4 受体的实验室毒株和临床分离株均具有强效抗 HIV 活性。 Mavorixafor (AMD070) 是首个用于治疗 HIV-1 感染的小分子口服生物利用度高的 CXCR4 拮抗剂 [1] - Mavorixafor (AMD070) 通过拮抗 CXCR4 受体发挥其抗 HIV-1 作用,从而抑制 T 嗜性 (X4) HIV-1 进入宿主细胞 [1]。在纤维化疾病模型中,Mavorixafor (AMD070) 可调节 CXCL12/CXCR4 信号通路,但不能有效减少肺纤维化或肝纤维化中的细胞外基质沉积;然而,它能改善博来霉素 (BLM) 诱导的肺损伤的死亡率,这可能是通过抑制早期炎症反应和/或血管渗漏实现的 [2]。Mavorixafor (AMD070) 是一种微创替代 AMD3100(一种皮下注射的 CXCR4 拮抗剂)的药物,可用于抑制头颈癌的 CXCR4 相关转移 [3]。 |
| 分子式 |
C₂₁H₂₇N₅
|
|
|---|---|---|
| 分子量 |
349.47
|
|
| 精确质量 |
349.226
|
|
| 元素分析 |
C, 72.17; H, 7.79; N, 20.04
|
|
| CAS号 |
558447-26-0
|
|
| 相关CAS号 |
Mavorixafor trihydrochloride; 2309699-17-8; 880549-30-4
|
|
| PubChem CID |
11256587
|
|
| 外观&性状 |
White to gray solid powder
|
|
| 密度 |
1.2±0.1 g/cm3
|
|
| 沸点 |
597.0±50.0 °C at 760 mmHg
|
|
| 熔点 |
108-110ºC
|
|
| 闪点 |
314.9±30.1 °C
|
|
| 蒸汽压 |
0.0±1.7 mmHg at 25°C
|
|
| 折射率 |
1.656
|
|
| LogP |
2.78
|
|
| tPSA |
70.83
|
|
| 氢键供体(HBD)数目 |
2
|
|
| 氢键受体(HBA)数目 |
4
|
|
| 可旋转键数目(RBC) |
7
|
|
| 重原子数目 |
26
|
|
| 分子复杂度/Complexity |
431
|
|
| 定义原子立体中心数目 |
1
|
|
| SMILES |
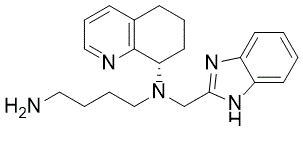
NCCCCN(CC1=NC2=C(N1)C=CC=C2)[C@@H]3C4=C(CCC3)C=CC=N4
|
|
| InChi Key |
WVLHHLRVNDMIAR-IBGZPJMESA-N
|
|
| InChi Code |
InChI=1S/C21H27N5/c22-12-3-4-14-26(15-20-24-17-9-1-2-10-18(17)25-20)19-11-5-7-16-8-6-13-23-21(16)19/h1-2,6,8-10,13,19H,3-5,7,11-12,14-15,22H2,(H,24,25)/t19-/m0/s1
|
|
| 化学名 |
N'-(1H-benzimidazol-2-ylmethyl)-N'-[(8S)-5,6,7,8-tetrahydroquinolin-8-yl]butane-1,4-diamine
|
|
| 别名 |
|
|
| HS Tariff Code |
2934.99.9001
|
|
| 存储方式 |
Powder -20°C 3 years 4°C 2 years In solvent -80°C 6 months -20°C 1 month 注意: 请将本产品存放在密封且受保护的环境中(例如氮气保护),避免吸湿/受潮。 |
|
| 运输条件 |
Room temperature (This product is stable at ambient temperature for a few days during ordinary shipping and time spent in Customs)
|
| 溶解度 (体外实验) |
|
|---|
| 制备储备液 | 1 mg | 5 mg | 10 mg | |
| 1 mM | 2.8615 mL | 14.3074 mL | 28.6148 mL | |
| 5 mM | 0.5723 mL | 2.8615 mL | 5.7230 mL | |
| 10 mM | 0.2861 mL | 1.4307 mL | 2.8615 mL |
1、根据实验需要选择合适的溶剂配制储备液 (母液):对于大多数产品,InvivoChem推荐用DMSO配置母液 (比如:5、10、20mM或者10、20、50 mg/mL浓度),个别水溶性高的产品可直接溶于水。产品在DMSO 、水或其他溶剂中的具体溶解度详见上”溶解度 (体外)”部分;
2、如果您找不到您想要的溶解度信息,或者很难将产品溶解在溶液中,请联系我们;
3、建议使用下列计算器进行相关计算(摩尔浓度计算器、稀释计算器、分子量计算器、重组计算器等);
4、母液配好之后,将其分装到常规用量,并储存在-20°C或-80°C,尽量减少反复冻融循环。
计算结果:
工作液浓度: mg/mL;
DMSO母液配制方法: mg 药物溶于 μL DMSO溶液(母液浓度 mg/mL)。如该浓度超过该批次药物DMSO溶解度,请首先与我们联系。
体内配方配制方法:取 μL DMSO母液,加入 μL PEG300,混匀澄清后加入μL Tween 80,混匀澄清后加入 μL ddH2O,混匀澄清。
(1) 请确保溶液澄清之后,再加入下一种溶剂 (助溶剂) 。可利用涡旋、超声或水浴加热等方法助溶;
(2) 一定要按顺序加入溶剂 (助溶剂) 。
| NCT Number | Recruitment | interventions | Conditions | Sponsor/Collaborators | Start Date | Phases |
| NCT03995108 | Active Recruiting |
Drug: Mavorixafor Drug: Placebo |
WHIM Syndrome | X4 Pharmaceuticals | October 24, 2019 | Phase 3 |
| NCT04154488 | Recruiting | Drug: Mavorixafor | Neutropenia | X4 Pharmaceuticals | October 16, 2020 | Phase 1 Phase 2 |
| NCT06056297 | Not yet recruiting | Drug: Mavorixafor Drug: Placebo |
Neutropenia | X4 Pharmaceuticals | February 2024 | Phase 3 |
| NCT04274738 | Completed | Drug: Mavorixafor Drug: Ibrutinib |
Waldenstrom's Macroglobulinemia | X4 Pharmaceuticals | April 30, 2020 | Phase 1 |
| NCT03005327 | Completed | Drug: X4P-001 | WHIM Syndrome | X4 Pharmaceuticals | December 2016 | Phase 2 |